-
火龙果(Hylocereus polyrhizus,pitaya)是仙人掌科(Cactaceae)量天尺属(Hylocereus)或蛇鞭柱属(Selenicereus)的热带果树[1]。截至2023年,中国火龙果种植面积已超过6.6万hm2,年产量超160万t,其中种植以‘金都一号’品种为代表的红皮红肉火龙果居多[2]。然而,红皮红肉火龙果成熟后鳞片会出现褪绿变红的现象。火龙果鳞片颜色主要调控色素为叶绿素和甜菜红素[3]。叶绿素是植物进行光合作用的必需色素[4]。当植物体受到逆境胁迫或衰老时,叶绿素含量会逐渐下降[5]。甜菜红素是存在于火龙果、红甜菜等植物中的水溶性含氮色素[6]。火龙果鳞片中的甜菜红素会随着果实成熟逐渐增多[7]。鳞片褪绿变红会极大地影响火龙果商品品质,给火龙果产业造成持续性的经济损失,此外,火龙果果实质量大小会直接影响火龙果种植的产量,进而决定火龙果产业利润的高低。因此,鳞片保绿与果实增重成为了火龙果优质栽培领域的重点与难点,急需进行技术突破。
植物生长调节剂(plant growth regulators,PGRs)是人工合成或从自然界提取的具有激素作用的生物化学物质[8],主要通过叶面喷施应用到植物栽培管理中[9]。可通过有效调节作物生长发育进程达到提升品质、作物增产、增加植物抗逆等目的[10 − 12]。然而,由于植物生长调节剂具有两重性[13],且对火龙果鳞片颜色的影响缺乏系统的探索,极大程度限制了其在栽培管理中的应用。值得注意的是,火龙果果皮较厚且具有蜡质层保护,植物生长调节剂很难渗入果肉,并且在采摘后会进行统一的洗果处理,去除果皮表面的药物残留,不会对消费者身体健康造成影响[14]。
因此,本研究选择农业中最常用的9种植物生长调节剂(氯吡脲,S-诱抗素、苄氨基嘌呤、乙烯利、赤霉酸、芸苔素内酯、胺鲜酯、复硝酚钠、萘乙酸),并根据田间施用建议质量浓度对火龙果进行叶面喷施。本研究的目的是系统筛选出能够促进火龙果鳞片保绿与果实增重的植物生长调剂种类及浓度,并探究农业中常用植物生长调节剂在火龙果生长栽培领域使用的可行性,为火龙果优质生产提供理论依据。
-
供试火龙果品种为‘金都一号’。试验地点位于海南省东方市板桥镇白穴村的海南恩红农业科技有限公司火龙果基地(18.81°N,108.74°E),属热带季风海洋性气候区,旱湿两季分明,年平均降雨量1 150 mm,年平均气温24~ 25 ℃。试验田被划分为3个平行处理试验区,每个平行处理试验区面积为50 m×30 m,平行试验区被划分为90个试验小区,每个试验小区面积为4 m×2.7 m,每个试验小区内火龙果株数≥12株,同一批次结果数≥20颗,每个处理在1个试验小区内进行。
-
试验分初筛试验与复筛试验两次。初筛试验时间为2023-04-03—2023-05-08。处理组:在火龙果授粉后第13 天(2023-03-31)与第23 天(2023-04-11)进行喷施,共有29个处理,除自然生长的对照组(CK)与自来水处理外,其他处理所使用生长调节剂种类及质量浓度为:氯吡脲(CPPU)50倍稀释液(20 mg·L−1)、100倍稀释液(10 mg·L−1))、200倍稀释液(5 mg·L−1);S-诱抗素250倍稀释液(4 mg·L−1)、500倍稀释液(2 mg·L−1)、1 000倍稀释液(1 mg·L−1);苄氨基嘌呤(6-BA)250倍稀释液(80 mg·L−1)、500倍稀释液(40 mg·L−1)、1 000倍稀释液(20 mg·L−1);乙烯利(ETH)250倍稀释液(1.6 g·L−1)、500倍稀释液(0.8 g·L−1)、1 000倍稀释液(0.4 g·L−1);赤霉酸(GA3)500倍稀释液(60 mg·L−1)、1 000倍稀释液(30 mg·L−1)、2 000倍稀释液(15 mg·L−1);芸苔素内酯(BR)250倍稀释液(0.3 mg·L−1)、500倍稀释液(0.15 mg·L−1)、1 000倍稀释液(0.075 mg·L−1);复硝酚钠1 000倍稀释液(18 mg·L−1)、2 000倍稀释液(9 mg·L−1)、4 000倍稀释液(4.5 mg·L−1);胺鲜酯(DA-6)1 000倍稀释液(50 mg·L−1)、2 000倍稀释液(25 mg·L−1)、4 000倍稀释液(12.5 mg·L−1);萘乙酸(NAA)
4000 倍稀释液(12.5 mg·L−1)、8000 倍稀释液(6.25 mg·L−1)、16 000倍稀释液(3.125 mg·L−1)。初筛试验在果实成熟之后(授粉后31~35 d,2023-05-04—2023-05-08进行采摘。复筛试验时间为2023−05−15—2023−06−24。处理组:在火龙果授粉后第5天(2023−05−20)、第13 天(2023−05−28)、第23 天(2023−06−07)进行喷施,共有22个处理,除自然生长的对照组(CK)外,使用肥料种类、浓度及其喷施时间为授粉后第5天喷施赤霉酸500倍、1 000倍、2 000倍稀释液,氯吡脲100倍、200倍稀释液,萘乙酸4 000倍、8 000倍稀释液;授粉后第13天喷施赤霉酸500倍、1 000倍、2 000倍稀释液,氯吡脲100倍、200倍稀释液,萘乙酸4 000倍、8 000倍稀释液;授粉后第23天喷施赤霉酸500倍、1 000倍、2 000倍稀释液,氯吡脲100倍、200倍稀释液,萘乙酸4 000倍、8 000倍稀释液。复筛试验在果实成熟之后(授粉后第30天至第32天,即2023−06−14—2023−06−16)进行采摘。
喷施及采摘要求为夜间对火龙果叶面进行喷施(重点喷施火龙果果实表面),喷施量以果面附着液珠不滴落为标准,每个试验小区喷施样品个数为30个,果实成熟后每小区随机选取10个果实进行测定。试验区内除试验所需叶面肥喷施外,在实验过程中均按生产常规进行管理。
激素包括:氯吡脲(四川国光农化股份有限公司,氯吡脲0.1%(V/V)),S-诱抗素(四川润尔科技有限公司,S-诱抗素0.1%(V/V)),苄氨基嘌呤(四川润尔科技有限公司,苄氨基嘌呤2%(V/V)),乙烯利(四川国光农化股份有限公司,乙烯利40%(V/V)),赤霉酸(四川润尔科技有限公司,赤霉酸3%(V/V)),芸苔素内酯(成都新朝阳作物科学股份有限公司,14-羟基芸苔素内酯甾醇0.007 5%(V/V)),复硝酚钠(深圳诺普信农化股份有限公司,5-硝基邻甲氧基苯酚钠0.3%(V/V),对硝基苯酚钠0.9%(V/V),邻硝基苯酚钠0.6%(V/V)),胺鲜酯(广东植物龙生物技术股份有限公司,胺鲜酯5%(V/V)),萘乙酸(四川润尔科技有限公司,萘乙酸20%(V/V))。
-
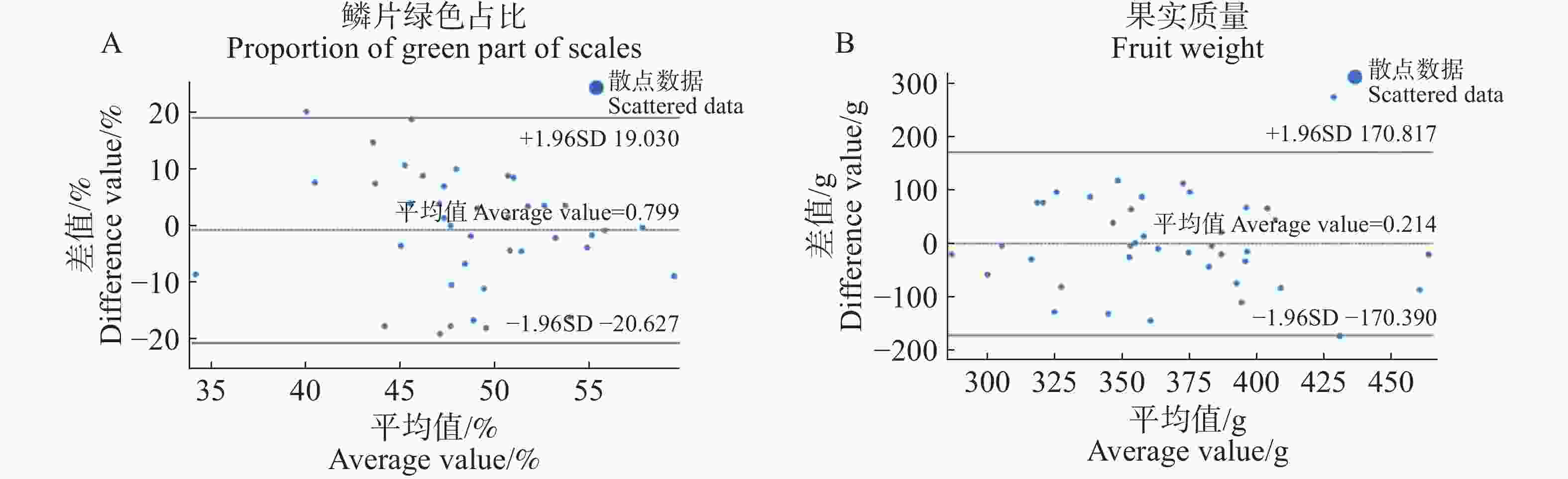
果实鳞片绿色占比测定:取待测果实样品直径最大处的鳞片,使用游标卡尺测定鳞片中轴绿色部分长度及鳞片总长度,计算每个样品鳞片绿色占比并求出果实鳞片绿色占比平均值。鳞片绿色占比(图1、2)公式:
$$ \begin{aligned} & 鳞片绿色占比(\text{%})=鳞片中轴处绿色部分长度/\\ & 鳞片总长度 \times 100 。\end{aligned}$$ 火龙果果实质量测定:取待测果实样品,测量单果果实质量,并计算平均果实质量。
-
试验数据采用Excel进行统计处理,用SPSS v19.0进行正态性检验、单因素方差分析和双因素方差分析,同时采用邓肯法进行多重比较分析;用SPSSAU进行Bland-Altman分析并评估数据的一致性;采用Orgin作图。
-
对火龙果进行自来水喷施(自来水处理组),同时以自然状态下生长的火龙果作为对照组。结果表明,对照组与自来水处理组的火龙果果实鳞片绿色占比和果实质量均在±1.96SD范围内,均占总数据的97.5%(图3)。这表明两组数据具有很高的一致性,且差异无统计学意义。因此,本研究用自然状态下生长的火龙果作为植物生长调节剂处理的对照组。
-
试验结果表明,氯吡脲处理的火龙果果实成熟时间相较于对照组推迟了4 d,即在授粉后的第35天。从表型观察,氯吡脲50倍、100倍和200倍稀释液处理火龙果果实体积均大于对照组处理,并且果皮与鳞片呈现出光泽艳丽,鳞片挺拔翠绿的效果。特别是氯吡脲100倍处理外观表型最佳,其次是氯吡脲200倍处理(图4)。表1结果表明,氯吡脲50倍、100倍和200倍稀释液处理后果实鳞片绿色占比显著高于对照组,分别提高了26.47%,24.01%和25.86%;果实质量显著高于对照组,分别提高了88.86、96.80、68.16 g。

图 4 不同质量浓度氯吡脲处理的火龙果果实及鳞片表型
Figure 4. Phenotypic effects of different concentrations of CPPU on pitaya fruit and fruit scales
表 1 不同质量浓度氯吡脲处理对火龙果鳞片颜色与果实质量的影响
Table 1. Effects of different concentrations of CPPU on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weight/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54b 367.27±58.69c 授粉后31 d
31 days after pollination氯吡脲50倍稀释液
500 times dilution of CPPU74.87±8.65a 456.13±46.19ab 授粉后35 d
35 days after pollination氯吡脲100倍稀释液
100 times dilution of CPPU72.41±5.97a 464.06±50.62a 授粉后35 d
35 days after pollination氯吡脲200倍稀释液
200 times dilution of CPPU74.26±7.38a 435.42±45.77b 授粉后35 d
35 days after pollination注:不同小写字母表示差异显著(P<0.05),CK为自然状态下火龙果果实数据,下同。 Note: Different lowercase letters indicate significant differences(P < 0.05); CK stands for the data of pitaya fruits in natural growth, similarly hereinafter. -
S-诱抗素处理果实成熟时间与对照组果实成熟时间相同。表2结果表明,S-诱抗素250倍、
1000 倍稀释液处理后果实鳞片绿色占比显著高于对照组果实鳞片绿色占比,较对照组分别上升了7.98%、13.25%,S-诱抗素500倍稀释液果实质量显著高于对照组,较对照组显著增加了28.26 g。表 2 不同质量浓度S-诱抗素处理对火龙果鳞片颜色与果实质量的影响
Table 2. Effects of different concentrations of S-ABA on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weight/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54b 367.27±58.69b 授粉后31 d
31 days after pollinationS-诱抗素250倍稀释液
250 times dilution of S-ABA56.38±14.04a 363.97±59.48b 授粉后31 d
31 days after pollinationS-诱抗素500倍稀释液
500 times dilution of S-ABA44.59±23.57b 395.53±36.79a 授粉后31 d
31 days after pollinationS-诱抗素1 000倍稀释液
1 000 times dilution of S-ABA61.65±6.65a 359.99±56.29b 授粉后31 d
31 days after pollination -
苄氨基嘌呤处理火龙果果实成熟时间与对照组果实成熟时间相同。表3结果表明,苄氨基嘌呤250倍稀释液处理后果实鳞片绿色占比显著高于对照组果实鳞片绿色占比,较对照组上升了9.09%,该处理果实质量与对照组无显著差异。
表 3 不同质量浓度苄氨基嘌呤处理对火龙果鳞片颜色与果实质量的影响
Table 3. Effects of different concentrations of 6-BA on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weight/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54b 367.27±58.69a 授粉后31 d
31 days after pollination苄氨基嘌呤250倍稀释液
250 times dilution of 6-BA57.49±11.55a 393.04±42.43a 授粉后31 d
31 days after pollination苄氨基嘌呤500倍稀释液
500 times dilution of 6-BA54.80±9.10ab 371.57±52.31a 授粉后31 d
31 days after pollination苄氨基嘌呤 1000 倍稀释液
1 000 times dilution of 6-BA52.10±20.90ab 380.33±51.64a 授粉后31 d
31 days after pollination -
赤霉酸处理果实成熟时间较对照组成熟时间推迟4 d。图3结果表明:外观上赤霉酸500倍、1 000倍、2 000倍处理火龙果果实体积大于对照组处理,果皮与鳞片相对于对照组更加光泽艳丽,鳞片挺拔翠绿,赤霉酸
1000 倍处理外观表型最佳,赤霉酸500倍、2000倍处理次之(图5)。表4结果表明,赤霉酸500倍、1000 倍、2 000倍稀释液处理后果实鳞片占比显著高于对照组果实鳞片绿色占比,较对照组上升了19.05%、23.54%、21.55%;果实质量显著高于对照组果实质量,较对照组增加了131.05、105.08、116.9 g。
图 5 不同浓度赤霉酸处理的火龙果果实及鳞片表型
Figure 5. Phenotypic effects of different concentrations of GA3 on pitaya fruit and fruit scales
表 4 不同质量浓度赤霉酸处理对火龙果鳞片颜色与果实质量的影响
Table 4. Effects of different concentrations of GA3 on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weight/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54c 367.27±58.69b 授粉后31 d
31 days after pollination赤霉酸500倍稀释液
500 times dilution of GA367.45±5.81b 498.32±68.01a 授粉后35 d
35 days after pollination赤霉酸1 000倍稀释液
1 000 times dilution of GA371.94±8.21a 472.34±62.12a 授粉后35 d
35 days after pollination赤霉酸2 000倍稀释液
2 000 times dilution of GA369.95±8.38ab 484.17±63.41a 授粉后35 d
35 days after pollination -
根据试验结果,芸苔素内酯处理的火龙果果实成熟时间与对照组相同,即在授粉后的第35天。表5结果表明,芸苔素内酯500倍、1 000倍稀释液处理后果实鳞片绿色占比显著高于对照组,较对照组提高了6.45%、7.52%,质量与对照组无显著差异。
表 5 不同质量浓度芸苔素内酯处理对火龙果鳞片颜色与果实质量的影响
Table 5. Effects of different concentrations of BR on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weight/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54b 367.27±58.69ab 授粉后31 d
31 days after pollination芸苔素内酯500倍稀释液
500 times dilution of BR54.85±6.33a 352.96±49.81b 授粉后31 d
31 days after pollination芸苔素内酯1 000倍稀释液
1 000 times dilution of BR55.92±8.14a 387.11±51.74a 授粉后31 d
31 days after pollination芸苔素内酯2000倍稀释液
2 000 times dilution of BR51.24±15.34ab 361.52±39.92ab 授粉后31 d
31 days after pollination -
根据试验结果,复硝酚钠处理的火龙果果实成熟时间与对照组相同,即在授粉后的第35天。表6结果表明,复硝酚钠1 000倍、2 000倍和4 000倍稀释液处理后果实鳞片绿色占比显著高于对照组,分别提高了9.53%,9.8%和10.94%;果实质量与对照组无显著差异。
表 6 不同质量浓度复硝酚钠处理对火龙果鳞片颜色与果实质量的影响
Table 6. Effects of different concentrations of CSN on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weight/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54b 367.27±58.69a 授粉后31 d
31 days after pollination复硝酚钠1 000倍稀释液
1 000 times dilution of CSN57.93±8.48a 373.85±43.00a 授粉后31 d
31 days after pollination复硝酚钠2 000倍稀释液
2 000 times dilution of CSN58.20±8.25a 359.49±64.38a 授粉后31 d
31 days after pollination复硝酚钠4 000倍稀释液
4 000 times dilution of CSN59.34±10.42a 362.10±55.74a 授粉后31 d
31 days after pollination -
根据试验结果,胺鲜酯处理的火龙果果实成熟时间与对照组相同,即在授粉后的第35天。表7结果表明,胺鲜酯1 000倍、2 000倍和4 000倍稀释液处理后果实鳞片绿色占比显著高于对照组,分别提高了8.54%,10.48%和8.47%;果实质量与对照组无显著差异。
表 7 不同质量浓度胺鲜酯处理对火龙果鳞片颜色与果实质量的影响
Table 7. Effects of different concentrations of DA-6 on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weighy/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54b 367.27±58.69a 授粉后31 d
31 days after pollination胺鲜酯1 000倍稀释液
1 000 times dilution of DA-656.94±7.30a 365.40±52.35a 授粉后31 d
31 days after pollination胺鲜酯2 000倍稀释液
2 000 times dilution of DA-658.88±7.84a 368.90±58.58a 授粉后31 d
31 days after pollination胺鲜酯4 000倍稀释液
4 000 times dilution of DA-656.87±9.37a 382.23±65.66a 授粉后31 d
31 days after pollination -
根据试验结果,萘乙酸处理的火龙果果实成熟时间相较于对照组推迟了4 d,即在授粉后的第35天。从表型观察,萘乙酸4 000倍、8 000倍和16 000倍稀释液处理火龙果果实体积均大于对照组处理,但果实基部有无法褪绿成熟的块状组织,其面积随萘乙酸浓度上升而增大(图6)。表8结果表明,萘乙酸4 000倍、8 000倍和16 000倍稀释液处理后果实鳞片占比均与对照组无显著差异;果实质量均显著高于对照组,分别增加了123.45、96.44、35.59 g。

图 6 不同质量浓度萘乙酸处理的火龙果果实及鳞片表型
Figure 6. Phenotypic effects of different concentrations of NAA on pitaya fruit and fruit scales
表 8 不同质量浓度萘乙酸处理对火龙果鳞片颜色与果实质量的影响
Table 8. Effects of different concentrations of NAA on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weight/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54a 367.27±58.69c 授粉后31 d
31 days after pollination萘乙酸4 000倍稀释液
4 000 times dilution of NAA46.01±22.17a 490.71±99.49a 授粉后35 d
35 days after pollination萘乙酸8 000倍稀释液
8 000 times dilution of NAA43.54±24.34a 463.71±49.64a 授粉后35 d
35 days after pollination萘乙酸16 000倍稀释液
16 000 times dilution of NAA52.86±17.81a 402.86±69.80b 授粉后35 d
35 days after pollination -
根据试验结果,乙烯利处理的火龙果果实成熟时间相较于对照组提前了1 d,即在授粉后的第30天。表9结果表明,乙烯利250倍、500倍和1 000倍稀释液处理后果实鳞片绿色占比均为0,显著低于对照组鳞片绿色占比;乙烯利250倍稀释液处理后果实质量显著高于对照组,较对照组增加了55.18 g。
表 9 不同质量浓度乙烯利处理对火龙果鳞片颜色与果实质量的影响
Table 9. Effects of different concentrations of ETH on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weight/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54a 367.27±58.69b 授粉后31 d
31 days after pollination乙烯利250倍稀释液
250 times dilution of ETH0±0b 422.45±74.75a 授粉后30 d
30 days after pollination乙烯利500倍稀释液
500 times dilution of ETH0±0b 391.48±70.45ab 授粉后30 d
30 days after pollination乙烯利1 000倍稀释液
1 000 times dilution of ETH0±0b 361.90±61.33b 授粉后30 d
30 days after pollination -
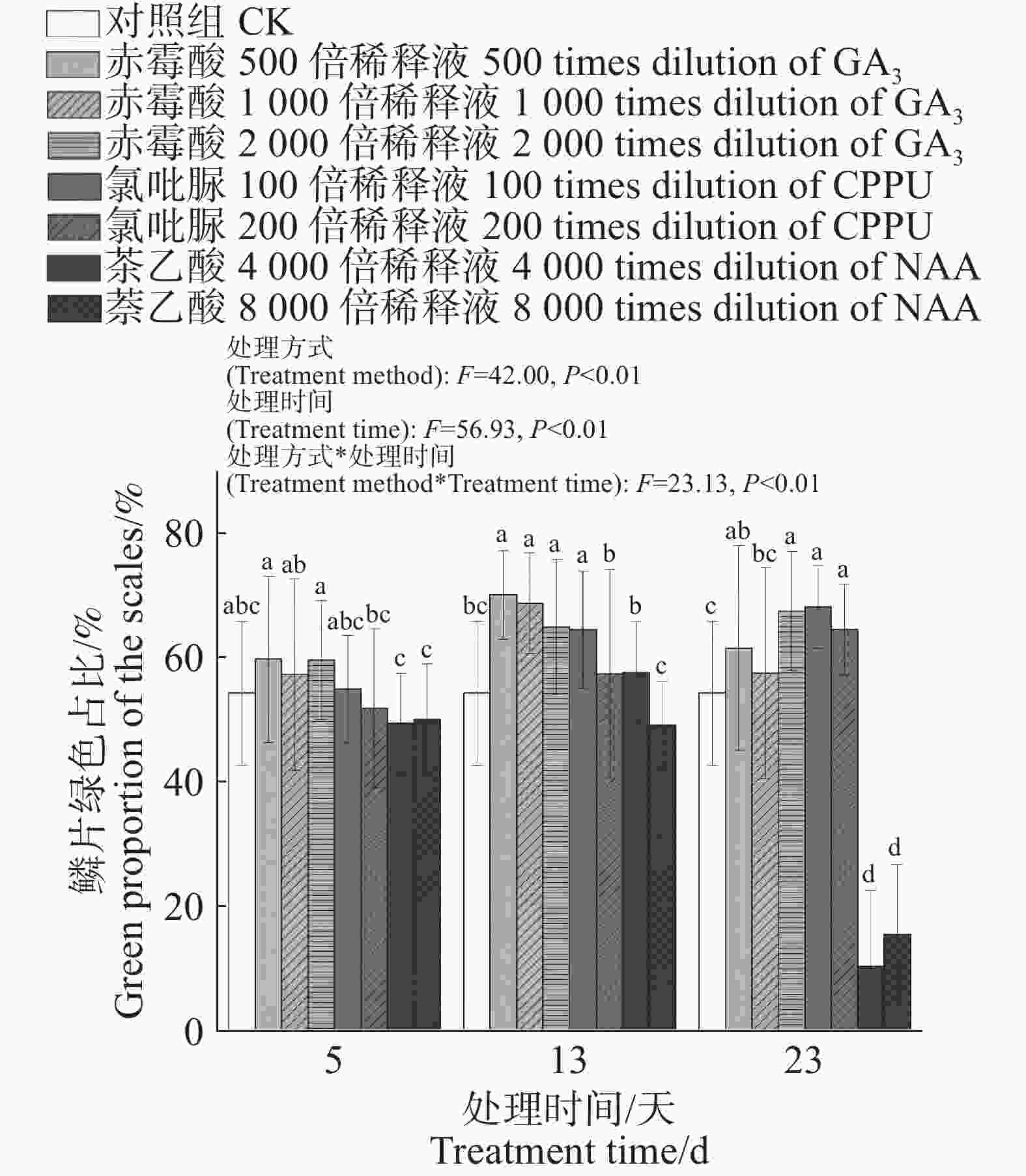
试验结果表明,授粉后第5天喷施植物生长调节剂后果实成熟时间较对照组推迟1 d,即授粉后第31天;授粉后第13天、授粉后第23天喷施植物生长调节剂后果实成熟时间较对照组推迟2 d,即授粉后第32天。图7结果表明,施加赤霉酸、萘乙酸,氯吡脲后对火龙果果实鳞片绿色占比有显著作用。双因素方差结果表明,植物生长调节剂喷施的时间与种类对火龙果果实鳞片绿色占比具有显著影响(P<0.01),此外喷施时间与植物生长调节剂的种类存在相互作用(P<0.01)。在授粉第5天对火龙果进行3种植物生长调节剂喷施并不能显著提高鳞片绿色占比;授粉第13天与授粉第23天对火龙果进行3种植物生长调节剂的处理,存在显著促进鳞片保绿的现象,其中,与对照处理相比,授粉后13 d喷施赤霉酸500倍稀释液、赤霉酸1 000倍稀释液、赤霉酸2 000倍稀释液和氯吡脲100倍稀释液均可显著增加鳞片绿色占比,分别提高了15.81%、14.48%、10.64%和10.19%,其中赤霉酸500倍效果最佳,鳞片绿色占比达70.2%;授粉后23 d喷施赤霉酸500倍、赤霉酸2 000倍、氯吡脲100倍和氯吡脲200倍稀释液均可显著增加鳞片绿色占比,分别提高了7.22%、13.21%、13.87%和10.21%,其中氯吡脲100倍效果最佳,鳞片绿色占比达68.26%。
-
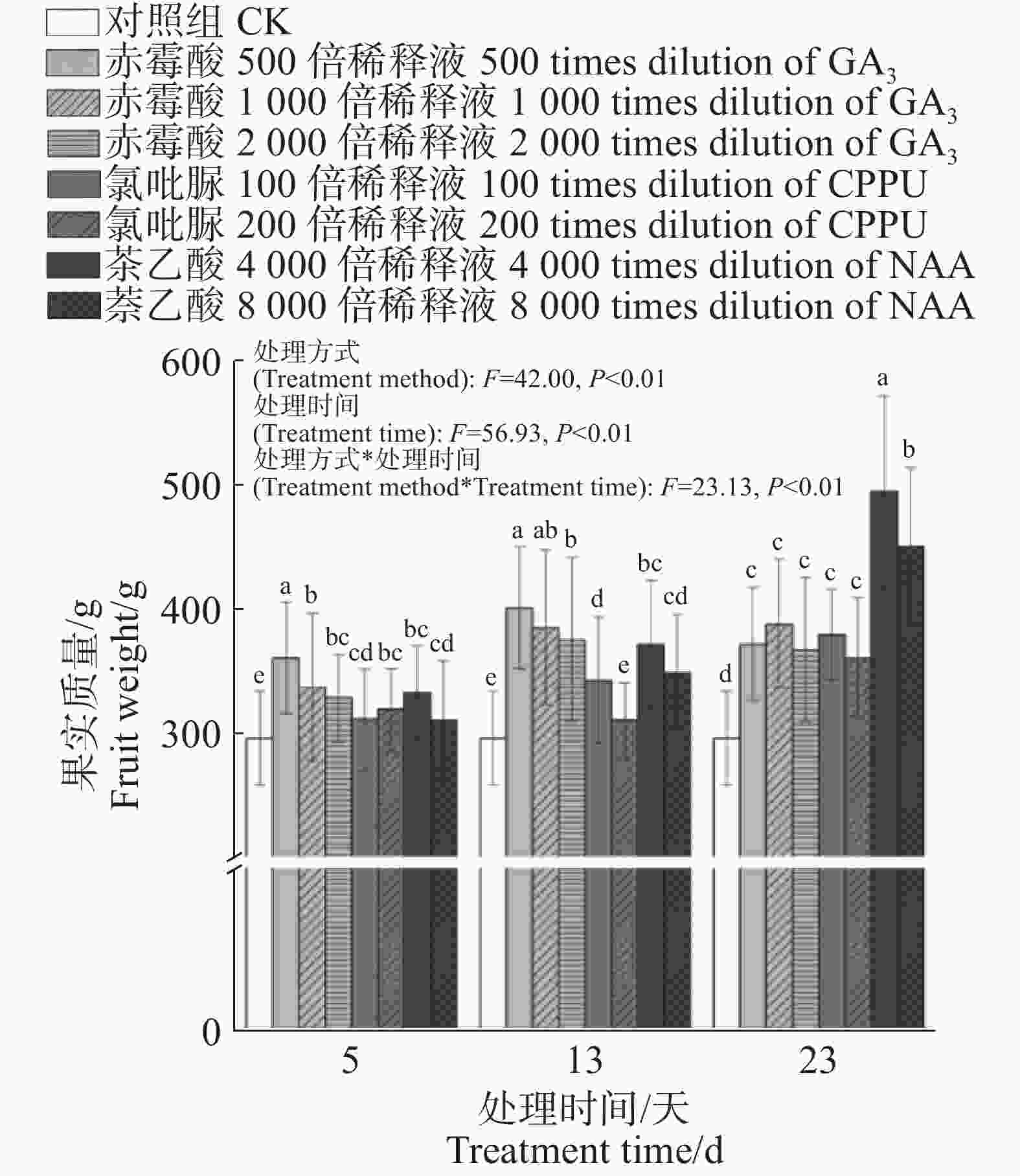
图8结果表明,施加赤霉酸、萘乙酸,氯吡脲后对火龙果果实质量有显著作用。双因素方差结果表明,植物生长调节剂喷施的时间与种类对火龙果果实质量具有显著影响(P<0.01),此外,喷施时间与植物生长调节剂的种类存在相互作用(P<0.01)。授粉第5天对火龙果进行3种植物生长调节剂不同浓度的喷施均能显著提高火龙果果实质量,其中,赤霉酸500倍稀释液处理后果实质量最高,为360.74 g,相较于对照组增加了65.64 g;授粉后第13天除氯吡脲2 000倍稀释液处理外其他处理均能显著增加果实质量,其中,赤霉酸500倍稀释液处理后果实质量最高,为401.33 g,相较于对照组增加了106.23 g;授粉后第23天对火龙果进行3种植物生长调节剂不同浓度的喷施,均能显著提高火龙果果实质量,其中萘乙酸4 000倍稀释液处理后果实质量达到最大值,为495.1 g,相较于对照组增加了200 g。
-
本研究选取9种植物生长调节剂,通过初筛与细筛试验系统筛选了促进火龙果鳞片保绿与果实增重的植物生长调剂种类及质量浓度。结果表明,合适的植物生长调节剂对火龙果鳞片保绿与果实增重有显著促进作用。
植物生长调节剂对火龙果鳞片保绿的促进作用。胺鲜酯、复硝酚钠、赤霉酸与氯吡脲均可显著促进火龙果鳞片保绿,其中氯吡脲与赤霉酸保绿效果最好。氯吡脲属于细胞分裂素类的植物生长调节剂[15]。因对叶绿素合成、细胞分裂具有促进作用,氯吡脲在农业中常被运用于延缓衰老与打破休眠等[16]。关于氯吡脲对于火龙果鳞片颜色的研究未有任何报道,但有大量试验证明氯吡脲可以延缓果皮褪绿转色,如朱敏等[17]指出5~100 mg·L−1的氯吡脲可以缓解杧果果皮中叶绿素的降解。Wei等[18]利用4 mg·L−1的氯吡脲喷施荔枝(Litchi chinensis)后发现果皮内花色苷合成显著推迟,果皮转色得到延缓。本试验结果表明,授粉后第13天与第23天喷施氯吡脲50~200倍稀释液可显著促进鳞片保绿,与上述试验结果一致。相关研究表明赤霉酸不仅能够抑制叶绿素的降解,还能抑制植物体衰老基因的表达[19]。Lewis等[20]研究发现,赤霉酸能够延缓脐橙果皮中叶绿素的分解。李文阳等[21]指出赤霉酸可以延缓葡萄果皮褪绿。在本研究中,授粉后第13天与第23天喷施赤霉酸500~2 000倍稀释液能够显著促进火龙果鳞片保绿,与上述试验结论一致。此外,邓会栋等[22]指出经50 mg·L−1赤霉酸处理后的绿橙(Citrus aurantium)果皮中的叶绿素含量降低。朱敏等[17]也提出,250、500 mg·L−1的高质量浓度赤霉酸溶液会促进果皮中类胡萝卜素与花青素的合成,使果皮褪绿变色。因此,低质量浓度的赤霉酸可以缓解果皮褪绿,高质量浓度则作用相反。
植物生长调节剂对火龙果果实增重的促进作用。赤霉酸、氯吡脲、S-诱抗素与芸苔素内酯均能促进火龙果果实增重,其中氯吡脲与赤霉酸增重效果最好(氯吡脲又称膨大剂,常被用于诱导果实增重[23])。伍梦婷等[24]使用氯吡脲溶液对猕猴桃(Actinidia chinensis)浸果后,果实质量较对照组显著上升了43.42 g。Retamales等[25]也通过试验发现氯吡脲可以显著提高蓝莓(Vaccinium uliginosum)质量。本试验结果表明,授粉后第13天与第23天喷施氯吡脲50~200倍稀释液可显著促进果实增重,与上述结论一致。赤霉酸能够促进细胞分裂增长,常被用于促进农作物果实膨大[26]。陈达庆等[27]利用50 mg·L−1赤霉酸对火龙果进行2次喷施后发现,火龙果平均较对照组上升了61.7 g,显著提高了单果质量。除对火龙果果实增重有显著促进作用以外,赤霉酸对黄瓜(Cucumis sativus)、葡萄(Vitis vinifera)等作物的果实增大均有显著促进作用[28 − 29],本试验结果表明,授粉后第13天与第23天喷施赤霉酸500~2 000倍稀释液可以显著促进果实增重,与上述试验结论一致。
本试验结果表明:1)在授粉后第13天与第23天喷施氯吡脲50倍、200倍、100倍稀释液鳞片保绿效果最好;2)在授粉后第13天喷施赤霉酸500倍稀释液,在授粉后第13天与第23天喷施赤霉酸500倍、2 000倍稀释液果实增重效果最好;3)若考虑成本问题,只在授粉后第13天喷施赤霉酸500倍稀释液可同时促进鳞片保绿与果实增重,还能降低人工费用,满足大田生产所需。
火龙果果实鳞片保绿和果实增重的植物生长调节剂筛选
DOI: 10.15886/j.cnki.rdswxb.20230135
 CSTR: 32425.14.j.cnki.rdswxb.20230135
CSTR: 32425.14.j.cnki.rdswxb.20230135
Screening of plant growth regulators for green-retaining of pitaya fruit scales and fruit-weight improvement
-
摘要: 通过田间初筛与复筛试验,研究氯吡脲,S-诱抗素、苄氨基嘌呤、乙烯利、赤霉酸、芸苔素内酯、胺鲜酯、复硝酚钠、萘乙酸9种植物生长调节剂对火龙果(Pitaya)果实鳞片保绿和果实增重的作用。研究结果表明,合理的植物生长调节剂可以促进火龙果鳞片保绿与果实增重。促进鳞片保绿效果最好的处理依次为,授粉后第13天与第23天喷施氯吡脲50倍、200倍、100倍稀释液,鳞片绿色占比为74.84%、74.26%与72.41%,上升比例为对照组的0.55、0.53与0.5倍;促进果实增重效果最好的处理依次为,授粉后第13天喷施赤霉酸500倍稀释液,授粉后第13天与第23天喷施赤霉酸500倍、2 000倍稀释液,果实质量分别为411.32、498.32、484.17 g,增重为对照组的0.39、0.32、0.31倍;考虑到实际生产中人工成本问题,仅对火龙果进行1次植物生长调节剂处理。研究结果表明,于火龙果授粉后第13天喷施赤霉酸500倍稀释液效果最好,喷施后鳞片绿色占比为70.2%,较对照组显著上升了15.8%,果实平均质量为411.3 g,与对照组相比增加了116.2 g,满足大田生产需求。Abstract: Through field preliminary screening and re-screening experiments, pitaya was treated by spraying after pollination with nine plant growth regulators, including chlorpropham (CPPU), trans-abscisic acid (S-ABA), 6-benzylaminopurine (6-BA), ethephon (ETH), gibberellic acid (GA3), brassinolide (BR), diethyl aminoethyl hexanoate (DA-6), compound sodium nitrophenolate (CSN), and 1-naphthaleneacetic acid (NAA), to observe the effect of the growth regulators on scales green-retaining and fruit weight improvement of pitaya. The results indicate that appropriate plant growth regulators can promote scales green-retaining and fruit weight improvement in pitaya fruits. Treatments with CPPU diluted at 50 times, 200 times, and 100 times on the 13th and 23rd days after pollination were best in retention of green scales, and their green scale ratios were 74.84%, 74.26%, and 72.41%, respectively, with an increase ratio of 0.55, 0.53, and 0.5 times compared to the control group. The most effective treatments for promoting fruit weight were those of spraying GA3 at a dilution of 500 times on the 13th day after pollination, and spraying GA3 at dilutions of 500 times and 2000 times on the 13th and 23rd days after pollination, and their fruit weights were 411.32 g, 498.32 g, and 484.17 g, respectively, with an increase in weight ratio of 0.39, 0.32, and 0.31 times compared to the control group. The labor cost was considered in actual production in this experiment, and pitaya was thus sprayed with the plant growth regulators for only one round. The results showed that the treatment with GA3 diluted 500-folds on the 13th day after pollination was the best among the treatments in green retention of scales and fruit weight gain. Under this treatment the proportion of green parts of scales was 70.2%, showing a significant increase of 15.8% compared to the control group, and the average fruit weight was 411.3 g, significantly higher by 116.2 g compared to the control group, meeting the requirements for field production.
-
Key words:
- pitaya /
- plant growth regulator /
- fruit scale color /
- fruit weight
-
图 7 不同处理对火龙果鳞片绿色占比的影响
处理时间为授粉后的天数;不同小写字母表示差异显著(P<0.05),CK为自然状态下火龙果果实数据,下同。
Fig. 7 The impact of different treatments on green proportion of pitaya fruit scales
Treatment time indicate days after polination; Different lowercase letters indicate significant differences (P < 0.05); CK stands for the data of pitaya fruits in natural growth, similarly hereinafter.
表 1 不同质量浓度氯吡脲处理对火龙果鳞片颜色与果实质量的影响
Table 1 Effects of different concentrations of CPPU on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weight/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54b 367.27±58.69c 授粉后31 d
31 days after pollination氯吡脲50倍稀释液
500 times dilution of CPPU74.87±8.65a 456.13±46.19ab 授粉后35 d
35 days after pollination氯吡脲100倍稀释液
100 times dilution of CPPU72.41±5.97a 464.06±50.62a 授粉后35 d
35 days after pollination氯吡脲200倍稀释液
200 times dilution of CPPU74.26±7.38a 435.42±45.77b 授粉后35 d
35 days after pollination注:不同小写字母表示差异显著(P<0.05),CK为自然状态下火龙果果实数据,下同。 Note: Different lowercase letters indicate significant differences(P < 0.05); CK stands for the data of pitaya fruits in natural growth, similarly hereinafter. 表 2 不同质量浓度S-诱抗素处理对火龙果鳞片颜色与果实质量的影响
Table 2 Effects of different concentrations of S-ABA on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weight/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54b 367.27±58.69b 授粉后31 d
31 days after pollinationS-诱抗素250倍稀释液
250 times dilution of S-ABA56.38±14.04a 363.97±59.48b 授粉后31 d
31 days after pollinationS-诱抗素500倍稀释液
500 times dilution of S-ABA44.59±23.57b 395.53±36.79a 授粉后31 d
31 days after pollinationS-诱抗素1 000倍稀释液
1 000 times dilution of S-ABA61.65±6.65a 359.99±56.29b 授粉后31 d
31 days after pollination表 3 不同质量浓度苄氨基嘌呤处理对火龙果鳞片颜色与果实质量的影响
Table 3 Effects of different concentrations of 6-BA on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weight/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54b 367.27±58.69a 授粉后31 d
31 days after pollination苄氨基嘌呤250倍稀释液
250 times dilution of 6-BA57.49±11.55a 393.04±42.43a 授粉后31 d
31 days after pollination苄氨基嘌呤500倍稀释液
500 times dilution of 6-BA54.80±9.10ab 371.57±52.31a 授粉后31 d
31 days after pollination苄氨基嘌呤 1000 倍稀释液
1 000 times dilution of 6-BA52.10±20.90ab 380.33±51.64a 授粉后31 d
31 days after pollination表 4 不同质量浓度赤霉酸处理对火龙果鳞片颜色与果实质量的影响
Table 4 Effects of different concentrations of GA3 on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weight/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54c 367.27±58.69b 授粉后31 d
31 days after pollination赤霉酸500倍稀释液
500 times dilution of GA367.45±5.81b 498.32±68.01a 授粉后35 d
35 days after pollination赤霉酸1 000倍稀释液
1 000 times dilution of GA371.94±8.21a 472.34±62.12a 授粉后35 d
35 days after pollination赤霉酸2 000倍稀释液
2 000 times dilution of GA369.95±8.38ab 484.17±63.41a 授粉后35 d
35 days after pollination表 5 不同质量浓度芸苔素内酯处理对火龙果鳞片颜色与果实质量的影响
Table 5 Effects of different concentrations of BR on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weight/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54b 367.27±58.69ab 授粉后31 d
31 days after pollination芸苔素内酯500倍稀释液
500 times dilution of BR54.85±6.33a 352.96±49.81b 授粉后31 d
31 days after pollination芸苔素内酯1 000倍稀释液
1 000 times dilution of BR55.92±8.14a 387.11±51.74a 授粉后31 d
31 days after pollination芸苔素内酯2000倍稀释液
2 000 times dilution of BR51.24±15.34ab 361.52±39.92ab 授粉后31 d
31 days after pollination表 6 不同质量浓度复硝酚钠处理对火龙果鳞片颜色与果实质量的影响
Table 6 Effects of different concentrations of CSN on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weight/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54b 367.27±58.69a 授粉后31 d
31 days after pollination复硝酚钠1 000倍稀释液
1 000 times dilution of CSN57.93±8.48a 373.85±43.00a 授粉后31 d
31 days after pollination复硝酚钠2 000倍稀释液
2 000 times dilution of CSN58.20±8.25a 359.49±64.38a 授粉后31 d
31 days after pollination复硝酚钠4 000倍稀释液
4 000 times dilution of CSN59.34±10.42a 362.10±55.74a 授粉后31 d
31 days after pollination表 7 不同质量浓度胺鲜酯处理对火龙果鳞片颜色与果实质量的影响
Table 7 Effects of different concentrations of DA-6 on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weighy/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54b 367.27±58.69a 授粉后31 d
31 days after pollination胺鲜酯1 000倍稀释液
1 000 times dilution of DA-656.94±7.30a 365.40±52.35a 授粉后31 d
31 days after pollination胺鲜酯2 000倍稀释液
2 000 times dilution of DA-658.88±7.84a 368.90±58.58a 授粉后31 d
31 days after pollination胺鲜酯4 000倍稀释液
4 000 times dilution of DA-656.87±9.37a 382.23±65.66a 授粉后31 d
31 days after pollination表 8 不同质量浓度萘乙酸处理对火龙果鳞片颜色与果实质量的影响
Table 8 Effects of different concentrations of NAA on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weight/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54a 367.27±58.69c 授粉后31 d
31 days after pollination萘乙酸4 000倍稀释液
4 000 times dilution of NAA46.01±22.17a 490.71±99.49a 授粉后35 d
35 days after pollination萘乙酸8 000倍稀释液
8 000 times dilution of NAA43.54±24.34a 463.71±49.64a 授粉后35 d
35 days after pollination萘乙酸16 000倍稀释液
16 000 times dilution of NAA52.86±17.81a 402.86±69.80b 授粉后35 d
35 days after pollination表 9 不同质量浓度乙烯利处理对火龙果鳞片颜色与果实质量的影响
Table 9 Effects of different concentrations of ETH on pitaya fruit weight and fruit scale color
处理
Treatment鳞片绿色占比/%
Proportion of green part of scales/%果实质量/g
Fruit weight/g果实成熟时间
Fruit ripening time对照组
CK48.40±18.54a 367.27±58.69b 授粉后31 d
31 days after pollination乙烯利250倍稀释液
250 times dilution of ETH0±0b 422.45±74.75a 授粉后30 d
30 days after pollination乙烯利500倍稀释液
500 times dilution of ETH0±0b 391.48±70.45ab 授粉后30 d
30 days after pollination乙烯利1 000倍稀释液
1 000 times dilution of ETH0±0b 361.90±61.33b 授粉后30 d
30 days after pollination -
[1] 程玉, 徐敏, 熊睿, 等. 滴灌条件下氮肥用量对火龙果果实的影响[J]. 热带生物学报, 2020, 11(1): 25 − 30. doi: 10.15886/j.cnki.rdswxb.2020.01.005 [2] 赵玉山. 我国火龙果产量跃居全球第一[J]. 中国果业信息, 2023, 40(2): 52. [3] 靳艺林. 套袋对火龙果果实发育和品质的影响[D]. 广州: 华南农业大学, 2019. doi: 10.27152/d.cnki.ghanu.2019.000143. [4] 关锦毅, 郝再彬, 张达, 等. 叶绿素提取与检测及生物学功效的研究进展[J]. 东北农业大学学报, 2009, 40(12): 130 − 134. doi: 10.3969/j.issn.1005-9369.2009.12.029 [5] 方志红, 董宽虎. NaCl胁迫对碱蒿幼苗叶绿素和甜菜红素含量的影响[J]. 畜牧与饲料科学, 2010, 31(2): 76 − 77. doi: 10.16003/j.cnki.issn1672-5190.2010.02.014 [6] 王萍, 闫明哲. 红甜菜色素稳定性影响因素研究进展[J]. 食品与生物技术学报, 2021, 40(7): 19 − 29. doi: 10.3969/j.issn.1673-1689.2021.07.003 [7] 郑伟, 王彬, 蔡永强, 等. 不同火龙果品种及不同生长调节剂对扦插育苗的影响[J]. 贵州农业科学, 2010, 38(1): 146 − 148. doi: 10.3969/j.issn.1001-3601.2010.01.044 [8] 李青超, 赵秀梅, 王立达, 等. 丙酰芸苔素内酯施用浓度对水稻植株性状和产量的影响[J]. 安徽农业科学, 2023, 51(21): 145 − 147. doi: 10.3969/j.issn.0517-6611.2023.21.033 [9] 郑强卿, 陈奇凌, 王晶晶, 等. 基于枣品质提升的库源激素调控[J]. 贵州农业科学, 2019, 47(7): 105 − 109. doi: 10.3969/j.issn.1001-3601.2019.07.023 [10] 刘彧. 自然生境下不同表型盐地碱蓬色素积累及光合特性的研究[D]. 济南: 山东师范大学, 2006. [11] 邓全恩. 油茶花器官发育逆境响应机制及植物生长调节剂调控技术研究[D]. 长沙: 中南林业科技大学, 2020. doi: 10.27662/d.cnki.gznlc.2020.000525. [12] 余志雄, 袁亚芳, 谢倩, 等. 植物生长调节剂对火龙果坐果率和果实生长的影响[J]. 亚热带植物科学, 2013, 42(4): 305 − 308. doi: 10.3969/j.issn.1009-7791.2013.04.006 [13] 高荧. 农杆菌介导小麦幼胚愈伤组织转化体系的建立[D]. 泰安: 山东农业大学, 2022. doi: 10.27277/d.cnki.gsdnu.2022.001215. [14] 王奕文. 蜜宝火龙果的自发气调包装及配套技术研究[D]. 天津: 天津科技大学, 2017. [15] 苏晓兰, 童巧云, 张雪梅, 等. CPPU对设施栽培玫瑰香葡萄无核化及果实品质的影响[J]. 山西农业科学, 2023, 51(11): 1290 − 1298. doi: 10.3969/j.issn.1002-2481.2023.11.08 [16] 孙润荻. 外源物质处理对薄皮甜瓜果实品质形成及采后贮藏的影响[D]. 武汉: 华中农业大学, 2023. doi: 10.27158/d.cnki.ghznu.2023.001507. [17] 朱敏, 邓穗生, 麦贤家, 等. GA3和CPPU对海南贵妃杧产量和果实品质的影响[J]. 热带作物学报, 2014, 35(9): 1784 − 1790. doi: 10.3969/j.issn.1000-2561.2014.09.021 [18] WEI Y Z, HU F C, HU G B, et al. Differential expression of anthocyanin biosynthetic genes in relation to anthocyanin accumulation in the pericarp of Litchi chinensis sonn[J]. PLoS One, 2011, 6(4): e19455. doi: 10.1371/journal.pone.0019455 [19] ROSENVASSER S, MAYAK S, FRIEDMAN H. Increase in reactive oxygen species (ROS) and in senescence-associated gene transcript (SAG) levels during dark-induced senescence of Pelargonium cuttings, and the effect of gibberellic acid[J]. Plant Science, 2006, 170(4): 873 − 879. doi: 10.1016/j.plantsci.2005.12.010 [20] LEWIS L N, COGGINS C W, LABANAUSKAS C K, et al. Biochemical changes associated with natural and gibberellin a3 delayed senescence in the navel orange rind[J]. Plant and Cell Physiology, 1967, 8(1): 151 − 160. doi: 10.1093/oxfordjournals.pcp.a079237 [21] 李文杨, 尹娟, 岳建华. GA3处理对葡萄叶片叶绿素含量和果实品质的影响[J]. 江苏农业科学, 2019, 47(11): 194 − 197. doi: 10.15889/j.issn.1002-1302.2019.11.044 [22] 邓会栋, 郭利军, 范鸿雁, 等. 不同植物生长调节剂对琼中绿橙落果及果实品质的影响[J]. 广东农业科学, 2017, 44(11): 32 − 37. doi: 10.16768/j.issn.1004-874X.2017.11.006 [23] 王艳玲. 减量膨大剂搭配不同植物生长调节剂对红心猕猴桃品质及产量的影响[D]. 雅安: 四川农业大学, 2023. doi: 10.27345/d.cnki.gsnyu.2023.001198. [24] 伍梦婷, 钟文奇, 陶俊杰, 等. 氯吡脲(CPPU)浸果对“奉黄1号”猕猴桃品质的影响[J]. 中国南方果树, 2023, 52(4): 100 − 107. doi: 10.13938/j.issn.1007-1431.20220461 [25] RETAMALES J B, LOBOS G A, ROMERO S, et al. Repeated applications of CPPU on highbush blueberry cv. Duke increase yield and enhance fruit quality at harvest and during postharvest[J]. Chilean Journal of Agricultural Research, 2014, 74(2): 157 − 161. doi: 10.4067/S0718-58392014000200005 [26] 李涛. GA3和CPPU对‘京蜜’葡萄果实生长及品质的影响研究[D]. 银川: 宁夏大学, 2021. doi: 10.27257/d.cnki.gnxhc.2021.001321. [27] 陈达庆, 胡子有, 黄黎芳, 等. 外源赤霉酸(GA3)对火龙果果实商品性状构成因素及产量的影响[J]. 西南农业学报, 2013, 26(6): 2462 − 2465. doi: 10.16213/j.cnki.scjas.2013.06.077 [28] 杨栋. 黄瓜中赤霉酸残留研究[D]. 南宁: 广西大学, 2016. [29] 王玉林, 莫光友, 刘丽萍, 等. 3种植物生长调节剂对不同葡萄品种果实生长的影响[J]. 现代农业科技, 2021(3): 112 − 115. doi: 10.3969/j.issn.1007-5739.2021.03.045 -





 下载:
下载: