-
微塑料,指粒径或长度小于5 mm的塑料碎片或颗粒[1]。海洋环境中的塑料垃圾会降解成数百万个微塑料碎片,导致海洋环境中的微塑料数量成几何倍数增加[2]。1986年以来,由于人类活动、地表径流、海上活动等因素[3,4],大量塑料废弃物持续进入沿海生态系统。作为一类新污染物,海洋微塑料污染不仅被联合国环境规划署定为全球十大新兴环境问题之一[5],也被列入我国新污染物治理行动计划,是全球共同面对且亟待解决的重大环境挑战。
海草床是全球最具生产力的水生生态系统之一,具有重要的碳汇功能,其固定的碳被称为“蓝碳”,虽仅覆盖全球海洋面积的0.2%,但年碳封存量可达全球海洋碳封存总量的10%~15%[6],在应对气候变化和实现“双碳”目标方面具有重要战略意义。然而,由于拖网、疏浚、水产养殖和富营养化等人为活动的干扰使得全球海草床生态系统在过去四十年中减少了九成,成为了全球性危机之一[7]。近年来,微塑料被发现是海草床生态系统的另一种潜在威胁,海草床生态系统已被确定为微塑料的长期汇集地,微塑料通过海流输送、大气沉降和陆源径流等途径进入海草床生态系统,在海草叶片表面、水体和沉积物中被频繁检出[8-11]。长期滞留的微塑料可能改变沉积物的物理化学性质,扰乱微生物群落,进而影响生物地球化学循环过程[9]。
氮循环是沉积物生物地球化学过程中的重要组成部分[12,13],沉积物中的氮主要以有机氮和无机氮两种形式赋存,其中无机氮包括铵态氮(NH4+-N)、硝态氮(NO3−-N)—和亚硝态氮(NO2−-N)或铵盐(NH4+-N),是反映沉积物氮转化过程最为活跃的组分[14]。这些氮转化通常由微生物驱动,主要过程包括氮固定、有机氮降解与合成、硝化、反硝化等[15],调控着生态系统的营养盐动态、初级生产力和温室气体(N2O)的排放。沉积物微生物作为这些过程直接参与者和调控者,其丰度、活性和群落结构对环境扰动极为敏感。Seeley等人研究表明添加聚乳酸(polylactic acid,PLA)和聚氨酯泡沫(polyurethane foam,PUF)微塑料促进沿海盐沼沉积物的硝化和反硝化反应,而聚氯乙烯(polyvinyl chloride,PVC)抑制这两个过程[16]。Fortin等人研究表明,PE、PLA和PVC微塑料的添加促进了生物膜中narG、nirS/K、nosZ等反硝化基因,驱动沉积物反硝化过程[17]。Wang等人研究同样表明微塑料显著增强了海水沉积物的反硝化作用(narG、nirS、nosZ上调、NO3−浓度降低,N2O释放增加)[18]。另一项研究表明,老化PLA显著促进淡水沉积物反硝化,老化聚苯乙烯(Polystyrene,PS)显著促进异化硝酸盐还原为铵(DNRA),而功能基因(narG、nirS、nosZ、hzo、nrfA)的富集是关键机制[19]。海草床作为蓝碳系统的关键组成部分,是微生物驱动的生物地球化学循环的热点[20],微塑料的输入可能通过提供非天然碳源或改变孔隙水氧环境,重塑氮循环功能微生物群落结构[21],进而影响海草床的营养盐平衡乃至整个生态系统健康与稳定。因此,有必要理清微塑料对海草床沉积物氮循环关键过程及其微生物群落的影响机制,对评估微塑料海洋生态风险和保障海草床生态系统的服务功能具有迫切的现实意义。
据此,本研究在海南岛文昌市采集海草床沉积物,并进行为期112天的微宇宙培养实验,探究不可降解(PE)和可降解微塑料(PLA)对沉积物氮形态、功能基因丰度及微生物群落结构的影响规律,为合理评估微塑料对海草床生态系统关键生物地球化学过程的影响提供理论依据。
-
本研究采用PE和PLA作为不可降解和可降解微塑料代表,从北京安科莱尔科技(Anterail)Anterail科技有限公司采购商业化的微塑料颗粒(粒径20~30目,约0.85~0.60 mm),经超纯水反复清洗,以去除松散附着的颗粒,随后在超洁净工作台垂直气流下干燥,用于微宇宙暴露实验。
供试沉积物采自海南岛文昌市港东村附近典型海草床(
19.4725833 °N,110.8106111 °E),于退潮后采集表层(0~20 cm)沉积物样品,去除杂质后自然风干过筛(孔径2 mm),备用。 -
实验设计3个处理组,分别为CK(未添加微塑料)、1%PLA处理组和1%PE处理组。微塑料添加浓度为沉积物干重的1%(质量比),该浓度参考了已有的微塑料对沉积物生态功能影响的研究[22]。称取250 g沉积物样品加入500 mL玻璃烧杯中,在微塑料处理组中加入2.5 g微塑料,搅拌均匀,使微塑料与沉积物充分混合。对于每个微观世界,瓶中加入250 g的沉积物,实验设计包括两种微塑料(PLA和PE),正式培养开始前,添加人工海水在饱和状态下进行一周的驯化以重新激活沉积物中的微生物群落。一周后,培养试验正式开始,每天添加人工海水(将33.33 g海盐溶解于1 L去离子水中制备),以保持沉积物表面上方2 cm的水柱以模拟海草床沉积物的厌氧环境。每个处理组设置3个平行重复,于气候培养箱中(25±1)℃黑暗环境中静置培养112天。分别在培养第0天和第112天采集沉积物样品,用于氮形态(NH4+-N、NO3−-N)、微生物群落及宏基因组分析。
-
沉积物铵态氮(NH4+-N)和硝态氮(NO3--N)均按照制造商说明,使用商业测定试剂盒(苏州科铭生物技术有限公司)进行定量。使用紫外可见光度计(UV-
1800 )在625 nm下测定铵态氮、而在双波长220 nm和275 nm处进行硝态氮的测定。 -
根据E.Z.N.A.® Soil DNA提取试剂盒(Omega Bio-Tek, Norcross, GA, U.S.)说明书[9]进行微生物群落总基因组DNA抽提,使用1%的琼脂糖凝胶电泳检测抽提物的质量,使用NanoDropTM 2000分光光度计(Thermo Fisher Scientific, Waltham, MA, USA)测定DNA浓度和纯度。每个样本重复3次。将同一样本的聚合酶链式反应(polymerase chain reaction, PCR)产物混合后使用2%琼脂糖凝胶回收,利用AxyPrepTM DNA凝胶回收试剂盒(Corning Incorporated, Union City, CA, USA)进行回收产物纯化,使用NEXTFLEX® Rapid DNA-Seq建库试剂盒(Bioo Scientific/PerkinElmer, Austin, TX, USA)对纯化后的PCR产物进行建库,分别利用Illumina公司的MiSeq(PE 300)和NovaSeq(PE 250)平台进行测序(上海美吉生物医药科技有限公司)。
-
利用E.Z.N.A.® Soil DNA提取试剂盒进行样品DNA抽提。完成DNA抽提后,检测DNA浓度和纯度,利用1%琼脂糖凝胶电泳检测DNA完整性。通过Covaris M220聚焦超声波破碎仪(Covaris, Woburn, MA, USA)将DNA片段化,筛选约350bp的片段,使用NEXTFLEX®建库试剂盒用于构建PE文库。使用Illumina NovaSeq和HiSeq X Ten测序平台进行宏基因组测序(上海美吉生物医药科技有限公司)。将预测基因与KEGG数据进行比对注释,筛选氮循环相关功能基因进行分析。本研究关注的氮循环关键功能基因如表1所示:
表 1 氮循环功能注释
Table 1. Functional annotation of nitrogen cycle
通路 Pathway 功能注释 Functional annotation 基因 Gene 硝化作用 Nitrification Methane/ammonia monooxygenase subunit A /B amoA/amoB 反硝化作用 Denitrification Nitrite reductase(NO-forming) nirK/nirS 固氮作用 Nitrogen fixation Nitrogenase molybdenum-iron protein alpha chain nifD/nifK -
所有实验数据均以基于三次重复的平均值±标准差(SD)表示。使用软件Microsoft Excel 2019和SPSS v25.0进行数据分析,使用Origin 2021绘制图形。主要对海草床沉积物的氮循环理化性质、微生物群落组成和氮循环相关功能基因指标等响应变量进行了统计分析。分析前,使用Kolmogorov-Smirnov检验(K-S检验)评估数据的正态性,然后使用Levene检验进一步验证数据是否满足方差的同质性,以确保方差分析(ANOVA)应用的适当性。采用单因素方差分析和独立样本检验分析比较来评估实验处理间差异的显著性,P≤0.05的差异具有统计学意义。利用上海美吉生物医药科技有限公司的Majorbio云平台(www.majorbio.com)进行基于Bray-Curtis相异性矩阵的主坐标分析(PCoA)评估β多样性并可视化不同处理之间沉积物微生物群落组成的差异和Circos样本与物种关系图通常用于展示不同微生物样本中存在的物种的分布情况。使用Spearman秩相关(阈值:r>0.65,p<0.05)进行共生网络分析,并通过软件Gephi v0.10.1中的Fruchterman-Reingold布局进行可视化。
-
氮形态分析揭示了随着时间的推移,微塑料的存在显著影响海草床沉积物中氮循环过程(图1)。在第0天的时候,PLA处理组的NH4+-N浓度显著低于对照组和PE处理组(图1A)。截止到112天,所有处理组均呈现NH4+-N消耗超过90%,表明硝化作用已进行完全。与对照组相比,PLA和PE处理组导致NO3−-N显著抑制,第112天浓度分别下降89%和88%(图1-B),表明反硝化活性增强,这些结果可能反映了MP对功能基因的间接影响。
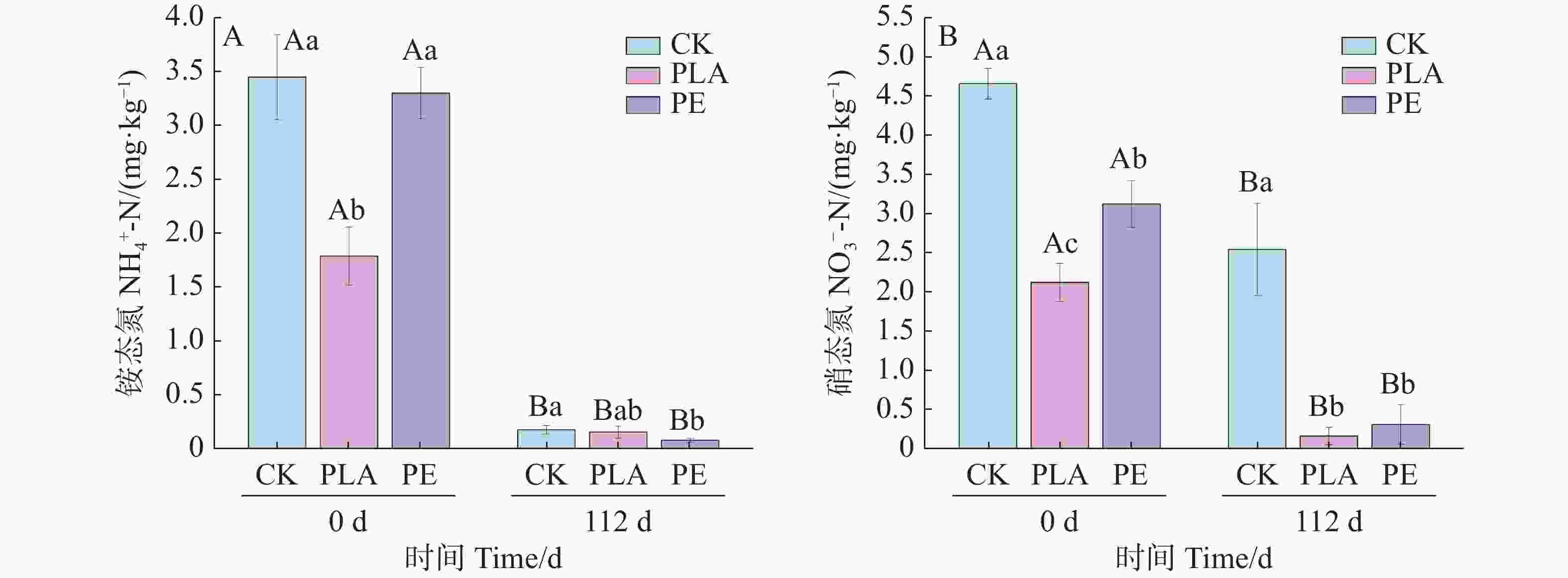
图 1 不同培养时间下暴露于不同微塑料类型时沉积物氮形态含量的变化趋势:NH4+-N(A),NO3−-N(B)。
Figure 1. Dynamics of sediment physicochemical properties exposed to different MP types at different incubation times: NH4+-N (A), NO3−-N (B).
随着时间的推移,与对照组相比,PLA和PE处理组的NH4+-N和NO3--N含量都较低,表明添加PLA和PE微塑料促进了氮循环中的硝化作用和反硝化作用,与前人的研究结果相一致[23]。产生这一现象的原因可能是微塑料的添加增加了沉积物的孔隙率并改变了氧通量,增加了硝化作用并降低了NH4+-N[24]。此外,已有研究提出,由于PLA的可生物降解的特性,可显著提高土壤溶解有机碳含量,改善土壤碳与氮比,并为微生物活动提供足够的碳源,加速土壤可用氮的流失[25]。而PE微塑料的添加增加了微生物对氮素的需求,促使它们从基质中获取氮,这可能增强对氨氮的吸收和转化[26]。
-
为阐明微塑料对氮循环的影响机制,通过宏基因测序评估了硝化(amoA和amoB)、反硝化(nirK和nirS)和固氮(nifD和nifK)相关基因的相对丰度变化。本研究表明,微塑料的存在会显著影响海草床沉积物氮循环功能基因的相对丰度(图2)。
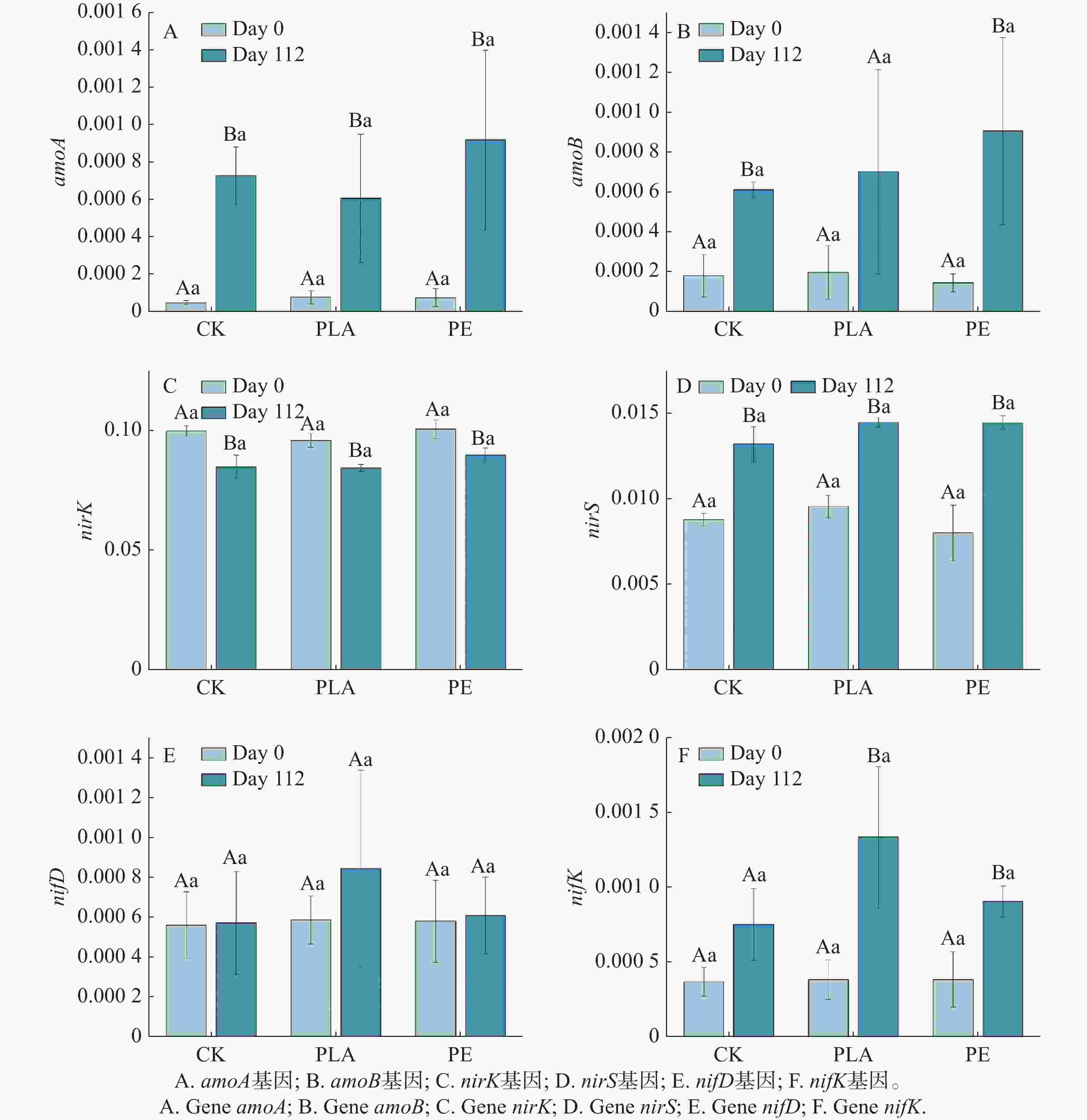
图 2 不同微塑料类型作用下沉积物中氮循环基因相对丰度的时间动态变化。
Figure 2. Temporal dynamics of nitrogen cycle genes in sediments under different MP types.
amoA和amoB基因是编码氨氧化酶的关键[27],氨氧化酶(ammonia monooxygenase,AMO)可以将氨氧化成羟胺,是硝化作用最经典的标志基因。微塑料对amoA和amoB基因的相对丰度影响如图2-A—B所示,随着培养时间的延长,所有处理组的amoA和amoB基因相对丰度均呈上升趋势,表明基因表达水平显著上调,硝化功能相关基因的富集效应明显。具体而言,在amoA基因层面,与对照组相比,培养至112天时,PLA处理组的amoA基因相对丰度显著低于对照组,而PE处理组则显著高于对照组,表明PE微塑料可促进amoA基因的上调表达,进而强化硝化作用进程。在amoB基因层面,微塑料处理组的基因相对丰度均高于对照组,表明微塑料对amoB基因的上调表达具有促进作用,且该促进效应可进一步推动硝化反应的进行。amoA和amoB基因常被作为硝化过程研究中的核心分子标志物,其编码的蛋白产物直接介导硝化速率调控的第一步反应[28]。本研究中,微塑料的添加显著促进了硝化作用,这一结果与amoB基因的表达特征高度契合,印证了amoB基因对氮循环中硝化过程的响应规律,即氨氧化细菌(AOB)在应对外部环境扰动时,较氨氧化古菌(AOA)展现出更高的硝化功能潜力[29]。硝化作用属于严格的好氧代谢过程,其高效进行依赖于充足的氧气供应[30],研究表明,较粗的晶粒尺寸加上碳酸盐沉积物中较高的沉积物孔隙率可以提高氧的渗透性[31],本研究中,微塑料的添加可能通过改变沉积物孔隙结构,显著提高了系统的氧气渗透性,为硝化微生物的代谢活动提供了有利的有氧环境,从而间接促进了硝化作用。
nirK和nirS基因编码亚硝酸盐还原酶,催化NO2−还原为NO,是反硝化区别于其他硝酸盐还原途径的关键步骤,被公认为反硝化标志基因[32],其对微塑料的响应特征如图2-C—D所示。在nirK基因方面,各处理组的基因相对丰度随培养时间延长呈逐渐下降趋势,整体表现为基因表达下调;与对照组相比,PLA处理组nirK基因相对丰度更低,而PE处理组则显著更高,表明PE微塑料可缓解nirK基因的下调趋势,促进其相对表达水平上调,进而增强反硝化作用,而PLA微塑料则对反硝化作用具有抑制效应。在nirS基因方面,各处理组的基因相对丰度随培养时间延长呈上升趋势,且PLA、PE微塑料处理组的基因相对丰度均高于对照组,表明两种微塑料均可促进nirS基因的上调表达,进而强化反硝化作用进程。上述结果表明,nirS基因的表达特征与微塑料介导下氮循环中反硝化过程的变化规律高度一致。Yu等人[33]的研究已证实,微塑料可显著提高氮循环相关功能基因(包括nirS和nirK)的丰度,本研究结果与之相符。在海洋沉积物环境中,微塑料处理后硝酸盐(NO3−-N)浓度的降低,间接证明了氮还原路径的增强。这一现象也支持了早期研究结论,即微塑料表面形成的生物膜可通过构建局部缺氧生态位,为反硝化细菌的生长代谢提供适宜环境,从而显著增强反硝化作用[34]。
nifD和nifK编码固氮酶钼铁蛋白α和β亚基,是固氮过程中的关键功能基因[32],其对微塑料的响应特征如图2E—F所示。结果显示,随着培养时间的延长,所有处理组nifD和nifK基因相对丰度均呈上升趋势,表明固氮功能相关基因表达水平上调,微塑料对固氮作用具有潜在促进效应。其中,在nifK基因层面,PLA和PE处理组均表现出显著上调特征,且基因相对丰度均高于对照组,且PLA处理组丰度显著高于PE处理组。上述结果表明,微塑料处理可显著上调nifD和nifK基因相对丰度,进而促进固氮作用;与传统PE微塑料相比,可生物降解PLA微塑料对沉积物中固氮作用的促进效果更为显著。Yin等人[35]同样发现,可生物降解微塑料能增加沉积微生物中固氮酶和固氮基因(如nifD、nifH和nifX)的丰度,这表明PLA在沉积物中的存在可能促使微生物表现出更高的固氮能力,与我们研究结果一致。
-
微生物是沉积物氮循环的主要驱动者,对环境的扰动极为敏感,微生物群落多样性越高,结构越复杂,更利于整体的稳定性,从而增强对外部干扰的抵抗能力[36]。在本研究中,随着培养时间的推移,所有处理组的Ace指数(图3-A)均呈上升趋势,这一结果表明微塑料的存在可显著促进沉积物中微生物的物种丰富度,使群落内微生物的物种数量增加。Shannon指数的变化特征(图3-A)则进一步揭示了群落多样性的差异:所有处理组Shannon指数均呈显著上升态势,表明群落的均匀度增加。培养至112天时,与对照组相比,PLA处理组Shannon指数更高,而PE处理组则低于对照组。综合来看,两类微塑料均能促进沉积物微生物的物种丰富度,但对群落多样性的调控效应存在明显差异:PLA可显著提升微生物群落多样性,而PE则表现出一定的抑制作用。微生物群落丰富度的提升,推测与微塑料可作为碳源被微生物降解利用,进而增强沉积物中微生物群落活性相关[37]。在培养第112天,PLA处理组的细菌群落丰富度与多样性高于PE处理组,这一差异可能源于两种微塑料的物理化学特性差异[38],PLA作为由乳酸单体聚合形成的生物基聚合物,易发生水解断裂及微生物风化降解,因而具有更高的碳利用效率;而PE为氯乙烯与乙烯单体聚合而成的线性烃类聚合物,其抗风化及抗降解能力更强,碳释放量较低,导致PE低于PLA[39]。
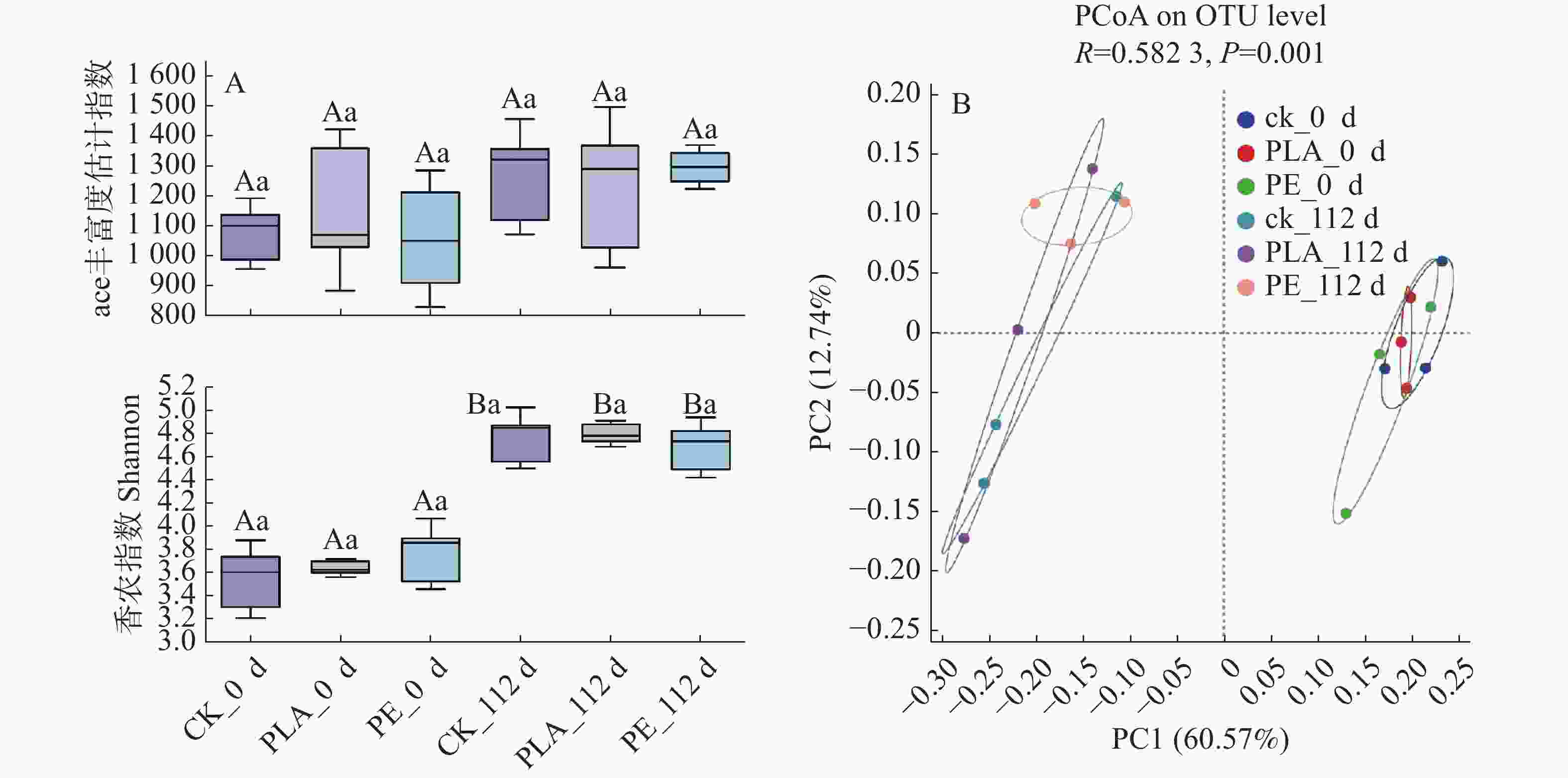
图 3 不同微塑料暴露下海草床沉积物微生物群落随时间的Alpha多样性(A)与主坐标分析(B)
Figure 3. Alpha diversity (A)and PCoA (B)analysis of microbial communities in seagrass bed sediments under different MP exposures over time
微生物群落β多样性通过PCoA进行评估(图2B),结果显示第一轴(PCoA1)为微生物群落组成差异的60.57%,第二轴(PCoA2)为12.74%,两轴累计解释度较高,能有效反映群落结构的变异特征。PCoA结果表明,培养时间的推移是驱动微塑料影响沉积物微生物群落演替的核心因素;同时,PLA、PE处理组与对照组(CK)的微生物群落存在明显聚类区分,进一步证实微塑料污染可显著改变沉积物细菌群落结构。
-
随培养时间延长,不同微塑料处理组下海草床沉积物微生物群落结构呈现出较高相似性。在门分类水平上(图4-A),变形菌门(Pseudomonadota,相对丰度29.19%~33.81%)、拟杆菌门(Bacteroidota,18.67%~38.18%)及原厚壁菌门(Bacillota,18.23%~23.76%)为优势微生物类群,累计相对丰度占所有样本沉积物微生物门类总序列的74.23%~90.45%,是构成海草床沉积物微生物群落的核心类群。结果显示,随着培养时间推移,变形菌门相对丰度呈上升趋势;培养至112天时,PLA处理组变形菌门相对丰度高于CK,而PE处理组则低于CK。这一现象表明,可降解微塑料PLA的添加对海草床沉积物中变形菌门的富集具有促进作用,且该门类在各处理组中变化幅度最小,是群落中占比主导且稳定性最强的类群。已有研究证实,部分变形菌可通过分泌胞外多糖及菌毛附着于微塑料表面[40],进而改变微塑料表面理化特性,为其降解过程创造有利条件;另有部分变形菌可合成特异性酶系统,将微塑料聚合物降解为小分子物质[41]。同时通过调控自身代谢途径以微塑料为碳源供能[42],这可能是PLA处理组变形菌门丰度增加的原因。本研究结果表明,PLA微塑料对沉积物细菌群落的多样性、物种组成及功能特征影响更为显著。其潜在机制可能在于,PLA作为乳酸单体聚合形成的可生物降解聚合物,更易发生水解断裂及微生物风化降解过程,具备更高的碳源利用率[43]。从而快速且显著地调控沉积物微生物群落结构及代谢活性[44],而传统不可降解微塑料(如PE)释放的有毒物质,也可能对微生物生理过程产生强烈干扰[45]。
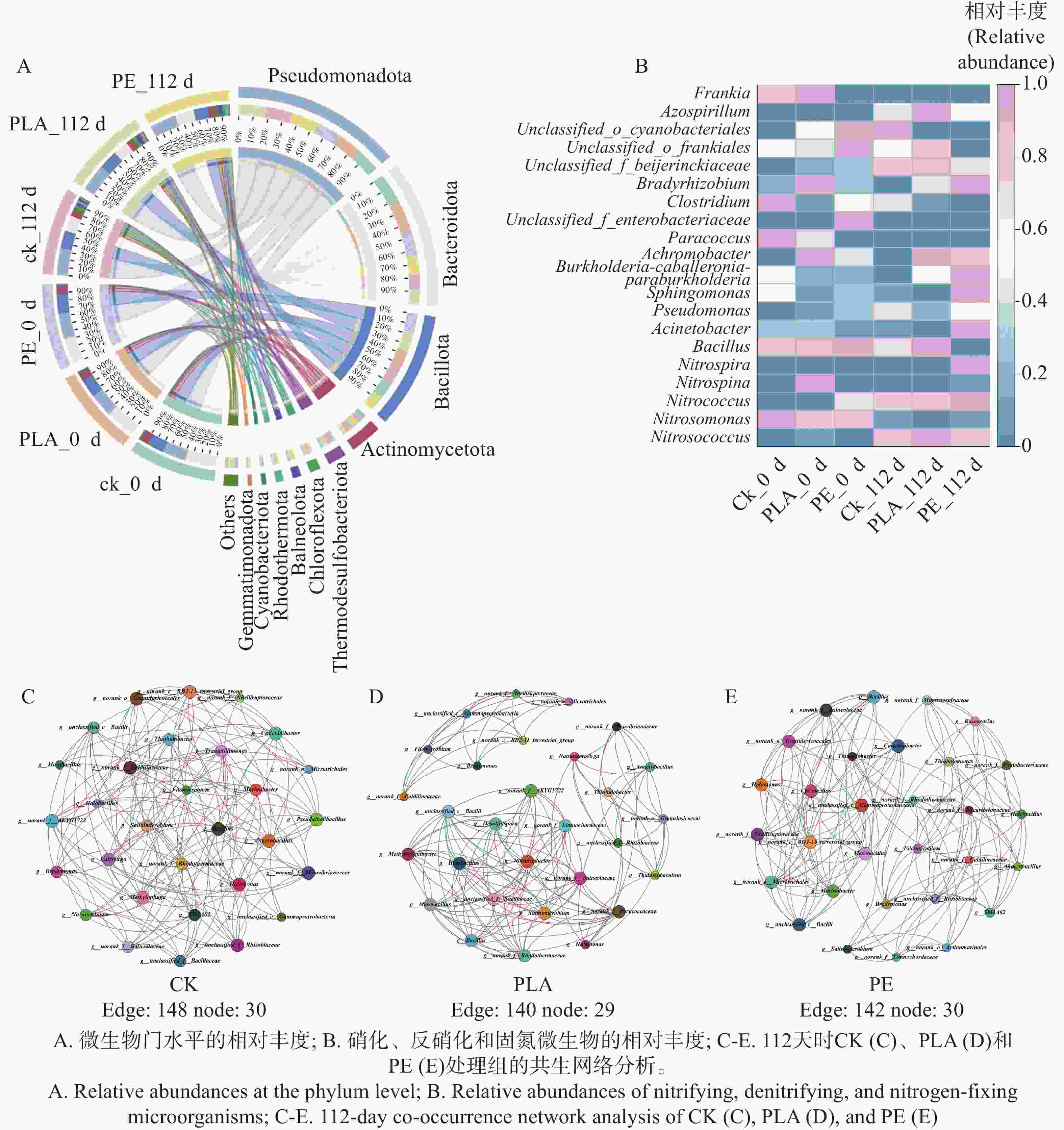
图 4 不同微塑料暴露条件下海草床沉积物微生物群落随时间变化情况
Figure 4. Changes in microbial communities in seagrass bed sediments under different microplastic (MP)exposure conditions over time
与之相反,拟杆菌门相对丰度在所有处理组中均呈显著下降趋势,其中对照组降幅最为明显(从38.2%降至19.7%),PE处理组降幅最小。已有研究指出,拟杆菌门类群对生态系统反硝化过程具有显著贡献[46],其丰度的普遍下降可能对海草床沉积物氮循环过程产生潜在影响。原厚壁菌门的变化特征则有所不同:除PE微塑料处理组外,其余各组中原厚壁菌门相对丰度均呈上升趋势,且PLA处理组表现出最高丰度,这可能与不同类型微塑料的理化特性差异密切相关。原厚壁菌门参与沉积物中有机物的降解与合成过程,同时在硝酸盐还原反应中发挥作用[47],表明该门类在海草床沉积物氮循环过程中具有广泛的功能参与性。
值得注意的是,氮循环相关功能微生物的响应不仅体现在门水平,在属水平的硝化功能菌中也表现出明显差异(图4-B),随着培养时间推移,所有处理组中参与硝化作用的硝化杆菌属(Nitrosococcus)相对丰度均呈显著上升趋势;培养至112天时,与对照组相比,PLA处理组中该菌属相对丰度更高,增幅达12.70%,而PE处理组则低于对照组。亚硝化单胞菌属(Nitrosomonas)的变化趋势与硝化杆菌属恰好相反,整体呈相对丰度下降态势,且除PLA处理组外,其余各组均表现出明显降幅;112天时,PE处理组亚硝化单胞菌属相对丰度高于对照组,而PLA处理组则低于对照组。与之形成呼应的是,硝化球菌属(Nitrococcus)相对丰度同样呈上升趋势,且各微塑料处理组丰度均高于对照组(图3-E),呈现出与硝化杆菌属一致的正向响应特征。典型硝化细菌(硝化杆菌属、硝化球菌属)在微塑料处理组中普遍呈现相对丰度提升的特征,这一结果证实了微塑料可通过为硝化细菌提供特定生态位,进而调控其群落结构[48]。
在反硝化过程中,不同反硝化功能微生物对微塑料的响应同样存在显著差异(图4-B)。其中,芽孢杆菌属(Bacillus)的相对丰度随时间呈现类型特异性变化:PLA处理组呈上升趋势,而对照组及PE处理组均呈下降趋势;培养至112天时,PLA处理组芽孢杆菌属相对丰度高于对照组,PE处理组则低于对照组,且PLA处理组该菌属丰度达到最高值。不动杆菌属(Acinetobacter)的时间动态响应更为复杂,培养初期(起始阶段),与对照组相比,PLA处理组该菌属相对丰度较高,PE处理组则较低;但随培养时间推进,这一趋势在112天时发生逆转,PE处理组不动杆菌属相对丰度升至最高,较对照组增幅达108.19%。假单胞菌属(Pseudomona)的响应特征则较为一致,112天时,各微塑料处理组该菌属相对丰度均低于对照组(图3-E)。已有研究表明,典型反硝化细菌可在PLA与PE微塑料处理组中实现富集[49],这类反硝化细菌在含PLA和PE微塑料的沉积物中显著富集,推测与其对微塑料的降解作用密切相关:PE微塑料对微生物的选择性筛选作用可能是关键原因,被富集的反硝化细菌或为潜在的PE微塑料降解菌[50],而PLA作为可生物降解微塑料,其降解过程也可能为反硝化细菌提供碳源或能量,进而促进其富集。
针对氮循环的固定关键环节,固氮微生物对微塑料的响应同样呈现明显的类群特异性及时空差异。培养至112天时,所有处理组中梭菌属(Clostridium)相对丰度均呈下降趋势,且均低于对照组,其中PLA微塑料处理组中该菌属的下降幅度最小,表现出一定的缓冲效应。慢生根瘤菌属(Bradyrhizobium)的响应特征则与之相反,微塑料处理组该菌属相对丰度均显著高于对照组,增幅介于2.5~5.15倍;其中PE处理组表现出最高丰度,较对照组增幅达415.90%,PLA处理组增幅为283.44%(图3-E)。已有研究证实PE微塑料可促进土壤中的固氮过程[51],这与本研究中PE处理组慢生根瘤菌属显著富集的结果相一致,进一步印证了PE对固氮过程的促进作用。此外,unclassified_f_Beijerinckiaceae的相对丰度在所有处理组中均呈上升趋势;培养至112天时,PLA处理组中该类群丰度高于对照组,而PE处理组则低于对照组,体现出固氮功能微生物对不同类型微塑料的差异化响应模式。
构建基于微生物共生网络进行分析,进一步研究微塑料对海草床沉积物微生物群落之间的相互作用。与CK组相比(图4-C,30个节点,148个边缘),PLA处理组(图4-D,29个节点,140个边缘)和PE处理组(图4-E,30个节点,142个边缘)表现出节点和边缘数量减少,这表明微塑料处理会导致海草床沉积物微生物网络规模缩小、结构简化,进而降低网络稳定性。这与既往研究结果一致:微塑料附着的土壤细菌网络相较于对照组土壤,节点与边缘数量显著减少[52];另有研究表明,覆塑农田的塑料圈群落中,微生物网络呈现更小规模、更高模块化程度及更强聚类特征[53]。此类相互作用模式的转变很可能源于微塑料表面引发的生态位分化[52]。已有研究表明,较弱的生态位分化可能增强微生物间的相互作用[54]。相较于塑料圈,周围环境可能更具均质性,生态位分化程度较低[55]。反观微塑料,其高碳含量特性[56]可能显著促进生态位分化,从而削弱不同物种间的相互作用[54]。综合上述研究结果可见,培养时间、微塑料类型均会对氮循环关键功能基因和微生物群落产生显著影响,进而调控氮循环过程的强度与方向。
-
本研究系统研究了不同微塑料类型对海草床氮循环及其微生物群落的影响。结果表明,不同类型微塑料暴露会显著降低沉积物中的NH4+-N和NO3−-N含量,同时,微塑料导致与氮循环相关的功能微生物分类发生变化。随培养时间延长,各微塑料处理组海草床沉积物微生物群落结构趋于相似,变形菌门、拟杆菌门、原厚壁菌门始终为核心优势类群。可降解PLA与不可降解PE微塑料对沉积物细菌群落及硝化、反硝化、固氮等氮循环相关功能微生物均表现出类群特异性、时间依赖性及类型差异性的影响。其中,PLA对群落多样性、组成及功能的影响更为显著,而PE则主要通过有毒添加剂的释放及其对菌群的选择性筛选发挥作用。在氮循环功能方面,微塑料通过作用于硝化,反硝化和固氮细菌,改变氮循环功能基因的表达模式:amoA和nirK基因丰度的上调,PLA和PE均能促进amoB、nirS、nifD和nifK基因丰度的上调,说明微塑料的存在促进了海草床沉积物中硝化、反硝化和固氮等氮循环关键过程的功能基因丰度。总体而言,这项研究揭示了微塑料如何影响海草床沉积物中的微生物及氮循环功能基因,然而,其对整个生态系统氮循环的长期影响效应,仍需通过原位观测与微观实验相结合的方法进行深入评估。
微塑料对海草床沉积物氮循环及微生物群落的影响
DOI: 10.15886/j.cnki.rdswxb.20260026
 CSTR: 32425.14.j.cnki.rdswxb.20260026
CSTR: 32425.14.j.cnki.rdswxb.20260026
Effect of microplastics on nitrogen cycling and microbial communities in seagrass bed sediments
-
摘要: 海草床沉积物已被证实是海洋微塑料的重要“汇”,其不断积累会对沉积物氮循环造成潜在威胁。为此,本研究设置不同材质类型(聚乙烯PE和聚乳酸PLA)的微塑料暴露实验,结合16S rRNA和宏基因组测序,评估微塑料的存在是否对海草床沉积物氮形态、功能基因丰度和微生物群落结构的影响。结果表明,PLA和PE显著降低沉积物中的NH4+-N和NO3--N含量。PLA通过富集变形菌门(Pseudomonadota)、和原厚壁菌门(Bacillota),PE通过富集拟杆菌门(Bacteroidota),促进了硝化(amoA和amoB)、反硝化(nirK和nirS)和固氮(nifD和nifK)相关基因丰度。其中,PE促进了amoA、nirK基因丰度的上调,而PLA和PE均能促进amoB、nirS、nifD、nifK基因丰度的上调。同时,这两种微塑料均能促进沉积物微生物的物种丰富度,但对群落多样性的调控效应存在明显差异:PLA可显著提升微生物群落多样性,而PE则表现出一定的抑制作用。本研究为评估微塑料对海草床生态系统生物地球化学循环的影响和保障海草床生态系统的服务功能提供理论和数据支撑。Abstract: Seagrass bed sediments have been confirmed as a significant “sink” for marine microplastics. The continuous accumulation of microplastics poses a potential threat to sediment nitrogen cycling. Thus, microplastic exposure experiments were conducted by using polyethylene (PE) and polylactic acid (PLA) to assess whether the presence of microplastics affects nitrogen forms, functional gene abundance, and microbial community structure in seagrass bed sediments through a combination of 16S rRNA and metagenomic sequencing. Results indicated that both PLA and PE significantly reduced the content of NH4+-N and NO3−-N in the sediments. PLA was enriched with Pseudomonadota and Bacillota, while PE enriched with Bacteroidota, collectively enhancing the abundances of functional genes associated with nitrification (amoA and amoB), denitrification (nirK and nirS), and nitrogen fixation (nifD and nifK). Specially, PE promoted the upregulation of amoA and nirK, whereas both PLA and PE contributed to the up-regulation of amoB, nirS, nifD, and nifK. Furthermore, both types of microplastics increased microbial species richness in the sediments, but their regulatory effects on community diversity differed significantly: PLA notably enhanced microbial community diversity, whereas PE exhibited a certain inhibitory effect. All these findings provide theoretical and data support for evaluating the impact of microplastics on the biogeochemical cycles of seagrass bed ecosystems and for safeguarding the ecosystem services of seagrass beds.
-
Key words:
- Microplastics /
- seagrass bed /
- microbial community /
- metagenomics /
- nitrogen cycling
-
图 4 不同微塑料暴露条件下海草床沉积物微生物群落随时间变化情况
A.微生物门水平的相对丰度;B.硝化、反硝化和固氮微生物的相对丰度;C-E.112天时CK(C)、PLA(D)和PE(E)处理组的共生网络分析。
Fig. 4 Changes in microbial communities in seagrass bed sediments under different microplastic (MP)exposure conditions over time
A Relative abundances at the phylum level; B Relative abundances of nitrifying, denitrifying, and nitrogen-fixing microorganisms; C-E 112-day co-occurrence network analysis of CK (C), PLA (D), and PE (E)
表 1 氮循环功能注释
Table 1 Functional annotation of nitrogen cycle
通路 Pathway 功能注释 Functional annotation 基因 Gene 硝化作用 Nitrification Methane/ammonia monooxygenase subunit A /B amoA/amoB 反硝化作用 Denitrification Nitrite reductase(NO-forming) nirK/nirS 固氮作用 Nitrogen fixation Nitrogenase molybdenum-iron protein alpha chain nifD/nifK -
[1] Thompson R C, Olsen Y, Mitchell R P, et al. Lost at Sea: where is all the Plastic? [J]. Science, 2004, 304(5672): 838. https://doi.org/10.1126/science.1094559 doi: 10.1126/science.1094559 [2] Law K L, Thompson R C. Microplastics in the Seas [J]. Science, 2014, 345(6193): 144−145. https://doi.org/10.1126/science.1254065 doi: 10.1126/science.1254065 [3] Haave M, Lorenz C, Primpke S, et al. Different stories told by small and large microplastics in sediment-first report of microplastic concentrations in an urban recipient in norway [J]. Marine Pollution Bulletin, 2019, 141: 501−513. https://doi.org/10.1016/j.marpolbul.2019.02.015 doi: 10.1016/j.marpolbul.2019.02.015 [4] Deng H, He J X, Feng D, et al. Microplastics pollution in mangrove ecosystems: a critical review of current knowledge and future directions [J]. Science of the Total Environment, 2021, 753: 142041. https://doi.org/10.1016/j.scitotenv.2020.142041 doi: 10.1016/j.scitotenv.2020.142041 [5] 环境署报告: 塑料污染威胁海洋生态环境| | 1联合国新闻[EB/OL] . (2014-06-23)[2026-03-11]. https://news.un.org/zh/story/2014/06/216502. [6] Fourqurean J W, Duarte C M, Kennedy H, et al. Seagrass ecosystems as a globally significant carbon stock [J]. Nature Geoscience, 2012, 5(7): 505−509. https://doi.org/10.1038/ngeo1477 doi: 10.1038/ngeo1477 [7] Orth R J, Carruthers T J B, Dennison W C, et al. A global crisis for seagrass ecosystems [J]. BioScience, 2006, 56(12): 987−996. https://doi.org/10.1641/0006-3568(2006)56[987:AGCFSE]2.0.CO;2 doi: 10.1641/0006-3568(2006)56[987:AGCFSE]2.0.CO;2 [8] 侯帅玲, 樊瑾珞, 任国梁, 等. 海草床生态系统中微塑料的检测方法、赋存特征及毒理效应研究进展[J]. 生态毒理学报, 2023, 18(6): 112−126. https://doi.org/10.7524/AJE.1673-5897.20230801002 doi: 10.7524/AJE.1673-5897.20230801002 [9] Hou S L, Wang J, Feng D, et al. Colonization time of plastisphere drives the dynamics of organic carbon stability and microbial communities in seagrass bed sediments [J]. Journal of Hazardous Materials, 2025, 492: 138078. https://doi.org/10.1016/j.jhazmat.2025.138078 doi: 10.1016/j.jhazmat.2025.138078 [10] Goss H, Jaskiel J, Rotjan R. Thalassia testudinum as a potential vector for incorporating microplastics into benthic marine food webs [J]. Marine Pollution Bulletin, 2018, 135: 1085−1089. https://doi.org/10.1016/j.marpolbul.2018.08.024 doi: 10.1016/j.marpolbul.2018.08.024 [11] Jones K L, Hartl M G J, Bell M C, et al. Microplastic accumulation in a Zostera marina L. bed at deerness sound, Orkney, Scotland [J]. Marine Pollution Bulletin, 2020, 152: 110883. https://doi.org/10.1016/j.marpolbul.2020.110883 doi: 10.1016/j.marpolbul.2020.110883 [12] 侯梓良, 冯民权, 赵直. 和川水库沉积物-水界面氮赋存特征及交换通量分析[J]. 人民黄河, 2023, 45(10): 90−95. https://doi.org/10.3969/j.issn.1000-1379.2023.10.016 doi: 10.3969/j.issn.1000-1379.2023.10.016 [13] 刘波, 周锋, 王国祥, 等. 沉积物氮形态与测定方法研究进展[J]. 生态学报, 2011, 31(22): 6947−6958. https://doi.org/10.20103/j.stxb.2011.22.031 doi: 10.20103/j.stxb.2011.22.031 [14] 冯冰聪, 马杰, 刘勇, 等. 氮素在农田土壤中迁移转化的研究进展[J]. 农业资源与环境学报, 2025, 42(2): 277−287. https://doi.org/10.13254/j.jare.2023.0825 doi: 10.13254/j.jare.2023.0825 [15] 陈晨, 李兵, 项鸿志, 等. 沉积物中氮转化过程及形态研究进展[J]. 广州化工, 2025, 53(21): 25−29. https://doi.org/10.20220/j.cnki.1001-9677.2025.21.008 doi: 10.20220/j.cnki.1001-9677.2025.21.008 [16] Seeley M E, Song B, Passie R, et al. Microplastics affect sedimentary microbial communities and nitrogen cycling [J]. Nature Communications, 2020, 11(1): 2372. https://doi.org/10.1038/s41467-020-16235-3 doi: 10.1038/s41467-020-16235-3 [17] Fortin S G, Uhlig K, Hale R C, et al. Microplastic biofilms as potential hotspots for plastic biodegradation and nitrogen cycling: a metagenomic perspective [J]. FEMS Microbiology Ecology, 2025, 101(5): fiaf035. https://doi.org/10.1093/femsec/fiaf035 doi: 10.1093/femsec/fiaf035 [18] Wang X D, Guo S, Zhang X L, et al. Microplastics as drivers of carbon and nitrogen cycling alterations in aquatic ecosystems: a meta-analysis [J]. Journal of Hazardous Materials, 2025, 491: 138033. https://doi.org/10.1016/j.jhazmat.2025.138033 doi: 10.1016/j.jhazmat.2025.138033 [19] She Y C, Wu L Y, Qi X, et al. Aging behaviors intensify the impacts of microplastics on nitrate bioreduction-driven nitrogen cycling in freshwater sediments [J]. Water Research, 2025, 279: 123448. https://doi.org/10.1016/j.watres.2025.123448 doi: 10.1016/j.watres.2025.123448 [20] Peng X F, Ji Q X, Angell J H, et al. Long-term fertilization alters nitrous oxide cycling dynamics in salt marsh sediments [J]. Environmental Science & Technology, 2021, 55(15): 10832−10842. https://doi.org/10.1021/acs.est.1c01542 doi: 10.1021/acs.est.1c01542 [21] Chen M L, Liu S S, Bi M H, et al. Aging behavior of microplastics affected DOM in riparian sediments: from the characteristics to bioavailability [J]. Journal of Hazardous Materials, 2022, 431: 128522. https://doi.org/10.1016/j.jhazmat.2022.128522 doi: 10.1016/j.jhazmat.2022.128522 [22] Wang H L, Zhong Y, Yang Q, et al. Coupling of sulfate reduction and dissolved organic carbon degradation accelerated by microplastics in blue carbon ecosystems [J]. Water Research, 2025, 279: 123414. https://doi.org/10.1016/j.watres.2025.123414 doi: 10.1016/j.watres.2025.123414 [23] Gao S H, Fu Y B, Peng X Y, et al. Microplastics trigger soil dissolved organic carbon and nutrient turnover by strengthening microbial network connectivity and cross-trophic interactions [J]. Environmental Science & Technology, 2025, 59(11): 5596−5606. https://doi.org/10.1021/acs.est.4c12546 doi: 10.1021/acs.est.4c12546 [24] Cluzard M, Kazmiruk T N, Kazmiruk V D, et al. Intertidal concentrations of microplastics and their influence on ammonium cycling as related to the shellfish industry [J]. Archives of Environmental Contamination and Toxicology, 2015, 69(3): 310−319. https://doi.org/10.1007/s00244-015-0156-5 doi: 10.1007/s00244-015-0156-5 [25] Wang Q L, Feng X Y, Liu Y Y, et al. Effects of microplastics and carbon nanotubes on soil geochemical properties and bacterial communities [J]. Journal of Hazardous Materials, 2022, 433: 128826. https://doi.org/10.1016/j.jhazmat.2022.128826 doi: 10.1016/j.jhazmat.2022.128826 [26] Liu X Y, Liu H T, Chen L, et al. Ecological interception effect of mangroves on microplastics [J]. Journal of Hazardous Materials, 2022, 423: 127231. https://doi.org/10.1016/j.jhazmat.2021.127231 doi: 10.1016/j.jhazmat.2021.127231 [27] Tang X F, Bao Y Y, Li J, et al. Microplastics promote N2O emissions by enhancing nitrification via ammonia-oxidizing bacteria in estuarine and coastal sediments [J]. Water Research, 2026, 293: 125458. https://doi.org/10.1016/j.watres.2026.125458 doi: 10.1016/j.watres.2026.125458 [28] Zhang Y, Tian Z, Liu M M, et al. High concentrations of the antibiotic spiramycin in wastewater lead to high abundance of ammonia-oxidizing archaea in nitrifying populations [J]. Environmental Science & Technology, 2015, 49(15): 9124−9132. https://doi.org/10.1021/acs.est.5b01293 doi: 10.1021/acs.est.5b01293 [29] Tang Y Q, Zhang X Y, Li D D, et al. Impacts of nitrogen and phosphorus additions on the abundance and community structure of ammonia oxidizers and denitrifying bacteria in Chinese fir plantations [J]. Soil Biology and Biochemistry, 2016, 103: 284−293. https://doi.org/10.1016/j.soilbio.2016.09.001 doi: 10.1016/j.soilbio.2016.09.001 [30] Van Kessel M A H J, Speth D R, Albertsen M, et al. Complete nitrification by a single microorganism [J]. Nature, 2015, 528(7583): 555−559. https://doi.org/10.1038/nature16459 doi: 10.1038/nature16459 [31] Qi W Q, Liu Y J, Jiang Z J, et al. Sulfide intrusion of seagrass Thalassia Hemprichii along a eutrophication gradient with carbonate and terrigenous sediments in tropical coastal sea [J]. Journal of Hazardous Materials, 2025, 491: 138005. https://doi.org/10.1016/j.jhazmat.2025.138005 doi: 10.1016/j.jhazmat.2025.138005 [32] Yin M Y, Yan B, Wang H, et al. Effects of microplastics on nitrogen and phosphorus cycles and microbial communities in sediments [J]. Environmental Pollution, 2023, 318: 120852. https://doi.org/10.1016/j.envpol.2022.120852 doi: 10.1016/j.envpol.2022.120852 [33] Yu H W, Qi W X, Cao X F, et al. Microplastic residues in wetland ecosystems: do they truly threaten the plant-microbe-soil system? [J]. Environment International, 2021, 156: 106708. https://doi.org/10.1016/j.envint.2021.106708 doi: 10.1016/j.envint.2021.106708 [34] Su X X, Yang L Y, Yang K, et al. Estuarine plastisphere as an overlooked source of N2O production [J]. Nature Communications, 2022, 13(1): 3884. https://doi.org/10.1038/s41467-022-31584-x doi: 10.1038/s41467-022-31584-x [35] Yin M Y, Yan B, Wang H, et al. Effects of microplastics on nitrogen and phosphorus cycles and microbial communities in sediments [J]. Environmental Pollution, 2023, 318: 120852. https://doi.org/10.1016/j.envpol.2022.120852 doi: 10.1016/j.envpol.2022.120852 [36] Zhang M J, Zhao Y R, Qin X, et al. Microplastics from mulching film is a distinct habitat for bacteria in farmland soil [J]. Science of the Total Environment, 2019, 688: 470−478. https://doi.org/10.1016/j.scitotenv.2019.06.108 doi: 10.1016/j.scitotenv.2019.06.108 [37] Pan X, Lin L, Cao X H, et al. Response of microbial communities and biogeochemical cycling functions to sediment physicochemical properties and microplastic pollution under damming and water diversion projects [J]. Science of the Total Environment, 2024, 940: 173209. https://doi.org/10.1016/j.scitotenv.2024.173209 doi: 10.1016/j.scitotenv.2024.173209 [38] Wang F Y, Wang Q L, Adams C A, et al. Effects of microplastics on soil properties: current knowledge and future perspectives [J]. Journal of Hazardous Materials, 2022, 424: 127531. https://doi.org/10.1016/j.jhazmat.2021.127531 doi: 10.1016/j.jhazmat.2021.127531 [39] Qi Y L, Ossowicki A, Yang X M, et al. Effects of plastic mulch film residues on wheat rhizosphere and soil properties [J]. Journal of Hazardous Materials, 2020, 387: 121711. https://doi.org/10.1016/j.jhazmat.2019.121711 doi: 10.1016/j.jhazmat.2019.121711 [40] Zhang P T, Yuan Y, Zhang J, et al. Specific response of soil properties to microplastics pollution: a review [J]. Environmental Research, 2023, 232: 116427. https://doi.org/10.1016/j.envres.2023.116427 doi: 10.1016/j.envres.2023.116427 [41] Janakiev T, Milošević Đ, Petrović M, et al. Chironomus riparius larval gut bacteriobiota and its potential in microplastic degradation [J]. Microbial Ecology, 2023, 86(3): 1909−1922. https://doi.org/10.1007/s00248-023-02199-6 doi: 10.1007/s00248-023-02199-6 [42] Li K, Jia W Q, Xu L B, et al. The plastisphere of biodegradable and conventional microplastics from residues exhibit distinct microbial structure, network and function in plastic-mulching farmland [J]. Journal of Hazardous Materials, 2023, 442: 130011. https://doi.org/10.1016/j.jhazmat.2022.130011 doi: 10.1016/j.jhazmat.2022.130011 [43] Wang Q L, Feng X Y, Liu Y Y, et al. Response of peanut plant and soil N-fixing bacterial communities to conventional and biodegradable microplastics [J]. Journal of Hazardous Materials, 2023, 459: 132142. https://doi.org/10.1016/j.jhazmat.2023.132142 doi: 10.1016/j.jhazmat.2023.132142 [44] Qi Y L, Ossowicki A, Yang X M, et al. Effects of plastic mulch film residues on wheat rhizosphere and soil properties [J]. Journal of Hazardous Materials, 2020, 387: 121711. https://doi.org/10.1016/j.jhazmat.2019.121711 doi: 10.1016/j.jhazmat.2019.121711 [45] Dal Bello M, Lee H, Goyal A, et al. Resource–diversity relationships in bacterial communities reflect the network structure of microbial metabolism [J]. Nature Ecology & Evolution, 2021, 5(10): 1424−1434. https://doi.org/10.1038/s41559-021-01535-8 doi: 10.1038/s41559-021-01535-8 [46] Li X, Wang A C, Wan W J, et al. High salinity inhibits soil bacterial community mediating nitrogen cycling [J]. Applied and Environmental Microbiology, 2021, 87(21): e01366−21. https://doi.org/10.1128/AEM.01366-21 doi: 10.1128/AEM.01366-21 [47] Ren M, Zhang Z F, Wang X L, et al. Diversity and contributions to nitrogen cycling and carbon fixation of soil salinity shaped microbial communities in Tarim Basin [J]. Frontiers in Microbiology, 2018, 9: 431. https://doi.org/10.3389/fmicb.2018.00431 doi: 10.3389/fmicb.2018.00431 [48] Harrison J P, Schratzberger M, Sapp M, et al. Rapid bacterial colonization of low-density polyethylene microplastics in coastal sediment microcosms [J]. BMC Microbiology, 2014, 14(1): 232. https://doi.org/10.1186/s12866-014-0232-4 doi: 10.1186/s12866-014-0232-4 [49] Chen C, Pan J Y, Xiao S X, et al. Microplastics alter nitrous oxide production and pathways through affecting microbiome in estuarine sediments [J]. Water Research, 2022, 221: 118733. https://doi.org/10.1016/j.watres.2022.118733 doi: 10.1016/j.watres.2022.118733 [50] Niu L H, Li Y Y, Li Y, et al. New insights into the vertical distribution and microbial degradation of microplastics in urban river sediments [J]. Water Research, 2021, 188: 116449. https://doi.org/10.1016/j.watres.2020.116449 doi: 10.1016/j.watres.2020.116449 [51] Zhang L Q, Tao Y Q. Ecological regime shifts enhanced the contribution of microplastics to the burial of polycyclic aromatic hydrocarbons by sediments [J]. Environmental Pollution, 2023, 335: 122329. https://doi.org/10.1016/j.envpol.2023.122329 doi: 10.1016/j.envpol.2023.122329 [52] Zou Z H, Yu Q D, Wang J Y, et al. Microplastic composition-dependent effects on N2O emissions driven by changes in soil N process and microbial communities [J]. Journal of Hazardous Materials, 2025, 495: 139022. https://doi.org/10.1016/j.jhazmat.2025.139022 doi: 10.1016/j.jhazmat.2025.139022 [53] Li K, Jia W Q, Xu L B, et al. The Plastisphere of biodegradable and conventional microplastics from residues exhibit distinct microbial structure, network and function in plastic-mulching farmland [J]. Journal of Hazardous Materials, 2023, 442: 130011. https://doi.org/10.1016/j.jhazmat.2022.130011 doi: 10.1016/j.jhazmat.2022.130011 [54] Ma B, Wang H Z, Dsouza M, et al. Geographic patterns of Co-occurrence network topological features for soil microbiota at continental scale in Eastern China [J]. The ISME Journal, 2016, 10(8): 1891−1901. https://doi.org/10.1038/ismej.2015.261 doi: 10.1038/ismej.2015.261 [55] Ma B, Wang Y L, Ye S D, et al. Earth microbial Co-occurrence network reveals interconnection pattern across microbiomes [J]. Microbiome, 2020, 8(1): 82. https://doi.org/10.1186/s40168-020-00857-2 doi: 10.1186/s40168-020-00857-2 [56] Fang J H, Sheng Z H, Liu J, et al. Interference of microplastics on autotrophic microbiome in paddy soils: shifts in carbon fixation rate, structure, abundance, Co-occurrence, and assembly process [J]. Journal of Hazardous Materials, 2024, 474: 134783. https://doi.org/10.1016/j.jhazmat.2024.134783 doi: 10.1016/j.jhazmat.2024.134783 -

 点击查看大图
点击查看大图
计量
- 文章访问数: 99
- HTML全文浏览量: 59
- 被引次数: 0



 下载:
下载:
