-
红树植物广泛分布于热带和亚热带地区的海岸带海陆交错区[1],是生物多样性、生产力最高的生态系统之一,具有巨大的生态价值[2]。水椰(Nypa fruticans)是一种隶属于棕榈科(Arecaceae)水椰属(Nypa)的真红树植物[3],具有防风固堤、净化空气的重要作用[4]。水椰的果肉富含矿物质、维生素,其羽状复叶可以编制工艺品,也拥有着较高的经济价值。此外,在热带植物区系、古生物学、海洋地质考古及古植物学等多个学科领域中水椰均展现出极高的科研价值[3]。2021年,中国正式将水椰列为二级保护植物,并将其纳入《国家重点保护野生植物名录》[5]。20%~30%的透光率最适宜阴生植物走马胎(Ardisia gigantifolia)生长[6]。江南油杉(Keteleeria fortunei var. Cyclolepis)幼苗在遮荫率为60%的环境下受光胁迫较小,其生长,叶片表观特征,光合能力以及生物量积累与分配等表现最优[7]。张孟文等[8]的研究表明,海南岛水椰群落高度多为8~10 m,郁闭度多为50%~80%。水椰高大、密集等特点降低了林下的光照环境,因此,通过探究水椰幼苗在低光照水平下的生理变化及转录组表达差异,旨在揭示水椰幼苗在低光照水平下的生理与转录组如何响应的问题,为水椰的繁育工作提供科学依据。
-
试验地点位于海南省海口市东寨港红树林保护区附近的桂南下村(19°56′52.86″N,110°34′28.26″E)。该区域日照充足,年平均日照时数超过2 000 h,太阳辐射量达到11~12万K。气候温暖湿润,年平均气温为24.4 ℃,最高平均气温约28 ℃,最低平均气温约18 ℃。年降水量丰富,年平均降水量为1 696.6 mm,而年平均蒸发量为1 834 mm。该区域的风向以东南风和东北风为主,年平均风速为3.4 m·s−1,海拔3 m[9]。这些气候条件为水椰幼苗的生长提供了良好的环境。
-
选取225株长势一致的水椰幼苗[1年苗龄、株高约为(45 ± 5)cm、基径约为(18 ± 3)cm]作为试验材料进行水椰幼苗遮阴试验(遮阴40 d)。转录组测序材料选自遮荫试验遮荫40 d的水椰幼苗叶片。
根据自然群落中拥有幼苗较多的郁闭度(50%~80%)且通过预试验筛选,设置了3个光强处理:通过使用不同透光度的黑色尼龙网得到相对自然光强的100%(CK,对照)、30%(Z1)和20%(Z2),于2023年5月11日开始,分别设置在5个小区,每个小区包含3个光强处理,每个处理有15株水椰幼苗,共225株。幼苗栽种于3.14 L的花盆中,每盆一株,放置于苗圃进行40 d的遮阴处理。在遮阴初期,选择了连续3 d的晴朗天气,采用文献[10]的方法测量每天9:00、12:00和15:00各遮阴棚内和全光照处理下的光量子通量密度(表1)。
表 1 各光照处理的相对光强
Table 1. Relative light intensity measured in the three light treatments
时间Time CK Z1 Z2 9:00 100 33.4 22.1 12:00 100 32.1 19.8 15:00 100 30.9 20.2 均值 Mean 100 32.3 20.7 -
在0 、10、20、30、40 d时随机采取各小区各处理的叶片,进行生理指标的测量;在第40天时各小区各处理内随机挑选一株进行生物量测量。在取样过程中,从每个处理中挑选了3株幼苗,并从每株幼苗中随机采集了3~4片新鲜且成熟的叶片,采集后用液氮处理,带回实验室−80 ℃冰箱进行保存,待40 d采样后进行指标测量。这些叶片被用于测定可溶性蛋白(Soluble proteins,SP)含量、丙二醛(Malondialdehyde,MDA)含量、叶绿素(Chlorophyll,Chl)含量以及超氧化物歧化酶(Superoxide dismutase,SOD)和过氧化物酶(Peroxidase,POD)的活性。在40 d时随机采取各小区各处理的叶片共15片,液氮处理后置于干冰中保存,送公司测序。
-
首先,使用电子天平(精度为0.000 1 g)称取大约0.3 g的新鲜叶片,并将其与预冷的提取液(包含磷酸缓冲液、EDTA-Na2和PVP)混合,在冰浴条件下研磨成匀浆。随后,在4 ℃条件下,以16 000 × g的离心力对混合物进行20 min的离心处理,以获取上清液,用于后续的SP含量和酶活性测定。在测定SP含量时,采用了考马斯亮蓝染色法,并使用牛血清蛋白作为标准曲线。对于SOD活性的测定,参考了文献[11]的方法,通过比较酶液与磷酸缓冲液在光化还原氮蓝四唑反应中的差异来计算酶活力单位(U),并将酶活性表示为U·g−1。对于POD活性的测定,则采用了文献[12]的方法,以OD470值的变化速率作为酶活力单位的衡量标准,酶活性表示为U·g−1·min−1。MDA含量的测定参照了文献[13]的方法(TBA法),MDA在高温及酸性条件下与TBA反应形成有色物,在532 nm波长处有最大吸收值,600 nm波长处有最小吸收值,而Chl含量的测定则遵循了文献[14]的方法(80%丙酮浸提法)将叶片细丝投入含5 mL 80%丙酮的刻度试管中,封管口后于暗中提取至细丝完全变为白色为止(过夜即可)。
-
用于转录组测序的材料来自水椰幼苗遮阴试验,采集遮阴40 d的幼苗叶片,液氮冷冻后干冰保存寄给公司进行测序,得到RANseq二代测序结果,对得到的原始测序数据用fastp软件进行质量控制,去除前端20个不稳定的碱基得到干净数据,经过严格的数据筛选过程,排除了存在接头、长度不足50 bp以及质量低于Q20的低质量Reads,确保最终数据的纯净度。经过这一步骤,成功获得了总计22.6 G的清洁碱基以及278 143个高质量的清洁读段。随后,利用这些精选的高质量序列进行了从头拼接,从而生成了转录本序列,即Unigene,统计后共有128 245条。对比了试验组(Z1和Z2)与对照组(CK)的基因表达差异。使用Trinity进行从头组装,利用BUSCO软件进行组装结果评估,去除冗余;利用bowtie2软件进行比对和定量,用Trinotate软件NR库进行注释,得到表达矩阵,用EDSeq2进行差异分析,利用微生信在线平台绘制了火山图,eggNOG-mapper对蛋白质序列进行注释,用R语言进行GO功能富集分析,Go注释的基因有39 491条;通过注释文本,筛选出有关植物光合作用、呼吸作用、抗氧化酶的基因共303条。用R语言进行自建GO数据库,进行GO富集分析。
-
数据用Microsoft Excel 2021软件计算平均值和标准误,采用SPSS Pro在线分析软件进行统计分析,当P < 0.05时表示有统计学意义。SOD活性、POD活性、MDA含量、SP含量和Chl含量使用单因素方差分析(One-way ANOVA)方法进行显著性检验,箱线图由cnsknowall在线平台绘制。
-
从表2可知,遮阴40 d后水椰幼苗的干质量和鲜质量在Z1、Z2、CK之间没有显著差异;根冠比Z1、Z2与CK之间有显著差异,根冠比Z1较CK低了57.6%,Z2较CK低了48.1%。Z1、Z2间的根冠比差异不显著。
表 2 遮阴40 d后水椰幼苗的生物量
Table 2. Biomass of Nypa fruticans seedlings after 40 days of shading
指标 Indicator Z1 Z2 CK 干质量 Dry weight/kg 0.128 ± 0.017ns 0.16 ± 0.016ns 0.106 ± 0.006ns 鲜质量 Fresh weight/kg 0.474 ± 0.062ns 0.534 ± 0.047ns 0.462 ± 0.032ns 根冠比 Root-shoot ratio 0.133 ± 0.025b 0.163 ± 0.023b 0.314 ± 0.034a 注:不同字母表示各光照处理之间存在显著差异(P < 0.05),ns表示无显著差异(P > 0.05)。 Note: Different letters indicate significant differences between various light treatments (P < 0.05); ns indicates no significant difference (P > 0.05). -
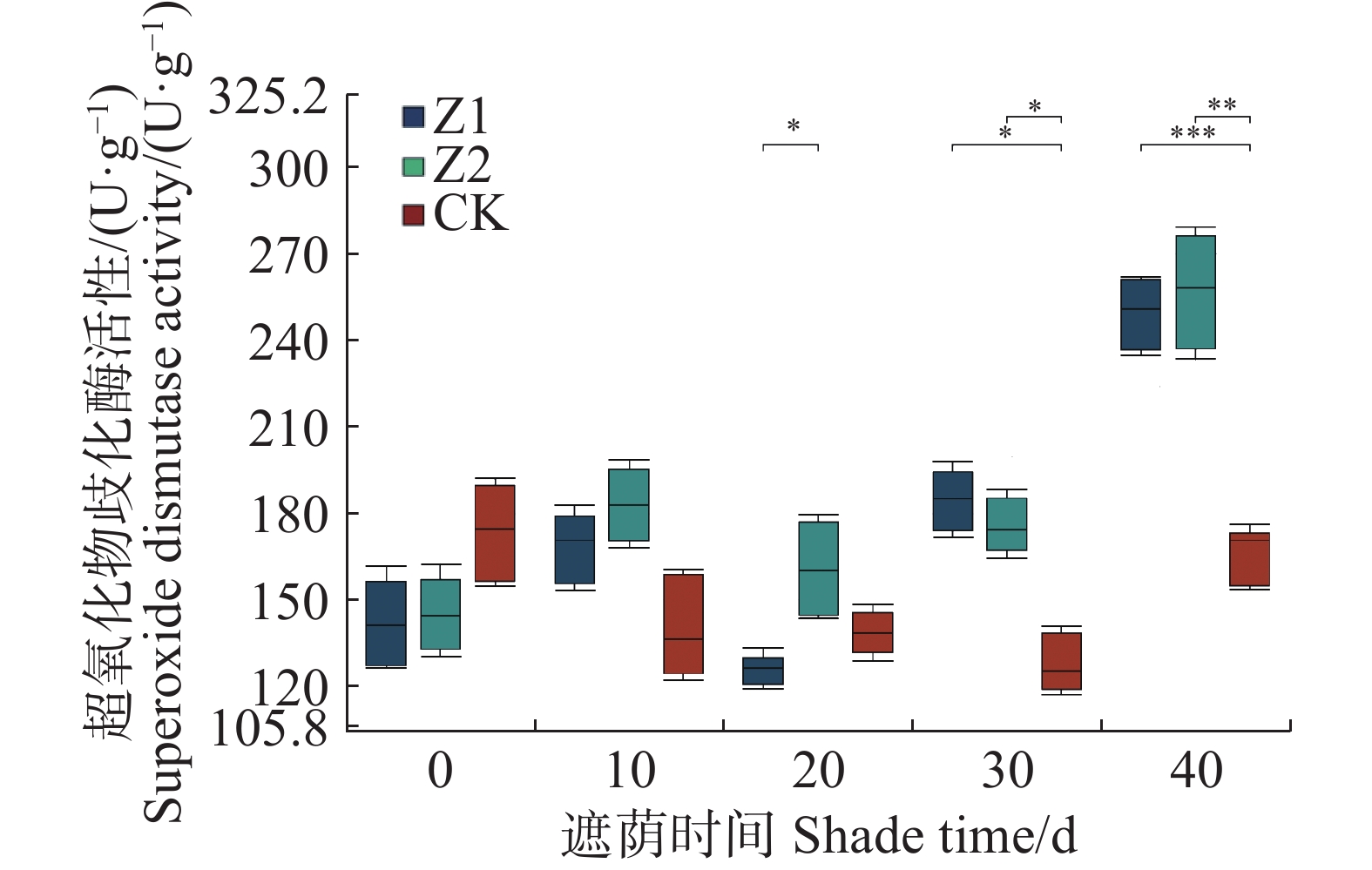
从图1可知,在试验0 和10 d时,遮阴处理(Z1和Z2)对水椰幼苗的SOD活性未产生统计学上的显著影响(P > 0.05)。在20 d时,Z1和Z2两种遮荫处理之间的SOD活性存在显著差异。30和40 d时,遮阴处理显著提高了SOD活性,与对照组(CK)相比,Z1处理下的SOD活性分别增加了39.3%和57.1%,Z2处理则分别增加了34.9%和62.1%。
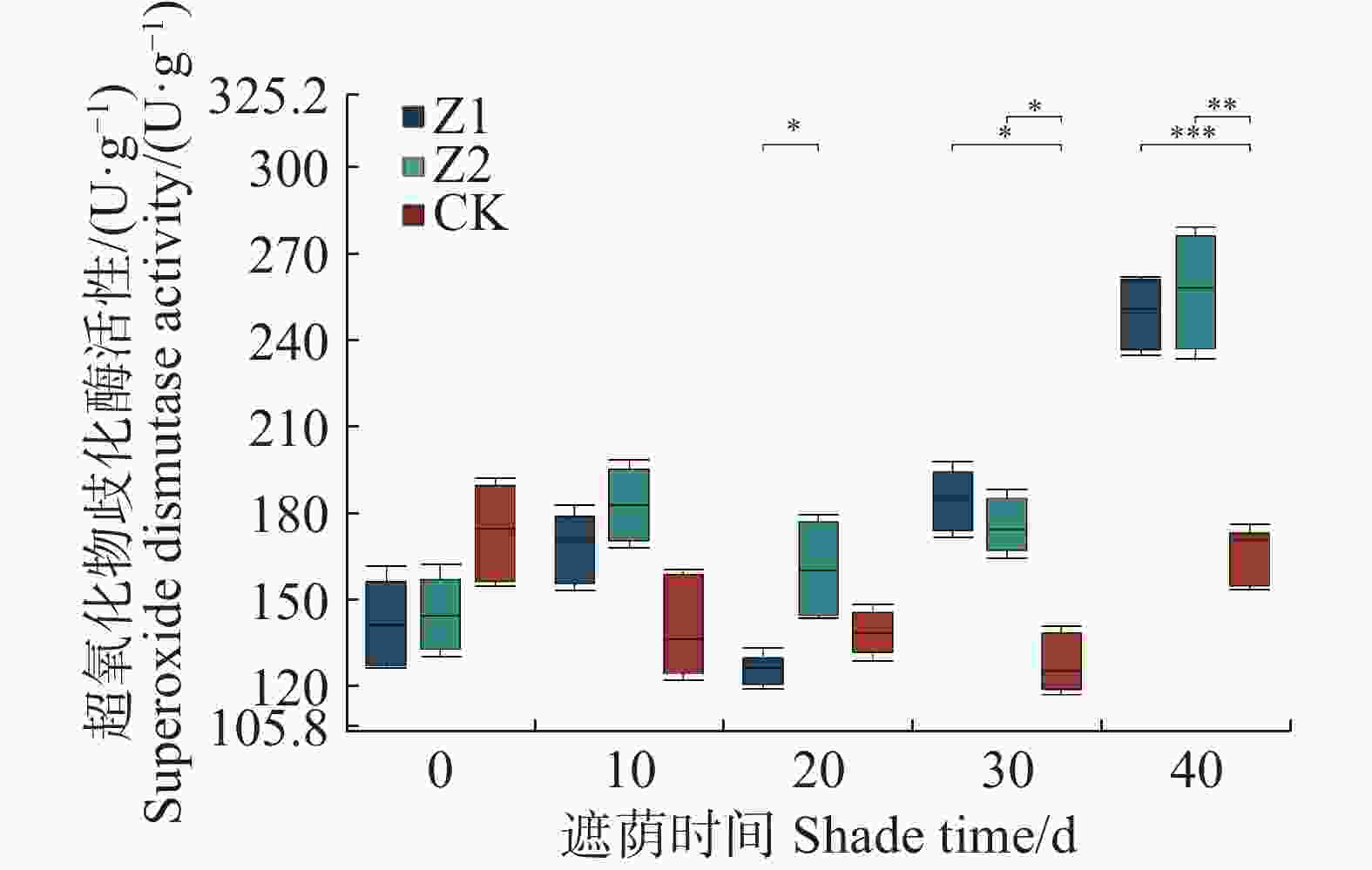
图 1 不同光照强度下水椰幼苗超氧化物歧化酶活性变化
Figure 1. Superoxide dismutase activity of Nypa fruticans seedlings under different light intensities
从图2可知,遮阴对水椰幼苗POD活性在0 和10 d没有产生显著影响(P > 0.05),Z1在40 d与CK相比有显著差异,比CK高41.2%,Z2在20、30、40 d与CK相比有显著差异,分别比CK高25.6%、16.8%、35.7%。Z1和Z2的光照处理之间没有显著差异。
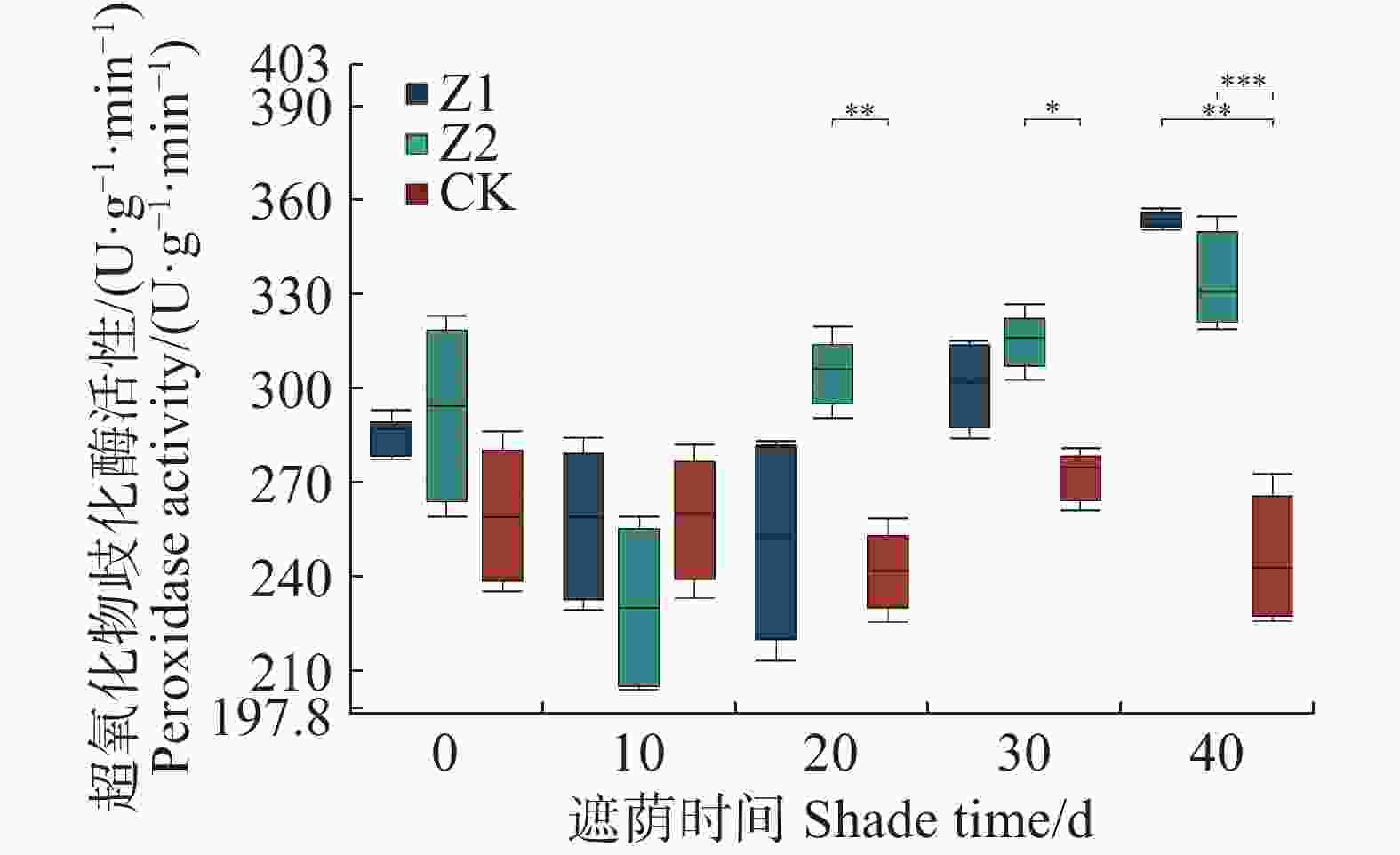
图 2 不同光照强度下水椰幼苗过氧化物酶活性变化
Figure 2. Changes in peroxidase activity of Nypa fruticans seedlings under different light intensities
从图3可知,遮阴对水椰幼苗MDA含量在0、10 d没有产生显著影响(P > 0.05);在20 、30 、40 d产生显著影响,Z1分别比CK低9.5%、47.3%、42.6%,Z2分别比CK低4.2%、41.9%、32.9%。Z1和Z2的光照处理之间没有显著差异。遮阴处理水椰幼苗的MDA含量比未遮阴的对照组更低。
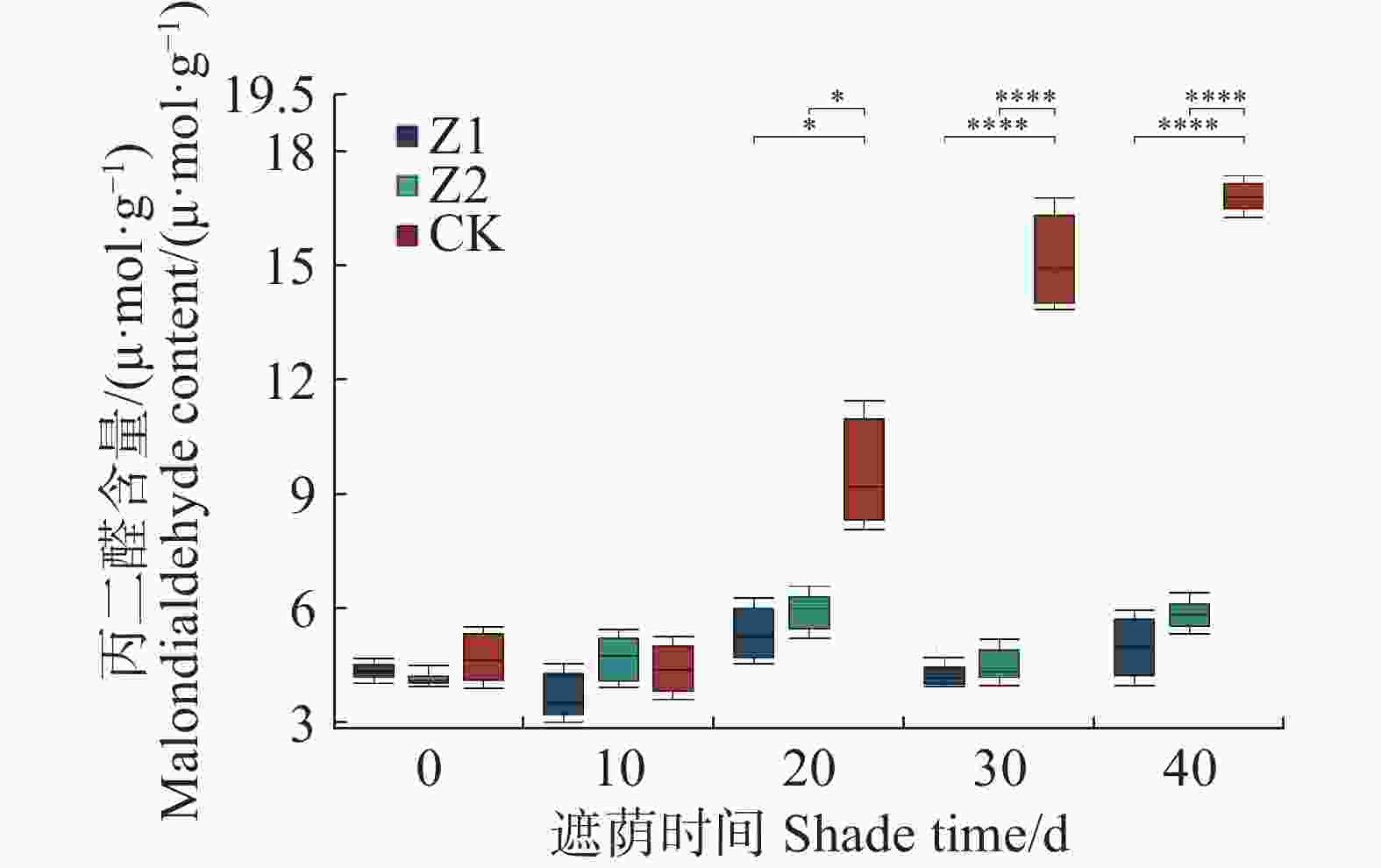
图 3 不同光照强度下水椰幼苗丙二醛含量变化
Figure 3. Changes in malondialdehyde content of Nypa fruticans seedlings under different light intensities
从图4可知,遮阴对水椰幼苗SP含量除10 d时Z1与CK存在显著差异外,其他无显著差异。
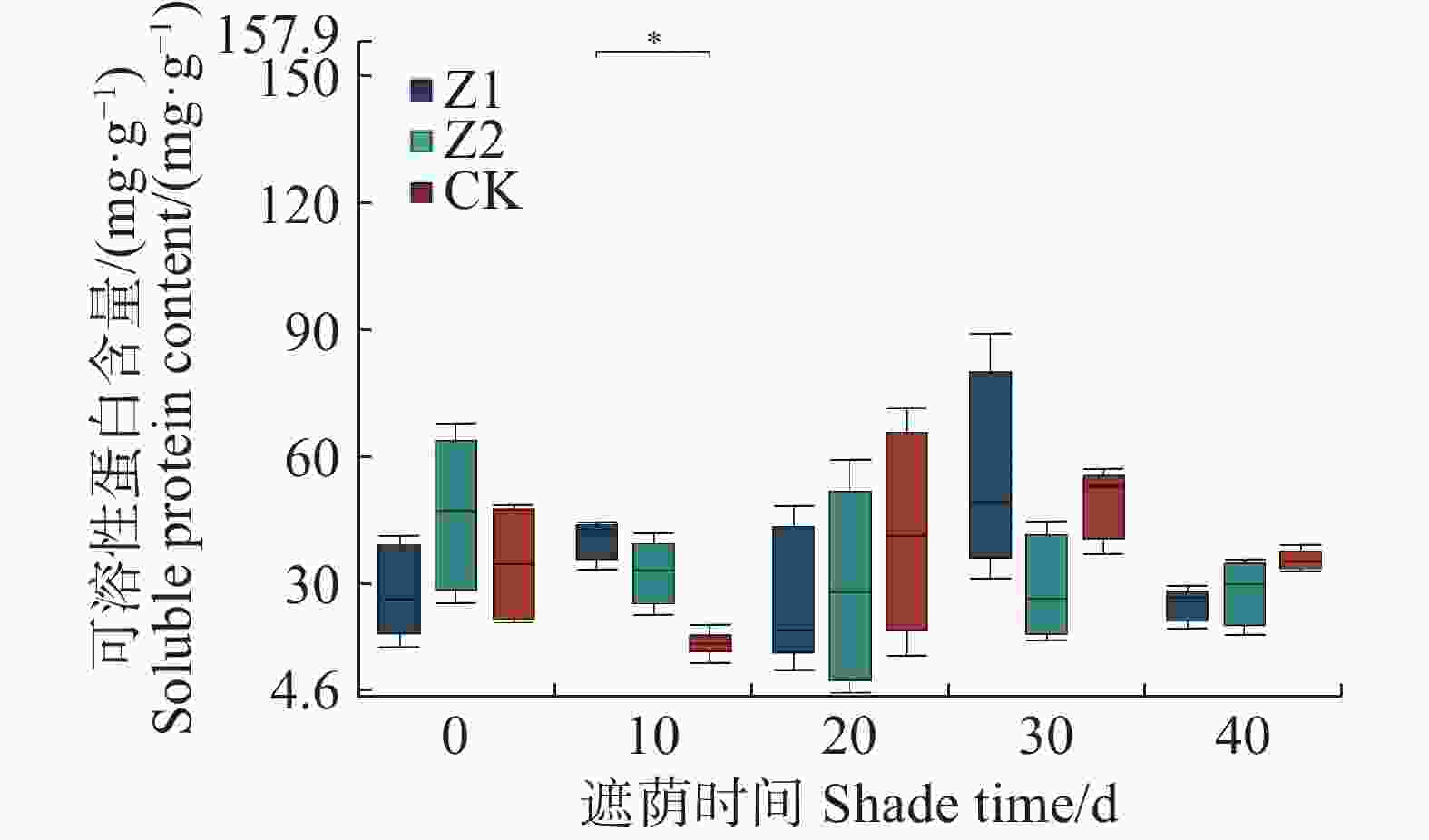
图 4 不同光照强度下水椰幼苗可溶性蛋白含量变化
Figure 4. Changes in soluble protein content of Nypa fruticans seedlings under different light intensities
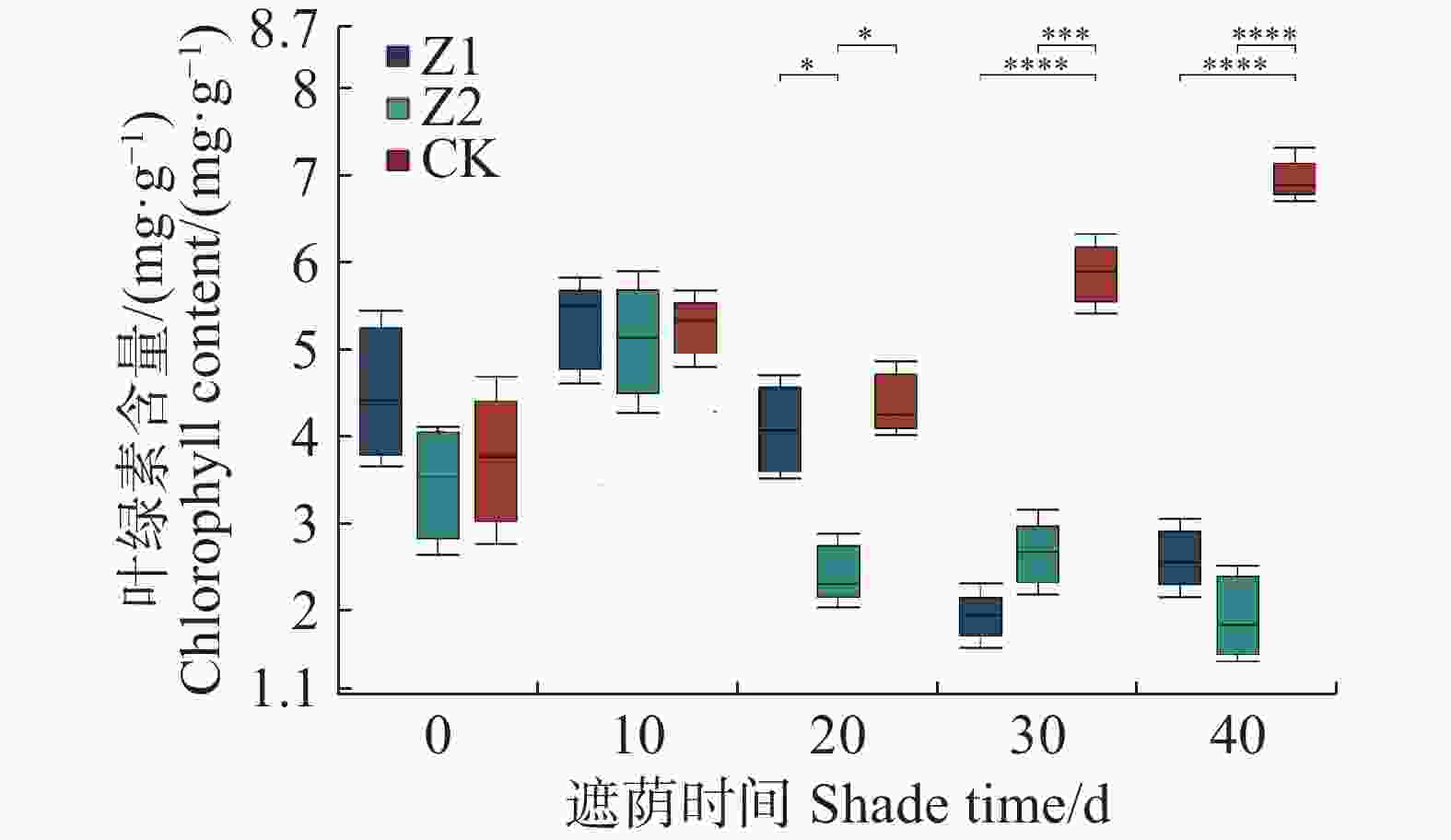
从图5可知,Chl含量与CK相比在30 、40 d产生显著影响,在20 d时Z2与Z1、CK存在显著差异;在10 d时相较于0 d较高有增加趋势,Z1分别比CK高26%、0.6%,Z2分别比CK低8.2%、高0.6%,在20 、30 、40 d时Z1、Z2的叶绿素含量下降,Z1分别比CK低10%、66.3%、61.1%,Z2分别比CK低42.7%、54.6%、70.3%,未遮荫的对照组的叶绿素含量持续上升。
-
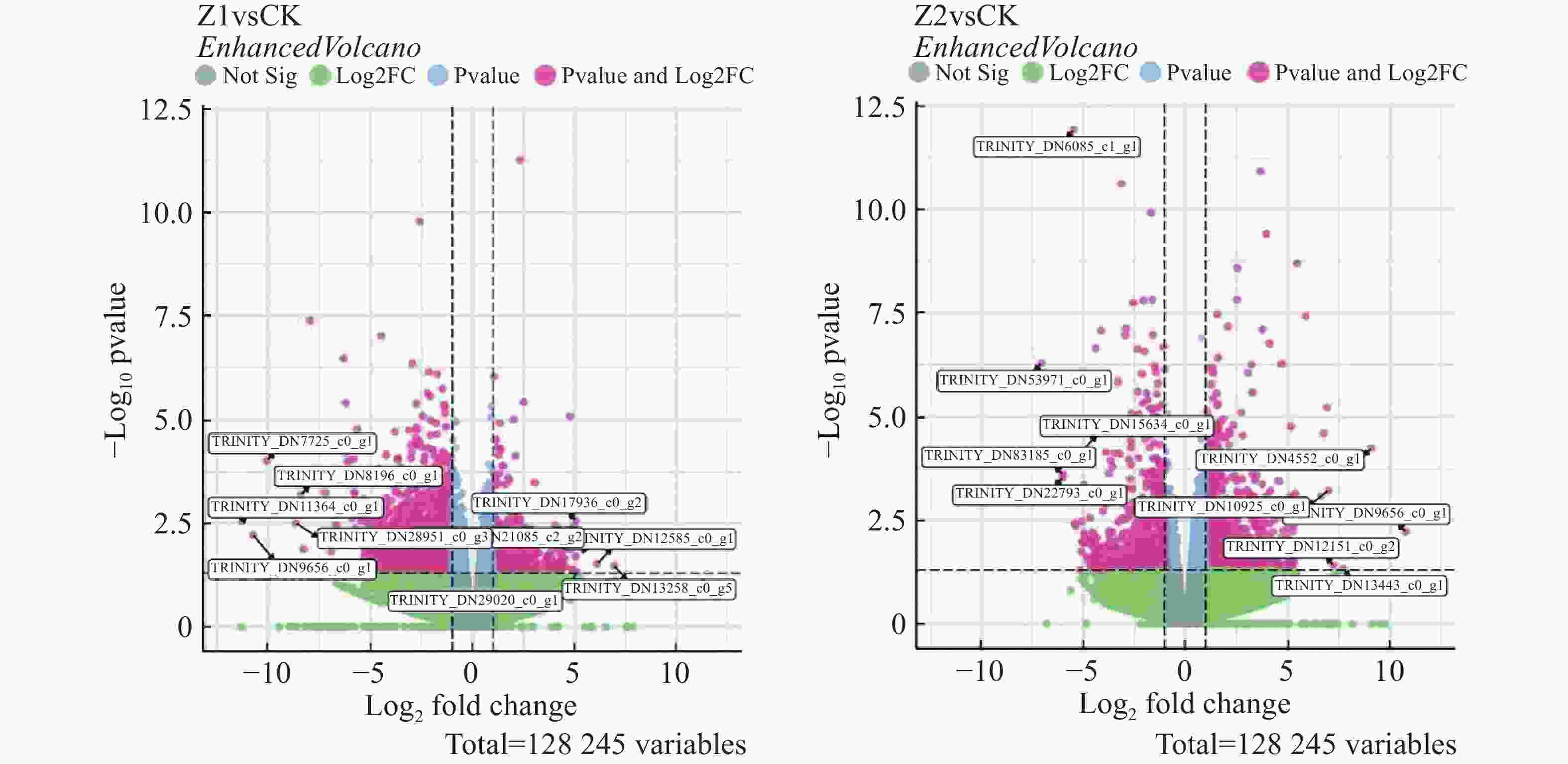
从图6可知,与CK相比,Z1组上调基因69 687条,其中显著差异(P < 0.05)的857条;下调基因58 558条,显著差异的1 970条。而在Z2组,上调基因73 322条,显著差异的1 856条;下调基因54 923条,显著差异的1 124条。
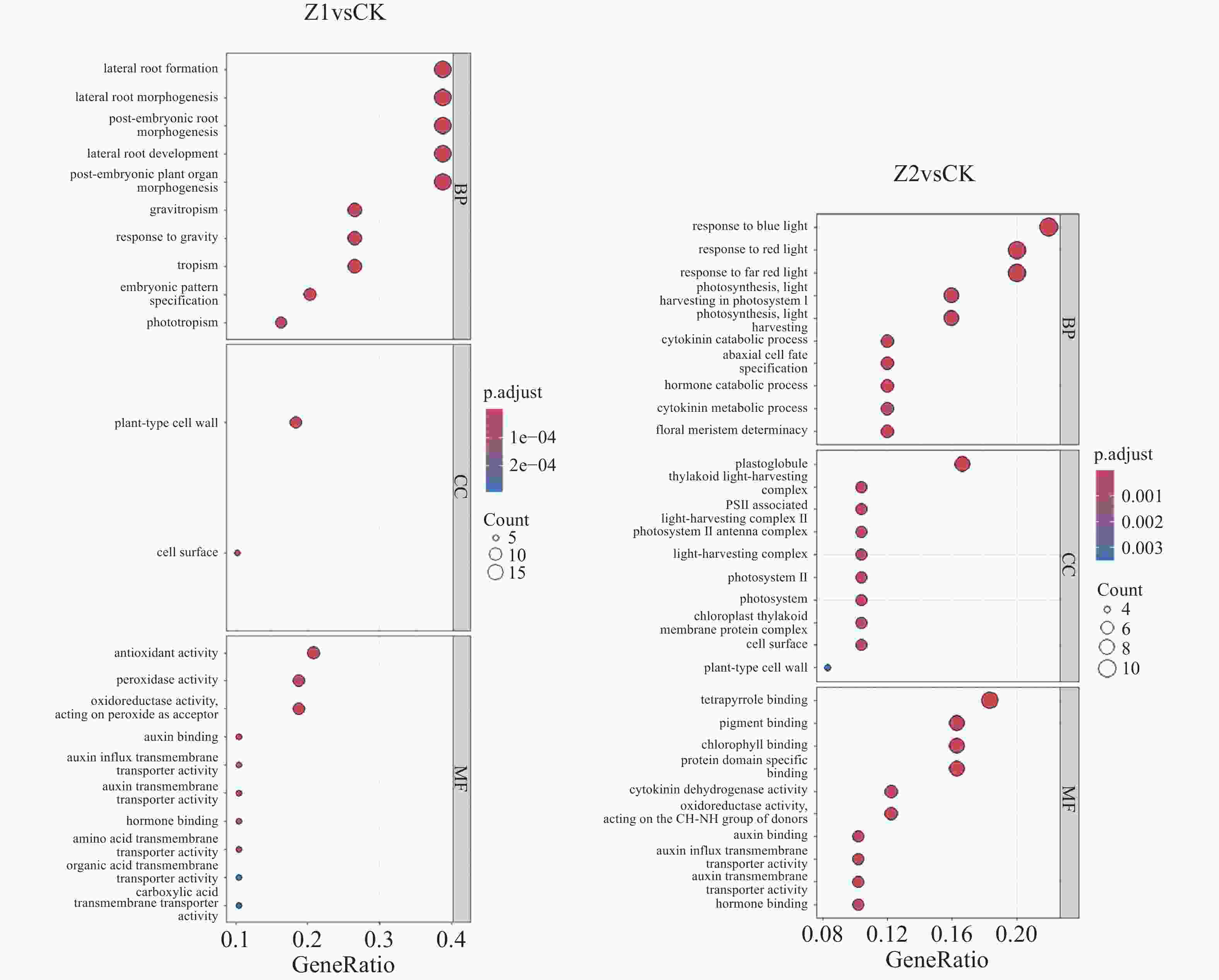
从图7可知,遮阴组Z1与对照组CK相比,生物学过程(BP)中基因差异比例大于0.1的有lateral root formation(侧根形成)、lateral root morphogenesis(侧根形态发育)、post-embryonic root morphogenesis(后生根形态发育)、lateral root development(侧根发育)、post-embryonic plant organ morphogenesis(后生植物器官形态发育)、gravitropism(向地性)、response to gravity(对重力的响应)、tropism(向性)、embryonic pattern specification(胚胎模式规范)、phototropism(向光性)。细胞成分(CC)中基因差异比例大于0.1的有plant-type cell wall(植物型细胞壁)、cell surface(细胞表面)。分子功能(MF)中基因差异比例大于0.1的有antioxidant activity(抗氧化活性)、peroxidase activity(过氧化物酶活性)、oxidoreductase activity,acting on peroxide as acceptor(以过氧化物为受体的氧化还原酶活性)。
遮阴组Z2与对照组CK相比,生物学过程(BP)基因差异比例大于0.1的有response to blue light(对蓝光的响应)、response to red light(对红光的响应)、response to far red light(对远红光的响应)、photosynthesis,light harvesting in photosystem Ⅰ(光合作用,光系统Ⅰ中的光捕获)、photosynthesis,light harvesting(光合作用,光捕获)、abaxial cell fate specification(背轴细胞命运决定)、cytokinin catabolic process(细胞分裂素分解代谢过程)、hormone catabolic process(激素分解代谢过程)、cytokinin metabolic process(细胞分裂素代谢过程)、floral meristem determinacy(花序分生组织决定性)。细胞成分(CC)基因差异比例大于0.1的有plastoglobule(质体小球)、thylakoid light-harvesting(类囊体光捕获)、PS Ⅱ(光系统Ⅱ)、light-harvesting complex Ⅱ(光捕获复合体Ⅱ)、photosystem Ⅱ antenna complex(光系统Ⅱ天线复合体)、light-harvesting complex(光捕获复合体)、photosystem Ⅱ(光系统Ⅱ)、photosystem(光系统)、chloroplast thylakoid membrane protein complex(叶绿体类囊体膜蛋白复合体)、cell surface(细胞表面)。分子功能(MF)基因差异比例大于0.1的有tetrapyrrole binding(四吡咯结合)、pigment binding(色素结合)、chlorophyll binding(叶绿素结合)、protein domain specific(蛋白质域特异性)、cytokinin dehydrogenase(细胞分裂素脱氢酶)、oxidoreductase activity(氧化还原酶活性)、auxin binding(生长素结合)、transporter activity(转运子活性)、auxin transmembrane(生长素跨膜转运)、auxin influx transmembrane(生长素内流跨膜转运)、hormone binding(激素结合)。
-
低光照水平(遮阴)对幼苗生长的影响具有双重性,适度的遮阴有助于幼苗的生长和发育,而过度的遮阴则会产生负面影响。如对于江南油杉幼苗来说,在遮阴率达到60%的条件下,其所受的光胁迫相对较小,从而有利于生物量的积累[7];轻度遮阴对莲叶桐幼苗的生长具有促进作用,有助于增加其生物量的积累[15]。然而,过度的遮阴则会削弱幼苗的光合作用[16],导致产生的养分不足以支持其生长需求,进而抑制其正常生长[17-18]。本研究发现,水椰幼苗在低光照水平下其超氧化物歧化酶(SOD)和过氧化物酶(POD)的活性会有所提升,MDA含量下降,可溶性蛋白维持稳定,叶绿素含量下降。
水椰幼苗在低光照水平下其超氧化物歧化酶(SOD)和过氧化物酶(POD)的活性会有所提升,有利于水椰幼苗适应低光照水平环境。这与孙彦等[19]和郭淑芸等[20]的研究结果一致。可溶性蛋白含量的下降,是逆境对植物造成的一种损害表现[21]。然而,耐阴性较强的植物在遮荫环境中,能够保持其可溶性蛋白的稳定含量,从而维持其正常生长和生理活动[22]。
O
$ {}_{2}^{-} $ 和H2O2是植物在代谢过程中产生的2种活性氧,它们对细胞膜脂质具有强烈的氧化损害作用,进而产生丙二醛(MDA)。适合水椰分布的年平均温为23.8~25.5 ℃,试验区域正午温度可达27 ℃以上,环境温度过高影响植物抗氧化系统清除活性氧的能力,在过度高温胁迫下,膜脂过氧化作用会被触发,导致酶活性中心的破坏、酶结构的改变或酶表达的抑制,未遮阴水椰的抗氧化酶通过增加活性来清除活性氧自由基的能力下降。水椰幼苗在较低的光照条件下的MDA含量降低与ZHANG等[23]的研究结果相符。一般植物应在低光照水平时增加叶绿素含量来维持稳定的光合速率,但本研究发现,遮阴20、30、40 d水椰幼苗的叶绿素含量比对照低。此结果产生可能是由于水椰幼苗是通过改变叶绿体的结构和功能,增加红光远红光的吸收,增长光合作用时间来维持稳定的光合产物累积造成的。
在荫阴条件下,可以减少水椰幼苗的蒸腾作用,使气孔导度增加,光合作用时间增加,更有利于植株的快速生长及生物量的增加[24]。SOD、POD活性提高,减少叶绿素含量生成,可溶性蛋白含量维持稳定的这些变化是提高水椰幼苗在低光环境下光能吸收和利用效率的重要策略。
-
本研究利用高通量测序技术对不同光照强度下遮阴40 d的水椰叶片进行转录组测序,筛选差异基因,获得了大量的数据和信息。遮荫组Z1与对照组CK相比,生物学过程(BP)中遮阴影响了植物幼苗的根系发育和形态发生过程。与对照组相比,遮阴组Z1的侧根形成增加,这有助于植物在光照不足的环境中扩大根系表面积,提高土壤资源的获取能力。同时,侧根形态发生和胚后根形态发生也发生了变化,使根系结构更加适应遮荫环境[25]。此外,植物还可以通过调节叶片微观结构来维持自身生理机能来适应外部光照变化[26]。细胞成分(CC)中遮荫对植物幼苗的细胞成分产生了显著影响。植物型细胞壁的成分和结构发生了调整,以适应遮阴环境。分子功能(MF)中遮阴导致植物幼苗的分子功能发生了广泛变化。过氧化物酶活性和氧化还原酶活性的调整有助于维持植物体内的氧化还原平衡,减轻由遮阴引起的氧化胁迫。抗氧化活性的增强有助于清除体内过多的活性氧,进而保护细胞免受氧化损伤。在激素调控方面,生长素结合与转运蛋白活性的变化,能够显著影响生长素在植物体内的分布和浓度。此外,激素结合和氨基酸跨膜转运蛋白活性的变化也反映了植物在遮阴环境中对激素和营养物质的利用和调控方式的调整。
遮阴组Z2与对照组CK相比,生物学过程(BP)中遮阴组Z2的光合作用及相关过程受到影响。由于光照减少,光系统Ⅰ中的光捕获能力发生变化,植物对红光、蓝光和远红光的响应也相应调整[27]。此外,细胞分裂素的分解代谢过程增强,这可能反映了植物在遮阴条件下对激素水平的精细调控。细胞成分(CC)中遮阴组Z2的光捕获复合体发生了显著变化。类囊体光捕获复合体、与光系统Ⅱ相关的光捕获复合体Ⅱ以及光系统Ⅱ天线复合体的差异变化,都表明植物在遮阴环境中对光能的捕获和利用进行了调整。此外,光系统Ⅱ、光系统以及藻蓝蛋白的变化也反映了植物在适应遮阴条件时叶绿体结构和功能的调整。叶绿体类囊体膜蛋白复合体的变化则可能影响了光能转换和电子传递的效率。分子功能(MF)中遮阴组Z2的色素结合能力发生了变化,这影响了植物对光的吸收和利用。叶绿素Ⅱ结合和四吡咯结合能力的改变也进一步证明了这一点。细胞分裂素脱氢酶的变化反映了植物在遮荫条件下对细胞分裂素的代谢调控。生长素结合和生长素流入跨膜转运蛋白活性的变化则影响了生长素在植物体内的分布和浓度,进而调控了植物的生长和发育。此外,氧化还原酶活性的变化,以及针对供体CH-NH基团起作用的氧化还原酶活性的变动,也反映了植物在遮阴环境中氧化还原状态的调整。
总而言之,水椰幼苗在低光照水平下(自然光照强度的20%、30%)拥有较高的抗氧化酶活性、较低的丙二醛含量、稳定的可溶性蛋白含量、低叶绿素含量和稳定的生物量,同时转录组差异分析发现,水椰幼苗在低光照水平下抗氧化酶、侧根形成、细胞壁组成、叶绿体对红光等基因表达差异显著。
水椰幼苗适应低光照环境的生理响应及转录组差异变化的研究
DOI: 10.15886/j.cnki.rdswxb.20240114
 CSTR: 32425.14.j.cnki.rdswxb.20240114
CSTR: 32425.14.j.cnki.rdswxb.20240114
Physiological response and transcriptome differential changes of Nypa fruticans seedlings under low light environment
-
摘要: 为了揭示水椰(Nypa fruticans)幼苗在低光照水平下的生理响应与转录组的差异变化,本研究通过遮荫试验,探究了水椰幼苗在低光照水平(CK为自然光强100%、Z1为自然光强30%、Z2为自然光强20%)下的生理变化和转录组表达差异。结果表明:低光照水平下水椰幼苗在40 d时,ZI的超氧化物歧化酶(SOD)活性比CK高57.1%,Z2比CK高62.1%,ZI的过氧化物酶(POD)活性比CK高41.2%,Z2比CK高35.7%,ZI的丙二醛(MDA)含量比CK低42.6%,Z2比CK低32.9%,ZI的叶绿素(Chl)含量比CK低61.1%,Z2比CK低70.3%,可溶性蛋白(SP)含量稳定无显著差异,ZI的根冠比比CK低57.6%,Z2比CK低48.1%。水椰幼苗在低光照水平的情况下,在10 d左右通过提升抗氧化酶活性、增加叶面积、侧根生长等方式来适应光照强度不足的环境变化。若是光照更弱,水椰会通过提高光吸收率和调节生长激素水平来适应环境变化。Abstract: An attempt was made to analyze the physiological changes and transcriptome expression differences in Nypa fruticans seedlings under low light levels (CK:100% of natural light intensity; Z1: 30% of natural light intensity; Z2: 20% of natural light intensity) through shading experiments to reveal the physiological responses and differential changes in the transcriptome of N. fruticans seedlings under low light levels, providing a scientific basis for the breeding of N. fruticans. The results indicated that at 40 days under low light conditions, the superoxide dismutase (SOD) activity in N. fruticans seedlings was 57.1% higher in Z1 and 62.1% higher in Z2 as compared to CK. Similarly, peroxidase (POD) activity was 41.2% higher in Z1 and 35.7% higher in Z2 compared to CK. Malondialdehyde (MDA) content was 42.6% lower in Z1 and 32.9% lower in Z2 compared to CK. However, chlorophyll (Chl) content was decreased by 61.1% in Z1 and 70.3% in Z2 compared to CK. Soluble protein (SP) content remained stable with no significant differences observed. The root-shoot ratio was 57.6% lower in Z1 and 48.1% lower in Z2 compared to CK. Under low light levels, N. fruticans seedlings were adapted to reduced light intensity within approximately 10 days by enhancing antioxidant enzyme activities, increasing leaf area, and promoting lateral root growth. Even in lower light availability, seedlings were further adapted to the environment by improving light absorption efficiency and regulating hormone levels.
-
Key words:
- Nypa fruticans /
- shading experiment /
- physiological response /
- transcriptome
-
图 6 差异表达基因分布图
-Log10 pvalue为对P值取以10为底的对数后再取负值;Log2 fold change中的fold change表示基因在2个样本之间的表达倍数变化。
Fig. 6 Distribution of differentially expressed genes
-Log10 pvalue is the negative value of the logarithm of the pvalue taken to the base of 10; Log2 fold change refers to the logarithm to the base of 2 of the fold change, where fold change represents the magnitude of change in gene expression between two samples.
表 1 各光照处理的相对光强
Table 1 Relative light intensity measured in the three light treatments
时间Time CK Z1 Z2 9:00 100 33.4 22.1 12:00 100 32.1 19.8 15:00 100 30.9 20.2 均值 Mean 100 32.3 20.7 表 2 遮阴40 d后水椰幼苗的生物量
Table 2 Biomass of Nypa fruticans seedlings after 40 days of shading
指标 Indicator Z1 Z2 CK 干质量 Dry weight/kg 0.128 ± 0.017ns 0.16 ± 0.016ns 0.106 ± 0.006ns 鲜质量 Fresh weight/kg 0.474 ± 0.062ns 0.534 ± 0.047ns 0.462 ± 0.032ns 根冠比 Root-shoot ratio 0.133 ± 0.025b 0.163 ± 0.023b 0.314 ± 0.034a 注:不同字母表示各光照处理之间存在显著差异(P < 0.05),ns表示无显著差异(P > 0.05)。 Note: Different letters indicate significant differences between various light treatments (P < 0.05); ns indicates no significant difference (P > 0.05). -
[1] 廖宝文. 红树林 中国海岸的"两栖植物"[J]. 森林与人类, 2019(3): 100 − 111. [2] 赖李佳子. 淇澳红树林湿地生态系统服务功能价值评估及其生态补偿研究 [D]. 广州: 华南师范大学, 2011. [3] 王萍, 刘立云, 陈思婷. 孑遗植物水椰的生物学特性及研究展望[J]. 中国野生植物资源, 2008, 27(3): 19 − 20. doi: 10.3969/j.issn.1006-9690.2008.03.006 [4] WIDODO P, SUKARSA, HERAWATI W, et al. Distribution and characteristics of Nypa palm (Nypa fruticans wurmb.) in southern part of cilacap regency[J]. IOP Conference Series: Earth and Environmental Science, 2020, 550(1): 012010. doi: 10.1088/1755-1315/550/1/012010 [5] 于永福. 中国野生植物保护工作的里程碑——《国家重点保护野生植物名录(第一批)》出台[J]. 植物杂志, 1999(5): 4. [6] 王文涛, 魏蓉, 徐幸酬, 等. 不同水分和光照处理对走马胎生理生化特性的影响[J]. 广西科学院学报, 2023, 39(4): 403 − 411. [7] 张培, 庞圣江, 刘士玲, 等. 遮荫对江南油杉幼苗生长和叶绿素荧光参数的影响[J]. 西北植物学报, 2023, 43(10): 1716 − 1722. doi: 10.7606/j.issn.1000-4025.2023.10.1716 [8] 张孟文, 钟才荣, 吕晓波, 等. 中国孑遗红树植物水椰的资源现状与种群特征[J]. 生态学杂志, 2023(42): 2918 − 2925. [9] 海口气象局信息网. 海口市气候概况[EB/OL]. [2024-06-24]. http://hkqx.net/Home/HaikouQX. [10] 朱一民, 李婷, 景宇杭, 等. 八种红树植物幼苗的叶片可溶性蛋白和抗氧化酶活性对光强的响应[J]. 广西植物, 2023, 43(4): 606 − 615. doi: 10.11931/guihaia.gxzw202203088 [11] GIANNOPOLITIS C N, RIES S K. Superoxide dismutases[J]. Plant Physiology, 1977, 59(2): 309 − 314. doi: 10.1104/pp.59.2.309 [12] 陈贻竹, 王以柔. 荔枝果实过氧化物酶 (POD) 的研究[J]. 中国科学院华南植物研究所集刊, 1989(5): 47 − 52. [13] 都浩, 王妮丽, 熊立仲. 水稻叶片中丙二醛(MDA)含量的测定[J]. Bio-protocol, 2018: e1010148. doi: 10.21769/BioProtoc.1010148. [14] 舒展, 张晓素, 陈娟, 等. 叶绿素含量测定的简化[J]. 植物生理学通讯, 2010, 46(4): 399 − 402. [15] 方赞山, 钟才荣, 程成, 等. 遮荫对莲叶桐幼苗生长及生物量分配的影响[J/OL]. 分子植物育种: 1−20. (2023-06-12)[2024-06-27]. http://kns.cnki.net/kcms/detail/46.1068.S.20230612.1151.004.html. [16] 陶巧静, 吴月燕, 付涛, 等. 弱光胁迫对西洋杜鹃生理特性和叶片超微结构的影响[J]. 林业科学, 2015, 51(3): 84 − 92. [17] 智西民, 王梦颖, 牛畔青, 等. 遮荫对青桐幼苗生长性状与化学计量特征的影响[J]. 生态学杂志, 2021, 40(3): 664 − 671. [18] 战丽杰, 张宏宝, 李宗泰, 等. 遮荫处理对芍药幼苗生长和矿质营养积累的影响[J]. 应用生态学报, 2020, 31(10): 3473 − 3479. [19] 江佳琳, 孙彦. 遮荫强度对不同来源白颖苔草形态和生理指标的影响[J]. 草地学报, 2013, 21(6): 1136 − 1143. [20] 李先民, 李春牛, 刘新亮, 等. 遮阴对杜鹃红山茶幼苗叶片生长特性及初生代谢的影响[J]. 西北植物学报, 2019, 39(2): 294 − 301. doi: 10.7606/j.issn.1000-4025.2019.02.0294 [21] DENG Y, LI C, SHAO Q, et al. Differential responses of double petal and multi petal jasmine to shading: Ⅰ. Photosynthetic characteristics and chloroplast ultrastructure[J]. Plant Physiology and Biochemistry: PPB, 2012, 55: 93 − 102. doi: 10.1016/j.plaphy.2012.03.006 [22] 郭淑芸, 朱亚祥, 李铁华. 遮荫与加氮对青冈栎幼苗生长与生理特性的影响[J]. 西南林业大学学报(自然科学), 2024, 44(6): 1 − 10 [23] ZHANG M, ZHANG G. A new combination of Caragana(Fabaceae)from China[J]. Zhiwu Yanjiu, 2004, 24(1): 5 − 6. [24] 苏泽阳, 杨再强, 龙宇芸, 等. 寡照条件下补光频率对番茄幼苗叶片光合特性的影响[J]. 中国农业气象, 2022, 43(9): 720 − 731. doi: 10.3969/j.issn.1000-6362.2022.09.004 [25] ZHANG W, FANG D, DONG K, et al. Insights into the environmental factors shaping lateral root development[J]. Physiologia Plantarum, 2023, 175(2): e13878. doi: 10.1111/ppl.13878 [26] 王玟玥,赵丹丹,张鸽香,等. 毛茛科3种植物在遮光下叶片解剖结构比较及耐阴性评价[J]. 南方农业学报, 2024, 55(6): 1713 − 1723. 王玟玥,赵丹丹,张鸽香,等. 毛茛科3种植物在遮光下叶片解剖结构比较及耐阴性评价[J]. 南方农业学报, 2024, 55(6): 1713 − 1723. [27] XIE X, CHENG H, HOU C, et al. Integration of light and auxin signaling in shade plants: from mechanisms to opportunities in urban agriculture[J]. International Journal of Molecular Sciences, 2022, 23(7): 3422. doi: 10.3390/ijms23073422 -




 下载:
下载: