-
我国部分沿海区域的海水和沉积都面临较严峻的重金属污染。位于热带和亚热带地区潮间带的红树林生态系统在海洋重金属生态修复过程中具有独特作用,红树林沉积作为重金属的储存库,能有效阻断重金属在食物链中的传递和富集[1-2],这主要与红树林沉积的一些特征密切相关。红树林沉积中硫含量通常较高(0.2%~0.4%),远高于土壤平均含硫量(0.07%)[3-6],另一方面,沉积中有机质含量高,厌氧沉积环境为硫酸盐还原菌的活动提供了良好条件,原位沉积中的硫酸盐还原菌(SRB)在分解红树林沉积中的有机物质时,丰富的硫被还原成大量S2−,S2−与重金属离子结合成生物难以利用的金属硫化物,从而降低重金属的毒性危害。SRB在红树林湿地生态系统中的物质循环和污染物净化过程中起着关键作用,因此,研究者们围绕红树林沉积中的SRB,在不同地域展开了相关研究[7-9]。丁海等[10]使用选择性培养基从东寨港红树林湿地的沉积样本中分离出11株厌氧硫酸盐还原菌,通过16S RNA测序技术鉴定其归属于6个属,即芽孢杆菌属(Bacillus)、弧菌属(Vibrio)、梭状芽孢杆菌属(Clostridium)、伯克霍尔德菌属(Burkholderia)、希瓦氏菌属(Shewanella)、海杆菌属(Marinobacterium);Alzubaidy 等[11]通过454-焦磷酸测序技术在红海红树植物海榄雌(Avicennia marina)根际微生物宏基因组的研究中,发现SRB占优势,且以δ-变形菌纲(Deltaproteobarteria)为主; Varon-lopez 等[12]分析巴西红树林沉积中硫氧化细菌和硫酸盐还原菌的丰度和群落结构,显示Deltaproteobacteria (δ-变形菌纲)丰度最大,在属分类水平上以脱硫杆菌和脱硫弧菌为主;Cabral等[13]通过宏转录组学研究巴西圣保罗州海岸红树林沉积中的微生物,发现自养脱硫杆菌(Desulfobacterium autotrophicum)在沉积中起着重要的抗重金属污染作用。王原[9]采用高通量测序技术发现珠江广州段沉积中的SRB主要类群为互营菌与厚壁菌、脱硫弧菌、脱硫杆菌及硝化螺旋菌四个分类族。采用基于功能基因dsrB的高通量测序技术研究硫酸盐还原菌群落结构,发现长江口及东海附近沉积中的硫酸盐还原菌主要为脱硫球茎菌科(Desulfobulbaceae)、互营杆菌科(Syntrophobacteraceae)、脱硫杆菌科(Desulfobacteraceae)、蛋白胨球菌科(Peptococcaceae)4个科[14]。这些研究揭示了海洋沉积中SRB群落的组成和结构特征,反映出SRB的多样性和地域性分布特点。目前,对红树林沉积中SRB群落的季节性变化以及SRB与沉积重金属赋存形态的关联性还未见相关研究报道。本研究采用高通量测序技术,研究了海南东寨港红树林沉积中SRB在不同季节下的群落结构差异,分析SRB群落结构与沉积理化性质、重金属赋存形态的相关性,为阐明红树林沉积中SRB在重金属生态修复过程中的作用提供依据。
-
采样地点位于海南岛东寨港红树林自然保护区附近(E110°32′~110°37′,N19°51′~20°1′),为热带海洋性季风气候,年平均气温23.8℃,水体表面温度年均24.5℃,年均降雨量为1676 mm;呈不规则全日潮,潮差平均约1.0 m;采样地点处的沉积主要以粉砂质和淤泥质为主,其沉积的厚度一般在0.1~1.5 m之间,有机质的含量较为丰富[15-16]。此处红树林主要由大面积生长的白骨壤 (Avicennia marina) 组成,林分郁闭度高,在林中穿行非常困难。
-
分别于2019年旱季(1月)和雨季(10月),在采样场地选择无可见人为干扰的区域,在红树林内以及林外无植被覆盖的低潮光滩区域分别采集表层沉积样品。样品的采集厚度为沉积表面以下0~5.0 cm之间的沉积物。每采样区域为3个平行样。挑出样品中的树枝、落叶和大型底栖动物等,每个样品均分为两部分,一部分迅速装入已灭菌的离心管中,置于冰盒中送回实验室,−80℃保存,用于微生物群落分析实验;另一部分样品封入样品袋,用于沉积样品的重金属赋存形态及沉积的理化性质检测。
-
在采集沉积样品前,现场测定沉积表层温度。使用pH计(梅特勒-托利多,FE-20)测量新鲜湿样的pH值(水土比为1∶1)。采用EDTA容量法测量Fe3+/Fe2+[17]。采用重量法测量沉积含水率[18]。 采用烧失量法测沉积的烧失量(LOI)。参照海洋调查规范第八部分[17]使用综合法对沉积中的粒径进行分析,参照Folk沉积三角分类图解对沉积进行分类和命名,拟合出各沉积的概率累积曲线之后,采用Folk和Ward公式计算各沉积的中值粒径。沉积样品经风干、研磨、过筛(120目标准筛)、消煮后,使用连续流动分析仪(AMS-Alliance,PROMIXA)进行总氮(TN)和总磷(TP)的测试。
采用改进BCR分步提取法[19]提取分析沉积中重金属的各赋存形态,包括可溶性金属离子、铁锰氧化物结合态金属、有机物/硫化物结合态金属和残渣态。经分步提取的样品烘干之后,采用微波消解法进一步消解重金属残渣态。使用原子吸收光谱仪(北京普析通用,TAS-990 Super AFG)分析沉积中重金属铜和锌的含量。
-
采用OMEGA M5635-02 (OMEGA公司)试剂盒提取沉积样品中总DNA。利用Nanodrop NC2000(Thermo Scientific)检测DNA质量,使用PCR扩增仪(ABI 2720) 扩增dsrB基因。扩增引物序列为DSR-p2060F(5′-CAA CAT CGT YCA YAC CCA GGG),DSR-4R(3′-GTG TAG CAG TTA CCG CA)[8]。PCR反应条件:在98℃预变性2 min;在98℃变性15 s,55℃退火30 s,72℃延伸30 s,25个循环,最后72℃延伸5 min 使用凝胶回收试剂盒(AXYGEN公司)进行纯化。最后采用MiSeq-PE250测序平台进行高通量测序(上海派森诺生物技术有限公司),最大读取长度为2×300 bp双末端测序,试剂盒为MiSeq Reagent Kit V3。
-
使用OriginPro 2020软件分析沉积样品的理化性质相关数据。使用QIIME软件,调用UCLUST这一序列比对工具,按照97%的序列相似度对OTUs(operational taxonomic units, 可操作分类单元)进行归并、划分,之后采用NCBI数据库作为OTU分类地位鉴定的模板序列,获得OTU丰度矩阵。获得OTU丰度矩阵之后,使用QIIME软件分别对每个样本计算Alpha多样性指数。使用OriginPro 2020软件进行α多样性指数差异显著性分析、SRB分类组成分析、SRB丰度聚类分析以及Pearson相关性分析。使用Canoco5进行冗余分析。
-
比较旱季和雨季沉积的理化性质特征(表1),发现沉积类型均为粉砂质砂,旱季沉积以及红树林内沉积的中值粒径相对较高。与旱季相比,雨季的烧失量(LOI)值、TN含量均较高,但TP含量较低;含水率和pH没有显著差异。
表 1 沉积理化性质
样品 含水率/% LOI/% Fe3+/Fe2+ TN/(mg·kg−1) TP/
(mg·kg−1)pH 温度/℃ 粒径/μm DA 35.59±0.47a 6.13±0.31a 0.79±0.04b 405.33±10.06d 447.64±8.99a 6.92 17.0 132.83 DB 34.19±0.34b 7.33±0.24a 0.32±0.01c 606.91±30.16c 248.22±5.35b 6.46 17.5 151.53 RA 35.75±0.20a 6.30±0.093a 1.20±0.097a 1088.67±30.01b 143.60±61.50c 7.11 27.8 111.60 RB 35.75±0.47a 14.68±0.51a 0.33±0.03c 1505.00±68.46a 106.53±1.33c 6.34 26.3 143.53 注:DA-旱季光滩,DB-旱季林内,RA-雨季光滩,RB-雨季林内; TN-总氮,TP-总磷;a、b、c和d为显著性( P <0.05)差异标记,下同。 -
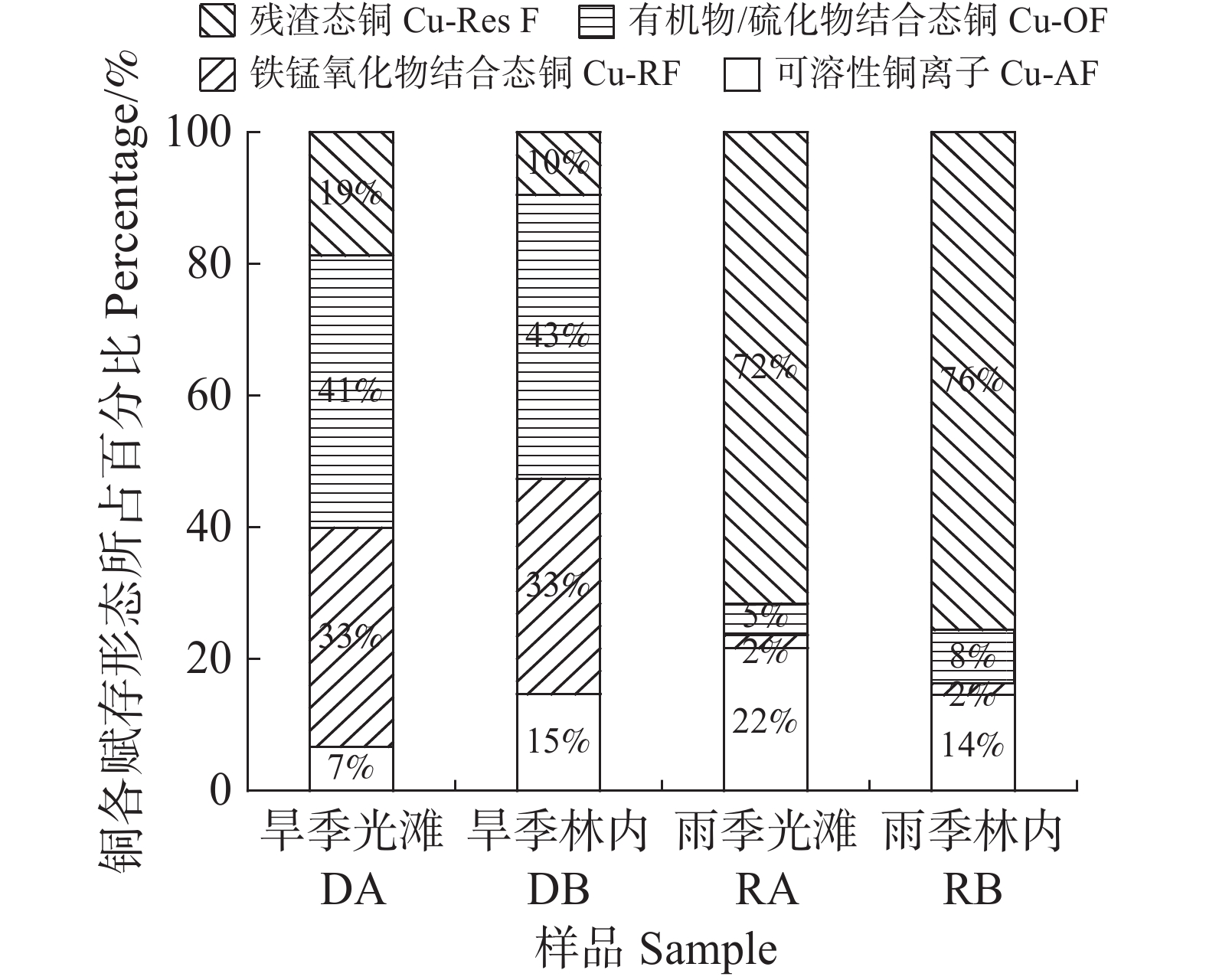
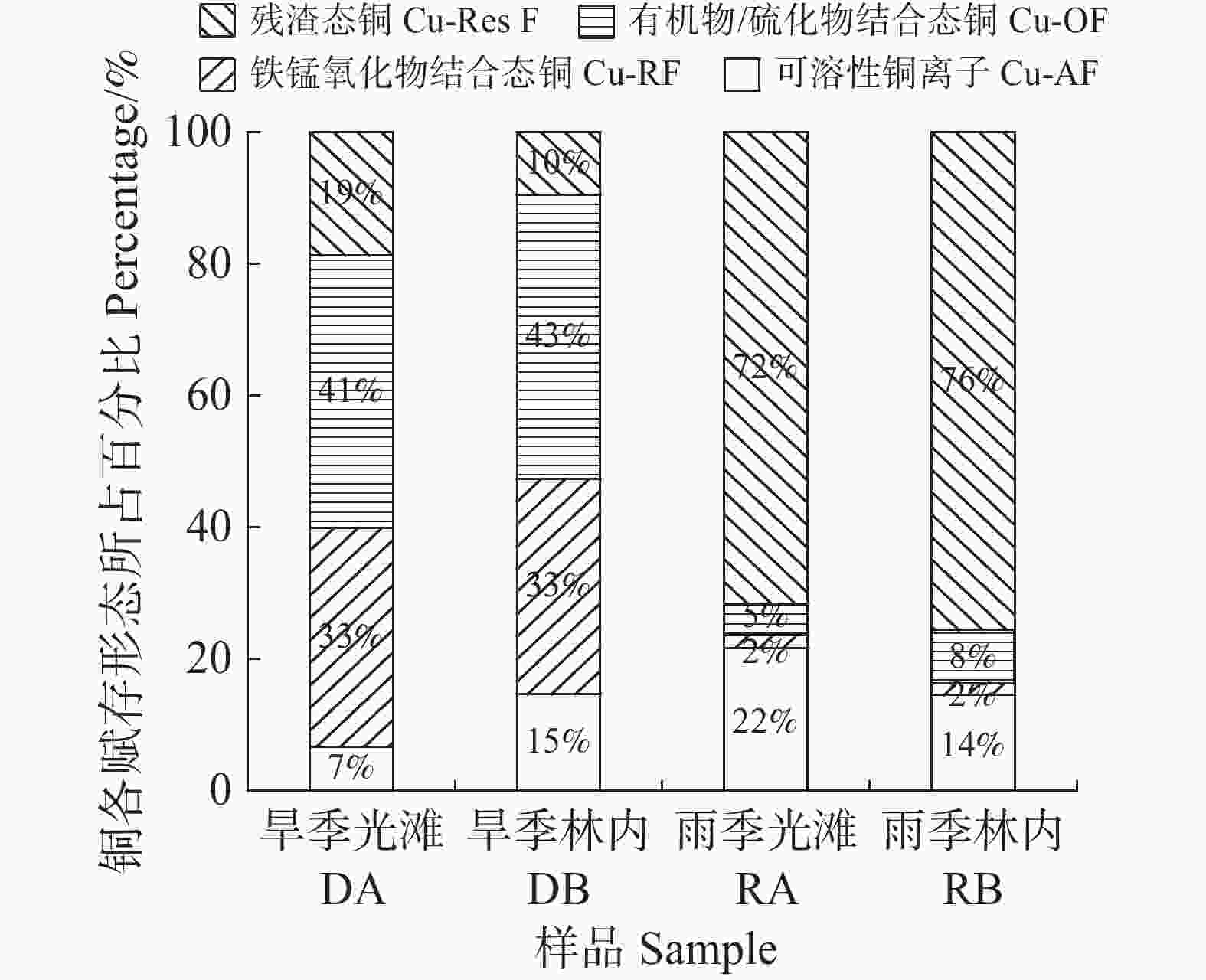
研究区域沉积中铜的总含量随季节变化明显,旱季光滩沉积中铜的总含量(35.19 mg·kg−1)是雨季的430%;旱季林内的铜含量是雨季林内的410%。在同一个季节,在光滩与红树林内的沉积中,铜的总含量都相近。在旱季,沉积中铜主要以铁锰氧化物结合态(Cu-RF)、有机物/硫化物结合态(Cu-OF)为主,其中,在光滩和林内,Cu-RF占比都为33%,OF分别为41%和43%;而可溶性铜离子(Cu-AF)含量较低,分别占7%和15%。在雨季,沉积中的铜主要以残渣态(Cu-Res F)为主,在光滩和林内Cu-Res F占比分别达到了72%和76% (表2,图1)。此外,旱季红树林沉积中可溶性铜离子含量(Cu-AF)是光滩的220%,而在雨季,林内的Cu-AF略低于光滩的。
表 2 不同沉积中铜的赋存形态量化分析
样品 Cu-AF/(mg·kg−1) Cu-RF/(mg·kg−1) Cu-OF/(mg·kg−1) Cu-Res F/(mg·kg−1) Cu总量/
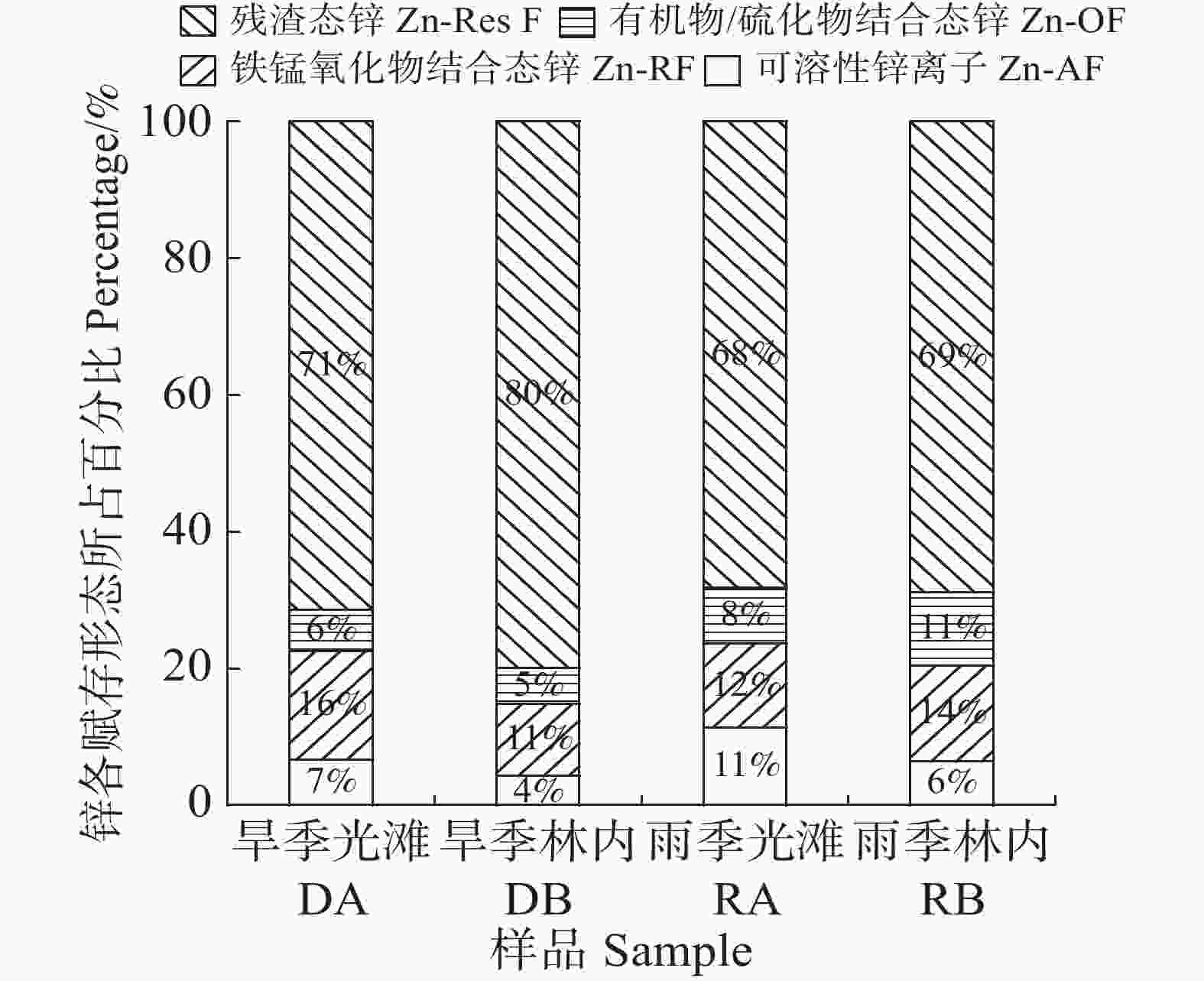
(mg·kg−1)DA 2.36±0.73b 11.7±1.21a 14.54±0.61a 6.60±0.46a 35.19±0.63a DB 5.19±0.52a 11.6±0.58a 15.28±1.73a 3.37±0.30b 35.43±1.15a RA 1.78±0.22b 0.16±0.14b 0.39±0.37b 5.90±0.78a 8.23±0.85b RB 1.26±0.12b 0.15±0.02b 0.71±0.57b 6.57±1.50a 8.69±1.15b 注:a和b为显著性差异标记。 在旱季和雨季的沉积中,锌都以残渣态(Zn-Res F)为主,其中,旱季与雨季的Zn-Res F所占比例相差不大,旱季林内的Zn-ResF所占比例略高于光滩的 (表3,图2);此外,旱季光滩沉积中可溶性锌离子 (Zn-AF) 含量是林内沉积的150%,而雨季此比值达210%;其余两种赋存形态锌的比例在旱季和雨季之间相差不大。
表 3 不同沉积中锌的赋存形态量化分析
样品 Zn-AF/
(mg·kg−1)Zn-RF/
(mg·kg−1)Zn-OF/
(mg·kg−1)Zn-Res F/
(mg·kg−1)Zn总量/
(mg·kg−1)DA 4.14±1.73ab 9.99±0.67a 3.79±1.08a 44.71±12.95a 62.63±10.52a DB 2.69±0.31b 6.75±0.38a 3.33±2.18a 50.89±5.72a 63.65±4.33a RA 5.94±0.39a 6.44±0.77a 4.32±2.17a 35.75±6.81a 52.43±5.23a RB 2.88±0.76b 6.37±4.09a 4.85±2.47a 31.15±10.20a 45.26±15.68a 注:a和b为显著性差异标记。 -
α多样性又称为生境内的多样性,指局域均匀生境下的物种多样性。常用Shannon多样性指数反映alpha多样性。Shannon值越大,表明群落多样性越高。旱季光滩沉积SRB群落的Shannon多样性指数最高,而雨季红树林内的最低。不论在旱季或雨季,光滩沉积SRB群落的Shannon指数都显著高(P<0.05)于红树林内的;而且,不论在光滩还是林内的沉积,旱季SRB群落的Shannon指数都显著(P<0.05)高于雨季的(表4)。
表 4 沉积中SRB的α多样性指数
样品 Shannon指数 Chao1指数 ACE指数 DA 9.71±0.093a 2278.40±150.33a 2406.14±161.95a DB 8.86±0.087 c 1840.54±179.54ab 1970.19±226.97ab RA 9.23±0.180 b 1898.19±351.04ab 1941.05±333.23ab RB 8.22±0.089 d 1588.67±197.46b 1656.44±203.55b Chao1指数用来估计物种总数,Chao1指数越大,表明OTU数目越多,该样本的物种数越多。ACE指数也常用来估计群落中OTU数目。Chao1指数或ACE指数表示沉积中SRB群落丰富度,在旱季光滩与雨季林内的样品中呈现显著差异 (P<0.05),其他各样品之间无显著差异(表4)。
-
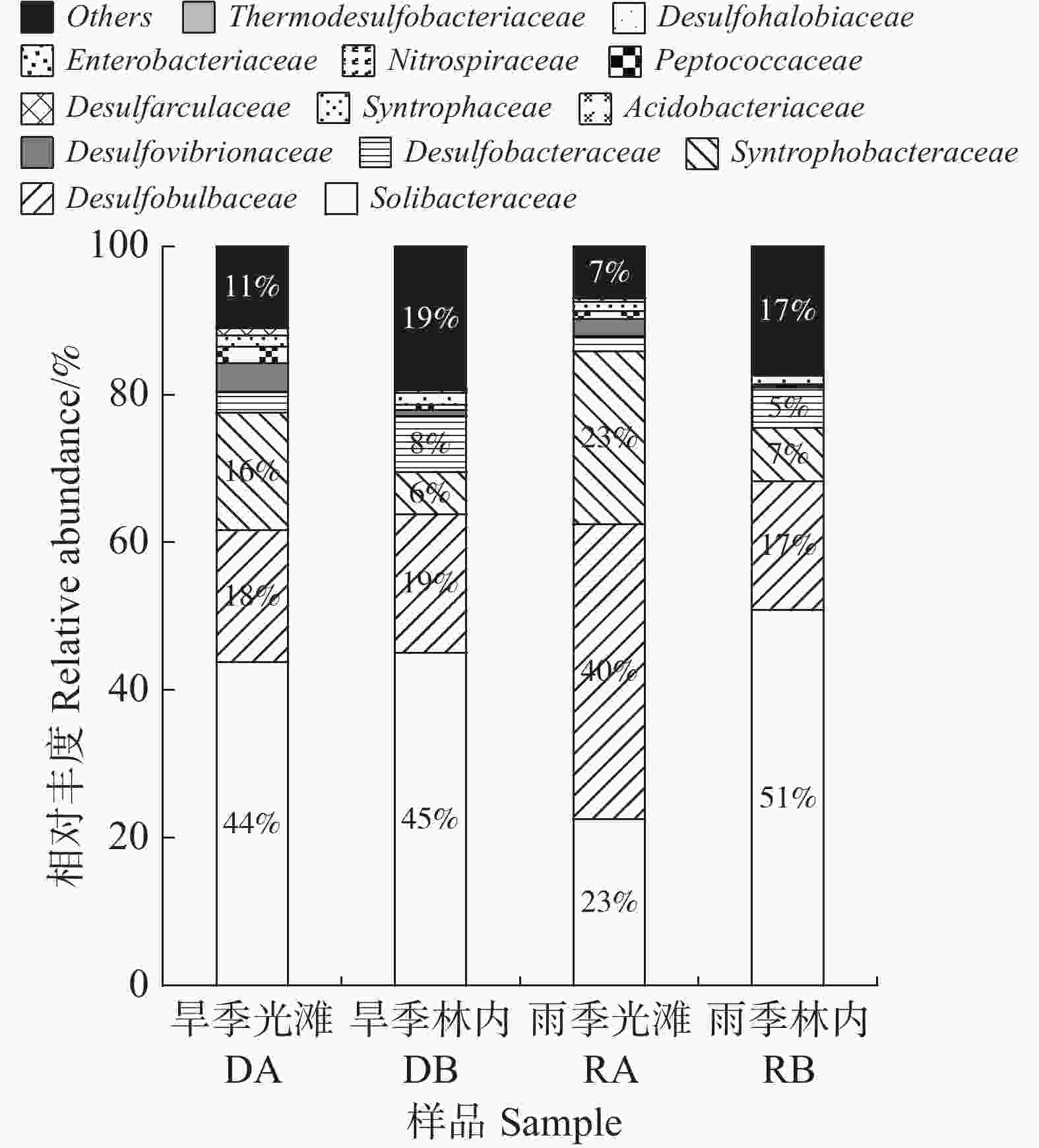
在所检测的沉积中发现硫酸盐还原菌隶属13个科,这些科都存在于4类沉积样品中,各科的相对丰度有差异,优势科都为索利氏菌科(Solibacteraceae),脱硫球茎菌科(Desulfobulbaceae), 互营杆菌科(Syntrophobacteraceae)和脱硫杆菌科(Desulfobacteraceae),4个优势科的相对丰度分别占了81% (DA旱季光滩)、78%(DB旱季林内)、88%(RA雨季光滩)、80%(RB雨季林内)。在旱季,光滩和林内沉积中索利氏菌科(Solibacteraceae)的相对丰度分别为44%与45%,脱硫球茎菌科(Desulfobulbaceae)的相对丰度分别为18%与19%,可见,这两个优势科的相对丰度在光滩与林内沉积中相近;但互营杆菌科(Syntrophobacteraceae)和脱硫杆菌科(Desulfobacteraceae)的相对丰度在光滩和林内的差异较大,互营杆菌科(Syntrophobacteraceae)相对丰度在光滩的(16%)是林内(6%)的267%,而脱硫杆菌科(Desulfobacteraceae)相对丰度在光滩的(3%)只有林内(8%)的37.5%。在雨季,光滩中索利氏菌科(Solibacteraceae)的相对丰度(23%)不及林内(51%)的1/2,但光滩中脱硫球茎菌科(Desulfobulbaceae)的相对丰度(40%)是林内的(17%)235%,互营杆菌科(Syntrophobacteraceae)的相对丰度(23%)是林内(7%)的328% (图3)。沉积中SRB的优势科随季节呈现明显变化。在光滩,雨季沉积中索利氏菌科(Solibacteraceae)和脱硫杆菌科(Desulfobacteraceae)的相对丰度较低,分别是旱季的52.3%和66.7%,而脱硫杆菌科(Desulfobulbaceae)和互营杆菌科(Syntrophobacteraceae)相对丰度较高,分别是旱季的220%和140%。在红树林内,雨季沉积中索利氏菌科(Solibacteraceae)和互营杆菌科(Syntrophobacteraceae)的相对丰度略高于旱季,分别是旱季的110%和120%,而脱硫球茎菌科(Desulfobulbaceae)和脱硫杆菌科(Desulfobacteraceae)的相对丰度低于旱季,分别是旱季的89.4%和62.5%。
-
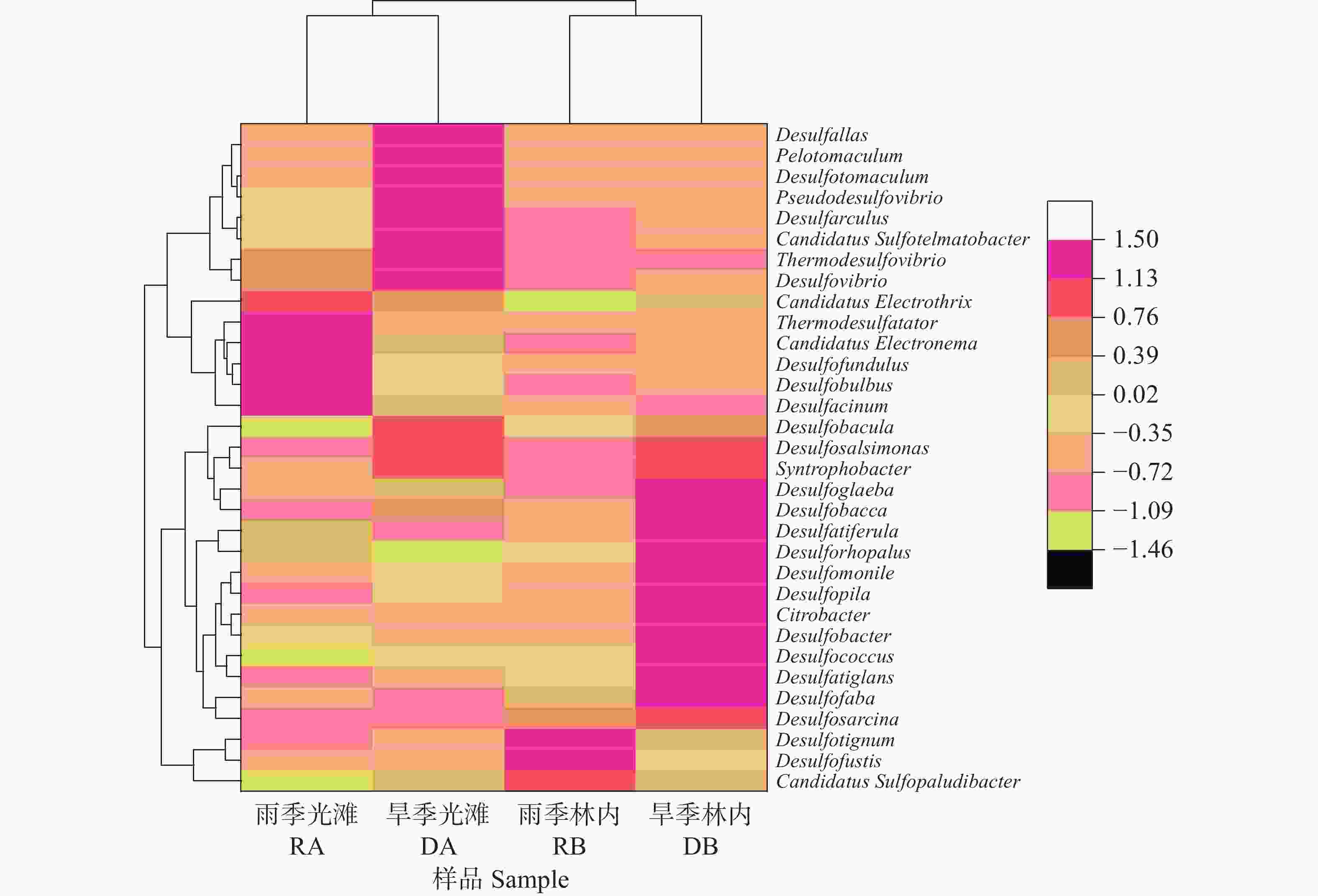
SRB的相对丰度聚类热图(图4)展现了32个属的相对丰度在各样本之间的差异。聚类分出光滩和林内两类,显示红树林林内与附近光滩沉积中SRB群落结构的差异,其特点是相对丰度较高的属各不相同,即在光滩沉积中相对丰度较高的SRB各属在林内则较低,如热脱硫杆菌属(Thermodesulfatator)、电缆细菌(Candidatus Electronema)、Desulfofundulus、脱硫球茎菌属(Desulfobulbus)、脱硫葡萄状菌属(Desulfacinum)等;而在光滩沉积中相对丰度较低的SRB各属在林内则较高,如Desulfoglaeba、Desulfobacca、Desulfatiferula、脱硫管状菌属(Desulforhopalus)、脱硫念珠菌属(Desulfomonile)、Desulfopila等。
此外,光滩沉积中SRB的相对丰度也呈现季节性差异,如热脱硫杆菌属(Thermodesulfatator)、电缆细菌(Candidatus Electronema)、Desulfofundulus、脱硫球茎菌属(Desulfobulbus)、脱硫葡萄状菌属(Desulfacinum)在雨季相对丰度较高,而在旱季相对丰度较低,Desulfallas、Pelotomaculum、脱硫肠状菌属(Desulfotomaculum)、Pseudodesulfovibrio、脱硫盒菌属(Desulfarculus)、Candidatus Sulfotelmatobacter、Thermodesulfovibrio在雨季相对丰度较低而在旱季相对丰度较高;林内沉积中的Desulfotignum、Desulfofustis在雨季相对丰度较高,而在旱季相对丰度较低,Desulfoglaeba、Desulfobacca、Desulfatiferula、脱硫管状菌属(Desulforhopalus)、脱硫念珠菌属(Desulfomonile)、Desulfopila、柠檬酸杆菌属(Citrobacter)、脱硫杆菌属(Desulfobacter)、脱硫球菌属(Desulfococcus)、Desulfatiglans、Desulfofaba在雨季相对丰度较低而在旱季相对丰度较高。
-
α多样性指数与理化因子的相关性分析显示(表5),pH、Fe3+/Fe2+与Shannon指数呈现显著正相关;总氮(TN)、总磷(TP)与3个α多样性指数均呈现显著相关,其中TN呈现负相关,TP呈现正相关。
表 5 α多样性指数与理化性质的Pearson相关性分析
α多样性
指数含水率 LOI Fe3+/Fe2+ TN TP pH 温度 Shannon 0.037 −0.55 0.64* −0.78* 0.78* 0.80* −0.45 Chao1 0.035 −0.57 0.41 −0.65* 0.80* 0.53 −0.48 ACE −0.053 −0.55 0.33 −0.70* 0.84* 0.47 −0.57 注: *显著相关(p<0.05,n=12) 分析α多样性指数与铜和锌赋存形态的相关性,发现Cu-RF、Zn-RF与ACE指数呈现显著正相关(p<0.05)(表6)。
表 6 α多样性指数分别与铜和锌赋存形态的Pearson相关性分析
α多样性
指数Cu-
AFCu-
RFCu-
OFCu-
Res FZn-
AFZn-
RFZn-
OFZn-
Res FSimpson 0.07 0.51 0.50 0.11 0.43 0.49 −0.07 0.34 Chao1 0.05 0.50 0.48 0.25 0.26 0.56 0.08 0.17 ACE 0.11 0.58* 0.56 0.15 0.17 0.62* 0.03 0.26 Shannon 0.08 0.50 0.48 0.12 0.45 0.52 −0.09 0.37 注:*显著相关(P<0.05,样本数n=12) -
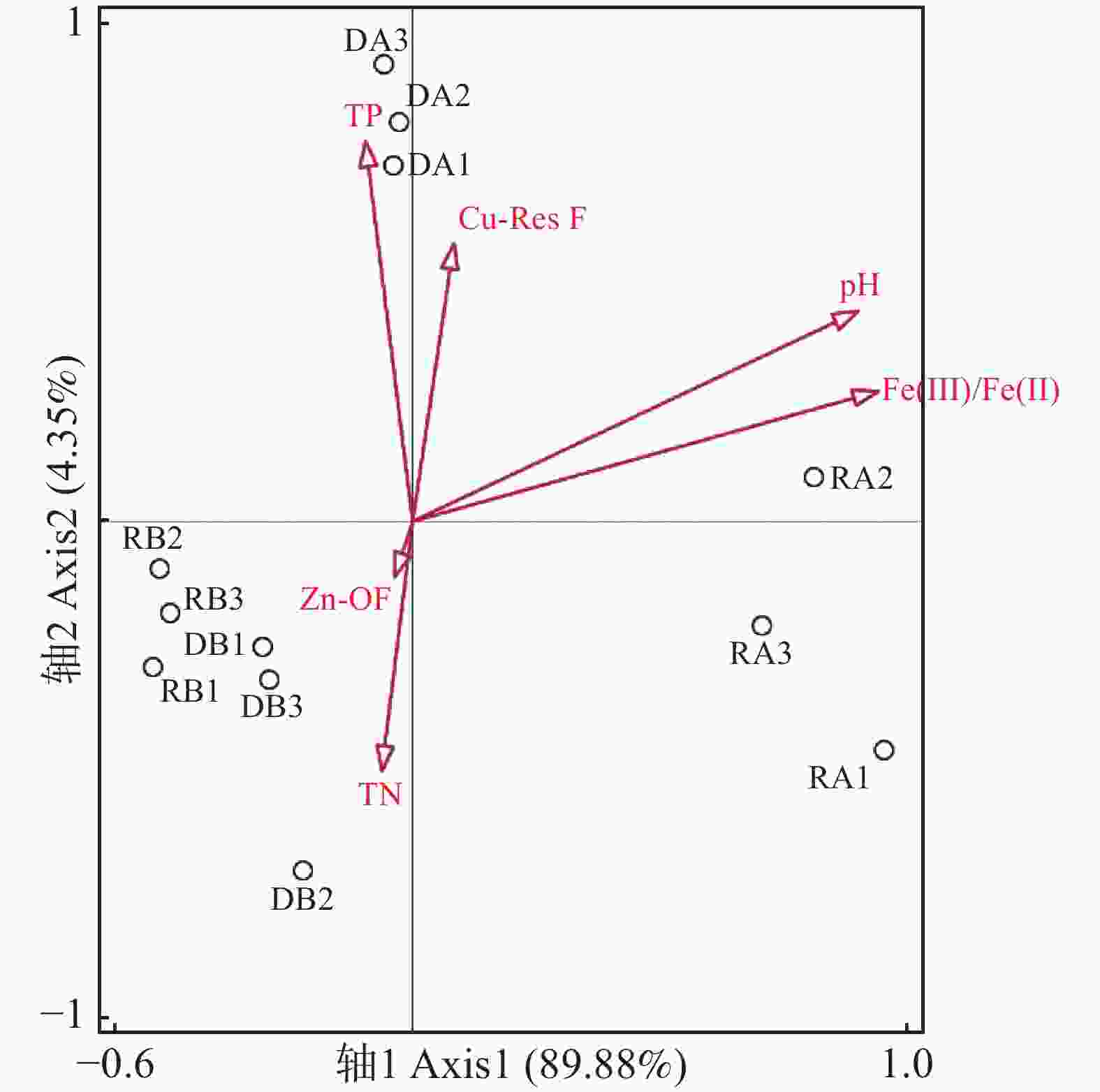
以高通量测序检测出的OTUs对应SRB群落中的物种,进行DCA分析(Detrended Correspondence Analysis),得到排序轴的最大梯度长度小于3.0, 因此选择线性模型冗余分析(RDA)解析理化因子对SRB群落影响(图5)。采用近似F检验和蒙特卡罗检验,综合分析筛选出环境因子中的pH、Fe3+/Fe2+、总氮、总磷、Cu-Res F、Zn-OF用于RDA分析,其中,pH、Fe3+/Fe2+为第一排序轴的主要影响因素,总氮、总磷、Cu-Res F、Zn-OF为第二排序轴的主要影响因素,这两个排序轴对微生物群落组成变化的解释程度达96.2%。影响SRB群落结构的主要影响因子是pH、Fe3+/Fe2+和TP。
-
华南滨海盐土的重金属环境背景值为Cu:(10.5 ± 5.18) mg·kg−1;Zn:(51.9 ± 29.6 )mg·kg−1[20], 2013年和2014年8月(雨季)东寨港红树林沉积的重金属含量为Cu:13.5 mg·kg−1,19.62 mg·kg−1;Zn:54.8 mg·kg−1,44.84 mg·kg−1[21],本次检测的雨季沉积样品中铜含量均低于以上数据,锌含量均与之相近。通常情况下,在重金属常见的4类赋存形态中,残渣态的稳定性最高,生态风险也相应较低;沉积中可氧化态的重金属相对稳定;而可还原态和酸可提取态重金属的生态风险较大[22-23]。实验结果显示沉积中重金属铜和锌的含量及其赋存形态随季节呈现明显差异,显示重金属的生态风险随季节发生明显变化。旱季红树林内外沉积中铜和锌的总含量都高于雨季的,实验场地周围不存在季节性变化的外源重金属输入,推测这可能与当地季节性气候特征相关。雨季时充沛的降雨和积水对浅表层沉积中的重金属浓度有一定的稀释,而且沉积中部分重金属也会随着降雨时暂时形成的小溪流入海洋,从而降低了沉积中重金属的含量;此外,红树植物白骨壤对重金属铜和锌都有一定的吸收作用[24],但其吸收能力是否存在季节性差异还有待进一步研究。在雨季,沉积中70%以上的铜为不易被生物利用的残渣态形式存在,但在旱季,残渣态铜占比不足20%,推测在研究位点区域铜的生态风险在旱季时高于雨季。此外,沉积中68%以上的锌以残渣态赋存形式,可见在研究区域锌的潜在生态风险不高,而且红树林沉积中锌的生态风险均低于光滩沉积的。
本研究在科和属分类水平上检测出的SRB各类群在实验样品中均有出现。在本实验沉积样品中的优势科脱硫球茎菌科(Desulfobulbaceae)和脱硫杆菌科(Desulfobacteraceae),在位于亚寒带地区的丹麦奥胡斯海滩(Aarhus Bay)表层沉积的SRB群落中也以超过50%的相对丰度占优势[25]。这与以往的研究结果类似,很多SRB类群具有较强的环境适应性,能在富含有机质和硫酸盐的低氧或厌氧沉积中广泛分布[26]。
实验还发现SRB各类群在不同样品中的相对丰度以及相应的多样性和群落结构都呈现差异,特别是不同样品中SRB相对丰度较高的属各不相同,推测这可能是SRB群落中不同属对环境因子响应不同而造成的。相关性分析揭示沉积中TN、TP、Cu-RF和Zn-RF显著影响SRB优势类群的相对丰度。与已有研究比较,除了本实验考虑重金属因素外,影响SRB群落结构的环境因子也呈现多样化差异。如在我国东海海域表层沉积中,温度、盐度、TOC及溶解无机氮是影响SRB群落结构季节性变化的主要因素[27-28];而胶州湾养殖区沉积物中的 SRB数量只与硫化物成显著正相关[29];在东太平洋大陆边缘的沉积中发现,SRB群落的多样性与碳可利用性密切相关[30];在闽江河口芦苇、短叶茳芏和互花米草沼泽湿地土壤的SRB群落组成结构与pH呈极显著相关,与土壤含水量显著相关[31];在云南洱海沉积中,春季和秋季SRB群落结构的不同与溶氧和温度相关 [32];乌梁素海湖滨湿地沉积物中的铵态氮和含水率对SRB 群落结构影响显著[33];在沙特阿拉伯红海海滨地区两种不同状态的红树林中,研究者们发现与未被啃食的红树林相比,暴露于动物啃食和潮水中的红树林沉积中SRB群落组成结构发生显著变化[34],显示外界干扰影响沉积中SRB群落结构。这些研究揭示海洋沉积中SRB的群落组成和结构特征受到多重生态环境因子的影响,起显著影响作用的因子因地而异,因时而异,其影响机理还有待探究,但可以推测这与研究地点的生态环境因子具体情况相关,例如与碳源相对匮乏的沉积地区相比,有机质比较丰富的地区,如东寨港红树林沉积,其源于碳的影响作用相对不显著。因此,利用红树林进行重金属修复时,应考虑当地实际环境因子对SRB群落结构的影响,并通过调节沉积相关的理化因子以达到高效的修复作用。
本研究结果表明,在海南北部红树林沉积中,SRB群落组成和结构特征在林内与林外光滩明显不同,同时也呈现出季节性差异。这些差异与沉积中的总氮、总磷、pH和特定赋存形态的铜和锌显著相关。在采用红树林进行重金属生态修复工程中,应关注这些生态环境因子。
致谢:海南大学分析测试中心对本实验给予了大力支持和帮助!
Community characteristics of sulfate-reducing bacteria in mangrove sediments in Hainan
-
摘要: 在海南北部的红树林及其附近光滩区域,通过高通量测序技术研究了原位沉积中硫酸盐还原菌(SRB)群落结构的季节差异,检测了重金属铜和锌的赋存形态,并分析了相关生态环境因子对SRB群落的影响。结果显示,红树林沉积中SRB的多样性在旱季显著高于雨季,旱季光滩中SRB的多样性最高;在科的水平上,红树林沉积中索利氏菌科(Solibacteraceae)的相对丰度在旱季和雨季都为最大,但SRB群落组成结构在旱季和雨季显著不同;在光滩沉积中,在旱季相对丰度最大的是索利氏菌科,而雨季则为脱硫球茎菌科(Desulfobulbaceae)。相关性分析表明,沉积中的总氮、总磷、pH和特定赋存形态的铜和锌与SRB群落结构的季节性差异显著相关。本研究结果有助于阐明红树林沉积中SRB群落结构特征的季节性差异及其影响机制,为利用红树林进行重金属生态修复提供参考。Abstract: Sediments in the mangrove stands and the adjacent low-tide mudflat in the northern Hainan Island were collected, and the physio-chemical properties were determined. The seasonal variation characteristics of the community structures of sulfate-reducing bacteria (SRB) of the in-situ sediments were analyzed by using high-throughput sequencing. The speciation of heavy metal copper and zinc in the sediments were examined and the effects of relevant eco-environmental factors on the SRB communities were analyzed. The results showed that the diversity of SRB in the mangrove sediments was significantly higher in dry season than in rainy season, and the highest in the low-tide adjacent mudflat sediments in dry season. In the family level the SRB community structure in the mangrove sediments was significantly different between dry and rainy seasons, though the relative abundance of Solibacteraceae was consistently the greatest family in both dry and rainy seasons. In the low-tide adjacent mudflat sediments Solibacteraceae was the highest in relative abundance in dry season, while Desulfobulbaceae the highest in rainy season. Correlation analysis showed that the seasonal changes of SRB community structure were significantly correlated with the total nitrogen, total phosphorus, pH and the speciation of copper and zinc in the sediments. The results preliminarily illustrated the seasonal variation of SRB community structure and the related eco-environmental factors in mangrove sediments, and might provide theoretical reference for the ecological restoration of heavy metals by mangroves.
-
Key words:
- mangrove /
- sulfate-reducing bacteria /
- community structure /
- heavy metals
-
表 1 沉积理化性质
样品 含水率/% LOI/% Fe3+/Fe2+ TN/(mg·kg−1) TP/
(mg·kg−1)pH 温度/℃ 粒径/μm DA 35.59±0.47a 6.13±0.31a 0.79±0.04b 405.33±10.06d 447.64±8.99a 6.92 17.0 132.83 DB 34.19±0.34b 7.33±0.24a 0.32±0.01c 606.91±30.16c 248.22±5.35b 6.46 17.5 151.53 RA 35.75±0.20a 6.30±0.093a 1.20±0.097a 1088.67±30.01b 143.60±61.50c 7.11 27.8 111.60 RB 35.75±0.47a 14.68±0.51a 0.33±0.03c 1505.00±68.46a 106.53±1.33c 6.34 26.3 143.53 注:DA-旱季光滩,DB-旱季林内,RA-雨季光滩,RB-雨季林内; TN-总氮,TP-总磷;a、b、c和d为显著性( P <0.05)差异标记,下同。 表 2 不同沉积中铜的赋存形态量化分析
样品 Cu-AF/(mg·kg−1) Cu-RF/(mg·kg−1) Cu-OF/(mg·kg−1) Cu-Res F/(mg·kg−1) Cu总量/
(mg·kg−1)DA 2.36±0.73b 11.7±1.21a 14.54±0.61a 6.60±0.46a 35.19±0.63a DB 5.19±0.52a 11.6±0.58a 15.28±1.73a 3.37±0.30b 35.43±1.15a RA 1.78±0.22b 0.16±0.14b 0.39±0.37b 5.90±0.78a 8.23±0.85b RB 1.26±0.12b 0.15±0.02b 0.71±0.57b 6.57±1.50a 8.69±1.15b 注:a和b为显著性差异标记。 表 3 不同沉积中锌的赋存形态量化分析
样品 Zn-AF/
(mg·kg−1)Zn-RF/
(mg·kg−1)Zn-OF/
(mg·kg−1)Zn-Res F/
(mg·kg−1)Zn总量/
(mg·kg−1)DA 4.14±1.73ab 9.99±0.67a 3.79±1.08a 44.71±12.95a 62.63±10.52a DB 2.69±0.31b 6.75±0.38a 3.33±2.18a 50.89±5.72a 63.65±4.33a RA 5.94±0.39a 6.44±0.77a 4.32±2.17a 35.75±6.81a 52.43±5.23a RB 2.88±0.76b 6.37±4.09a 4.85±2.47a 31.15±10.20a 45.26±15.68a 注:a和b为显著性差异标记。 表 4 沉积中SRB的α多样性指数
样品 Shannon指数 Chao1指数 ACE指数 DA 9.71±0.093a 2278.40±150.33a 2406.14±161.95a DB 8.86±0.087 c 1840.54±179.54ab 1970.19±226.97ab RA 9.23±0.180 b 1898.19±351.04ab 1941.05±333.23ab RB 8.22±0.089 d 1588.67±197.46b 1656.44±203.55b 表 5 α多样性指数与理化性质的Pearson相关性分析
α多样性
指数含水率 LOI Fe3+/Fe2+ TN TP pH 温度 Shannon 0.037 −0.55 0.64* −0.78* 0.78* 0.80* −0.45 Chao1 0.035 −0.57 0.41 −0.65* 0.80* 0.53 −0.48 ACE −0.053 −0.55 0.33 −0.70* 0.84* 0.47 −0.57 注: *显著相关(p<0.05,n=12) 表 6 α多样性指数分别与铜和锌赋存形态的Pearson相关性分析
α多样性
指数Cu-
AFCu-
RFCu-
OFCu-
Res FZn-
AFZn-
RFZn-
OFZn-
Res FSimpson 0.07 0.51 0.50 0.11 0.43 0.49 −0.07 0.34 Chao1 0.05 0.50 0.48 0.25 0.26 0.56 0.08 0.17 ACE 0.11 0.58* 0.56 0.15 0.17 0.62* 0.03 0.26 Shannon 0.08 0.50 0.48 0.12 0.45 0.52 −0.09 0.37 注:*显著相关(P<0.05,样本数n=12) -
[1] 罗松英, 邢雯淋, 梁绮霞, 等. 湛江湾红树林湿地表层沉积物重金属形态特征、生态风险评价及来源分析[J]. 生态环境学报, 2019, 28(2): 348 − 358. [2] 陈明, 蔡青云, 徐慧, 等. 水体沉积物重金属污染风险评价研究进展[J]. 生态环境学报, 2015, 24(6): 1069 − 1074. [3] 龚子同, 张效朴. 中国的红树林与酸性硫酸盐土[J]. 土壤学报, 1994, 31(1): 86 − 94. doi: 10.3321/j.issn:0564-3929.1994.01.014 [4] 丁苏丽, 张祁炅, 董俊, 等. 深港红树林沉积物微生物群落多样性及其与重金属的关系[J]. 生态学杂志, 2018, 37(10): 3018 − 3030. [5] 廖家隆, 姚素平, 丁海. 滨海红树林泥炭沉积物中硫的赋存特点及其控制因素[J]. 高校地质学报, 2008, 14(4): 620 − 630. doi: 10.3969/j.issn.1006-7493.2008.04.016 [6] 林慧娜, 傅娇艳, 吴浩, 等. 中国主要红树林湿地沉积物中硫的分布特征及影响因素[J]. 海洋科学, 2009, 33(12): 79 − 82. [7] 林慧娜. 我国红树林湿地中硫的分布特征及影响因素[D]. 厦门: 厦门大学, 2008. [8] GEETS J, BORREMANS B, DIELS L, et al. DsrB gene-based DGGE for community and diversity surveys of sulfate-reducing bacteria [J]. Journal of Microbiological Methods, 2006, 66(2): 194 − 205. doi: 10.1016/j.mimet.2005.11.002 [9] 王原. 珠江沉积物中SRB的群落结构、分离筛选和生理生化特性鉴定[D]. 广州: 华南理工大学, 2013. [10] 丁海, 姚素平, 刘桂建, 等. 海南红树林湿地可培养硫酸盐还原菌的垂直分布特征研究[J]. 高校地质学报, 2016, 22(4): 621 − 630. [11] ALZUBAIDY H, ESSACK M, MALAS T B, et al. Rhizosphere microbiome metagenomics of gray mangroves (Avicennia marina) in the Red Sea [J]. Gene, 2016, 576(2): 626 − 636. doi: 10.1016/j.gene.2015.10.032 [12] VARON-LOPEZ M, DIAS A C F, FASANELLA C C, et al, Sulphur-oxidizing and sulphate-reducing communities in Brazilian mangrove sediments[J]. Environmental Microbiology, 2014, 16(3): 845-855. [13] CABRAL L, LACERDA JÚNIOR G V, de SOUSA S T P, et al. Anthropogenic impact on mangrove sediments triggers differential responses in the heavy metals and antibiotic resistomes of microbial communities[J]. Environmental Pollution, 2016, 216: 460-469. [14] HE H, ZHEN Y, MI T Z, et al. Community composition and distribution of sulfate- and sulfite-reducing prokaryotes in sediments from the Changjiang estuary and adjacent East China Sea [J]. Estuarine Coastal & Shelf Science, 2015, 165: 75 − 85. [15] 王丽荣, 李贞, 蒲杨婕, 等. 近50年海南岛红树林群落的变化及其与环境关系分析——以东寨港、三亚河和青梅港红树林自然保护区为例[J]. 热带地理, 2010, 30(2): 16 − 22. [16] 刘美龄, 叶勇, 曹长青, 等. 海南东寨港红树林土壤粒径分布的分形特征及其影响因素[J]. 生态学杂志, 2008, 27(9): 105 − 109. [17] GB/T 12763.8-2007.海洋调查规范 第8部分:海洋地质地球物理调查[S].2007. [18] GB 17378.5-2007. 海洋监测规范 第5部分: 沉积物分析[S]. 2007 [19] KARTAL S, AYDIN Z, TOKALIOGLU S. Fractionation of metals in street sediment samples by using the BCR sequential extraction procedure and multivariate statistical elucidation of the data [J]. Journal of Hazardous Materials, 2006, 132(1): 80 − 89. doi: 10.1016/j.jhazmat.2005.11.091 [20] 李健, 郑春江. 环境背景值数据手册[Z]. 北京: 中国环境科学出版社, 1989. [21] 季一诺, 赵志忠, 吴丹, 等. 东寨港红树林沉积物中铜、锌、镉、铅的空间分布特征[J]. 江苏农业科学, 2015, 43(11): 462 − 465. [22] 黄莹, 李永霞, 高甫威, 等. 小清河表层沉积物重污染区重金属赋存形态及风险评价[J]. 环境科学, 2015, 36(6): 2046 − 2053. [23] 周怀东, 袁浩, 王雨春, 等. 长江水系沉积物中重金属的赋存形态[J]. 环境化学, 2008, 27(4): 515 − 519. doi: 10.3321/j.issn:0254-6108.2008.04.023 [24] 罗松英, 梁艺琼, 陈碧珊, 等. 徐闻南山镇红树林沉积物及红树植物中重金属的累积特征与迁移规律. 热带地理, 2019, 39(3): 347-356. [25] JOCHUM L M, CHEN X, LEVER M A, et al. Depth distribution and assembly of sulfate reducing microbial communities in marine sediments of Aarhus Bay [J]. Applied and Environmental Microbiology, 2017, 83(23): e01547 − 17. [26] RABUS R, VENCESLAU S S, WÖHLBRAND L, et al. Chapter Two-A post-genomic view of the ecophysiology, catabolism and biotechnological relevance of sulphate-reducing prokaryotes [J]. Advances in Microbial Physiology, 2015, 66: 55 − 321. [27] 张玉, 贺惠, 米铁柱, 等. 东海海域表层沉积物中硫酸盐还原菌分布特征研究[J]. 中国环境科学, 2016, 36(12): 3750 − 3758. doi: 10.3969/j.issn.1000-6923.2016.12.029 [28] LIU X D, BAGWELL C E, WU L Y, et al. Molecular diversity of sulfate-reducing bacteria from two different continental margin habitats [J]. Applied and Environmental Microbiology, 2003, 69(10): 6073 − 6081. doi: 10.1128/AEM.69.10.6073-6081.2003 [29] ZHANG Y, WANG X G, ZHEN Y, et al. Microbial diversity and community structure of sulfate-reducing and sulfur-oxidizing bacteria in sediment cores from the East China Sea [J]. Frontiers in Microbiology, 2017, 8(8): 2133. [30] 陈敏. 胶州湾养殖区硫酸盐还原菌的群落结构与功能特征研究[D]. 青岛: 中国海洋大学. 2013. [31] 佘晨兴. 闽江河口潮汐沼泽湿地土壤产甲烷菌和硫酸盐还原菌群落结构和丰度的研究[D] . 福州: 福建师范大学. 2014. [32] 张伟, 张丽丽. 云南洱海沉积物中硫酸盐还原菌的时空分布特征[J]. 地球与环境, 2016, 44(2): 177 − 184. [33] 刘建丽, 赵吉, 武琳慧. 乌梁素海湖滨湿地硫酸盐还原菌群落多样性及系统发育分析[J]. 安全与环境学报, 2016, 16(3): 343 − 348. [34] BALK M, KEUSKAMP J, LAANBROEK H J. Potential activity, size, and structure of sulfate-reducing microbial communities in an exposed, grazed and a sheltered, non-grazed mangrove stand at the Red Sea coast [J]. Frontiers in Microbiology, 2015, 6: 1478. -




 下载:
下载: