-
香蕉为芭蕉科(Musaceae)芭蕉属(Musa)的重要热带水果[1],是第四大粮食作物,香蕉主要分为“香牙蕉”(Musa AAA Group Cavendish)、‘粉蕉’(Musa acuminata ABB Group Fenjiao)、“皇帝蕉”(Musa paradisiaca AA)、“主食蕉”和“加工型蕉”等。其中,“香牙蕉”是最为常见的商业栽培品种,具有肉质软糯、香甜可口的特点,广泛流通于市场。‘粉蕉’则口感细腻,风味独特,甜度较高。“皇帝蕉”体型小巧,果实饱满,香气浓郁。“主食蕉”主要用于食用,在一些地区是重要的粮食来源。“加工型蕉”则因自身特性,更适合加工成各类食品,如香蕉干、香蕉片等。《2024—2029年中国香蕉行业深度调研及投资机会分析报告》显示,2021年中国“香牙蕉”种植面积约占香蕉种植面积的75%,‘粉蕉’占20%,“皇帝蕉”占2%,“主食蕉”和“加工型蕉”各占1.5%,到2025年,特色蕉种植面积比例预计达到25%~30%[2 − 5]。特色蕉中的“皇帝蕉”包含‘贡蕉’(Musa ‘Gong’)和‘海贡蕉’(Musa AA),由于贡蕉易感枯萎病,因此,生产上绝大多数皇帝蕉实为枯萎病抗性强的‘海贡蕉’。‘海贡蕉’又称‘Pisang Empat Puluh Hari’(马来西亚名称)、‘Inarnibal’(菲律宾名称)、‘Pisang Lampung’(印度尼西亚名称),商品名为“皇帝蕉”或“抗病皇帝蕉”,是国内香蕉商业品种中唯一纯A基因、天然高抗香蕉枯萎病4号小种、对香蕉枯萎病1号小种免疫的品种[6]。‘贡蕉’由中国华侨李木清1963年从印尼引进,目前海南、广东和广西等地皆有种植[7]。‘海贡蕉’种植面积占香蕉种植总面积的2%,截至2021年,‘海贡蕉’种植面积5 002.5 hm2,其中,海南省澄迈县有4 067 hm2。
中、微量矿质营养元素对植物的生长发育和生理功能起着至关重要的作用,但目前中、微量元素缺乏对香蕉光合特性的影响的研究并不多[8 − 9]。镁(Mg)、锌(Zn)是植物光合作用中不可或缺的元素,缺乏会对植物光合特性产生重要影响[10]。镁胁迫会降低叶绿素含量、抑制光合速率、干扰产物转运等,进而影响糖分从源到库的转运过程;锌胁迫不仅会干扰线粒体与叶绿体之间的质体交换[11],还会抑制光合作用、影响植物叶绿素的合成,阻碍光系统的电子传递,抑制希尔反应,进而影响植物的光合作用,导致植物生长减缓,影响产量[12]。叶绿素是自然界中对光能吸收、传递和转换的一种最重要的色素[13],其代谢水平除与植物种质有关外,还与环境因子的相互作用有关[14]。叶绿素荧光技术是一种利用植物叶绿素分子在光照下发出荧光的特性,可用来测量植物光合作用过程及其生理状态,可以反映出光合作用的效率和植物对环境胁迫的响应[15],与其他生态生理学方法(如气体交换方法)相比,其优点是测量快且无损[16]。苗期是香蕉生育期的基础,是香蕉高产优质的关键[17 − 19]。本研究通过测定Mg、Zn元素不同含量协同缺乏处理下‘海贡蕉’幼苗生长情况及光合生理的差异,旨在发现‘海贡蕉’幼苗对Mg、Zn缺乏的生理响应,为‘海贡蕉’健康生长提供数据支持和理论依据。
-
供试植株为‘海贡蕉’(Musa AA),符合一级苗出圃标准(NY/T357—2007 香蕉组培苗),选择大小和健康状况一致且没有病虫害问题的‘海贡蕉’幼苗作为实验材料。‘海贡蕉’幼苗采用蛭石盆栽培养,培养杯规格为15 cm×13 cm,将培养杯装满蛭石。幼苗移栽前,用清水小心清洗‘海贡蕉’幼苗根部泥土,随后将‘海贡蕉’幼苗放置于清水中,使用清水浸泡12 h,进行12 h的“养分饥饿”预处理,以去除‘海贡蕉’幼苗根系中的土壤及杂质。12 h后将‘海贡蕉’幼苗移至含有蛭石的培养杯中进行为期120 d的培养,所有培育的种苗植株将被用于测定不同指标。
-
实验采用2因素3水平正交实验,其中2因素为镁、锌,3水平为正常含量的0%、50%、100%。本实验共9个处理,分别记为M1Z1(0%Mg、0%Zn)、M1Z2(0%Mg、50%Zn)、M1Z3(0%Mg、100%Zn)、M2Z1(50%Mg、0%Zn)、M2Z2(50%Mg、50%Zn)、M2Z3(50%Mg、100%Zn)、M3Z1(100%Mg、0%Zn)、M3Z2(100%Mg、50%Zn)、M3Z3(100%Mg、100%Zn),其中M3Z3为正常处理,浇灌正常浓度营养液。实验时间为2024−03−07—2024−07−31,实验地点位于中国热带农业科学院海口实验站113,日均温为27 ℃,为确保光照充足,使用植物生长灯进行光照补充,每5天浇灌1次Hoagland营养液,营养液参照陈海斌文献进行配置[10],每次50 mL,间隔3~4天浇1次水,每株约为30 mL。
-
每15天对‘海贡蕉’幼苗农艺性状(株高、茎粗、总根长、叶长、叶宽)、叶绿素(SPAD)含量进行测定;每20天对‘海贡蕉’幼苗荧光动力学参数(Fv/Fm、Y(Ⅱ)、NPQ)进行测定,每隔30 d对光合指标(Pn、Ci、Tr、Gs)进行测定,并对株高相对生长率(relative growth rate,RGR)进行计算。其中,FV/Fm表示光系统Ⅱ(PSⅡ)最大光化学效率;YⅡ表示实际光化学效率;NPQ表示非光化学淬灭;Pn为净光合速率;Ci为胞间CO浓度;Tr为蒸腾速率;Gs为气孔导度。
$$ RGR=\frac{\mathrm{l}\mathrm{n}W_2-\mathrm{l}\mathrm{n}W_1}{t_2-t_1}\ 。 $$ 式中,W1为第t1天幼苗株高,W2为间隔15 d后第t2天同一幼苗株高;t1为株高初始测定日,t2为间隔15 d的株高后续测定日。
-
对测得数据使用Excel进行整理,使用IBM SPSS Statistics 26.0进行数据分析,对所有处理的数据使用SigmaPlot15.0、GraphPad Prism 9进行图形绘制。
-
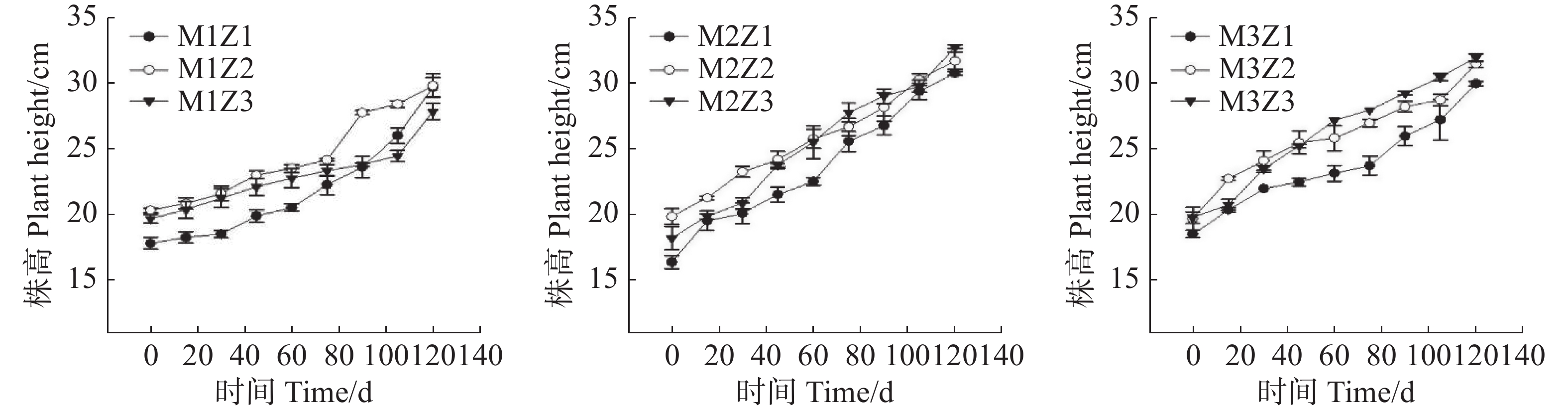
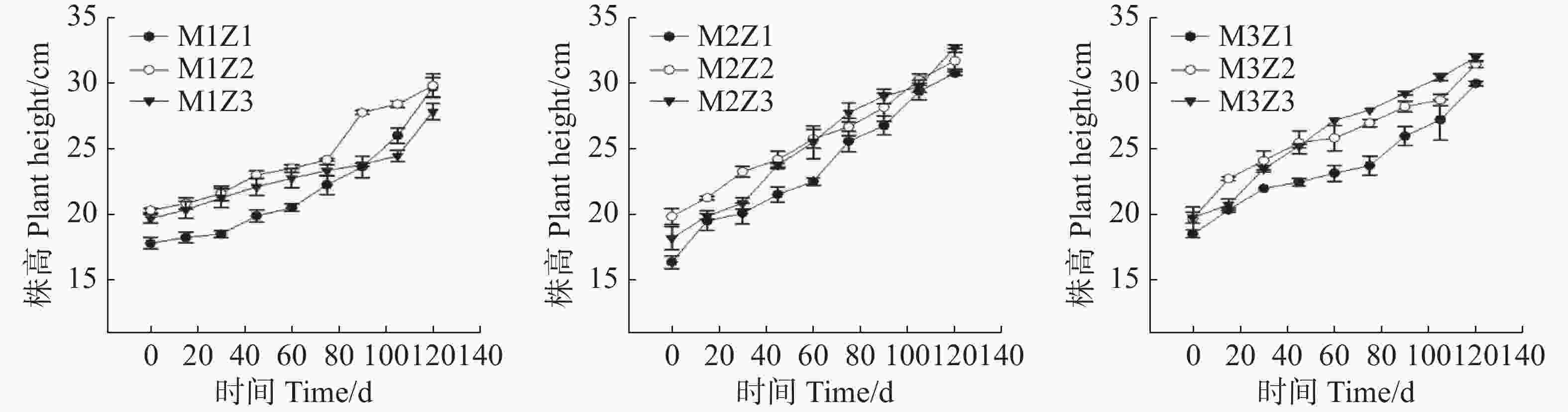
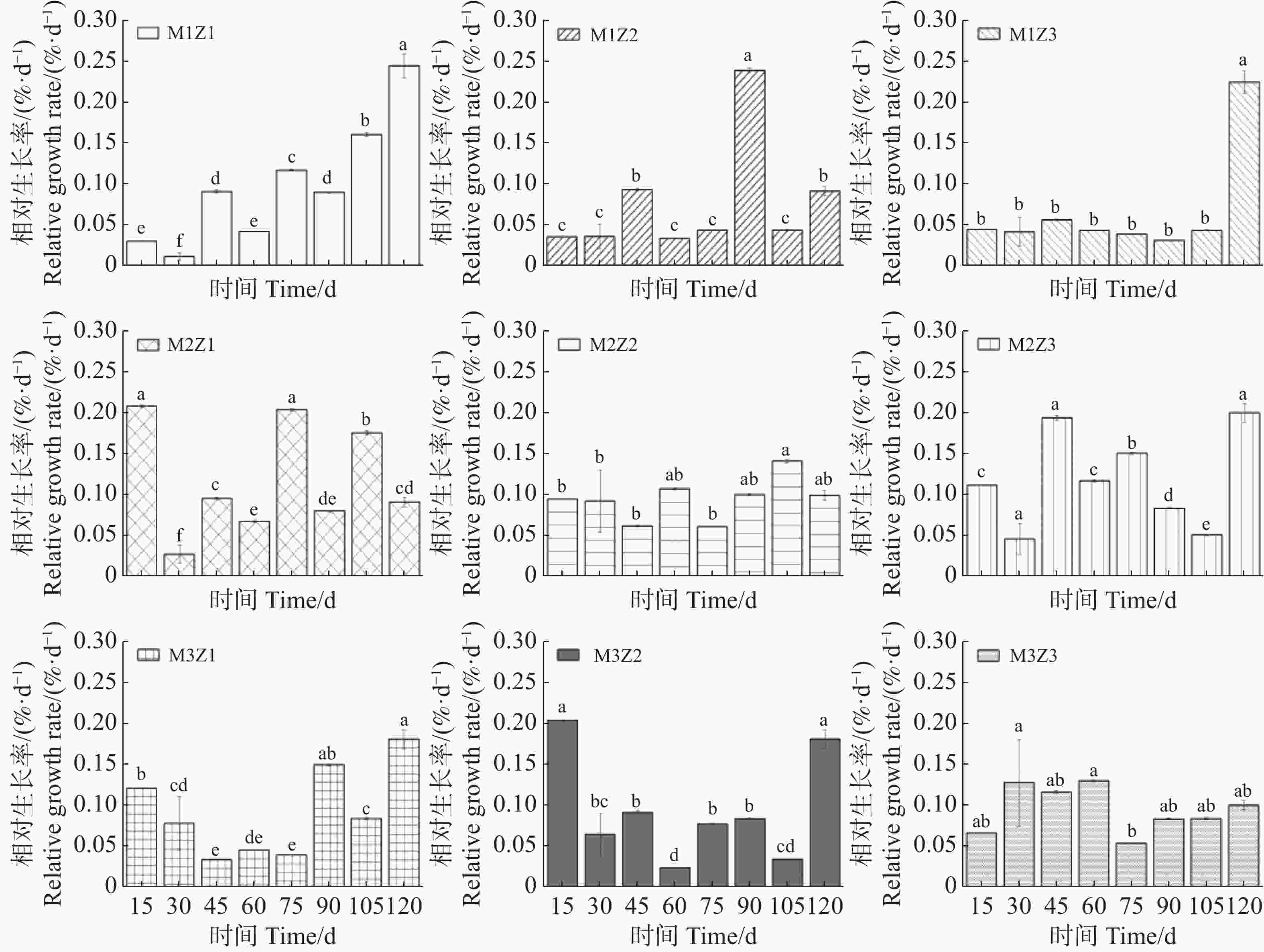
实验期内,不同处理下‘海贡蕉’幼苗株高生长动态趋势基本一致,呈现上升趋势(图1),但M1Z1、M1Z2和M1Z3协同缺乏处理下‘海贡蕉’幼苗株高较矮且生长缓慢,虽然M3Z1处理和M3Z2处理株高长势优于其他处理,但也低于正常处理。镁完全缺乏(M1Z3)、锌完全缺乏(M3Z1)处理下,‘海贡蕉’幼苗株高显著低于正常处理。镁、锌协同缺乏处理(M1Z1、M1Z2、M2Z1、M2Z2、M2Z3、M3Z2)第30天,M1Z1处理的株高仅为20.3 cm,为所有处理组中最低。生长第120天,正常处理的‘海贡蕉’幼苗株高为32 cm,M1Z1、M1Z2、M1Z3、M2Z1、M2Z2、M3Z1、M3Z2协同缺乏下的‘海贡蕉’幼苗株高分别较正常处理降低了7.28%、6.88%、13.03%、3.91%、0.94%、6.25%、1.56%。M2Z3处理下株高比正常处理高2.34%。镁锌协同缺乏处理对幼苗株高相对生长率的影响复杂且具有阶段性(图2)。生长期内,不同处理下‘海贡蕉’株高相对生长率保持在0.011 6~0.244 9,变化幅度较大。其中,镁锌完全缺乏(M1Z1)处理下,株高相对生长率整体偏低,生长受严重抑制且不稳定;正常处理下株高相对生长率较高;其他缺乏处理下,株高相对生长率变化波动较大,无明显规律,但总体来看,低于正常处理组。此外,相对生长率不会随生长时间变化而呈现一定的趋势。
-
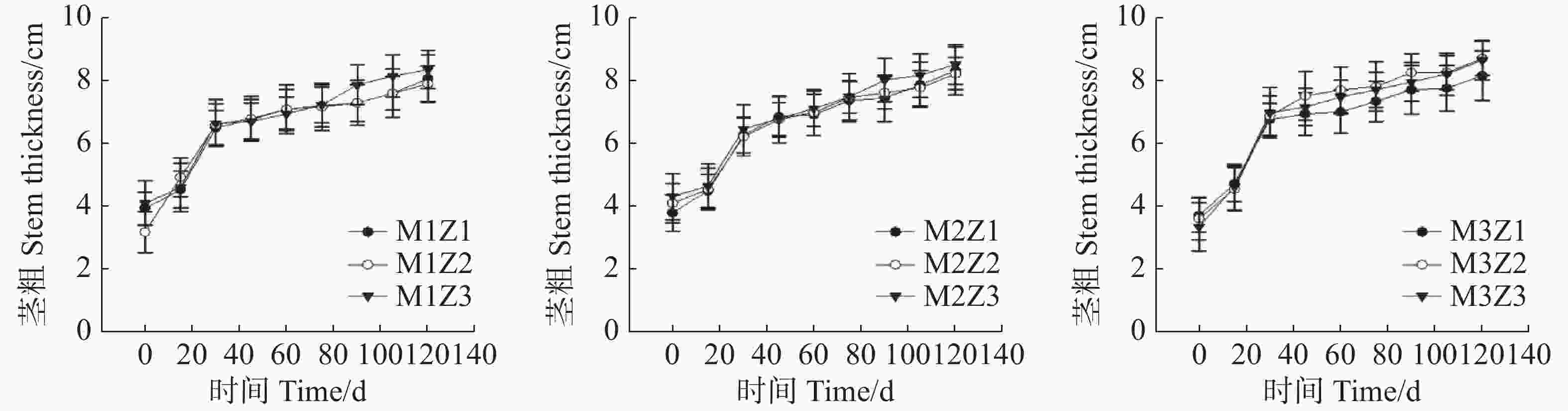
生长0~120天,不同处理下‘海贡蕉’苗茎粗呈现出相似的增长趋势(图3)。生长第120天,正常处理‘海贡蕉’幼苗茎粗达到8.65 cm。协同缺乏处理下,M1Z1协同缺乏处理下的‘海贡蕉’幼苗茎粗为8.07 cm,M1Z2处理下为7.90 cm,M1Z3处理下为8.35 cm,M2Z1处理下为8.30 cm,M2Z2处理下为8.20 cm,M2Z3处理下为8.50 cm,M3Z1处理下为8.15 cm,M3Z2处理下为8.70 cm。整体来看,在幼苗生长期间,镁、锌协同缺乏对‘海贡蕉’幼苗茎粗生长影响较小,‘海贡蕉’幼苗茎粗不会随着缺乏程度及缺乏时间而表现出明显差异。
-
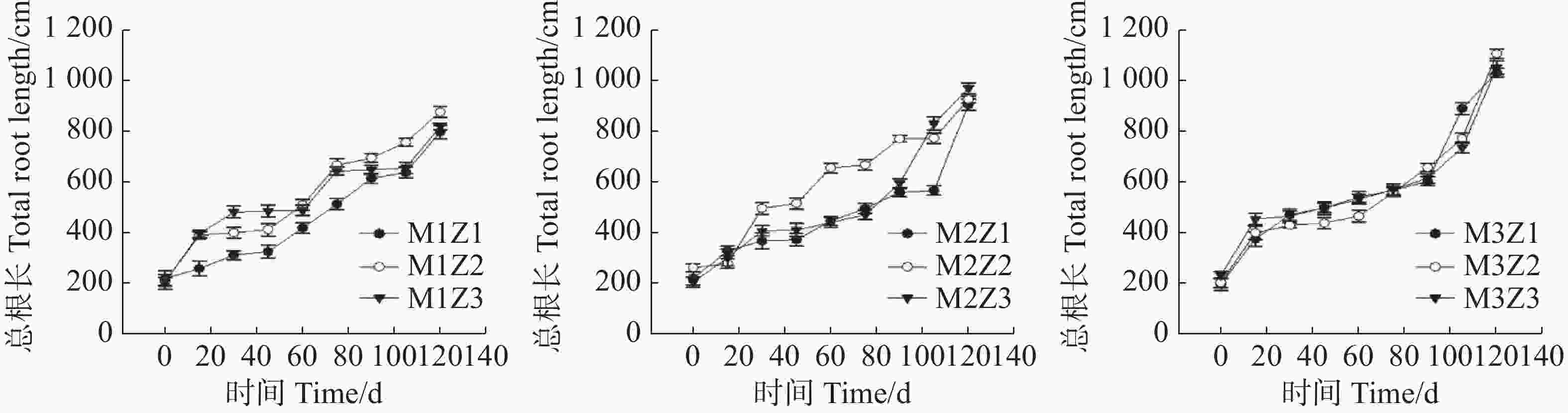
正常处理下,生长初期总根长增长幅度相对较大,幼苗生长中期,增长幅度相对较为平稳,总根长逐步上升。生长后期,总根长增长幅度又有所增大(图4)。在生长第15天,M1Z1、M1Z2、M1Z3、M2Z1、M2Z2、M2Z3、M3Z1、M3Z2处理下‘海贡蕉’幼苗总根长分别降低了16.34%、24.70%、18.56%、9.75%、11.67%、11.35%、15.36%、19.89%。生长第30~105天,M1Z1、M1Z2、M1Z3处理下总根长显著低于其他处理。生长第30天,M1Z1、M1Z2、M1Z3、M2Z1、M2Z2、M2Z3、M3Z1、M3Z2协同缺乏处理下‘海贡蕉’幼苗总根长较正常处理分别下降了19.21%、25.66%、16.55%、3.92%、5.88%、10.43%、12.23%、6.35%,第105天,分别下降了16.84%、16.76%、11.70%、7.30%、5.51%、11.17%、5.90%、9.25%。M1Z1、M1Z2、M1Z3处理下,‘海贡蕉’幼苗根系生长最差;M2Z1、M2Z2、M2Z3处理下,‘海贡蕉’根系生长较好,总根长M2Z3>M2Z2>M2Z1;M3Z1、M3Z2、M3Z3处理下,‘海贡蕉’幼苗长势最好,总根长M3Z2>M3Z3>M3Z1。协同缺乏处理组的总根长较正常处理组均有不同程度的降低。
-
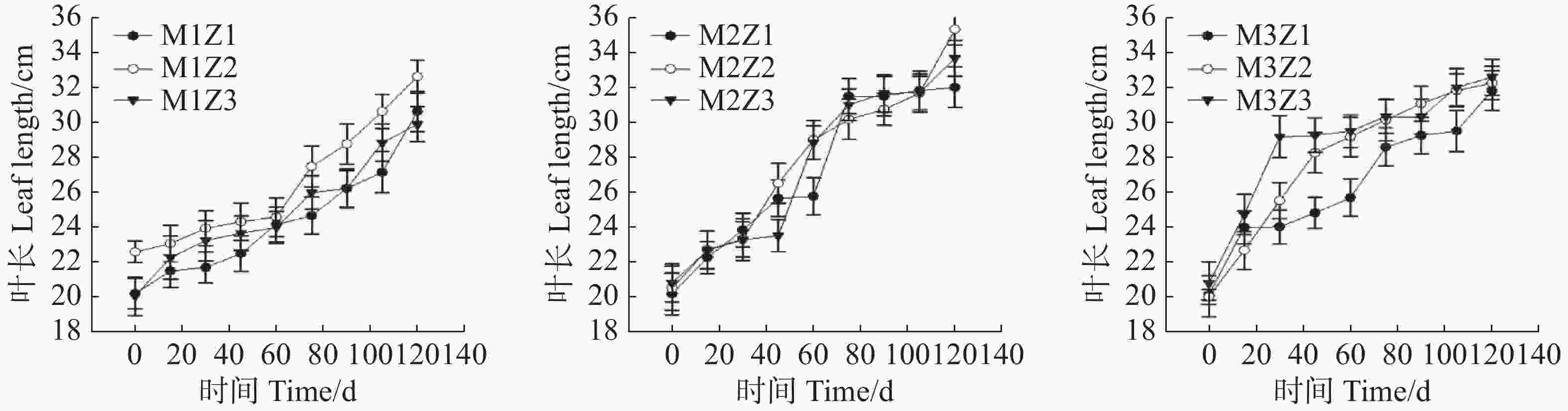
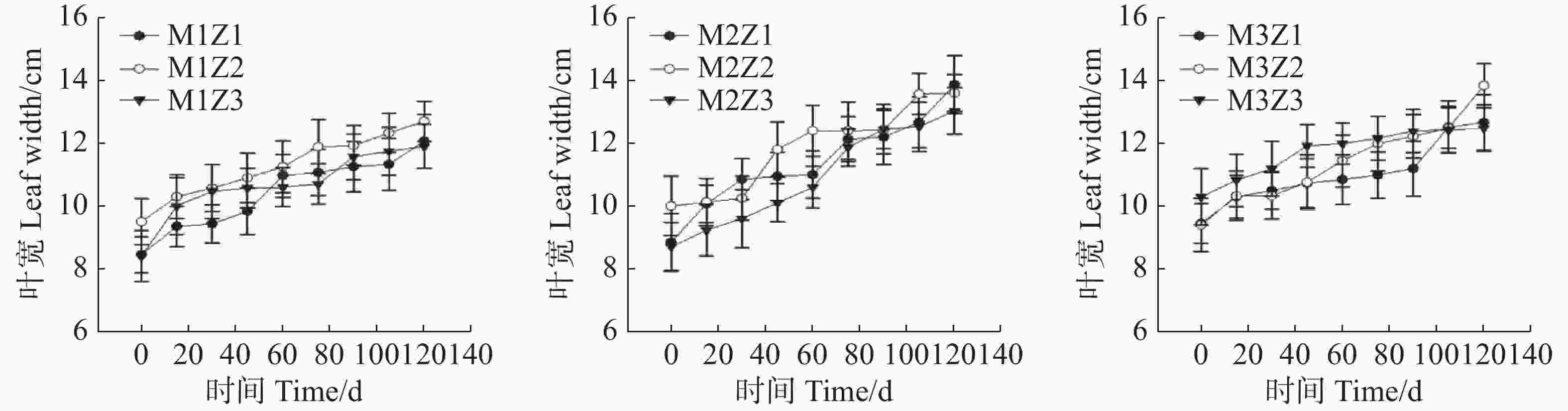
‘海贡蕉’幼苗叶长(图5)和叶宽(图6)随着生长期的延长表现出增长趋势,生长0~120天,叶长、叶宽呈现增长态势,第0天,M1Z1、M1Z2、M1Z3、M2Z1、M2Z2、M2Z3、M3Z1、M3Z2,M3Z3叶长分别为20.20 cm、22.60 cm、20.05 cm、20.17 cm、20.50 cm、20.80 cm、20.10 cm、20.00 cm、20.77 cm,生长至第120天,不同处理叶长分别增长了51.83%、44.56%、49.27%、58.65%、72.34%、61.88%、58.36%、61.25%、57.05%。生长第0天,叶宽分别为8.45 cm、9.50 cm、8.40 cm、8.85 cm、10.00 cm、8.70 cm、9.45 cm、9.40 cm、10.30 cm;生长第120天,叶宽分别增长了42.84%、33.68%、41.67%、56.72%、36.00%、49.77%、34.07%、47.34%、21.36%。整个生长期内,叶长长势较好,且协同缺乏处理与正常处理差异不显著,叶宽生长也表现出同样的趋势。
-
镁、锌协同缺乏极显著降低了‘海贡蕉’幼苗叶片SPAD含量,SPAD值整体变化趋势呈现“上升–下降–上升”的趋势(表1)。生长第0天,M1Z1、M1Z2、M1Z3、M2Z1、M2Z2、M2Z3、M3Z1、M3Z2处理下SPAD值分别为41.57、39.50、38.23、40.87、39.13、38.40、39.83、40.44、42.07。生长第30天,叶绿素含量显著上升,各处理组叶绿素含量分别增长了16.60%、26.66%、34.11%、28.00%、33.66%、27.94%、39.42%、33.04%、32.33%。生长第30~60天,叶绿素含量却出现了下降的趋势,不同协同缺乏处理分别下降了11.67、12.43、15.60、11.73、11.00、8.16、16.93、10.53、7.57。生长第60~120天,叶绿素含量再次回升。生长的第60天,正常处理叶绿素含量显著高于各协同缺乏处理组。M1Z1、M1Z2、M1Z3叶绿素含量低于其他处理。生长第30~120天,正常处理‘海贡蕉’幼苗SPAD值均高于协同缺乏处理。
表 1 不同含量镁、锌协同缺乏处理SPAD值
Table 1. SPAD values of the seedlings under the treatment of synergistic deficiency of magnesium and zinc at different gradient concentrations
处理
Treatment时间 Time/d 0 30 60 90 120 M1Z1 46.57±4.21a 48.47±2.28f 36.80±3.35f 44.63±4.76c 46.03±5.98e M1Z2 39.50±0.36e 58.03±2.92b 44.60±2.63b 42.53±5.85d 40.87±7.10f M1Z3 38.23±4.05f 57.27±1.44b 35.67±2.76g 49.27±2.31a 51.43±2.05b M2Z1 40.87±1.04c 52.30±1.47d 40.57±3.50d 45.50±3.01b 57.07±6.59a M2Z2 36.13±0.67g 44.30±5.78e 41.30±6.03d 39.07±6.94e 47.07±0.50d M2Z3 38.40±4.21f 59.13±3.38a 40.97±4.00d 45.53±2.25b 51.00±1.15b M3Z1 39.83±2.24de 55.53±2.62c 38.60±3.02e 41.87±3.06d 49.50±7.47c M3Z2 40.44±1.94cd 50.80±1.08g 43.27±2.00c 46.13±2.39b 51.17±4.83b M3Z3 42.07±1.08b 55.67±0.50c 48.10±8.61a 42.20±0.15d 51.20±4.07b 注:此结果为平均值±标准误差,不同字母表示差异显著(LSD,P < 0.05)。 Note: This result is the mean value ± standard error. Different letters indicate significant differences (LSD, P < 0.05). -
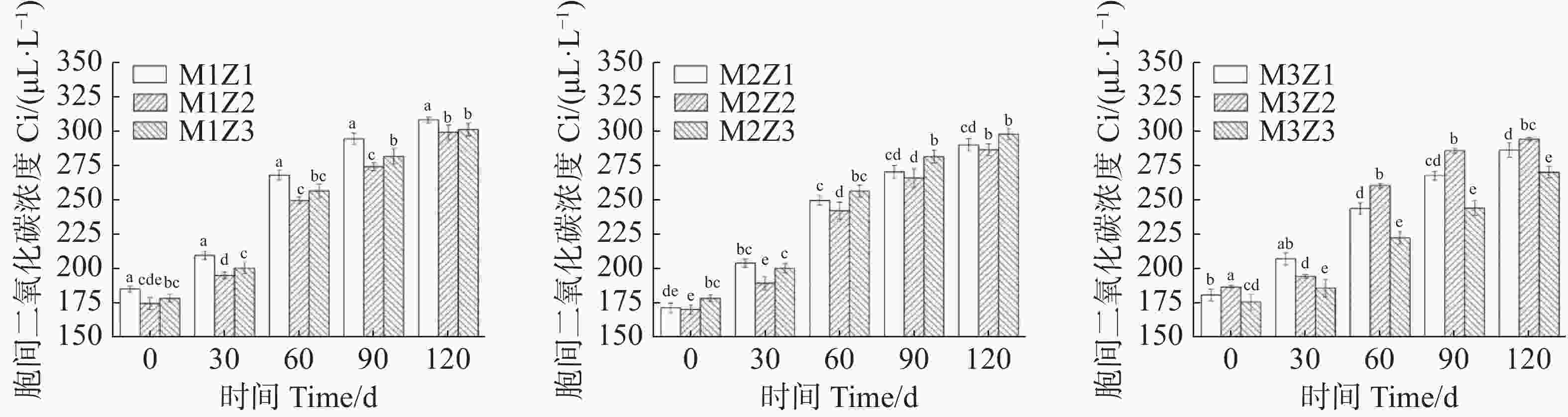
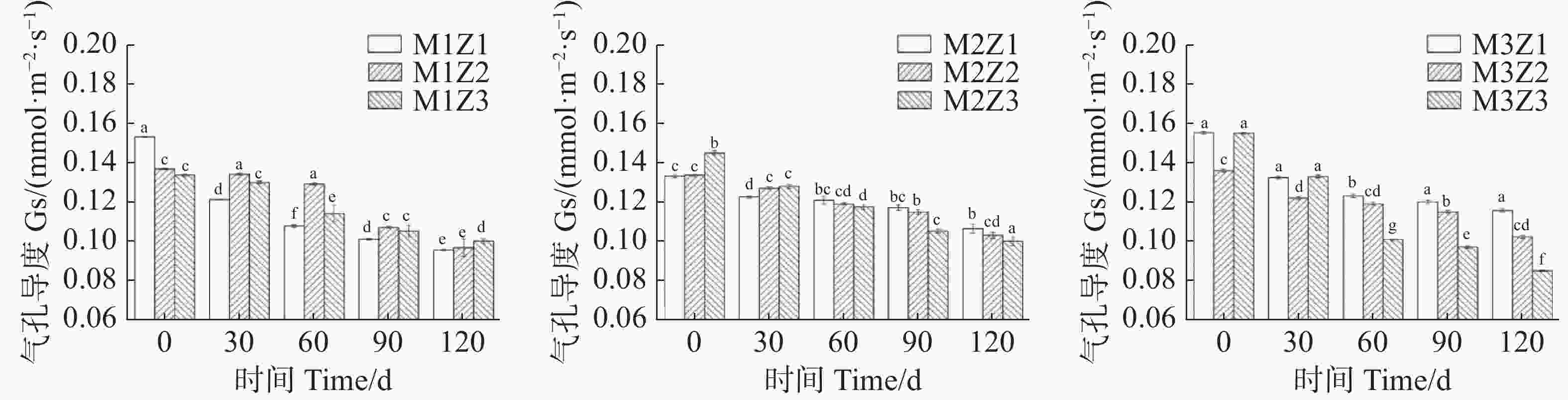
正常处理下‘海贡蕉’幼苗净光合速率Pn(图7)、蒸腾速率Tr(图8)、胞间CO2浓度Ci(图9),随着生长期的延长呈上升趋势,气孔导度Gs(图10)呈下降趋势。协同缺乏处理下,‘海贡蕉’幼苗Pn值增长缓慢,但Ci值却显著高于正常处理,协同缺乏处理下,Tr值、Gs值呈明显下降趋势,Tr值明显低于正常处理,但Gs却高于正常处理。生长第120天,正常处理下幼苗Pn值为11.68 µmol·m−2·s−1,M1Z1、M1Z2、M1Z3、M2Z1、M2Z2、M2Z3、M3Z1、M3Z2处理较正常处理分别降低了64.70%、60.96%、57.27%、57.45%、58.48%、56.16%、26.03%、19.42%;正常处理下Tr值为
0.000166 mmol·m−2·s−1,协同缺乏处理下较正常处理分别低了68.45%、67.85%、67.80%、61.87%、61.77%、62.00%、61.95%,但M3Z2处理Tr值却高于正常处理;正常处理下Ci值为 270.1 μL·L−1,M1Z1、M1Z2、M1Z3、M2Z1、M2Z2、M2Z3、M3Z1、M3Z2协同缺乏处理下Ci值较正常处理值分别高了14.07%、10.78%、11.50%、7.44%、6.11%、10.36%、5.92%、8.88%。正常处理下Gs值为0.085 mmol·m−2·s−1,协同缺乏处理下Gs值分别比正常处理高了12.24%、13.65%、17.65%、25.18%、21.18%、17.65%、36%、20.19%。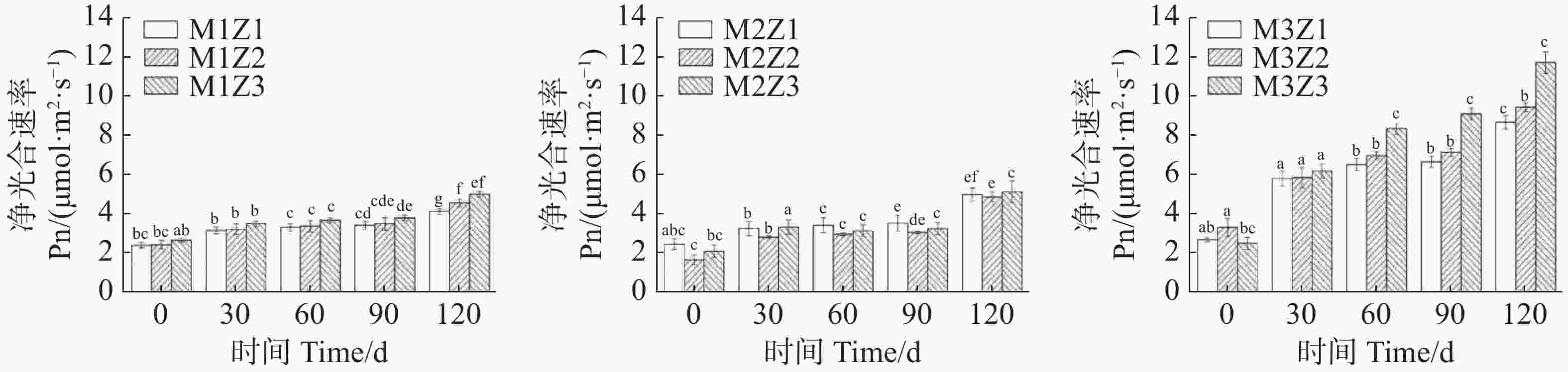
图 7 不同含量镁、锌协同缺乏处理净光合速率(Pn)
Figure 7. Net photosynthetic rate (Pn) of the banana seedlings under the treatment of synergistic deficiency of magnesium and zinc at different gradient concentrations
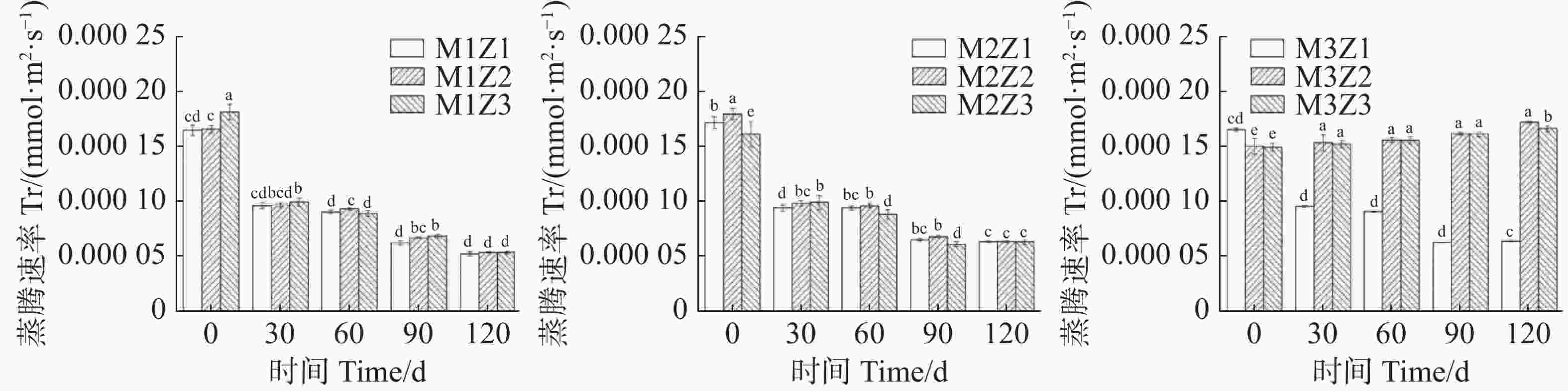
图 8 不同含量镁、锌协同缺乏处理蒸腾速率(Tr)
Figure 8. Transpiration rate (Tr) of the seedlings under the treatment of synergistic deficiency of magnesium and zinc at different gradient concentrations
-
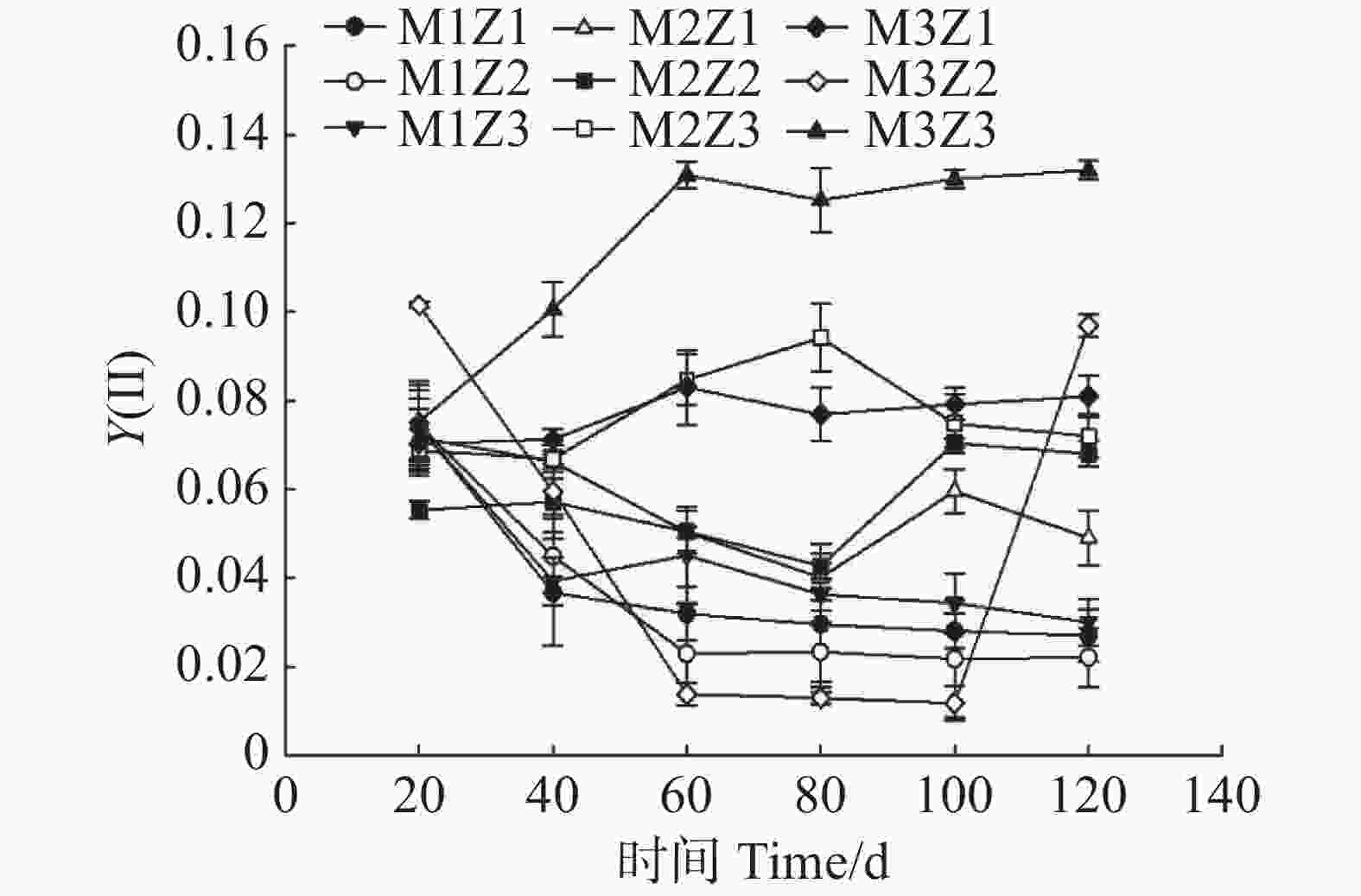
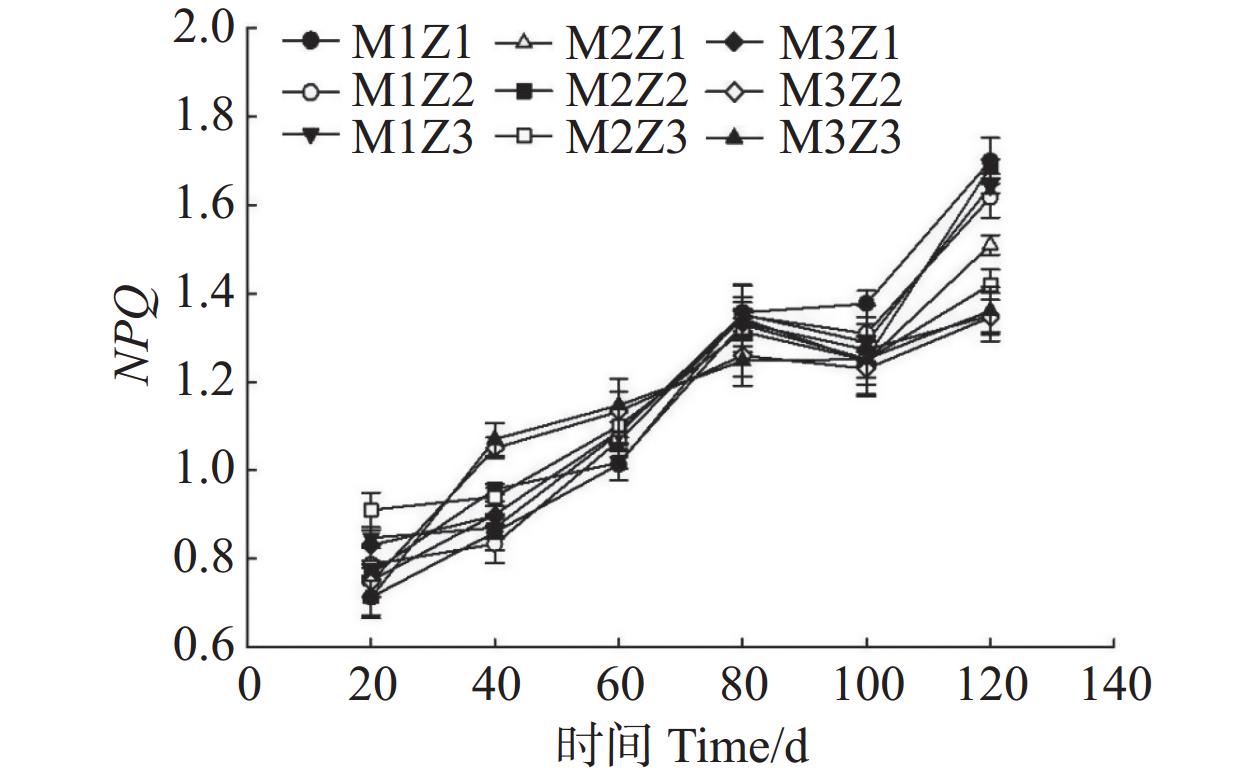
由图11—图13可知,正常处理下Fv/Fm值呈现出稳定的变化趋势。在第0~120天,Fv/Fm值仅增长了0.06。M1Z1、M1Z2、M1Z3、M2Z1、M2Z2、M2Z3、M3Z1、M3Z2处理下,Fv/Fm值分别较正常处理降低了15.88%、16.41%、18.42%、18.38%、12.75%、11.49%、13.09%、1.58%。且协同缺乏程度越轻,Fv/Fm值的变化越小。正常处理下‘海贡蕉’幼苗的Y(Ⅱ)值呈现“先上升,后稳定波动”的趋势,Y(Ⅱ)值从第0天的0.08增长至第120天的0.23,M3Z2与正常处理变化相似,但Fv/Fm值显著低于正常处理。M1Z1、M1Z2、M1Z3处理下,‘海贡蕉’幼苗Y(Ⅱ)值呈下降趋势,第0~40天下降较快,随后缓慢下降,表现为M1Z2<M1Z1<MZ1Z3。M2Z1、M2Z2在生长第0~80天时,Y(Ⅱ)值呈下降趋势随后波动上升,M2Z3、M3Z1处理下Y(Ⅱ)值呈“下降–上升–下降”趋势。正常处理下Y(Ⅱ)值为0.23,生长期内第20~120天,各缺乏处理下该值均显著低于正常处理。NPQ值随着生长期的延长,整体呈波动上升趋势。正常处理下,NPQ值呈稳定上升趋势。协同缺乏处理下,生长第0~80天呈上升趋势,第80~100天呈下降趋势,生长第100~120天继续上升,在协同缺乏第120天,正常处理的NPQ值为1.361。其中,M3Z1、M3Z2的处理组NPQ值与正常处理组差异较小,分别为
1.3500 、1.3467 ;M1Z1、M1Z2、M1Z3、M2Z1、M2Z2、M2Z3处理下NPQ值较正常处理分别高了24.89%、18.80%、20.70%、10.93%、23.94%、4.32%,明显高于正常处理组。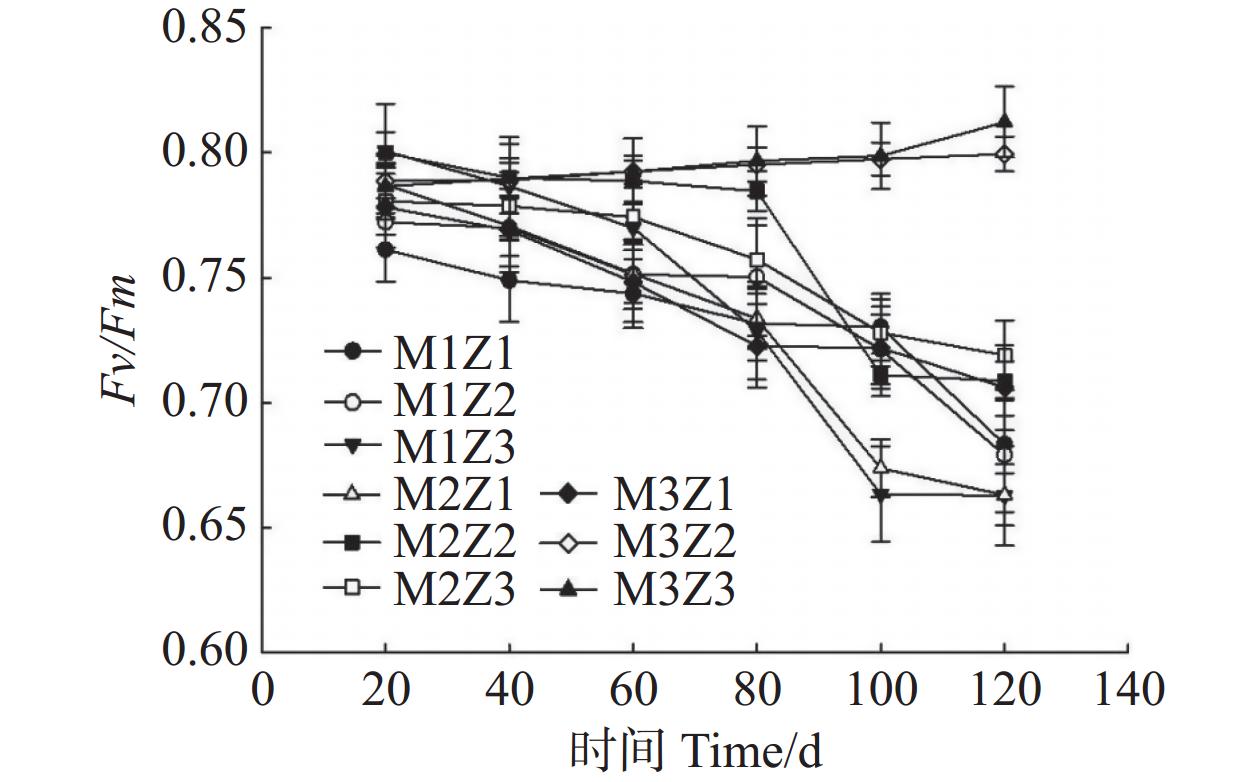
图 11 不同含量镁、锌协同缺乏处理Fv/Fm值
Figure 11. Fv/Fm values of the seedlings under the treatment of synergistic deficiency of magnesium and zinc at different gradient concentrations
-
镁、锌协同缺乏对‘海贡蕉’幼苗的生长进程影响显著,所有缺乏处理下‘海贡蕉’幼苗株高、总根长较正常处理表现出生长受到抑制,此结果与陈海斌[10]、黄筱涵等[20]的研究相互印证,他们通过研究得出,随着镁胁迫时间的延长,香蕉株高抑制效果更明显;锌胁迫下,凹叶厚朴幼苗各生长指标值下降至最低,显著抑制植株地上部分及根系的生长。镁、锌协同缺乏抑制‘海贡蕉’株高生长,可能是其影响了细胞伸长和分裂,从而导致茎尖生长受阻,进而使株高增长减缓[21 − 23]。镁、锌缺乏处理下茎粗和叶片生长未表现出显著变化,这可能是因为香蕉对缺镁胁迫的响应较慢[23]。镁、锌协同缺乏处理对幼苗株高相对生长率产生复杂、阶段性的影响,可能是因为‘海贡蕉’幼苗在不同生长阶段对镁锌的需求不同,但整体来看,镁锌缺乏对株高相对生长率具有不利的影响;限制光合作用的因素分为气孔因素和非气孔因素[24 − 26],本研究表明镁、锌协同缺乏时限制‘海贡蕉’幼苗光合作用的主要是非气孔因素。镁、锌缺乏限制‘海贡蕉’幼苗的光合作用,具体表现为幼苗生长期,Pn、Ci值整体呈现上升趋势,而Tr、Gs值呈下降趋势。在光合效率方面,所有镁锌缺乏处理导致‘海贡蕉’幼苗Pn显著降低。协同缺乏下Pn、Tr值较正常处理明显下降,Ci、Gs值显著升高。该结论在毛红椿(Toona ciliata var. pubescens)[27]、油茶(Camellia oleifera )、厚朴(Houpoea officinalis)中也相同。从叶绿素代谢角度来看,镁锌协同缺乏不仅干扰了叶绿素的正常合成途径,还加速了其分解进程,导致镁锌协同缺乏下叶绿素含量显著低于正常生长下叶绿素的含量[28]。这与葛晋金等[29]、黄筱涵等[20]研究结果相一致。
叶绿素荧光技术通过测定作物体内叶绿素荧光参数来反映植物光合作用的变化特征[30 − 31],常被作为光合作用与生理和环境适应性的检测信号[32 − 34]。生长期内,正常处理下‘海贡蕉’幼苗的Fv/Fm、Y(Ⅱ)、NPQ值均呈现稳定波动上升趋势,但协同缺乏处理下Fv/Fm值和Y(Ⅱ)值较正常处理呈现下降趋势,胁迫程度越深,下降越明显。协同缺乏处理的NPQ值高于正常处理值,镁锌缺乏程度越深,NPQ值越高。结论与高吉权[27]、夏倩[35]、刘韵诗[36]研究结果一致。NPQ值的上升反映了PSⅡ调节性能量耗散机制的启动和增强,植物通过增加热耗散来消耗过剩的光能,以保护光合机构,但这也间接表明光合作用的正常光化学途径受到了抑制。Mg含量为0%,Zn含量为0%、50%、100%时,叶绿素荧光参数波动较大,表明镁对叶绿素荧光参数的影响较大。叶绿素荧光技术在植物环境胁迫响应、生长发育和光合作用上具有很好的应用前景[37 − 39]。
镁、锌元素对‘海贡蕉’幼苗的生长有着显著影响,同时也会作用于‘海贡蕉’幼苗的光合能力,在此过程中,叶绿素荧光参数具有一定研究意义。中微量元素在植物生长中扮演着极为关键的角色,然而在实际生产环节,它们却常常被忽视。因此,在生产过程中,必须更加重视合理、科学的施肥。通过测定光合作用与叶绿素荧光参数,能够快速判断植物是否遭受胁迫,而且不会对植物的正常生长造成干扰,是检测植物胁迫情况的有效手段。不过,光合特性与叶绿素荧光测定也存在局限性,即无法确切指出植物具体缺乏何种元素。本研究仅聚焦于镁、锌胁迫及镁锌协同缺乏的情况,至于其他元素对植物的影响,仍有待进一步深入探究。此外,本实验存在一定的不足之处。镁属于中量元素,锌属于微量元素,镁对幼苗生长的影响天然强于锌,这一特性可能对镁锌协同缺乏效应的精准判断有干扰。同时,在组培苗培育过程中,幼苗体内积累了一定量的锌,而且在配置营养液的水中,难以将锌元素完全去除,导致锌缺乏处理(包括无锌处理)对幼苗生长的影响被削弱,无法充分模拟极端锌缺乏的环境。如此一来,不利于准确剖析锌在幼苗生长过程中的真实作用,以及镁锌协同缺乏的综合影响,在一定程度上限制了实验结果对镁锌协同缺乏作用机制的深入揭示。
镁锌缺乏对‘海贡蕉’幼苗生长及光合特性的影响
DOI: 10.15886/j.cnki.rdswxb.20250010
 CSTR: 32425.14.j.cnki.rdswxb.20250010
CSTR: 32425.14.j.cnki.rdswxb.20250010
Effects of magnesium and zinc deficiency on the growth and photosynthetic characteristics of Musa. AA seedlings
-
摘要: 为探究镁锌协同缺乏对‘海贡蕉’(Musa AA)幼苗生长及叶片光合作用的影响,分别以镁(Mg)、锌(Zn)两种元素正常含量的0%、50%、100%对其进行缺素处理。结果表明,生长第120天,Mg、Zn协同缺乏处理抑制‘海贡蕉’幼苗的生长及光合生理。正常处理下株高为32 cm、茎粗为8.65 cm、总根长为1 051.47 cm;缺乏处理株高、茎粗、总根长均有不同程度降低,叶片无显著差异,不同处理下株高相对生长率具有一定的差异性。光合特性方面,正常处理与缺乏处理在SPAD值、Pn值、Tr值、Ci值、Gs值等指标上也有明显差距,且缺乏处理下Y(Ⅱ)值、Fv/Fm值降低,NPQ值波动。本研究监测了Mg、Zn缺乏下‘海贡蕉’幼苗的生长及光合生理,为制定精准养分管理方案提供参考。Abstract: Banana 'Haigong' (Musa AA) seedlings were treated with magnesium (Mg) and zinc (Zn) at gradient concentrations of 0%, 50%, and 100% of normal levels to observe the effects of magnesium and zinc deficiency on the growth and photosynthesis of the seedlings. The results show that after 120 days of treatment, the combined deficiency of Mg and Zn inhibited the growth and photosynthetic physiology of 'Haigong' seedlings. Under normal treatment, the plant height was 32 cm, stem diameter was 8.65 cm, and total root length was 1,051.47 cm; under deficiency treatment, plant height, stem diameter, and total root length were all reduced to varying degrees, with no significant difference in leaf morphology, and the relative growth rate of plant height varied among treatments. In terms of photosynthetic characteristics, there were significant differences in SPAD value, Pn value, Tr value, Ci value, and Gs value between normal and deficiency treatments, and under deficiency treatment the Y(Ⅱ) value and Fv/Fm value decreased, while the NPQ value fluctuated. This study monitored the growth and photosynthetic physiology of banana 'Haigong' seedlings under Mg and Zn deficiency, providing a reference for precise nutrient management.
-
Key words:
- Musa AA /
- magnesium, zinc /
- photosynthetic characteristics
-
图 2 镁、锌协同缺乏处理下‘海贡蕉’幼苗株高的相对生长率
图中不同字母代表各处理组数据存在统计学显著性差异,相同字母代表组间无显著差异。下同。
Fig. 2 The relative growth rate of the plant height of banana 'Haigong' seedlings under the treatment of synergistic deficiency of magnesium and zinc
Different letters in the figure indicate that there are statistically significant differences in the data among different treatment groups, while the same letters indicate no significant differences between groups.Similarly hereinafter.
表 1 不同含量镁、锌协同缺乏处理SPAD值
Table 1 SPAD values of the seedlings under the treatment of synergistic deficiency of magnesium and zinc at different gradient concentrations
处理
Treatment时间 Time/d 0 30 60 90 120 M1Z1 46.57±4.21a 48.47±2.28f 36.80±3.35f 44.63±4.76c 46.03±5.98e M1Z2 39.50±0.36e 58.03±2.92b 44.60±2.63b 42.53±5.85d 40.87±7.10f M1Z3 38.23±4.05f 57.27±1.44b 35.67±2.76g 49.27±2.31a 51.43±2.05b M2Z1 40.87±1.04c 52.30±1.47d 40.57±3.50d 45.50±3.01b 57.07±6.59a M2Z2 36.13±0.67g 44.30±5.78e 41.30±6.03d 39.07±6.94e 47.07±0.50d M2Z3 38.40±4.21f 59.13±3.38a 40.97±4.00d 45.53±2.25b 51.00±1.15b M3Z1 39.83±2.24de 55.53±2.62c 38.60±3.02e 41.87±3.06d 49.50±7.47c M3Z2 40.44±1.94cd 50.80±1.08g 43.27±2.00c 46.13±2.39b 51.17±4.83b M3Z3 42.07±1.08b 55.67±0.50c 48.10±8.61a 42.20±0.15d 51.20±4.07b 注:此结果为平均值±标准误差,不同字母表示差异显著(LSD,P < 0.05)。 Note: This result is the mean value ± standard error. Different letters indicate significant differences (LSD, P < 0.05). -
[1] 何应对. 香蕉幼苗根系对缺钾胁迫的响应及分子机制研究[D]. 武汉: 华中农业大学, 2021. doi: 10.27158/d.cnki.ghznu.2021.000152 [2] 曾鸿运, 吴元立, 黄秉智. 中国香蕉育种研究进展[J]. 果树学报, 2023, 40(11): 2446 − 2465. doi: 10.13925/j.cnki.gsxb.20230151 [3] HUANG P H, CHENG Y T, LU W C, et al. Changes in nutrient content and physicochemical properties of Cavendish bananas var. Pei chiao during ripening[J]. Horticulturae, 2024, 10(4): 384. doi: 10.3390/horticulturae10040384 [4] ANYASI T A, JIDEANI A I O, MCHAU G A. Morphological, physicochemical, and antioxidant profile of noncommercial banana cultivars[J]. Food Science & Nutrition, 2015, 3(3): 221 − 232. doi: 10.1002/fsn3.208 [5] 王芳, 谢江辉. 我国香蕉产业“十三五” 回顾与“十四五” 展望[J]. 中国热带农业, 2022(3): 15 − 22 doi: 10.3969/j.issn.1673-0658.2022.03.003 [6] 许林兵, 张锡炎, 甘东泉, 等. ‘海贡蕉’引种试种研究[J]. 热带农业科学, 2013, 33(8): 24 − 28. doi: 10.3969/j.issn.1009-2196.2013.08.007 [7] 黄思豪, 王丽霞, 刘永霞, 等. 基于机器学习算法预测香蕉产量[J]. 热带生物学报, 2025, 16(1): 21 − 30. doi: 10.15886/j.cnki.rdswxb.20240031 [8] 刘雪红, 吴坤林, 陈国华, 等. “金手指”香蕉的组织培养和快速繁殖[J]. 中国南方果树, 2006, 35(1): 34 − 35. doi: 10.3969/j.issn.1007-1431.2006.01.017 [9] 唐文, 李凯, 李羽佳, 等. 优质绿色皇帝蕉栽培管理技术[J]. 分子植物育种, 2018, 16(8): 2730 − 2735. doi: 10.13271/j.mpb.016.002730 [10] 陈海斌. 香蕉氮磷钾钙镁硫胁迫下的营养特性与营养诊断研究[D]. 广州: 华南农业大学, 2017. [11] 王衍安. 苹果树锌运转分配及缺锌对其生理特性影响的研究[D]. 泰安: 山东农业大学, 2007. doi: 10.7666/d.Y1094387 [12] CHEN L H, XU M, CHENG Z X, et al. Effects of nitrogen deficiency on the photosynthesis, chlorophyll a fluorescence, antioxidant system, and sulfur compounds in Oryza sativa[J]. International Journal of Molecular Sciences, 2024, 25(19): 10409. doi: 10.3390/ijms251910409 [13] SHENG Y J, DING Y W, FU Y Y, et al. The research development of the response mechanisms to magnesium stresses in plants[J]. Botanical Research, 2015, 4(5): 97 − 106. doi: 10.12677/BR.2015.45012 [14] ZHOU Z X, STRUIK P C, GU J F, et al. Enhancing leaf photosynthesis from altered chlorophyll content requires optimal partitioning of nitrogen[J]. Crop and Environment, 2023, 2(1): 24 − 36. doi: 10.1016/j.crope.2023.02.001 [15] 侯扶江, 郑文菊. 紫外线-B辐射与3种植物幼苗的光合作用: 光合作用对紫外线-B敏感性的比较[J]. 西北植物学报, 2000, 20(2): 218 − 223. doi: 10.3321/j.issn:1000-4025.2000.02.011 [16] HAVAUX M, LANNOYE R, 周宽余. 用叶绿素荧光试验快速测定硬粒小麦栽培品种的抗旱性[J]. 麦类作物学报, 1987(2): 32 − 33. [17] LICHTENTHALER H K, RINDERLE U. The role of chlorophyll fluorescence in the detection of stress conditions in plants[J]. C R C Critical Reviews in Analytical Chemistry, 1988, 19(S1): 29 − 85. doi: 10.1080/15476510.1988.10401466 [18] 周春艳. 植物叶片叶绿素荧光动力学成像探测方法与应用研究[D]. 西安: 西安理工大学, 2019. doi: 10.27398/d.cnki.gxalu.2019.000026 [19] HE H S, WU X R, KHAN S, et al. Phenotypic variations in banana cultivars in the utilization and tolerance to different magnesium levels[J]. Horticulturae, 2023, 9(9): 1017. doi: 10.3390/horticulturae9091017 [20] 黄筱涵, 宋思情, 龙丽君, 等. 铅锌胁迫对凹叶厚朴幼苗生理特性的影响[J]. 中南林业科技大学学报, 2023, 43(7): 82 − 90. doi: 10.14067/j.cnki.1673-923x.2023.07.008 [21] 安晓静, 刘尚年, 王海英, 等. 中微量营养元素在药用植物栽培中的应用进展[J]. 中药材, 2024, 47(4): 1045 − 1052. doi: 10.13863/j.issn1001-4454.2024.04.041 [22] 刘桂兰. 微量元素对植物生长发育的作用[J]. 现代农村科技, 2009(3): 55. doi: 10.3969/j.issn.1674-5329.2009.03.056 [23] 林姜岑, 王子豪, 王子琨, 等. 钙、镁缺乏对香蕉幼苗生长及养分吸收的影响[J]. 中国果树, 2023(5): 70 − 75. doi: 10.16626/j.cnki.issn1000-8047.2023.05.012 [24] WINTER K, SCHRAMM M J. Analysis of stomatal and nonstomatal components in the environmental control of CO2 exchange in leaves of Welwitschia mirabilis[J]. Plant Physiology, 1986, 82(1): 173 − 178. doi: 10.1104/pp.82.1.173 [25] THOMAS D S, TURNER D W. Banana (Musa sp. ) leaf gas exchange and chlorophyll fluorescence in response to soil drought, shading and Lamina folding[J]. Scientia Horticulturae, 2001, 90(1/2): 93 − 108. doi: 10.1016/S0304-4238(00)00260-0 [26] FARQUHAR G D, SHARKEY T D. Stomatal conductance and photosynthesis[J]. Annual Review of Plant Biology, 1982, 33: 317 − 345. doi: 10.1146/annurev.pp.33.060182.001533 [27] 高吉权. 铅锌胁迫对毛红椿叶片气体交换和叶绿素荧光的影响[D]. 长沙: 中南林业科技大学, 2019. [28] 陈晓亚, 汤章城. 植物生理与分子生物学[M]. 3版. 北京: 高等教育出版社, 2007. [29] 葛晋金, 孙晓娜, 张丽平, 等. 缺钾对香蕉光合特性和矿质元素含量的影响[J]. 江苏农业科学, 2022, 50(4): 105 − 109. doi: 10.15889/j.issn.1002-1302.2022.04.018 [30] 李紫琴. 不同水分处理下棉花叶片光合参数与叶绿素荧光的高光谱监测研究[D]. 阿拉尔: 塔里木大学, 2023. doi: 10.27708/d.cnki.gtlmd.2023.000370 [31] KALAJI H M, SCHANSKER G, LADLE R J, et al. Frequently asked questions about in vivo chlorophyll fluorescence: practical issues[J]. Photosynthesis Research, 2014, 122(2): 121 − 158. doi: 10.1007/s11120-014-0024-6 [32] GUO Y, TAN J L. Recent advances in the application of chlorophyll a fluorescence from photosystem Ⅱ[J]. Photochemistry and Photobiology, 2015, 91(1): 1 − 14. doi: 10.1111/php.12362 [33] PORCAR-CASTELL A, MALENOVSKÝ Z, MAGNEY T, et al. Chlorophyll a fluorescence illuminates a path connecting plant molecular biology to Earth-system science[J]. Nature Plants, 2021, 7(8): 998 − 1009. doi: 10.1038/s41477-021-00980-4 [34] BOLHÀR-NORDENKAMPF H R, ÖQUIST G. Chlorophyll fluorescence as a tool in photosynthesis research[M]//HALL D O, SCURLOCK J M O, BOLHÀR-NORDENKAMPF H R, et al. Photosynthesis and Production in a Changing Environment. Dordrecht: Springer, 1993: 193−206. doi: 10.1007/978-94-011-1566-7_12 [35] 夏倩. 基于叶绿素荧光的水稻干旱检测技术研究[D]. 无锡: 江南大学, 2023. doi: 10.27169/d.cnki.gwqgu.2023.002565 [36] 刘韵诗. 缺素与黄龙病对柑橘叶片叶绿素荧光特性和初生代谢的影响[D]. 福州: 福建农林大学, 2023. doi: 10.27018/d.cnki.gfjnu.2023.000602 [37] FRIEDL C, FEDOROV D G, RENGER T. Towards a quantitative description of excitonic couplings in photosynthetic pigment-protein complexes: quantum chemistry driven multiscale approaches[J]. Physical Chemistry Chemical Physics, 2022, 24(8): 5014 − 5038. doi: 10.1039/D1CP03566E [38] ARIEF M A A, KIM H, KURNIAWAN H, et al. Chlorophyll fluorescence imaging for early detection of drought and heat stress in strawberry plants[J]. Plants, 2023, 12(6): 1387. doi: 10.3390/plants12061387 [39] 董贞芬. 低温胁迫下番茄幼苗叶绿素荧光成像的分析及研究[D]. 沈阳: 沈阳农业大学, 2019. doi: 10.27327/d.cnki.gshnu.2019.000682 -




 下载:
下载: