-
植物工厂是一种依托现代数字化技术与智慧农业精准理念构建的集约化农业生产系统[1],其核心是通过可控的垂直栽培平台对作物生长环境进行精细化管理,消除自然条件波动以及病虫害对作物生长的影响[2]。这种高效种植模式相较于传统的大田种植模式具有非常显著的特点:1)植物工厂环境完全可控,借助传感设备、智能调控技术,对光照、温度、湿度以及水肥配比等作物生长核心要素进行实时调节,保障作物生长环境的稳定[3];2)种植高效化,植物工厂采用垂直栽培模式,实现向上要空间的发展理念,大幅度提升单位面积的利用率,同时可通过人为控制光照时长和强度,促进作物的生长发育过程,缩短生长周期[4];3)生产模式绿色节约,植物工厂采用水循环系统培养作物,不仅大大减少了水资源的消耗,还显著减少了肥料用量,又因其环境可控无菌,可以实现零病虫害和零农药使用[5];4)植物工厂布局灵活,因其对土地条件无要求,可以在集装箱、城区房屋等非耕地空间搭建,不受地域和气候的制约[6]。目前,全球粮食安全正面临着前所未有的严峻挑战,耕地面积锐减、土壤盐碱化严重、人口数量上升与极端天气频发的叠加影响,已导致传统大田农业生产的稳定性遭受严重冲击[7],急需新型农业生产模式来破解粮食安全困局。而植物工厂这一先进的农业新质生产力,凭借其环境精准可控的优势,成为应对粮食安全困局的重要手段,可消除传统种植对自然环境及土地的依赖,有效推动农业从“看天吃饭”的传统模式向“按需生产”的工业化模式跨越[8],对推动农业产业结构升级、提升粮食生产稳定性及拓展主粮生产新空间具有不可替代的支撑作用。
小麦(Triticum aestivum)作为最重要的粮食作物之一,是全球35%~40%人口的主粮,其种植区覆盖亚、欧、美等大洲的主要农业区,是全世界的第一大口粮作物[9]。近些年,随着耕地资源日趋紧张、极端气候频发、人口规模激增,对小麦产业的健康稳定发展提出了更高的要求。随着植物工厂的兴起,为小麦工厂化种植提供了实现路径,也成为满足这一要求的全新解决方案。但目前尚无适宜于植物工厂化生产的小麦品系(种),育种空白直接制约工厂化小麦生产的实施。因此,创制出适合植物工厂生产的矮秆早熟的小麦新材料,填补这一技术缺口,已成为保障粮食安全、推动小麦工厂化生产的迫切任务。目前,已报道的小麦矮秆基因有28个,但大田生产中广泛利用的较少[10],且其作用机理基本清晰。关于小麦生育期调控的报道高度集中在少数经典调控通路的核心基因,其中春化基因(Vrn系列)与光周期基因(Ppd系列)的研究最为深入[11]。在春化基因方面,Yan等[12]首次克隆出小麦春化基因Vrn1,证实了其作为春化响应的核心基因,通过春化解除Vrn1基因沉默从而启动小麦花芽分化,而Vrn2则以负调控因子的身份抑制开花进程,Vrn3(即FT1)则可介导春化信号下游通路,加速生育进程,这3类基因的等位变异组合直接决定小麦对低温春化的需求时长,是区分冬小麦、半冬小麦与春小麦的关键遗传基础。在光周期途径中,Beales等[13]对Ppd-D1基因的克隆与功能验证揭示,该基因通过感知日照长度调控从营养生长到生殖生长(开花)的转换,其显性等位基因可显著缩短小麦对长日照的依赖时间,促使小麦提早开花。Zhang等[14]针对Ppd-A1和Ppd-B1的研究进一步补充,不同亚基因组的Ppd基因存在功能冗余与协同作用,其变异类型与小麦在不同纬度地区的种植适配性密切相关。此外,开花基因也是研究热点之一,如Trevaskis等[15]的研究证实,FT基因家族作为开花信号的“整合子”,可整合春化、光周期信号,通过在叶片中表达并向茎尖分生组织转运,启动开花相关基因的级联表达;而SOC1、LFY等下游基因则通过调控花器官发育,最终影响小麦从营养生长向生殖生长转换的节点,进而调控全生育期长度[16]。但是现有研究体系依旧存在显著的局限性。首先是研究对象局限于上述已知基因家族,对小麦基因组中其他潜在生育期调控基因的挖掘严重不足,且多数研究聚焦单一基因的功能验证,忽略了不同基因间的互作网络及多基因聚合对生育期的综合调控效应。其次是现有研究多基于大田自然环境开展,不适用于植物工厂环境。
本研究希望通过遗传分析,定位到控制小麦生育期的新遗传位点。因此,本研究以生育期较短且产量表现优异的小麦品种‘科农9204’为母本,以矮化材料且株型优良的小麦株系‘R3764-310’作为父本,通过人工杂交手段获得F1代群体。采用PCR以及电泳检测技术对F1代植株进行基因型鉴定[17],获得‘K310-4’、‘K310-6’2株杂合植株,通过对比2个材料的株高、穗长、穗粒数等表型数据后,最终确定以‘K310-4’作为核心实验材料,进一步繁育获得80株F2代植株。通过表型观测发现,F2代植株的生育期存在显著差异,其中,最短生育期为63 d,最长生育期为120 d。基于上述表型数据,采用混池测序技术(BSA-seq)进行遗传定位分析,最终在1B染色体上检测到1个全新的与小麦生育期性状显著关联的候选区域及特征SNP位点。同时,本研究通过表型观测等方法,在4代的自交后代中连续选择具有株矮和早熟特性的小麦材料,最终成功获得了适宜于植物工厂生产的株矮早熟小麦新品系。
-
本研究的实验材料包括119份矮化小麦材料(株高<50 cm)、‘科农2009’、‘科农2007’、‘科农9204’、‘济试42’、‘济麦20’、‘小偃503’、‘二芒麦’、‘兰考86’和‘矮抗58’等多个小麦品种,所有材料均为凌宏清老师课题组提供。其中,‘R3764-310’为‘宛原选9’与‘石
4185 ’杂交后获得的遗传稳定矮秆小麦品系,属冬性小麦;‘科农9204’为中国科学院遗传与发育生物学研究所农业资源研究中心以‘89-6021 ’与‘SA502’为亲本杂交选育而成的半冬性小麦品种。所有实验材料均在崖州湾国家实验室植物工厂内完成栽培试验。植物工厂情况如下:配备6套栽培模组,每套模组设3层,每层高度为70 cm;每层上方配置VE02灯管11根,下方设置规格为900 mm×600 mm×30 mm的定植板。栽培系统采用深液流循环方式,每3套模组共用1个独立水箱。工厂内部设有中央空调系统、控湿系统及新风系统,用于调控温度、湿度及空气环境,外接灯光控制系统以实现光照时间的精准设定。
播种前,所有小麦材料均以纯水浸种6 h,随后置于铺有湿润滤纸的培养皿中,在室温、黑暗条件下进行催芽。待种子露白后,将其播种于吸饱水分的海绵块中,海绵块放置于规格为60 cm×29.5 cm×4.9 cm的幼苗托盘内,在每天12 h光照条件培养7 d,期间每2天补充1次叶菜类营养液(购自福建省中科生物股份有限公司)。当幼苗株高达到5 ~ 8 cm时,在10℃、22 h·d−1光照的条件下春化30 d。春化结束后,将幼苗定植于定植板上,株距为10 cm×10 cm,定植后光周期设定为每天18 h光照,环境温度(20± 3)℃,相对湿度(60± 5 )%,并设置超限报警机制。定植后每3天对营养液浓度及pH值进行监测与调节。其中,营养液浓度以电导率(EC)表示:定植初期EC值设定为(1.2±0.1)mS · cm−1,随后每周递增0.1 mS · cm−1,最终稳定在(1.6±0.1)mS · cm−1,pH5.5 ~ 6.5。
-
本研究前期在植物工厂条件下对所有材料进行了多轮栽培评价,发现‘R3764-310’在119份矮化品系中较矮且穗部性状较好,而‘科农9204’无需春化就可正常抽穗结实。因此,本研究以‘科农9204’为母本、‘R3764-310’为父本,进行杂交获得F1后,通过自交获得F2分离群体,用于早熟遗传位点定位。
进行早熟位点定位时选用外显子混池测序,该方法具有成本低、通量高、数据量小等特点,可从大规模群体中直接筛选出功能区域的共性变异,是进行初步基因筛查和定位的高效工具。在F2群体中,根据抽穗时间筛选出“早熟”和“晚熟”极端表型个体各20株,分别取其幼嫩叶片,提取DNA,并进行均一化处理后,构建两个极端表型DNA混池(即“早熟池”和“晚熟池”)。对2个DNA混池进行超声破碎处理,将基因组DNA随机打断为300 ~ 500 bp的片段,经琼脂糖凝胶电泳回收目标长度片段后进行末端修复,并在片段两端连接含样本索引序列的测序接头,以区分不同混池。随后通过PCR扩增富集文库片段,并采用磁珠法纯化PCR产物以去除引物二聚体及非特异性扩增片段,获得合格的测序文库。文库构建完成后进行高通量测序,采用150 bp双端测序模式。对获得的原始测序数据进行质量控制,去除接头序列及低质量reads(Q值<20),获得高质量清洁数据(Clean reads)约50 Gb,对应小麦全基因外显子区域平均覆盖深度约100×。将清洁数据与小麦参考基因组进行比对(采用BWA软件),并利用GATK工具检测两个混池中的单核苷酸多态性(SNP),筛选覆盖深度≥5×、基因型质量值(QUAL≥40的高质量变异位点。在此基础上,进一步筛选在“早熟池”和“晚熟池”之间存在显著等位基因频率差异的多态性SNP,并分析其在染色体上的分布特征,从而定位与小麦生育期性状显著关联的候选QTL区域。最后,根据候选区域内的多态性SNP位点开发分子标记(表1)。
表 1 本研究所用的引物
Table 1. The primers used in this experimentf
引物名称Primer 序列(5'−3')
Sequence(5'−3')位置
Location大小/bp
Size/bp8F ATCATACAGTCTAGCCCACA 35281088 141 8R CGTCATGTTCTAATTCGTTCC 11F CATCCCAAAACCTCCTCCTC 5612495 151 11R GCAAGAAAGAACACCACAAGATTC 29F CTCTGAGCTTTCTTCCTCCTC 25976456 183 29R GGACAAGACAGAGAGAGAAAC 32F CGTACAAGATGGGCCAGTTCGATC 9782974 103 32R GCATACATGATCCAAGAGTGATGG -
观察和记录抽穗期,小麦成熟后统计株高、有效穗数、穗长、穗粒数等指标,其中株高为海绵块上端至主穗顶端(不含芒)的长度,有效穗数为正常结实穗的数量,穗长为穗基部到顶部(不含芒)的长度,穗粒数为主穗结实的粒数。粒长、粒宽、千粒重等指标通过TPKZ-1-G自动考种分析仪获得。
所有数据采用Microsoft Excel进行整理与统计,图表绘制采用Origin软件完成。
-
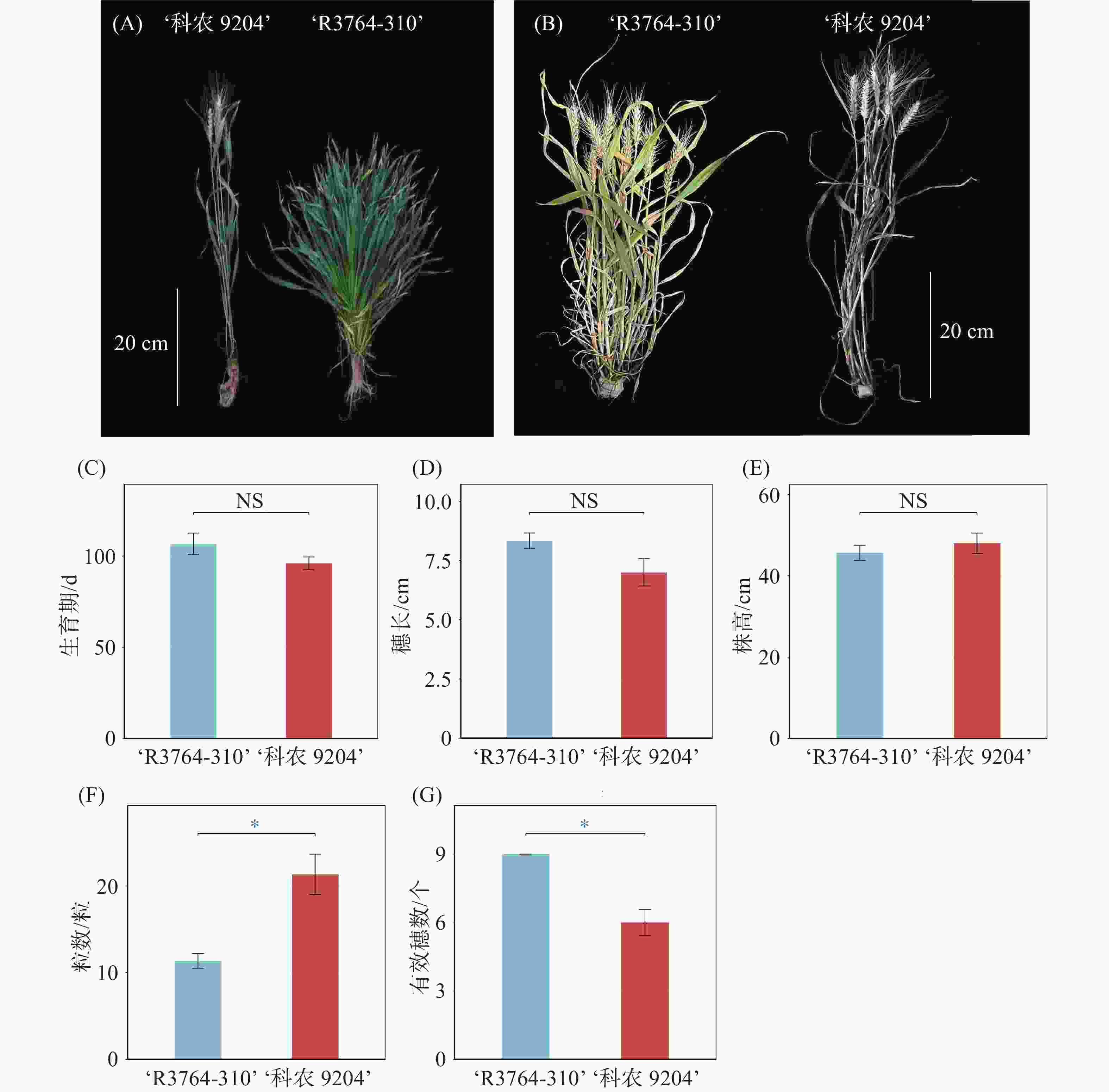
考虑到植物工厂集约化栽培模式需要株矮、早熟且产量优良的小麦品种。因此,将前期选育获得的119份矮化(株高<50 cm)小麦材料在植物工厂条件下进行了3次栽培实验,评价其工厂化栽培适应性,发现‘R3764-310’品系在植物工厂栽培条件下的综合表现良好,其株高为46 cm,适合植物工厂对小麦株高的培养需求。但该材料不经春化处理时不能正常抽穗结实(图1-A),经过1个月的春化处理后,能正常开花结实,整个生育期为108 d,同时该材料在植物工厂中其他农艺性状均较好(图1-B)。由于该品系需要春化,生育期相对较长,不符合植物工厂快速生产的要求,并会增加生产成本,需要进行改良。同时,选取‘科农2009’、‘科农2007’、‘科农9204’、‘济试42’、‘济麦20’、‘小偃503’、‘二芒麦’、‘兰考86’、‘矮抗58’等多个小麦品种,于植物工厂环境中进行种植评价。结果表明‘科农9204’无需春化处理即可正常生长,其生育期约90 d,平均单株穗数为5个,平均每穗达25粒,且株型笔直粗壮,抗倒伏能力强,株高为51 cm,可作为改良‘R3764-310’的亲本(图1-B)。‘科农9204’和‘R3764-310’能够完美地在株高、穗数、生育期、穗粒数等关键性状(如产量和株型)方面形成良好互补,可以满足杂交对亲本性状互补的核心需求,因此,我们以‘科农9204’为母本,‘R3764-310’为父本进行矮秆、早熟小麦新材料的创制。
-
为了获得矮秆、早熟适宜于植物工厂栽培的小麦新种质,用上述筛选出的适宜植物工厂栽培的早熟品种‘科农9204’为母本,以矮秆品系‘R3764-310’为父本,进行杂交,获得7株F1代植株。为了进一步确认杂交的准确性,设计了在‘科农9204’和‘R3764-310’之间存在多态性的InDel(Insertion and Deletion)标记,对F1代植株进行PCR扩增与电泳检测后发现,编号为‘K310-4’和‘K310-6’的植株扩增产物呈现出两条清晰可辨的条带,且两条条带分别与父本‘R3764-310’、母本‘科农9204’的特征条带完全对应(图2-A),表明它们同时携带双亲的遗传物质,可明确判定为杂合基因型植株。
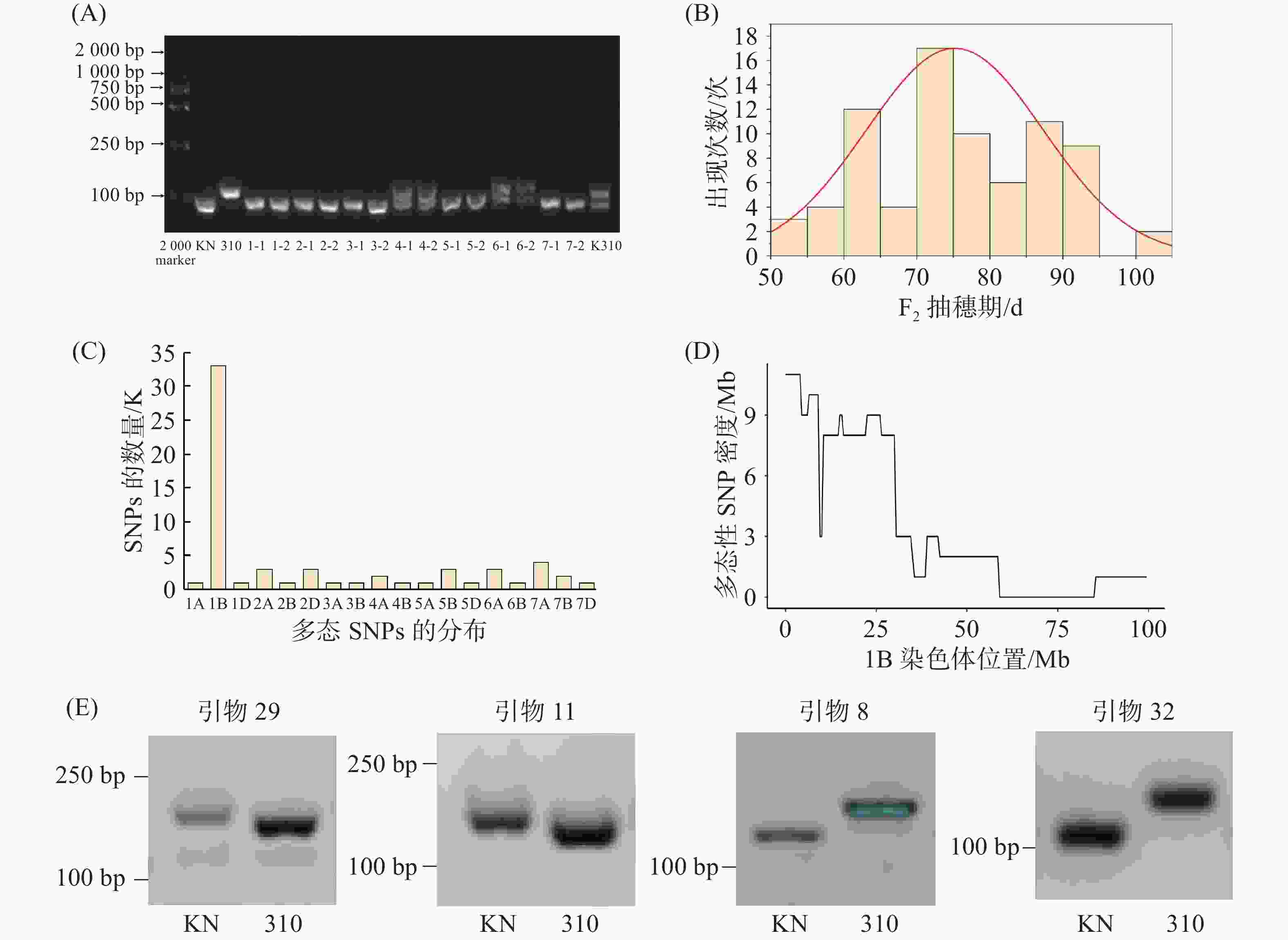
图 2 F1植株鉴定结果和早熟位点的定位
Figure 2. Confirmation of heterozygous F1 plants and mapping of the early mature locus
进一步以‘K310-4’为实验对象,通过自交获得了F2的分离群体。表型观察发现,F2代植株在没有春化处理时生育期呈明显分离,早抽穗到晚抽穗的表型差异显著,且该群体生育期呈正态分布,最早成熟的材料生育期为63 d,而最晚成熟材料的生育期则为120 d(图2-B)。
-
为了解析‘科农9204’与‘R3764-310’衍生的F2群体中控制早熟的遗传位点,我们在该F2群体中分别挑选了20株早抽穗单株和20株晚抽穗单株,构建了“早熟池”和“晚熟池”。然后对“早熟池”和“晚熟池”DNA进行外显子捕获测序,并通过生物信息学分析,鉴定“早熟池”和“晚熟池”之间的多态性SNP,并统计其在小麦21条染色体上的分布。结果显示,不同染色体的多态性SNP位点数量差异显著:1B染色体检测到33个,数量最多;7A染色体次之,为4个;2A、2D、5B、6A各3个;4A、7B各2个;1A、1D等12条染色体各1个(图2-C)。其中,1B染色体的多态性SNP位点数量远高于其他染色体,提示该染色体可能含有调控生育期的相关遗传区域。为了进一步确定控制早熟位点在1B染色体上的准确位置,本研究对1B染色体上多态性SNPs的分布密度进行了分析,最终将小麦生育期相关基因的候选区域锁定在1B染色体的3~45 Mb区间内(图2-D)。通过与前人已发表的早熟位点进行对比分析表明,该位点是一个全新的小麦生育期控制位点。在此基础上,笔者在该候选区间内根据SNP多态性,设计了4个分子标记(图2-E),对该群体检测,结果发现,这4个SNPs均与生育期呈现紧密连锁,可作为检测该位点的分子标记,为后续精细定位和深入解析该小麦生育期遗传位点提供了分子标记基础。
-
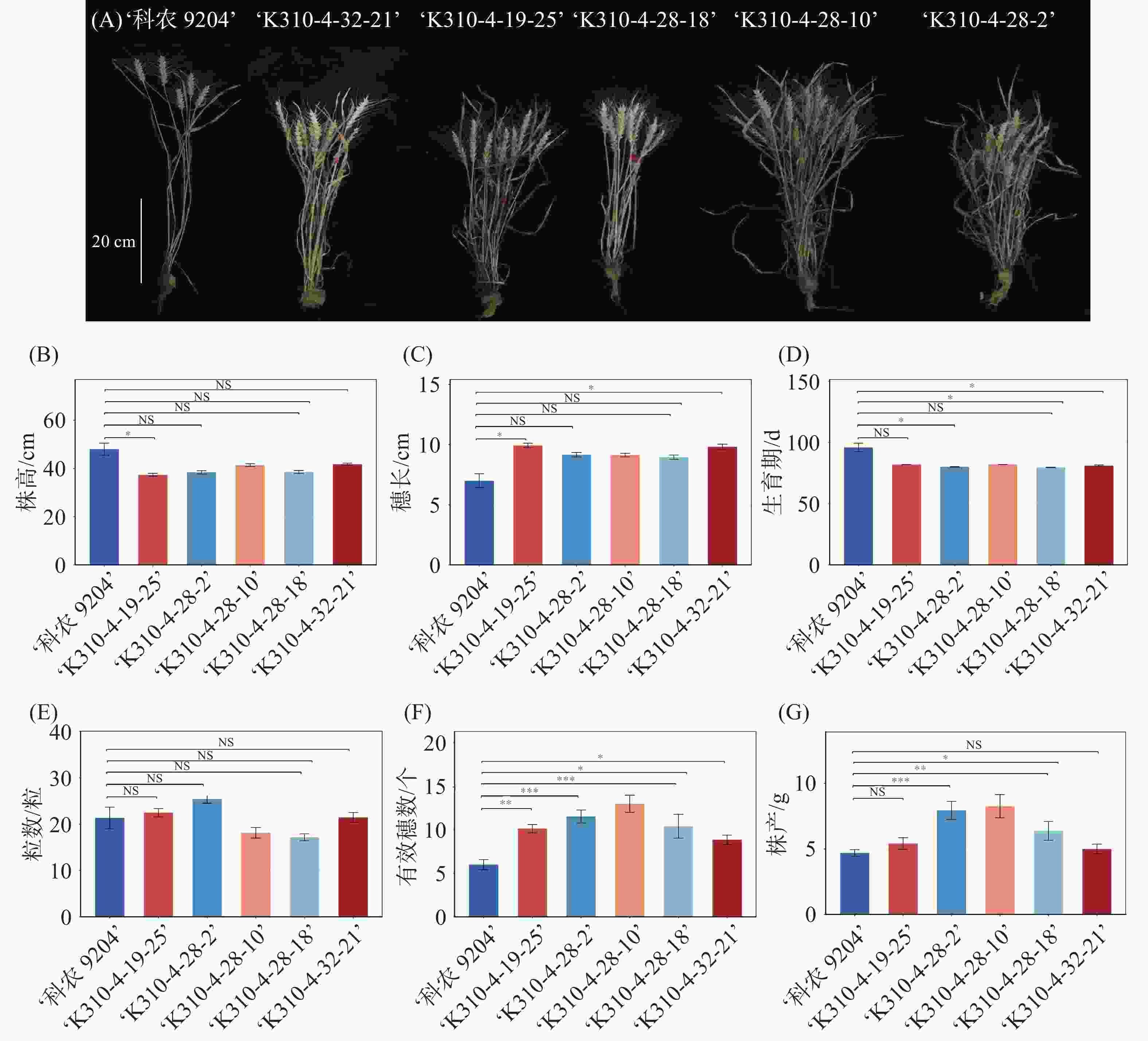
通过将‘科农9204’与‘R3764-310’进行杂交,获得F1代杂合植株‘K310-4’,将该材料通过“多代自交+表型鉴定”的方法,围绕植物工厂规模化种植对小麦“矮化、早熟、高产”的核心需求进行选育。首先本研究确定了筛选指标体系:以株高30~45 cm、生育期60~90 d为筛选材料的第1标准,同时将矮化与早熟性状二者兼顾并重,在此基础上进一步选取株型紧凑、分蘖数量多、穗粒数多、单株产量表现优异的材料。在F2~F4各世代的种植过程中,按上述指标逐代进行单株筛选与自交纯化,通过连续4代的定向选择,逐步淘汰性状分离的个体材料、富集具有优良性状的个体,最终在F4代750株材料的种植群体中,获得遗传背景相对稳定、矮化特性稳定且生育期短的优良品系5份:‘K310-4-19-25’、‘K310-4-28-10’、‘K310-4-28-2’、‘K310-4-28-18’和‘K310-4-32-21’。这5份优良品系的株高稳定在37~42 cm,生育期缩短至80 d左右,有效分蘖可达到9~13个,符合植物工厂规模化种植对“株高、成熟期、分蘖力及单株产量”的需求,在植物工厂条件下1年至少可以收获4代,为培育适宜于植物工厂栽培的小麦新品(系)种提供了重要的材料基础,也为未来工厂化小麦生产打下了良好基础。
-
植物工厂作为依托数字化技术与智慧农业理念的集约化生产系统,其核心优势为小麦育种带来了突破性支撑[18]。该系统通过传感设备与智能调控技术,实现了光照、温度、湿度及水肥配比的精准控制,彻底消除了自然环境波动与病虫害的干扰,可为小麦生长提供稳定均一的最优环境。而本研究采取每天18 h光照、6 h黑暗的光照组合可有效缩短小麦的生长周期,配合循环水培系统,既可减少水资源与肥料消耗,又实现了零农药使用的绿色生产[19]。在全球耕地资源紧张、极端天气频发的背景下,植物工厂突破了传统大田农业的局限,推动小麦生产向标准化、规模化、高效化的工业化模式转型。本研究以植物工厂为载体,定向创制适宜于特定栽培场景的小麦种质,为后续其他作物在植物工厂中的种质创制提供了可靠经验。
-
小麦生育期是决定品种区域适应性及育种周期的核心农艺性状,主要受春化和光周期通路协同调控。其中,春化调控通路相关基因包括Vrn-1、Vrn-2、Vrn-3和Vrn-4,Vrn-1是开花促进因子,在6倍体小麦基因组中有3个同源基因:Vrn-A1、Vrn-B1和Vrn-D1,分别定位在5AL、5BL和5DL上;Vrn-2是开花抑制因子,定位在第五同源群染色体短臂上;Vrn-3与拟南芥和大麦的FT基因同源,受低温和长日照协同调控,是小麦开花正调控因子,定位于第七同源群染色体上;Vrn-4基因定位于5D染色体短臂靠近着丝粒区域,功能与Vrn-B1、Vrn-D1相似[20-22]。光周期相关基因主要为Ppd-A1、Ppd-B1和Ppd-D1,分别定位在2AS、2BS和2DS上[21, 23]。本研究在1B染色体3~45 Mb区间定位到控制生育期的相关候选区域及特征SNP位点,与已报道的生育期相关基因定位区域均不同,是目前尚未见报道的全新遗传位点,这一发现为小麦生育期调控提供了新的基因资源和材料资源。笔者认为,该位点的成功挖掘可能与植物工厂独特的种植环境密切相关。
现有小麦生育期研究多基于大田自然环境或传统温室开展,传统温室常采用单一蓝光或红光光源[24-25],而本研究使用的植物工厂配备了VE02灯管组合光源,其光谱更为全面,结合精准调控的温湿度、光周期及营养液,形成了更贴近小麦生长需求的最优环境。传统研究中,单一或受限的生长条件可能导致该位点的功能被掩盖,而在植物工厂稳定的栽培条件下,使其调控生育期的效应得以充分显现。这一结果也表明,植物工厂不仅是优质生产平台,更是挖掘作物潜在遗传位点的新研究载体。
-
通过杂交育种与连续4代自交筛选,本研究培育的小麦新种质完美契合植物工厂规模化种植需求,展现出显著的性状优势。在生育期方面,选育新种质实现了82 d的成熟周期,相较于母本‘科农9204’的90 d生育期缩短了8 d,远优于父本‘R3764-310’的108 d,充分满足了植物工厂高效生产的核心需求。而株高方面,所有优良品系的株高均控制在30~45 cm范围内,符合植物工厂垂直栽培对矮化性状的要求,有效避免了倒伏风险,也为多层栽培的空间利用提供了保障。产量性能上,新种质整合了母本‘科农9204’穗粒数多与父本‘R3764-310’分蘖能力强的优良特性,通过性状互补实现了单株产量的提升,其单株产量优于母本‘科农9204’,为植物工厂小麦规模化生产的高产目标奠定了坚实基础。这些优良性状的聚合,证明了通过定向杂交与多代筛选,能够创制出适配植物工厂环境的专用小麦种质,也为后续主粮作物的工厂化栽培提供了可行的育种思路。
-
在极端天气频发,耕地紧张,粮食需求不断增大的今天,传统小麦大田生产模式在保障粮食稳定供给的方面,面临严峻的挑战。植物工厂凭借着高度可控且稳定的生产环境与无场地限制的特性,为主粮作物规模化生产在非传统农业空间中的生产开辟出一条新的道路,尤其适用于青海、西藏等耕地资源有限或成都等人口高度集中的地区。本研究创制的矮秆早熟小麦新种质在植物工厂条件下表现出稳定的早熟特性和良好的综合农艺性状,揭示了适宜于植物工厂小麦新种质在未来小麦工厂化规模化种植的潜力。此外,本研究材料在植物工厂条件下可实现1年4代连续生产,相较于传统小麦生产模式显著提高了单位时间和单位空间的生产效率。这种全新高效的生产模式不仅有助于提升粮食供给能力,也为加快优良性状的遗传改良和新品种选育提供了有利条件。从应用角度来看,位于1B染色体上的早熟新位点及其所携带的矮秆早熟种质,为植物工厂专用小麦的进一步改良提供了关键的遗传基础。后续研究可围绕该位点开展更为精细的定位与功能解析,并在不同植物工厂运行条件下,对相关新品种的产量表现和稳定性进行系统评估。同时,结合商业化生产条件下的规模化试验,进一步分析其通过提高年复种指数所带来的单位面积经济效益提升潜力。
-
本研究围绕植物工厂规模化种植对矮秆、早熟小麦种质的需求,以定向杂交、多代自交筛选与分子遗传定位为核心技术路线开展研究,最终达成预计目标。首先通过筛选出性状互补的亲本,为种质创制奠定基础;其次,借助外显子混池测序技术在1B染色体3~45 Mb区间成功定位到与小麦生育期显著关联的候选区域并开发紧密连锁SNP标记,填补了植物工厂环境下小麦生育期调控新基因的研究空白。再者,通过连续4代自交与定向表型筛选,创制出5份适配植物工厂栽培的小麦新种质,其株高稳定在30~45 cm、生育期缩短至82 d(可实现1年4代),且所选材料聚合了双亲分蘖能力强与穗粒数多的优势,单株产量皆优于母本‘科农9204’,符合植物工厂株矮,生育期短和产量高的需求;同时,验证了植物工厂作为小麦育种与遗传研究平台的独特价值,其精准可控的环境不仅保障育种筛选准确性,还能显现传统环境中被掩盖的遗传位点功能,为作物专用种质定向创制提供新路径。此外,研究因样本量限制未能充分挖掘更极端优异材料,未来可通过扩大群体规模,精细定位目标基因、验证基因功能,并进一步优化新种质的产量与环境适应性。本研究创制的新种质及相关技术方法,也为植物工厂小麦规模化生产及其他主粮作物工厂化适配育种提供了新材料和新思路。
矮秆早熟的植物工厂小麦品种创制及早熟位点定位
DOI: 10.15886/j.cnki.rdswxb.20250205
 CSTR: 32425.14.j.cnki.rdswxb.20240005
CSTR: 32425.14.j.cnki.rdswxb.20240005
Development of dwarf early-maturing wheat for cultivation in plant factories and identification of early-maturing loci
-
摘要: 在耕地资源日趋紧张、极端气候频发和人口规模激增的当下,植物工厂因其占地面积少、生产环境可控等优势,已逐渐成为农业生产的重要形式。但目前尚缺乏适用于植物工厂种植与生产的小麦专用品种,因此,本研究以创制适宜于植物工厂生产的小麦新种质为目标,通过分子标记辅助选择,成功创制出了适宜于植物工厂生产的矮秆、早熟小麦新种质。并通过外显子混池测序定位到了一个全新的控制小麦早熟的遗传位点(1B染色体)。矮秆早熟新种质的创制和早熟新遗传位点的定位,为小麦工厂化生产奠定了坚实的材料和理论基础。Abstract: With arable land resources becoming increasingly scarce, extreme weather events occurring more frequently, and population growth accelerating, plant factories have gradually emerged as a vital form of agricultural production due to their advantages of minimal land requirements and controllable production environments. However, there remains a lack of wheat varieties specifically suited for cultivation and production in plant factories. Therefore, an attempt was made to develop new wheat germplasm suitable for plant factory production. Through marker-assisted selection, new accessions of dwarf, early-maturing wheat germplasm suitable for plant factory production were successfully developed. Furthermore, through exome sequencing, a novel genetic locus controlling wheat early maturity was identifiedon chromosome 1B. The development of these dwarf, early-maturing wheat germplasm and the identification of a novel genetic locus for early maturity provide a robust material and theoretical foundation for the industrialized production of wheat.
-
Key words:
- plant factory /
- wheat /
- early-maturing /
- plant height /
- gene mapping
-
图 2 F1植株鉴定结果和早熟位点的定位
注:(A)F1代植株的PCR分子标记检测结果:KN为母本‘科农9204’,310为父本‘R3764-310’,1-7代表7个F1单株,-1与-2为单株重复样本,‘K310’为‘科农9204’与‘R3764-310’混合样本;(B)‘KN9204’与‘R3764-310’衍生的F2群体抽穗期分布直方图;(C)基于多态性SNP定位到1B染色体上的生育期基因;(D)候选区间内双亲多态性SNP分布密度图;(E)开发标记在亲本中的检测结果。
Fig. 2 Confirmation of heterozygous F1 plants and mapping of the early mature locus
Note: (A) PCR-based molecular marker detection results of F1 plants: KN represents the maternal line ‘Kenong 9204’; 310 represents the paternal line ‘R3764-310’; numbers 1-7 denote seven individual F1 plants; -1 and -2 indicate replicate samples of the same plant; K310 represents a mixed sample of ‘Kenong 9204’ and ‘R3764-310’. (B) Distribution histogram of heading date in the F2 population derived from ‘KN9204’ and ‘R3764-310’; (C) Localization of the growth period gene on chromosome 1B based on polymorphic SNPs. (D) Distribution density plot of polymorphic SNPs between the two parents within the candidate interval. (E) Detection results of the developed markers in the parental lines.
图 3 F4代优秀选系的表型及农艺性状统计分析
注:(A)亲本‘科农9204’与衍生选系‘K310-4-32-21’、‘K310-4-19-25’、‘K310-4-28-18’、‘K310-4-28-10’、‘K310-4-28-2’的表型对比;(B)株高、(C)穗长、(D)生育期、(E)粒数、(F)有效穗数和(G)株产等农艺性状的统计比较。
Fig. 3 Phenotypes and statistic analysis of agronomic traits of selected elite F4 lines
Note: (A) Phenotypic comparison of the parental line ‘Kenong 9204’ with its derived selected lines ‘K310-4-32-21’, ‘K310-4-19-25’, ‘K310-4-28-18’, ‘K310-4-28-10’, and ‘K310-4-28-2’; (B) Statistical comparison of agronomic traits, including plant height (B), panicle length (C), growth period (D), grain number (E), number of effective panicles (F), and yield per plant (G).
表 1 本研究所用的引物
Table 1 The primers used in this experimentf
引物名称Primer 序列(5'−3')
Sequence(5'−3')位置
Location大小/bp
Size/bp8F ATCATACAGTCTAGCCCACA 35281088 141 8R CGTCATGTTCTAATTCGTTCC 11F CATCCCAAAACCTCCTCCTC 5612495 151 11R GCAAGAAAGAACACCACAAGATTC 29F CTCTGAGCTTTCTTCCTCCTC 25976456 183 29R GGACAAGACAGAGAGAGAAAC 32F CGTACAAGATGGGCCAGTTCGATC 9782974 103 32R GCATACATGATCCAAGAGTGATGG -
[1] Kaya C. Intelligent environmental control in plant factories: integrating sensors, automation, and AI for optimal crop production [J]. Food and Energy Security, 2025, 14(1): e70026. https://doi.org/10.1002/fes3.70026 doi: 10.1002/fes3.70026 [2] Bhattarai K, Ogden A B, Pandey S, et al. Improvement of crop production in controlled environment agriculture through breeding [J]. Frontiers in Plant Science, 2025, 15: 1524601. https://doi.org/10.3389/FPLS.2024.1524601 doi: 10.3389/FPLS.2024.1524601 [3] 郭威, 吴华瑞, 郭旺, 等. 特色农产品设施环境下品质智能管控技术研究现状与展望 [J]. 智慧农业(中英文), 2024, 6(6): 44−62. https://doi.org/10.12133/j.smartag.SA202411017 doi: 10.12133/j.smartag.SA202411017 [4] 李鑫龙, 张玉琪, 程瑞锋, 等. 植物工厂环境调控及栽培措施对玉米生长的影响 [J]. 农业工程学报, 2025, 41(18): 227−234. [5] Asaduzzaman M, Asao T. Autotoxicity in strawberry under recycled hydroponics and its mitigation methods [J]. The Horticulture Journal, 2020, 89(2): 124−137. https://doi.org/10.2503/hortj.UTD-R009 doi: 10.2503/hortj.UTD-R009 [6] Avgoustaki D D, Xydis G. Plant factories in the water-food-energy Nexus era: a systematic bibliographical review [J]. Food Security, 2020, 12(2): 253−268. https://doi.org/10.1007/s12571-019-01003-z doi: 10.1007/s12571-019-01003-z [7] Sowmya C, Anand M, Rani C I, et al. Recent developments and inventive approaches in vertical farming [J]. Frontiers in Sustainable Food Systems, 2024, 8: 1400787. https://doi.org/10.3389/fsufs.2024.1400787 doi: 10.3389/fsufs.2024.1400787 [8] Ahmed N, Zhang B G, Deng L S, et al. Advancing horizons in vegetable cultivation: a journey from ageold practices to high-tech greenhouse cultivation−a review [J]. Frontiers in Plant Science, 2024, 15: 1357153. https://doi.org/10.3389/FPLS.2024.1357153 doi: 10.3389/FPLS.2024.1357153 [9] 金艳, 宋全昊, 宋佳静, 等. 69份小麦种质资源的综合性评价[J]. 中国农业科技导报, 2024, 26(2): 33−45. https://doi.org/10.13304/j.nykjdb.2023.0583 doi: 10.13304/j.nykjdb.2023.0583 [10] 李彩华, 赵彦坤, 李占坤, 等. 小麦矮秆基因研究进展[J]. 生物技术进展, 2024, 14(6): 980−992. https://doi.org/10.19586/j.2095-2341.2024.0084 doi: 10.19586/j.2095-2341.2024.0084 [11] 高振贤, 赵彦坤, 班进福, 等. 河北省小麦重要农艺性状的KASP标记检测[J]. 分子植物育种, 2021, 19(2): 518−528. https://doi.org/10.13271/j.mpb.019.000518 doi: 10.13271/j.mpb.019.000518 [12] Yan L, Loukoianov A, Tranquilli G, et al. Positional cloning of the wheat vernalization gene VRN1 [J]. Proceedings of the National Academy of Sciences of the United States of America, 2003, 100(10): 6263−6268. https://doi.org/10.1073/pnas.0937399100 doi: 10.1073/pnas.0937399100 [13] Yan L L, Loukoianov A, Blechl A, et al. The wheat VRN2 gene is a flowering repressor down-regulated by vernalization [J]. Science, 2004, 303(5664): 1640−1644. https://doi.org/10.1126/science.1094305 doi: 10.1126/science.1094305 [14] Beales J, Turner A, Griffiths S, et al. A Pseudo-Response Regulator is misexpressed in the photoperiod insensitive Ppd-D1a mutant of wheat (Triticum aestivum L. ) [J]. Theoretical and Applied Genetics, 2007, 115(5): 721−733. https://doi.org/10.1007/s00122-007-0603-4 doi: 10.1007/s00122-007-0603-4 [15] Trevaskis B, Bagnall D J, Ellis M H, et al. MADS box genes control vernalization-induced flowering in cereals [J]. Proceedings of the National Academy of Sciences of the United States of America, 2003, 100(22): 13099−13104. https://doi.org/10.1073/pnas.1635053100 doi: 10.1073/pnas.1635053100 [16] Benaouda S, Stöcker T, Schoof H, et al. Transcriptome profiling at the transition to the reproductive stage uncovers stage and tissue-specific genes in wheat [J]. BMC Plant Biology, 2023, 23(1): 25. https://doi.org/10.1186/S12870-022-03986-Y doi: 10.1186/S12870-022-03986-Y [17] Ali M, Polgári D, Sepsi A, et al. Rapid and cost-effective molecular karyotyping in wheat, barley, and their cross-progeny by chromosome-specific multiplex PCR [J]. Plant Methods, 2024, 20(1): 37. https://doi.org/10.1186/s13007-024-01162-x doi: 10.1186/s13007-024-01162-x [18] 吕艳. 数字植物工厂技术正式步入家庭生活[J]. 农业工程技术(温室园艺), 2010(34): 58−59. https://doi.org/10.3969/j.issn.1673-5404-B.2010.12.020 doi: 10.3969/j.issn.1673-5404-B.2010.12.020 [19] 陈龙, 高志强, 金宇豪. 植物工厂条件下不同光通量密度对水稻生长发育的影响[J]. 中国稻米, 2025, 31(3): 30−36. https://doi.org/10.3969/j.issn.1006-8082.2025.03.005 doi: 10.3969/j.issn.1006-8082.2025.03.005 [20] 杨芳萍,韩利明,阎俊,等.春化和光周期基因等位变异在23个国家小麦品种中的分布[J].作物学报,2011,37(11):1917−1925. [21] Balashova I , Fait V .Allele frequencies of Ppd-D1a, Ppd-B1a, and Ppd-B1c of photoperiodic sensitivity genes in spring bread wheat varieties (Triticum aestivum L.) of various origin[J].Agricultural Science and Practice, 2021, 8(1):3−13. Balashova I , Fait V .Allele frequencies of Ppd-D1a, Ppd-B1a, and Ppd-B1c of photoperiodic sensitivity genes in spring bread wheat varieties (Triticum aestivum L.) of various origin[J].Agricultural Science and Practice, 2021, 8(1):3−13. [22] Singh S , Singh A , Jain N ,et al.Molecular Characterization of Vernalization and Photoperiod Genes in Wheat Varieties from Different Agro-climatic Zones of India[J].Cereal Research Communications, 2013, 41(3):376−387. [23] Li W L , Nelson J C , Chu C Y ,et al.Chromosomal locations and genetic relationships of tiller and spike characters in wheat[J].Euphytica, 2002, 125(3):357−366. [24] Goins G D, Yorio N C, Sanwo M M, et al. Photomorphogenesis, photosynthesis, and seed yield of wheat plants grown under red light-emitting diodes (LEDs) with and without supplemental blue lighting [J]. Journal of Experimental Botany, 1997, 48(7): 1407−1413. https://doi.org/10.1093/jxb/48.7.1407 doi: 10.1093/jxb/48.7.1407 [25] Zheng Y J, Zhang Y T, Liu H C, et al. Supplemental blue light increases growth and quality of greenhouse pak choi depending on cultivar and supplemental light intensity [J]. Journal of Integrative Agriculture, 2018, 17(10): 2245−2256. https://doi.org/10.1016/S2095-3119(18)62064-7 doi: 10.1016/S2095-3119(18)62064-7 -

 点击查看大图
点击查看大图
计量
- 文章访问数: 702
- HTML全文浏览量: 155
- 被引次数: 0



 下载:
下载: