-
辣椒疫霉(Phytophthora capsici)是一种具有高度破坏力的卵菌病原物,能够侵染包括辣椒(Capsicum annuum L.)、黄瓜(Cucumis sativus L.)、西瓜(Citrullus lanatus Matsum.)、番茄(Solanum lycopersicum L.)、茄子(Solanum melongena L.)以及部分花卉和热带经济作物[1]。自1922年在美国新墨西哥州首次发现并报道辣椒疫霉以来,其分布范围持续扩大,现已在全球温带与热带地区均有报道[2]。辣椒疫霉具有多重致病特征,包括对多种寄主的侵染、在土壤中的长期存活的能力以及对常用化学药剂和寄主抗性的快速适应[3]。目前,田间针对防治辣椒疫霉菌的常用方法主要是使用甲霜灵等杀菌剂,并结合轮作、水分管理(如排水或灌溉管理)等措施,减少游动孢子在田间的传播机会,降低病害暴发风险。然而,随着化学药剂的频繁使用,辣椒疫霉菌与其他卵菌已对某些单一作用位点的药剂产生显著的抗药性,导致防治效果下降[4- 5]。此外,出于农药残留和生态影响等方面的考量,合成农药使用面临更为严格的限制。因此寻找并研发新型生物农药变得迫在眉睫。
新绿原酸(Neochlorogenic acid)、绿原酸(Chlorogenic acid)、隐绿原酸(Cryptochlorogenic acid)是由咖啡酸(Caffeic acid)与奎宁酸(Quinic acid)通过酯键形成的酚酸类化合物[6]。由于酯化位点不同,绿原酸、新绿原酸、隐绿原酸在熔点、极性和抗氧化活性等理化性质上存在显著差异,这三种化合物广泛存在于多种植物中,如咖啡豆、果实和部分药用植物中。研究表明果实中新绿原酸和绿原酸含量的动态变化与果实成熟过程中病害抗性变化有关[7]。绿原酸类化合物(Chlorogenic acids)具有广谱生物活性,可通过破坏病原体细胞膜、诱导细胞裂解来抑制多种植物病原真菌的生长[8],为绿原酸类化合物作为天然防控剂的开发应用提供了科学依据。此外,有研究发现高含量的新绿原酸能有效抑制真菌黑色素合成[9- 10]、降低病原菌活性[11],这表明新绿原酸可能在防控某些真菌性病害中发挥关键作用。上述研究主要聚焦于真菌病原体,而在卵菌防控方面,已有报道指出植物根系分泌的酚酸类物质能够抑制孢子囊的生长及游动孢子的萌发和运动[12]。虽然已有研究表明绿原酸类物质对真菌具有抑制作用,但针对新绿原酸对卵菌的系统研究仍显不足。因此,为明确新绿原酸等绿原酸异构体对辣椒疫霉菌的抑制活性及作用特点,本研究系统比较了绿原酸、新绿原酸与隐绿原酸对辣椒疫霉菌菌丝生长、无性繁殖、游动孢子行为及活体致病力的影响,并评估了三种绿原酸异构体在辣椒疫病防控中的应用潜力。
-
绿原酸(Chlorogenic acid)、新绿原酸(Neochlorogenic acid)和隐绿原酸(Cryptochlorogenic acid)购自成都普思生物科技股份有限公司。植物材料为辣椒(Capsicum annuum)品种“HUNCBO226”幼苗,选取6~8叶龄、长势一致且无病虫害的健康植株作为供试材料。病原菌材料为辣椒疫霉(Phytophthora capsici)野生型菌株LT1534,由本实验室保存并提供。
-
TA培养基(用于培养卵菌):用纱布过滤番茄汁至300 mL,加入3.5 g碳酸钙后加入去离子水至3 L,每100 mL加入1.5 g琼脂粉,高压蒸汽121℃,20 min灭菌。
-
购买纯度为98%的绿原酸、新绿原酸、隐绿原酸原药。称取适量绿原酸药品粉末,提前准备好灭菌的干净 50 mL 圆底试管。将称量纸上的药品尽数倒进试管中。在超净工作台中加入适量 DMSO,轻晃试管使药品充分溶解在 DMSO 中,配制成100 mmol·L−1母液。用锡纸将试管整体包裹起来(药品需避光保存)。将包好的装有药品溶液的试管放在 4℃冰箱保存。
-
辣椒疫霉野生型菌株 LT1534 在TA平板培养基上25℃黑暗培养,待菌落直径达 3~4 cm 取边缘活性菌块。将预先配制并高压灭菌的 TA 培养基加热融化,冷却至约50~55℃后按比例加入绿原酸工作液,混匀后倒入 90 mm 培养皿。每一浓度设置5个重复,并设置溶剂对照及空白对照。用打孔器取直径 5 mm 圆形菌饼接种于平板中心,石蜡膜封口,25℃黑暗培养 4 d后采用十字交叉法测定菌落直径,拍照记录。独立生物学重复3次。
表 1 生长实验中不同浓度处理组母液的加入量
Table 1. , The amount of mother liquor added to different concentration treatment groups in the growth experiment
绿原酸浓度/ μmol·L−1 每200 mL培养基加入母液量/ μL 30 60.0 50 100.0 100 200.0 150 300.0 200 400.0 250 500.0 300 600.0 -
将1.2中的LT1534在4 LS、27℃光照培养3 d。用无菌双蒸水轻轻冲洗孢子囊,收集成为2 mL悬浮液。取10 µL悬浮液置血球计数板,计算单位体积孢子囊数量。每处理5次技术重复,生物学重复3次。
-
取新鲜生长4 d的LT1534菌落,27℃、4LS光照培养 2 d 的富集孢子囊。用2 mL不同浓度绿原酸溶液轻洗使孢子囊入悬浮液;后将悬浮液调至在(10×物镜)视野平均约20个孢子囊,轻轻混匀。将湿盒内喷雾保湿。将疏水性盖玻片3片为一组置于载玻片上,每片点加 40 µL 孢子囊悬浮液,设0、30、60 min三个时间梯度。湿盒密闭后置 4℃冰箱诱导释放。到时取出,立即在显微镜(20×物镜)下观察并拍照。每片随机取10个视野、每处理3个生物学重复,并统计释放率(%)。
-
取新鲜生长4 d的LT1534菌落,27℃、4 LS光照培养2 d的富集孢子囊,用4℃无菌水润洗,4℃处理20 min后置室温10 min诱导释放;用4℃无菌水轻洗收集游动孢子,经无纺擦镜纸一次性过滤去菌丝碎片,定容至2 mL。加入绿原酸母液配成目标浓度的游动悬浮液。按1.6的载玻片布置与时间点设置(0、30、60 min)。到时在20×物镜观察并拍照。每片随机5个视野。生物学重复 3 次。
-
选取长势健康、生理状态一致的辣椒叶片作为接种材料。按照既定梯度配制体积为5 mL 的一系列不同浓度的绿原酸、新绿原酸、隐绿原酸工作液。借助微型喷壶将处理液均匀喷布于靶标叶片的正反两面,随后静置 30~40 min,至叶表水分自然风干。同步制备辣椒疫霉游动孢子悬浮液,将接种体浓度校准至 1× 105~2 ×105个·mL−1。利用移液器在每片风干的叶面上定点接种20 μL病原菌悬浮液。接种完毕后,将叶片移入保湿盒中置于室温下孵育,每隔 6 h适度喷洒无菌水以维持高湿侵染微环境。前期进行24 h全暗黑处理,以促进病原菌侵染起始,其后转换为 12 h/12 h光暗交替的光周期继续培养。于接种后 72 h全面评估并测量叶片的发病面积及水渍状病斑的扩展程度,同时进行影像学记录。致病性评估实验需独立重复至少3次。
-
通过Excel对数据记录与处理,并使用GraphPad Prism 9软件进行单因素方差分析,通过Photoshop进行制图。
-
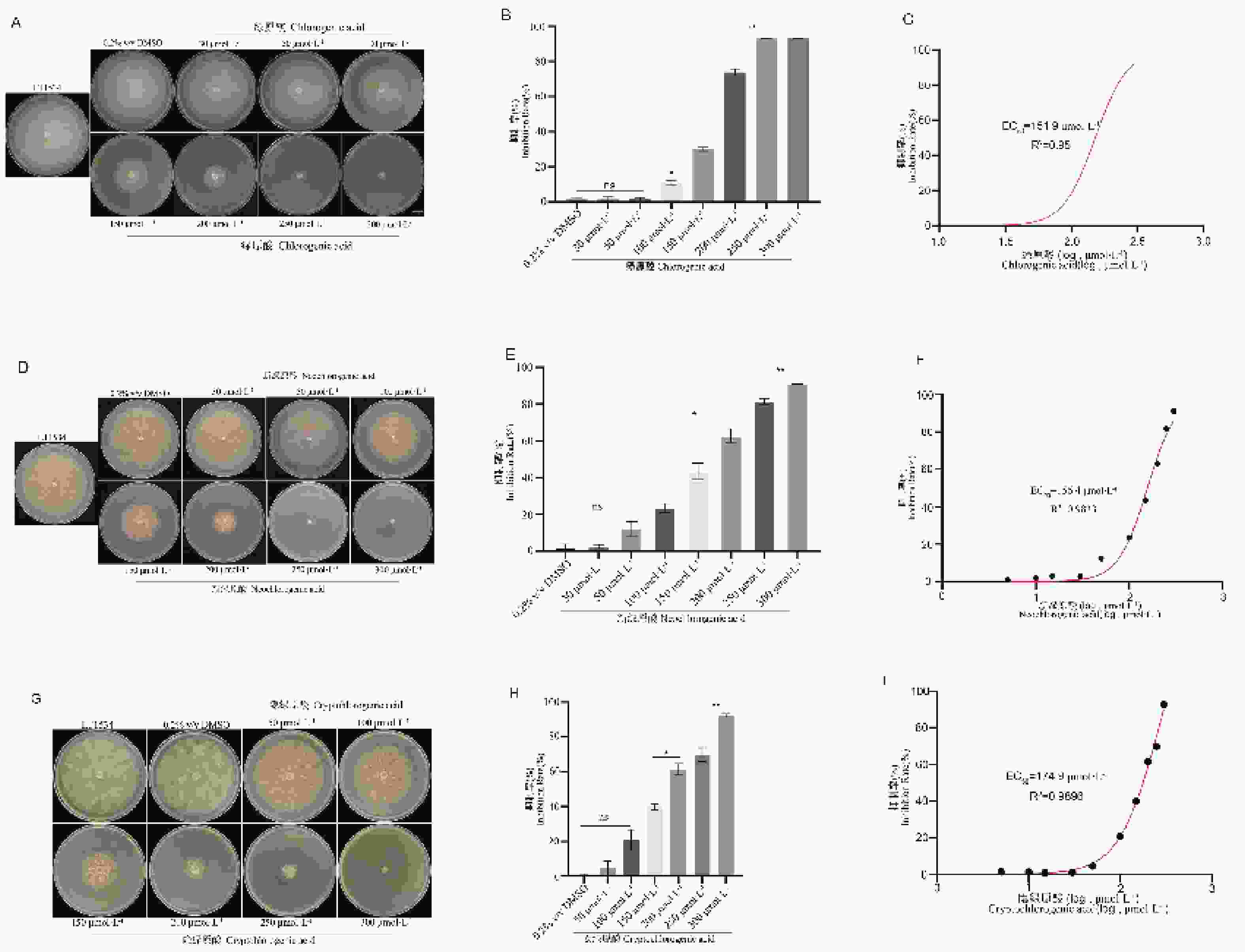
图1-A、D、G结果表明,绿原酸、新绿原酸、隐绿原酸这三种化合物均对辣椒疫霉菌丝生长具有明显的剂量依赖性抑制作用。与对照组相比,随着绿原酸、新绿原酸、隐绿原酸浓度的升高,菌落生长受到抑制,表型显示气生菌丝减少的趋势。与对照组相比,绿原酸在100 μmol·L−1时差异显著(*,P<0.05),在150~300 μmol·L−1时差异极显著(**,P<0.01)(图1-B);新绿原酸在100~200 μmol·L−1时差异显著(*,P<0.05),在250~300 μmol·L−1时差异极显著(**,P<0.01)(图1-E);隐绿原酸在150~200 μmol·L−1时差异显著(*,P<0.05),在250~300 μmol·L−1时差异极显著(**,P<0.01)(图1-H)。剂量—反应曲线拟合结果显示,得到绿原酸、新绿原酸、隐绿原酸对辣椒疫霉菌丝生长的有效中浓度(EC50)分别为151.9 μmol·L−1(R2=0.95)、156.4 μmol·L−1(R2=0.96)、174.9 μmol·L−1(R2=0.99)(图1-C、F、I),表明绿原酸与新绿原酸对辣椒疫霉菌丝生长的抑制活性显著优于隐绿原酸,三者均能有效干扰病原菌的营养生长阶段。
-
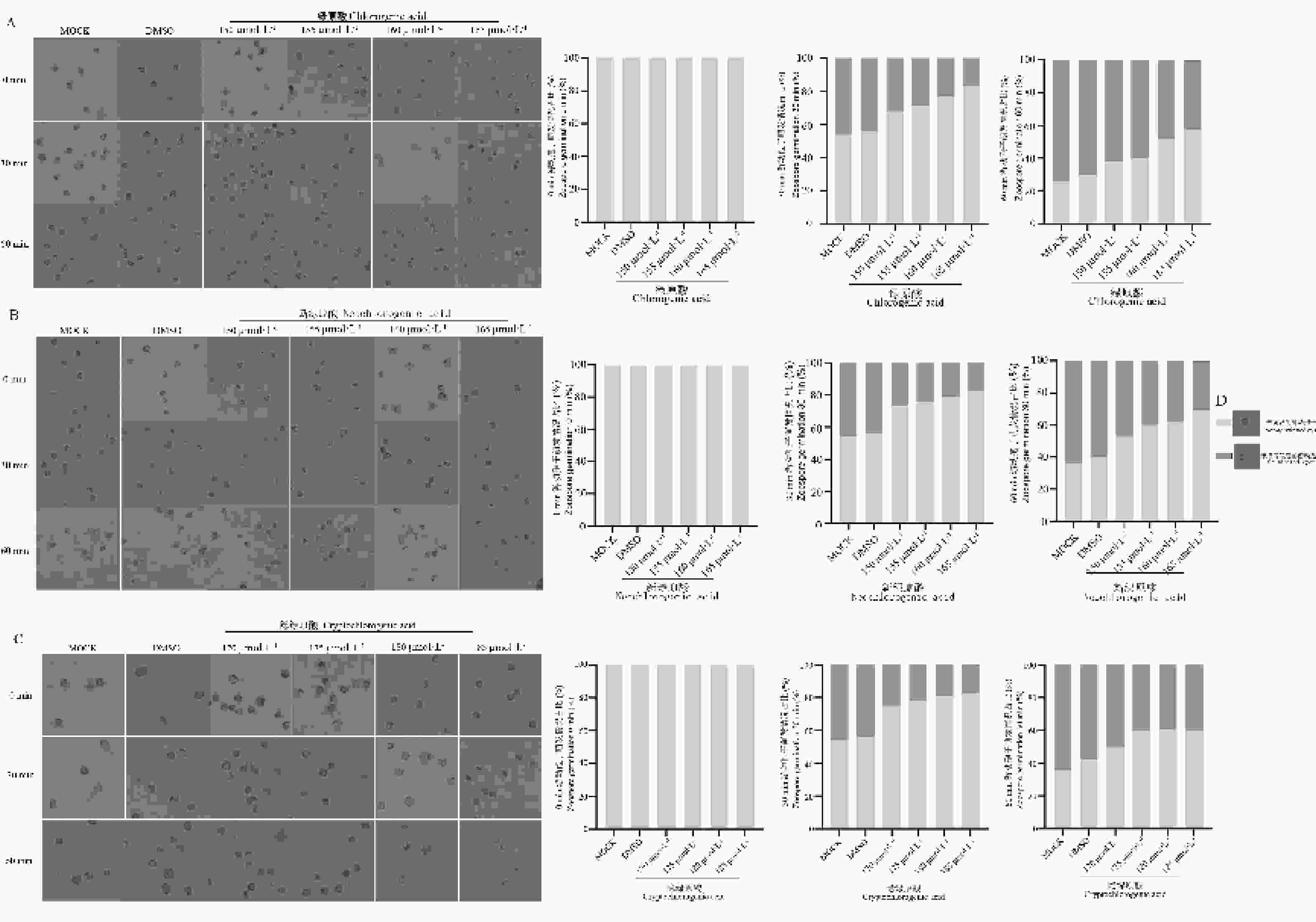
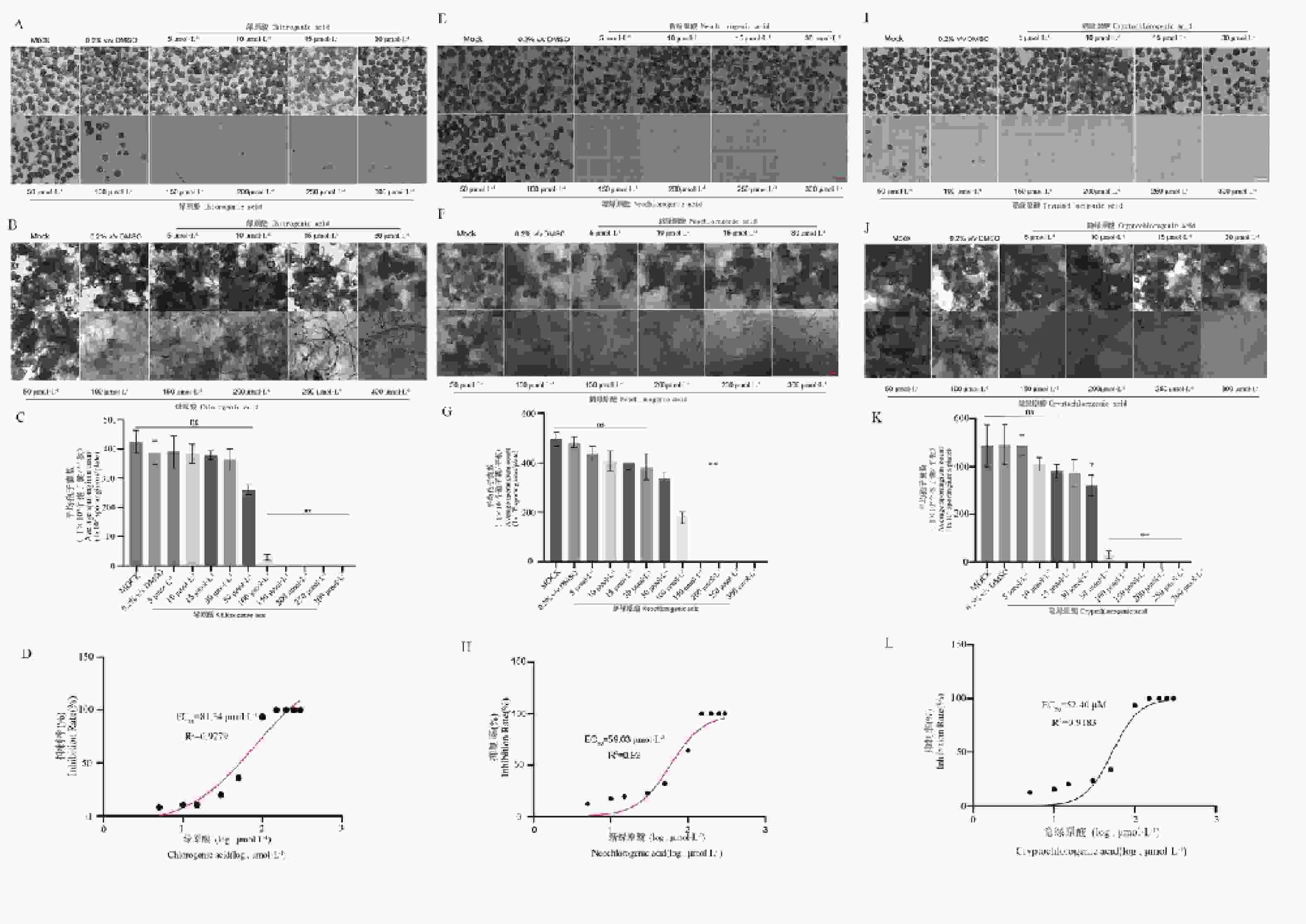
在辣椒疫霉的侵染循环过程中,孢子囊构成其无性繁殖与传播的核心单位。结果显示,三种化合物对辣椒疫霉孢子囊产生的抑制效果随浓度升高显著增强(图2)。与对照组相比,三种化合物均显著抑制了辣椒疫霉孢子囊的产生,且抑制效果随浓度增加而增强。体现出了明显的浓度依赖效应。其中,在50 μmol·L−1浓度下绿原酸、新绿原酸和隐绿原酸处理组孢子囊数量较对照分别减少 32.6%、30.1%、27.8%;150 μmol·L−1浓度下,三者均能完全抑制孢子囊产生(图2-A、B、C)。剂量—反应曲线显示,三者对孢子囊产生的 EC50值分别为 81.34 μmol·L−1(R2=0.92)、59.03 μmol·L−1(R2=0.92)、52.40 μmol·L−1(R2=0.91),表明绿原酸类化合物对辣椒疫霉无性繁殖阶段的抑制活性显著高于对菌丝生长的抑制活性(图2-D、E、F)。
-
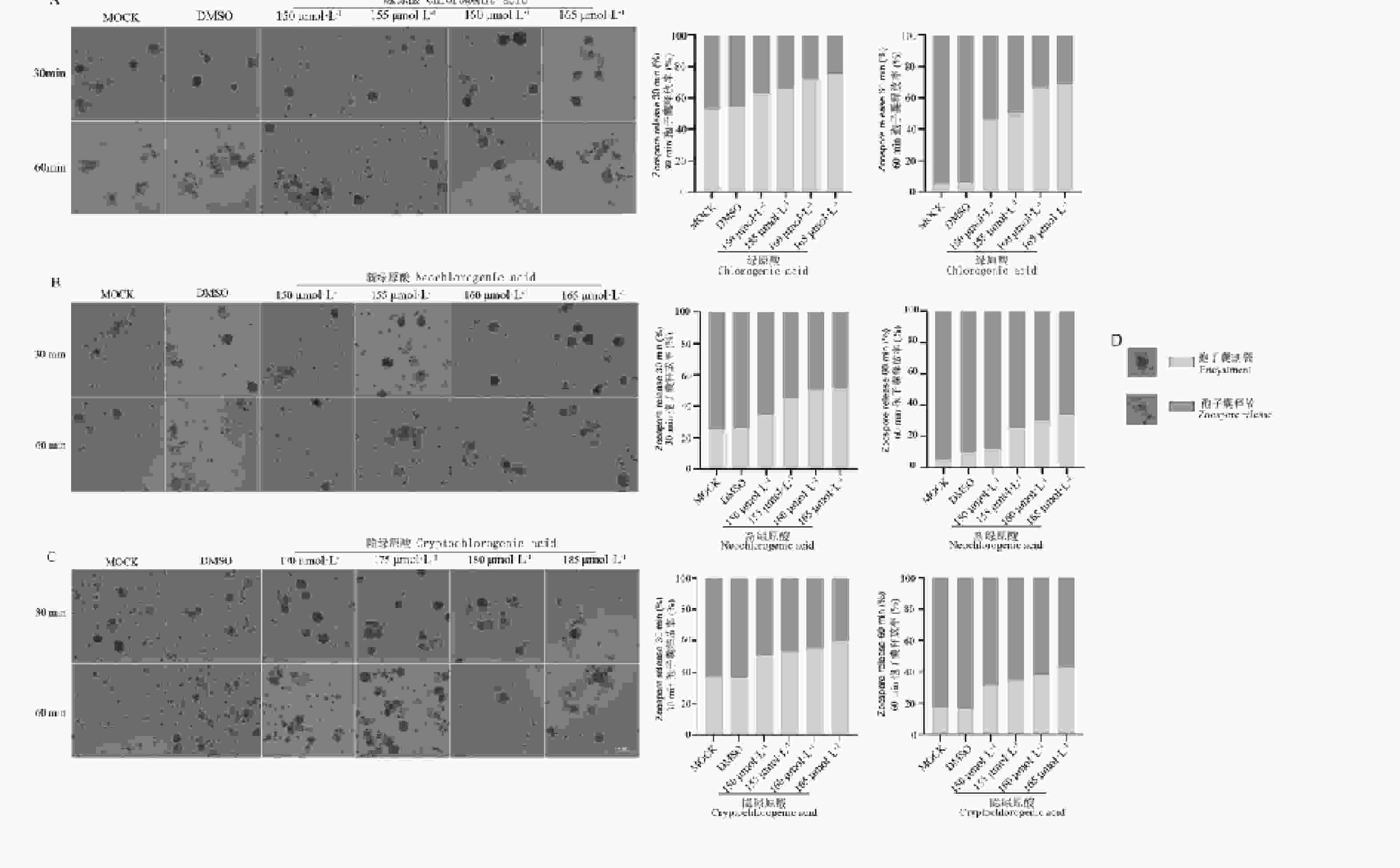
游动孢子的释放与萌发是辣椒疫霉侵染寄主的关键步骤。由图3可知,随着浓度的增加,三种化合物对辣椒疫霉的孢子囊游动孢子释放产生了不同程度的抑制效果,与对照组相比,绿原酸、新绿原酸和隐绿原酸处理在60 min时释放率下降约40%~60%。其中,绿原酸对辣椒疫霉的孢子囊游动孢子释放的抑制效果最佳。图4结果表明,三种化合物对辣椒疫霉的孢子囊释放的游动孢子萌发均产生了抑制效果,且新绿原酸的60 min的萌发数量相较于其他化合物,游动孢子的萌发数量均处于一个较低的水平。综合上述结果,绿原酸、新绿原酸和隐绿原酸对辣椒疫霉菌的孢子囊游动孢子释放与游动孢子萌发在整个观察时间内均表现出轻微的抑制作用。
-
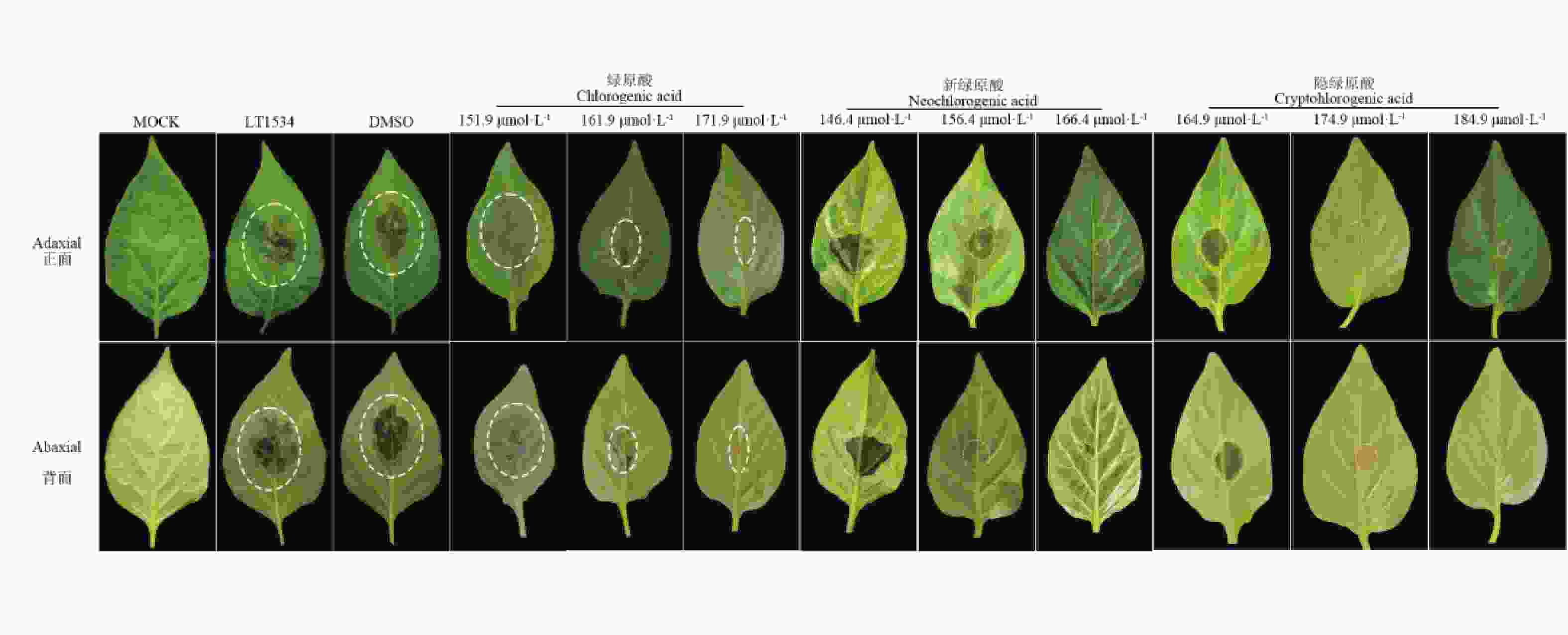
为了验证绿原酸类化合物的活体防护活性,对盆栽辣椒植株的叶片进行了接种辣椒疫霉菌悬浮液。在接种后72 h后,结果如图5,对照组叶片出现了典型的水渍状病斑,与此形成鲜明对比的是,喷施新绿原酸的叶片,病害症状显著减轻,且病斑直径随绿原酸类化合物浓度的升高而递减。其中,与对照组相比,经有效中浓度(EC50)的绿原酸类化合处理后,辣椒植株的发病情况明显下降。综上所述,绿原酸类化合物能够有效抑制辣椒疫霉菌在活体植株上的侵染过程,显著降低病害的严重程度。
-
辣椒疫霉可导致辣椒根腐病、茎基腐病、叶部和果实疫病,常引起地上部急性萎蔫,严重的可导致整株死亡[13-16]。该病原菌寄主广泛,可以侵染多种茄科和葫芦科作物[17]。已有研究表明,绿原酸、新绿原酸能够抑制或杀灭多种植物病原真菌,同时可以诱导活性氧积累及细胞凋亡[7, 18]。基于此,本研究评估了绿原酸、新绿原酸和隐绿原酸对辣椒疫霉的活性特征与生物学意义。
已有研究通过离体和活体抑菌实验探究了绿原酸对采后桃果实灰霉病的影响,结果表明,绿原酸能够抑制灰葡萄孢菌的菌落生长,且抑制作用随时间延长而减弱;此外,绿原酸还能有效抑制孢子萌发,诱导菌丝体变粗和缩短,并显著降低灰葡萄孢菌细胞活力[19]。本研究同样发现,绿原酸类化合物对辣椒疫霉具有的阶段特异性抑制作用,并证实绿原酸类化合物主要靶向病原菌营养生长与无性繁殖阶段,而对侵染关键的释孢与游动孢子萌发阶段影响较弱,这一特征与卵菌的生理代谢特性密切相关:辣椒疫霉菌丝生长与孢子囊形成过程中,细胞壁多糖(β-葡聚糖、纤维素)合成与细胞膜重塑活跃[20],而绿原酸类化合物可通过破坏细胞膜完整性、诱导活性氧积累干扰微生物代谢[21]。
已有研究表明绿原酸在多种不同的病原菌中能够引发细胞膜的异常形成与活性氧积累的应激反应[22]。胡居吾等[23]在研究三种叶绿原酸提取物的抑菌和抗氧化作用试验中发现,绿原酸提取物具有较强的抑菌活性和抗氧化作用,不同种类的抑菌能力具有一定的差异。本研究中,绿原酸与新绿原酸对菌丝生长的EC50显著低于隐绿原酸,推测可能与三者的分子结构差异有关,新绿原酸的酯键位置可能增强其与病原菌细胞膜的结合能力,从而提升抑制活性,这需要后续通过分子对接实验进一步验证。
已有研究表明,孜然酸、白芷毒素等化合物可影响辣椒疫霉的菌丝生长、孢子囊产生、游动孢子的释放以及萌发,然而各个阶段的EC50并不相同,呈现出显著的阈值差异与阶段选择性[24- 25]。相比之下,较高剂量的香茅醛能够同时影响菌丝形态、抑制游动孢子萌发并改变膜通透性[26],与本研究的不同阶段的特异性抑制形成鲜明对比。此外,三种化合物对孢子囊产生的抑制活性显著高于对菌丝生长的活性,表明 “抑制产孢” 可能是其防控辣椒疫病的核心机制,即减少田间孢子囊数量可直接降低病原菌传播风险,这对防控依赖孢子传播的卵菌病害具有重要实践意义。本研究还发现了绿原酸、新绿原酸和隐绿原酸在体外对多种植物病原真菌亦表现抑制活性,体现了其作为天然产物先导化合物用于防治辣椒疫病的潜在应用价值,为新型农药的开发提供了科学的依据,为辣椒疫病绿色防控提供了新选择。
Evaluation of the biological activity of chlorogenic acid isomers against Phytophthora capsici
-
摘要: 本研究系统评估了绿原酸(Chlorogenic acid)、新绿原酸(Neochlorogenic acid)与隐绿原酸(Cryptochlorogenic acid)对辣椒疫霉(Phytophthora capsici)的抑制活性与作用特性。通过体外实验测定三种化合物对辣椒疫霉(Phytophthora capsici)菌丝生长、孢子囊产生、孢子囊释孢及游动孢子萌发的影响;同时采用盆栽实验验证这三种化合物对辣椒疫霉活体致病力的抑制效果。结果表明,三种化合物均呈剂量依赖方式抑制辣椒疫霉菌丝生长,绿原酸与新绿原酸的有效中浓度(EC50)分别为 151.9、156.4 μmol·L-1 ,显著优于隐绿原酸(174.9 μmol·L-1 );三种化合物能够显著抑制孢子囊的产生,EC50介于 52.40 ~61.20 μmol·L-1 ,绿原酸、新绿原酸和隐绿原酸在150 μmol·L-1下均可完全抑制孢子囊产生;三种化合物对孢子囊释孢与游动孢子萌发仅表现轻度抑制。本研究揭示绿原酸类化合物对辣椒疫霉菌的作用具有明显的阶段特异性,主要靶向营养生长与产孢阶段,具备开发为天然源杀菌先导化合物的良好潜力,可为辣椒疫病及相关植物真菌病害的绿色防控提供了科学依据。Abstract: An attempt was made to systematically evaluate the inhibitory activities and action characteristics of chlorogenic acid, neochlorogenic acid, and cryptochlorogenic acid against Phytophthora capsici. In vitro assays were conducted to determine the effects of the three compounds on mycelial growth, sporangium production, zoospore release, and zoospore germination of P. capsici. Furthermore, pot experiments were employed to verify their inhibitory efficacy against the in vivo pathogenicity of P. capsici. The results demonstrated that all the three compounds inhibited mycelial growth in a dose-dependent manner. The half maximal effective concentrations (EC50) of chlorogenic acid and neochlorogenic acid were 151.9 μmol·L-1 and 156.4 μmol·L-1, respectively, which were significantly lower than that of cryptochlorogenic acid (174.9 μmol·L-1). The three compounds also significantly suppressed sporangium production, with EC50 values ranging from 52.4 μmol·L-1 to 61.2 μmol·L-1, and they completely inhibited sporangium formation at a concentration of 150 μmol·L-1. In contrast, the compounds exhibited only mild inhibition on zoospore release and zoospore germination. All these findings reveal that the action of chlorogenic acid compounds against P. capsici exhibits distinct stage-specificity, primarily targeting the vegetative growth and sporulation stages. These compounds demonstrate strong potential to be developed as natural fungicide lead compounds, providing a scientific basis for the eco-friendly control of pepper blight.
-
图 2 绿原酸、新绿原酸与隐绿原酸对辣椒疫霉菌(Phytophthora capsici)孢子囊产生的影响
注:图2(C、G、K):三种绿原酸类化合物对 P. capsici 孢子囊产生的影响。与对照组比较采用单因素方差分析(one-way ANOVA)并进行 Dunnett 多重比较校正。显著性标注:ns,P≥0.05; *P<0.05; **P<0.01。
Fig. 2 Dose-dependent inhibition by chlorogenic acid, neochlorogenic acid, and cryptochlorogenic acid of sporangium formation in Phytophthora capsici.
Note: Fig.2C, G, K: Effects of three chlorogenic acid–related compounds on sporangium production in P. capsici. Differences relative to the control were analyzed by using one-way ANOVA followed by Dunnett’s test for multiple comparisons. Significance is indicated as follows: ns: P≥0.05; *: P<0.05; **: P<0.01.
表 1 生长实验中不同浓度处理组母液的加入量
Table 1 , The amount of mother liquor added to different concentration treatment groups in the growth experiment
绿原酸浓度/ μmol·L−1 每200 mL培养基加入母液量/ μL 30 60.0 50 100.0 100 200.0 150 300.0 200 400.0 250 500.0 300 600.0 -
[1] Kamoun S, Furzer O, Jones J D G, et al. The Top 10 oomycete pathogens in molecular plant pathology [J]. Molecular Plant Pathology, 2015, 16(4): 413−434. https://doi.org/10.1111/mpp.12190 doi: 10.1111/mpp.12190 [2] Quesada-Ocampo L M, Parada-Rojas C H, Hansen Z, et al. Phytophthora capsici: recent progress on fundamental biology and disease management 100 years after its description [J]. Annual Review of Phytopathology, 2023, 61: 185−208. https://doi.org/10.1146/annurev-phyto-021622-103801 doi: 10.1146/annurev-phyto-021622-103801 [3] Yin Y N, Miao J Q, Shao W Y, et al. Fungicide resistance: progress in understanding mechanism, monitoring, and management [J]. Phytopathology® , 2023, 113(4): 707−718. https://doi.org/10.1094/PHYTO-10-22-0370-KD doi: 10.1094/PHYTO-10-22-0370-KD [4] Guo Y F, Krasnow C S, Hausbeck M K. Characterizing the dynamics of virulence and fungicide resistance of Phytophthora capsici in Michigan vegetable fields reveals loci associated with virulence [J]. Plant Disease, 2024, 108(2): 332−341. https://doi.org/10.1094/PDIS-03-23-0576-RE doi: 10.1094/PDIS-03-23-0576-RE [5] Siegenthaler T B, Hansen Z R. Sensitivity of Phytophthora capsici from Tennessee to mefenoxam, fluopicolide, oxathiapiprolin, dimethomorph, mandipropamid, and cyazofamid [J]. Plant Disease, 2021, 105(10): 3000−3007. https://doi.org/10.1094/PDIS-08-20-1805-RE doi: 10.1094/PDIS-08-20-1805-RE [6] Kremr D, Bajer T, Bajerová P, et al. Unremitting problems with chlorogenic acid nomenclature: a review [J]. Química Nova, 2016, 39(4): 530−533. https://doi.org/10.5935/0100-4042.20160063 doi: 10.5935/0100-4042.20160063 [7] Martínez G, Regente M, Jacobi S, et al. Chlorogenic acid is a fungicide active against phytopathogenic fungi [J]. Pesticide Biochemistry and Physiology, 2017, 140: 30−35. https://doi.org/10.1016/j.pestbp.2017.05.012 doi: 10.1016/j.pestbp.2017.05.012 [8] Lou Z X, Wang H X, Zhu S, et al. Antibacterial activity and mechanism of action of chlorogenic acid [J]. Journal of Food Science, 2011, 76(6): M398−M403. https://doi.org/10.1111/j.1750-3841.2011.02213.x doi: 10.1111/j.1750-3841.2011.02213.x [9] Lim W, Konings M, Parel F, et al. Inhibiting DHN- and DOPA-melanin biosynthesis pathway increased the therapeutic value of itraconazole in Madurella mycetomatis infected Galleria mellonella [J]. Medical Mycology, 2022, 60(2): myac003. https://doi.org/10.1093/mmy/myac003 doi: 10.1093/mmy/myac003 [10] Mustafa M H, Corre M N, Heurtevin L, et al. Stone fruit phenolic and triterpenoid compounds modulate gene expression of Monilinia spp. in culture media [J]. Fungal Biology, 2023, 127(7/8): 1085−1097. https://doi.org/10.1016/j.funbio.2023.06.004 doi: 10.1016/j.funbio.2023.06.004 [11] Shetty R, Fretté X, Jensen B, et al. Silicon-induced changes in antifungal phenolic acids, flavonoids, and key phenylpropanoid pathway genes during the interaction between miniature roses and the biotrophic pathogen Podosphaera pannosa [J]. Plant Physiology, 2011, 157(4): 2194−2205. https://doi.org/10.1104/pp.111.185215 doi: 10.1104/pp.111.185215 [12] Zhang H, Yang Y X, Mei X Y, et al. Phenolic acids released in maize rhizosphere during maize-soybean intercropping inhibit Phytophthora blight of soybean [J]. Frontiers in Plant Science, 2020, 11: 886. https://doi.org/10.3389/fpls.2020.00886 doi: 10.3389/fpls.2020.00886 [13] Foster J M, Hausbeck M K. Resistance of pepper to Phytophthora crown, root, and fruit rot is affected by isolate virulence [J]. Plant Disease, 2010, 94(1): 24−30. https://doi.org/10.1094/PDIS-94-1-0024 doi: 10.1094/PDIS-94-1-0024 [14] Mohammadbagheri L, Nasr-Esfahani M, Al-Sadi A M, et al. Screening for resistance and genetic population structure associated with Phytophthora capsici-pepper root and crown rot [J]. Physiological and Molecular Plant Pathology, 2022, 122: 101924. https://doi.org/10.1016/j.pmpp.2022.101924 doi: 10.1016/j.pmpp.2022.101924 [15] Naegele R P, Hausbeck M K. Evaluation of pepper fruit for resistance to Phytophthora capsici in a recombinant inbred line population, and the correlation with fruit shape [J]. Plant Disease, 2014, 98(7): 885−890. https://doi.org/10.1094/PDIS-03-13-0295-RE doi: 10.1094/PDIS-03-13-0295-RE [16] Qi Z Q, Li L N, Xu C F, et al. The sodium/calcium exchanger PcNCX1-mediated Ca2+ efflux is involved in cinnamaldehyde-induced cell-wall defects of Phytophthora capsici [J]. Agronomy, 2022, 12(8): 1763. https://doi.org/10.3390/agronomy12081763 doi: 10.3390/agronomy12081763 [17] Ji P S, Koné D, Yin J F, et al. Soil amendments with Brassica cover crops for management of Phytophthora blight on squash [J]. Pest Management Science, 2012, 68(4): 639−644. https://doi.org/10.1002/ps.2308 doi: 10.1002/ps.2308 [18] Lu H J, Tian Z M, Cui Y Y, et al. Chlorogenic acid: a comprehensive review of the dietary sources, processing effects, bioavailability, beneficial properties, mechanisms of action, and future directions [J]. Comprehensive Reviews in Food Science and Food Safety, 2020, 19(6): 3130−3158. https://doi.org/10.1111/1541-4337.12620 doi: 10.1111/1541-4337.12620 [19] 戴冰儿. 绿原酸对采后桃果实灰霉病的抑菌机制及其纳米体系的构建和应用[D]. 杭州: 浙江工商大学, 2024. doi: 10.27462/d.cnki.ghzhc.2024.001302 [20] Ah-Fong A M V, Kim K S, Judelson H S. RNA-seq of life stages of the oomycete Phytophthora infestans reveals dynamic changes in metabolic, signal transduction, and pathogenesis genes and a major role for calcium signaling in development [J]. BMC Genomics, 2017, 18(1): 198. https://doi.org/10.1186/s12864-017-3585-x doi: 10.1186/s12864-017-3585-x [21] Mélida H, Sandoval-Sierra J V, Diéguez-Uribeondo J, et al. Analyses of extracellular carbohydrates in oomycetes unveil the existence of three different cell wall types [J]. Eukaryotic Cell, 2013, 12(2): 194−203. https://doi.org/10.1128/EC.00288-12 doi: 10.1128/EC.00288-12 [22] Kang M J, Kim D K. Synergistic antimicrobial action of chlorogenic acid and ultraviolet-A (365 nm) irradiation; mechanisms and effects on DNA integrity [J]. Food Research International, 2024, 196: 115132. https://doi.org/10.1016/j.foodres.2024.115132 doi: 10.1016/j.foodres.2024.115132 [23] 胡居吾, 韩晓丹, 付建平, 等. 三种绿原酸提取物的抑菌和抗氧化效果比较[J]. 天然产物研究与开发, 2017, 29(11): 1928−1933. https://doi.org/10.16333/j.1001-6880.2017.11.019 doi: 10.16333/j.1001-6880.2017.11.019 [24] He L M, Wang M K, Wang H J, et al. iTRAQ proteomic analysis of the inhibitory effect of 1, 6-O, O-diacetylbritannilactone on the plant pathogenic oomycete Phytophthora capsici [J]. Pesticide Biochemistry and Physiology, 2022, 184: 105125. https://doi.org/10.1016/j.pestbp.2022.105125 doi: 10.1016/j.pestbp.2022.105125 [25] Wang Y, Sun Y, Zhang Y, et al. Antifungal activity and biochemical response of cuminic acid against Phytophthora capsici Leonian [J]. Molecules, 2016, 21(6): 756. https://doi.org/10.3390/molecules21060756 doi: 10.3390/molecules21060756 [26] Song W, Yin Z Y, Lu X Y, et al. Plant secondary metabolite citral interferes with Phytophthora capsici virulence by manipulating the expression of effector genes [J]. Molecular Plant Pathology, 2023, 24(8): 932−946. https://doi.org/10.1111/mpp.13340 doi: 10.1111/mpp.13340 -

 点击查看大图
点击查看大图
计量
- 文章访问数: 735
- HTML全文浏览量: 176
- 被引次数: 0



 下载:
下载: