-
蜜蜂是世界上最重要的传粉昆虫,在农业生产和全球生态系统中发挥着至关重要的作用。在中国,约80%的农作物依赖蜜蜂授粉,每年授粉产生的价值可达300亿元[1-2]。近年来,蜜蜂数量的减少对全球粮食生产构成了威胁[3]。据报道,农药的广泛使用,特别是新烟碱类杀虫剂是导致蜜蜂和野生蜂种群下降的主要原因之一[4-5]。众所周知,花粉和花蜜是蜜蜂的食物,采集蜂外出采集被污染的花粉和花蜜后将其运回蜂巢储存,从而造成了蜂蜜、花粉和蜂粮中农药残留的迁移和转化[6]。研究表明,失去蜂巢内的工蜂(主要为内勤蜂)比失去采集的工蜂对蜂群健康的影响更大[7-8]。摄入蜂粮和蜂蜜是蜂箱内勤蜂暴露农药残留的唯一途径,因此,评估蜂巢暴露越来越被推荐用于量化蜂箱内蜜蜂农药暴露的影响[9]。
拟除虫菊酯类、新烟碱类、有机磷类、双酰胺类等杀虫剂,以及三唑类、甲氧基丙烯酸酯类等杀菌剂在作物上广泛使用。据报道,密歇根蓝莓花期蜜蜂采集的花粉分析中发现,蜂群平均同时暴露于35种杀虫剂中[10]。此外,在蜂粮和蜂蜜中检测到农药残留现象国内外均有报道,如Giroud等[11]在蜂粮中检测到啶虫脒和噻虫啉质量比超过170 ng·g−1,高效氯氟氰菊酯的残留质量比为5.0 ng·g−1;Villalba[12]等在蜂粮中检测到毒死蜱质量比为3.63 ng·g−1;Tong[13]等在蜂粮样品中检测到31种农药残留,其中多菌灵质量比高达14 532.6 ng·g−1,联苯菊酯质量比达4 946.2 ng·g−1;Xiao[14]等通过连续 4 年监测采集的蜂粮和蜂蜜中农药残留分析,发现拟除虫菊酯类杀虫剂中位质量比为 134.3~279.0 µg·kg−1,联苯菊酯的检出率为19.7%。
亚致死剂量的农药残留不仅会影响蜜蜂的生长发育,也会影响蜜蜂的行为。研究表明,亚致死剂量的农药影响工蜂的运动、觅食、学习记忆能力及寿命,最终损害蜜蜂的授粉能力[15-18]。此外,蜜蜂同时接触多种农药会对蜜蜂的死亡率产生协同毒性增效效应[19-20]。
中华蜜蜂(Apis cerana cerana)是中国特有的本土蜂种,具备一系列适应中国气候和蜜源条件的生物学特性,在维持中国农业经济发展和生态平衡方面发挥着重要作用[21]。目前中华蜜蜂的分布区域和种群数量比上个世纪要少,其种群数量的减少很可能与蜜蜂对农药的慢性中毒有关。当前,中国蜂粮中检测到的农药残留主要包括多菌灵、氟氰胺菊酯、联苯菊酯、毒死蜱、高效氯氟氰菊酯、甲氰菊酯、氰戊菊酯、三唑酮、吡虫啉、溴氰菊酯、蝇毒磷、噻虫嗪、戊唑醇等[14]。针对不同蜂粮检测出药剂的种类和质量浓度的差异,本研究以联苯菊酯为主,配制一种或几种混合物,研究其对中华蜜蜂工蜂(内勤蜂)的嗅觉敏感性及学习能力的影响,以期为中国蜜蜂授粉产业的健康可持续发展提供理论依据。
-
供试昆虫:实验用蜜蜂采自中国热带农业科学院环境与植物研究所楼前空地饲养的健康中华蜜蜂蜂群。热科院内蜜源植物较多,平时很少喷洒农药。实验前,蜂群未作任何处理。
供试试剂(纯度如无特别说明,均为质量分数):97%联苯菊酯原药、97.05%毒死蜱原药、96%吡虫啉原药、97%戊唑醇原药均由海南博士威生物科技有限公司提供;98%多菌灵原药购自广东云星生物技术有限公司;98%壬醛购自Sigma-Alorich公司、99%正己醇购自上海麦克林生化科技股份有限公司;蔗糖购自广东遇果食品有限公司;食用盐购自海南莺歌海盐场有限公司。
实验器材:实验蜂盒(13 cm × 6 cm × 10 cm的长方体钢盒,正面为玻璃板,顶部设饲喂口,底部设通风口)、饲喂器(塑料小盖子,每个可装1~2 mL蔗糖溶液,敞口面以封口膜覆盖以防蔗糖溶液蒸发,膜上用针扎小孔方便蜜蜂取食)、TLE204E 电子天平(梅特勒-托利多仪器有限公司),BILON–XH–D 涡旋混匀器(上海比朗仪器制造有限公司),自制人工气候室(面积3.8 m2)、蜂王标记笔、塑料吸管等。
实验条件:温度(27±1)℃、相对湿度 50%~70%、黑暗条件。
-
准确称取适量的原药并溶解于丙酮,然后用50%蔗糖溶液将药剂稀释至所需质量浓度(蔗糖溶液中丙酮终质量分数不高于0.3%)。所配制的药剂为:1)联苯菊酯蔗糖溶液(B,质量浓度为
0.2324 mg·L−1);2)联苯菊酯 + 吡虫啉混合蔗糖溶液(BI,质量浓度为0.2324 mg·L−1) + 9.1×10−3 mg·L−1),预实验表明,吡虫啉蜂粮实际浓度处理中华蜜蜂工蜂的过程中,致使工蜂大量死亡,因此为保障工蜂处于亚健康状态不至于死亡以及后续实验的顺利进行,故将吡虫啉浓度降低至蜂粮测定浓度的一半);3)联苯菊酯 + 多菌灵混合蔗糖溶液(BC,质量浓度为0.2324 mg·L−1 +0.6671 mg·L−1);4)联苯菊酯 + 戊唑醇混合蔗糖溶液(BT,质量浓度为0.2324 mg·L−1 + 2.59×10−2 mg·L−1);5)联苯菊酯 + 吡虫啉 + 多菌灵混合蔗糖溶液(BIC,质量浓度为0.2324 mg·L−1 + 9.1×10−3 mg·L−1 +0.6671 mg·L−1);6)联苯菊酯 + 吡虫啉 + 多菌灵 + 戊唑醇混合蔗糖溶液(BICT,质量浓度为0.2324 mg·L−1 + 9.1×10−3 mg·L−1 +0.6671 mg·L−1 + 2.59×10−2 mg·L−1);7)联苯菊酯 + 吡虫啉 + 多菌灵 + 戊唑醇 + 毒死蜱混合蔗糖溶液(BICTCh,质量浓度为0.2324 mg·L−1 + 9.1×10−3 mg·L−1 +0.6671 mg·L−1 + 2.59×10−2 mg·L−1 + 8.18×10−2 mg·L−1)。药剂配置好后保存于4℃冰箱备用。 -
从健康的3箱蜂群内抽取封盖即将羽化的子脾拿回实验室,放置于光照培养箱内,待成虫羽化。每日固定时间从蜂脾中捕捉新羽化的1日龄工蜂,并用蜂王标记笔在其背板标记后放回原来的3个蜂箱(不同时间捕捉的1日龄工蜂用不同颜色标记),待8 d后回捕作为实验材料。将回捕的工蜂置于实验蜂盒中,每盒30头,每个处理组设置6个蜂盒,共设6个重复(即8个处理组,每组含6个蜂盒)。静待1 h后,从盒中挑出受伤和死亡的工蜂,留下健康工蜂,进行给药。将配置好的药剂溶液分别加入不同饲喂器,放入不同的实验蜂盒,并进行标记。对照组只饲喂50%蔗糖溶液。每24 h 更换一次新鲜药液,并将死亡工蜂挑出统计死亡虫数,持续10 d。给药结束后,将工蜂冷冻麻醉并称量体质量后,用于下面的实验。
-
根据El Hassani等[22]报道的方法,并做一定改进。采用喙伸反应(proboscis extension reflex,PER)测试工蜂对不同浓度蔗糖溶液的反应。实验按以下4步进行:1)用蒸馏水配制质量分数为0.1%、1.0%、3.0%、10.0%、30.0%和50.0%的蔗糖溶液;2)将工蜂冷冻麻醉后,用镊子将其放入直径0.5 cm的塑料吸管中,露出头部和前足,用昆虫针从侧面插入吸管,并从工蜂胸部和腹部的节结处穿过,卡住工蜂,然后将塑料吸管固定在泡沫板上,放置在人工气候室中,等待工蜂苏醒;3)将苏醒的工蜂移出人工气候室,选取正常、活泼的进行分组,并对工蜂进行2 h的饥饿处理;4)用玻璃棒蘸水后靠近工蜂触角,观察并记录工蜂伸喙情况。同样方法分别依次用玻璃棒从低浓度到高浓度蘸取少量蔗糖溶液刺激工蜂,每只工蜂每次测试间隔3 min,每次测试最多15 s,观察并记录工蜂的伸喙反应。每个浓度设置3组重复,每组重复20只工蜂。将其中能对50%蔗糖溶液产生反应的工蜂挑出进行后续实验。
-
参考Smith [23]等气味联想性学习过程,进行PER行为实验。将1.2.3中对50%蔗糖溶液触碰工蜂触角引发PER行为的工蜂作为实验对象。本实验采用两种具有刺激性气味的药品(壬醛和正己醇)作为条件刺激,气味通过使用移液枪呈现给工蜂触角。训练中,壬醛作为条件刺激,让工蜂在伸喙时得到50% 蔗糖溶液作为奖励;正己醇作为非条件刺激,工蜂伸喙时则会进行盐水惩罚。
训练开始前,先测试工蜂对两种气味的自发反应,要求实验使用的工蜂皆不会对两种气味有反应。在整个训练中,保证实验环境的通风,并在一组训练结束后进行通风,待气味完全散去再进行下一组训练。两组训练应交替进行,每组进行5次。训练中,首先将工蜂处于壬醛气味中,并在施加气味3 s后向工蜂提供少量50%蔗糖溶液5 s作为奖励(同时依旧施加气味),若工蜂在前3 s内伸喙,则表示工蜂将该气味与蔗糖溶液形成关联,记为“+”,反之则记为“-”,到此完成一组实验。接着待气味完全散去后,将工蜂置于正己醇气味中,并在施加气味3 s后向工蜂提供5 s盐水作为惩罚(同时依旧施加气味),且应注意盐水不应过多,否则可能会导致工蜂出现钠中毒,若工蜂在前3 s内伸喙,则记为“-”,反之记为“+”,到此完成该组实验。训练过程中,两组训练应交替进行,每组进行5次。
-
在给药过程中,每天记录处理组和对照组死蜂数,利用GraphPad Prism v8.0 软件 Survival 中的 Kaplan-Meier生存分析确定不同实验组药剂处理后工蜂的存活情况,绘制生存曲线;工蜂对不同浓度蔗糖溶液的反应以及工蜂学习能力的实验中,均统计喙伸反应率。喙伸反应率(%)= (发生喙伸反应的工蜂数 / 受试工蜂数)×100。给药结束后不同处理组工蜂的存活率、体重、喙伸反应率之间的显著性差异采用单因素方差分析(one way ANOVA,Tukey HSD,α=0.05)。
-
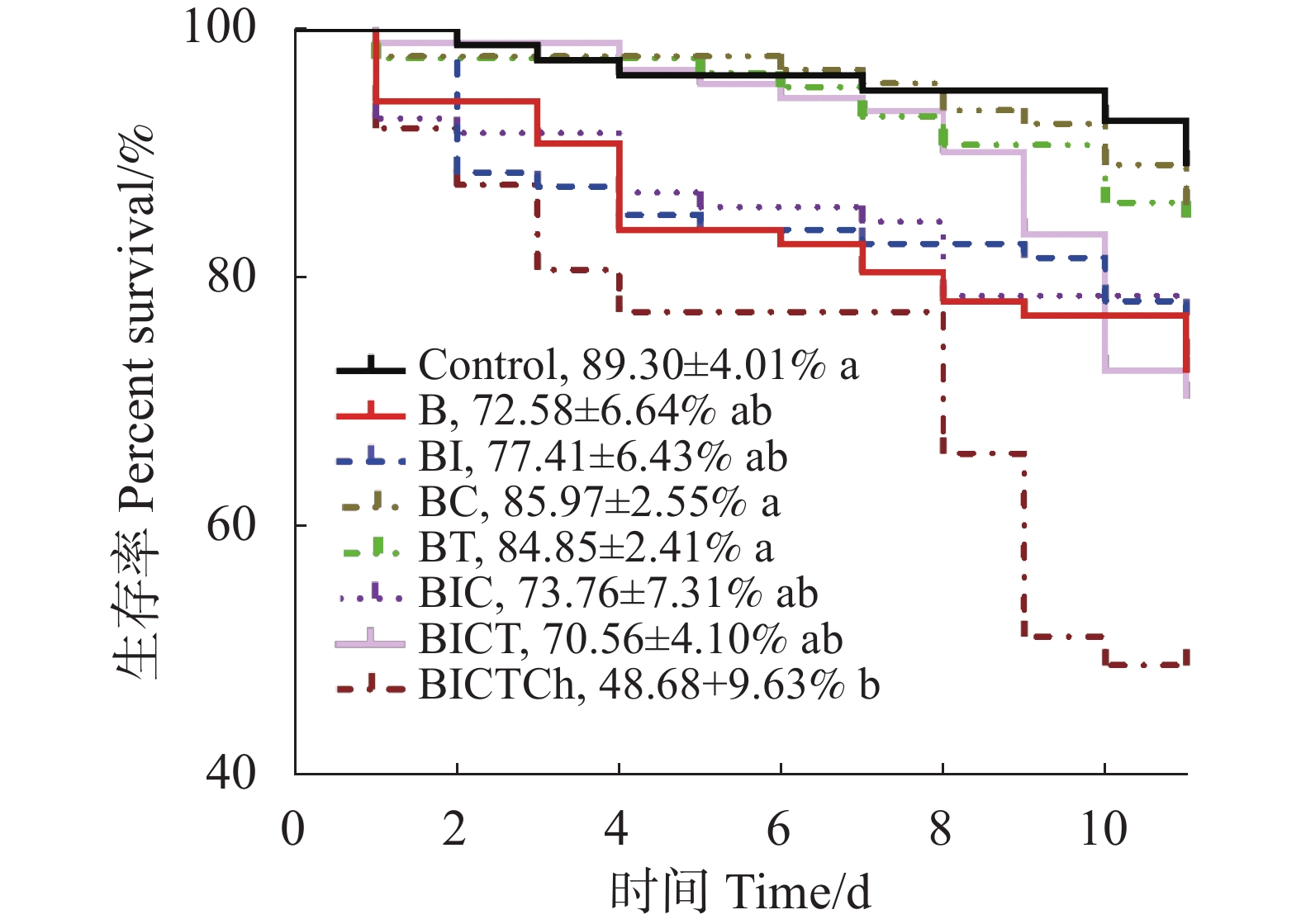
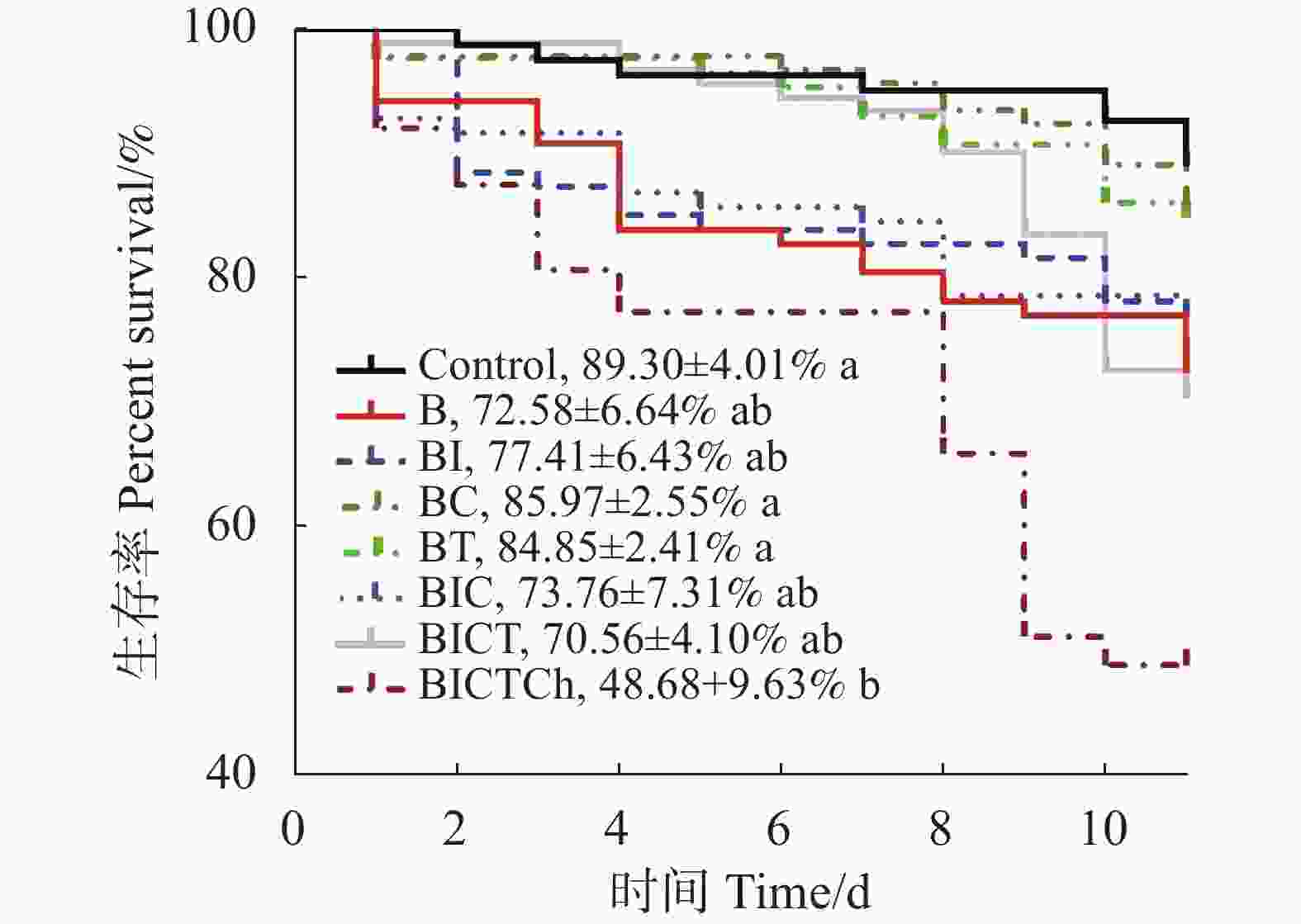
相同发育时间的中华蜜蜂工蜂经蜂粮中测定的联苯菊酯及其不同药剂残留量的混剂饲喂10 d,在第11 天对各处理组工蜂的生存情况进行了统计分析,并绘制了生存曲线图(图1)。如图1所示,药剂处理组的工蜂存活曲线与对照组相比有下降的趋势。对照组工蜂在第11 天平均存活率为(89.30±4.01)%,联苯菊酯 + 吡虫啉 + 多菌灵 + 戊唑醇 + 毒死蜱(BICTCh)处理组的工蜂存活率为(48.68±9.63)%,显著低于对照组(F7,16=4.722, P=0.005)。虽然联苯菊酯(B)、联苯菊酯 + 吡虫啉(BI)、联苯菊酯 + 吡虫啉 + 多菌灵(BIC)、联苯菊酯 + 吡虫啉 + 多菌灵 + 戊唑醇(BICT)处理组工蜂的存活率与对照相比都有所下降,但经统计分析,未达到统计学意义。从各处理组的存活曲线可以看出,工蜂暴露于联苯菊酯与多种农药的混剂并不一定比单独暴露于联苯菊酯死亡率更高。但混配不同作用机制的农药种类越多,对中华蜜蜂毒性机制越复杂,尤其是多种不同作用机制的农药,即使以残留剂量混用也会加大其死亡概率。
-
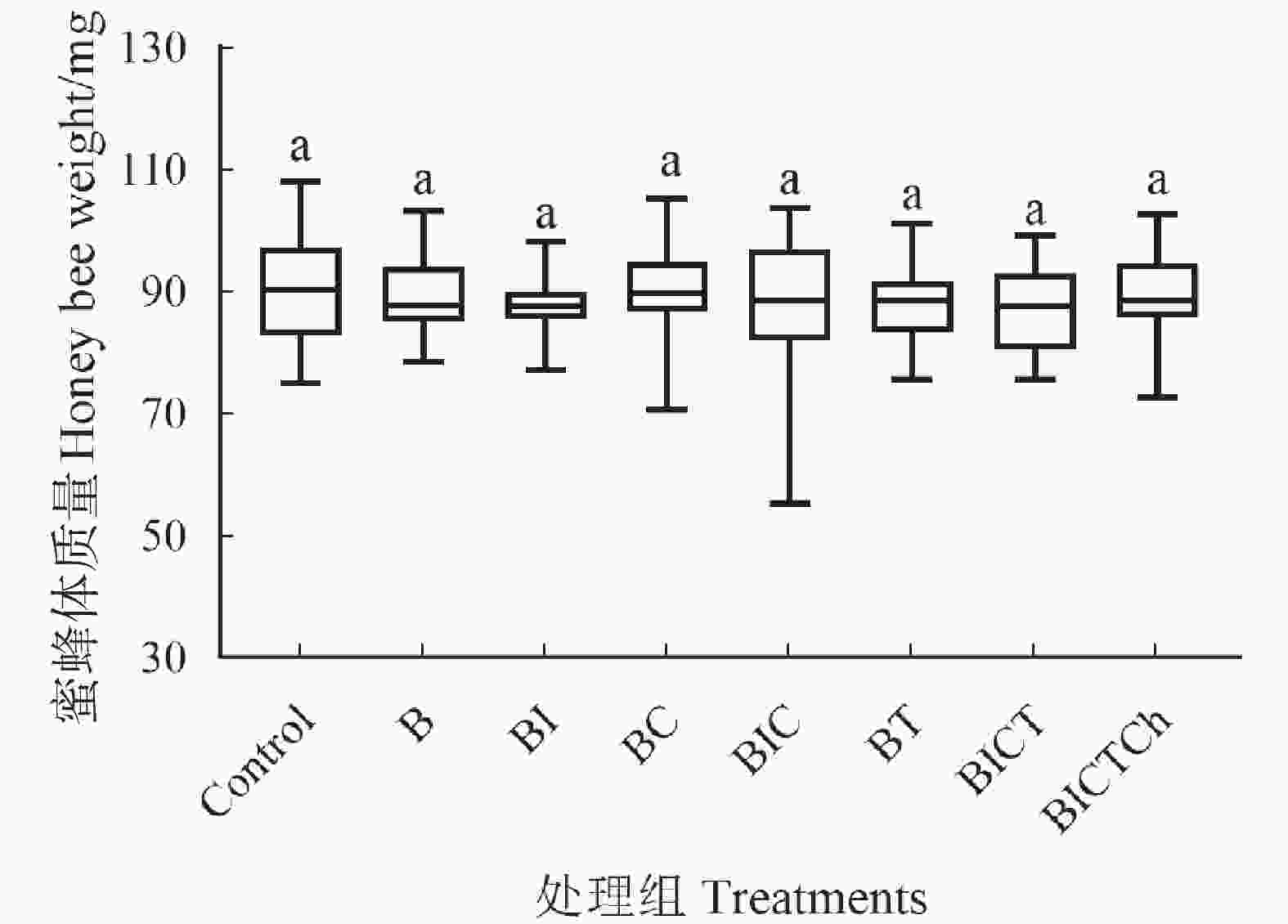
在给药实验结束后,将工蜂冷冻麻醉时测量其体质量,观察不同处理组工蜂之间的体质量差异。如图2所示,各处理组工蜂的平均体质量无显著性差异(F7, 215=0.994, P=0.442)。此结果表明联苯菊酯及其与不同药剂的混剂在蜂粮实际残留剂量下对工蜂体质量没有明显的影响。
-
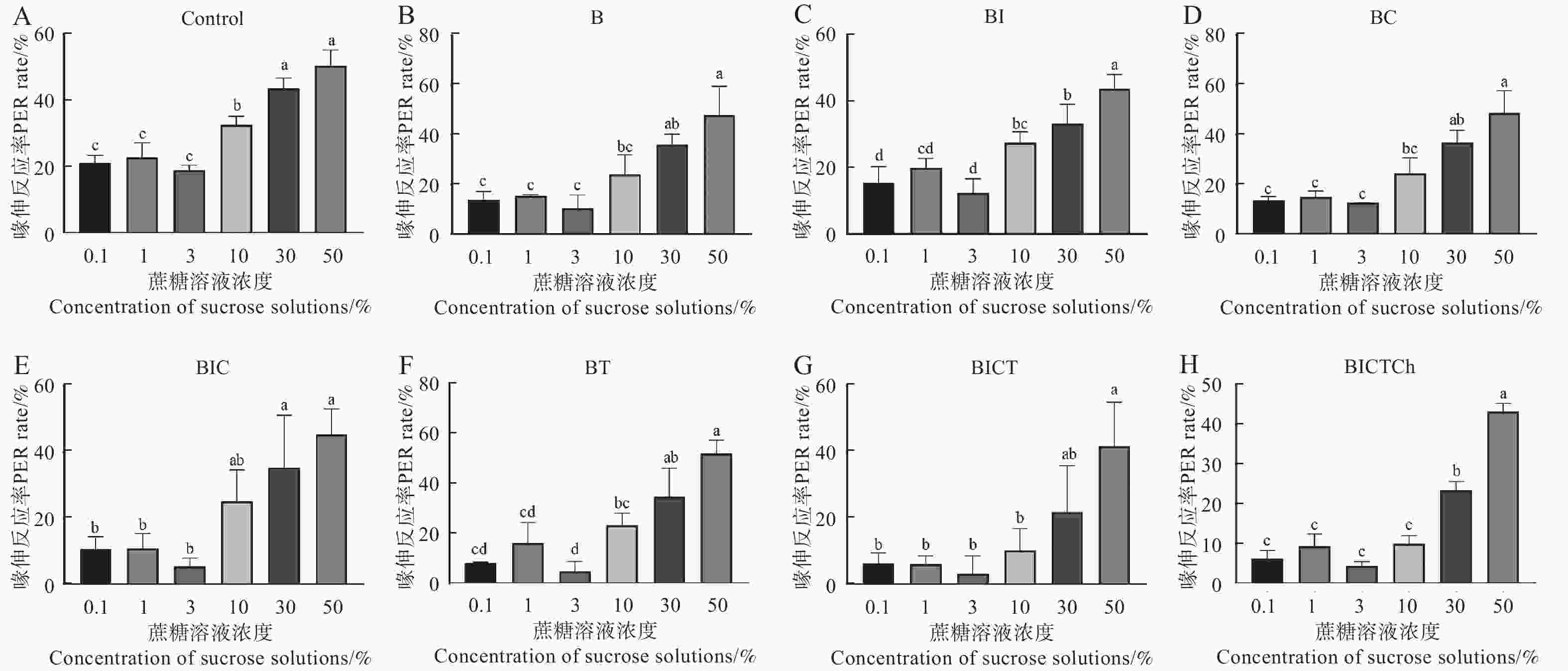
图3显示了不同处理组工蜂对相同浓度蔗糖溶液的敏感性。从图中可以看出,经口饲喂联苯菊酯及其不同药剂残留剂量10 d后,联苯菊酯 + 吡虫啉 + 多菌灵 + 戊唑醇 + 毒死蜱(BICTCh)处理组对0.1%、1%、3%、10%和30%的蔗糖溶液刺激的喙伸反应率显著下降(图3-A–E),仅对50%蔗糖溶液的刺激无明显变化;联苯菊酯 + 吡虫啉 + 多菌灵 + 戊唑醇(BICT)处理组对0.1%、1%、3%和10%的蔗糖溶液刺激的喙伸反应率显著下降(图3-A–D)。此外,联苯菊酯 + 吡虫啉 + 多菌灵(BIC)、联苯菊酯 + 戊唑醇(BT)处理组对0.1%和1%的蔗糖溶液刺激的喙伸反应率也显著下降(图3-A–B),而联苯聚酯(B)、联苯菊酯 + 吡虫啉(BI)、联苯菊酯 + 多菌灵(BC)处理组的喙伸反应率与对照相比无显著性差异(P>0.5)。
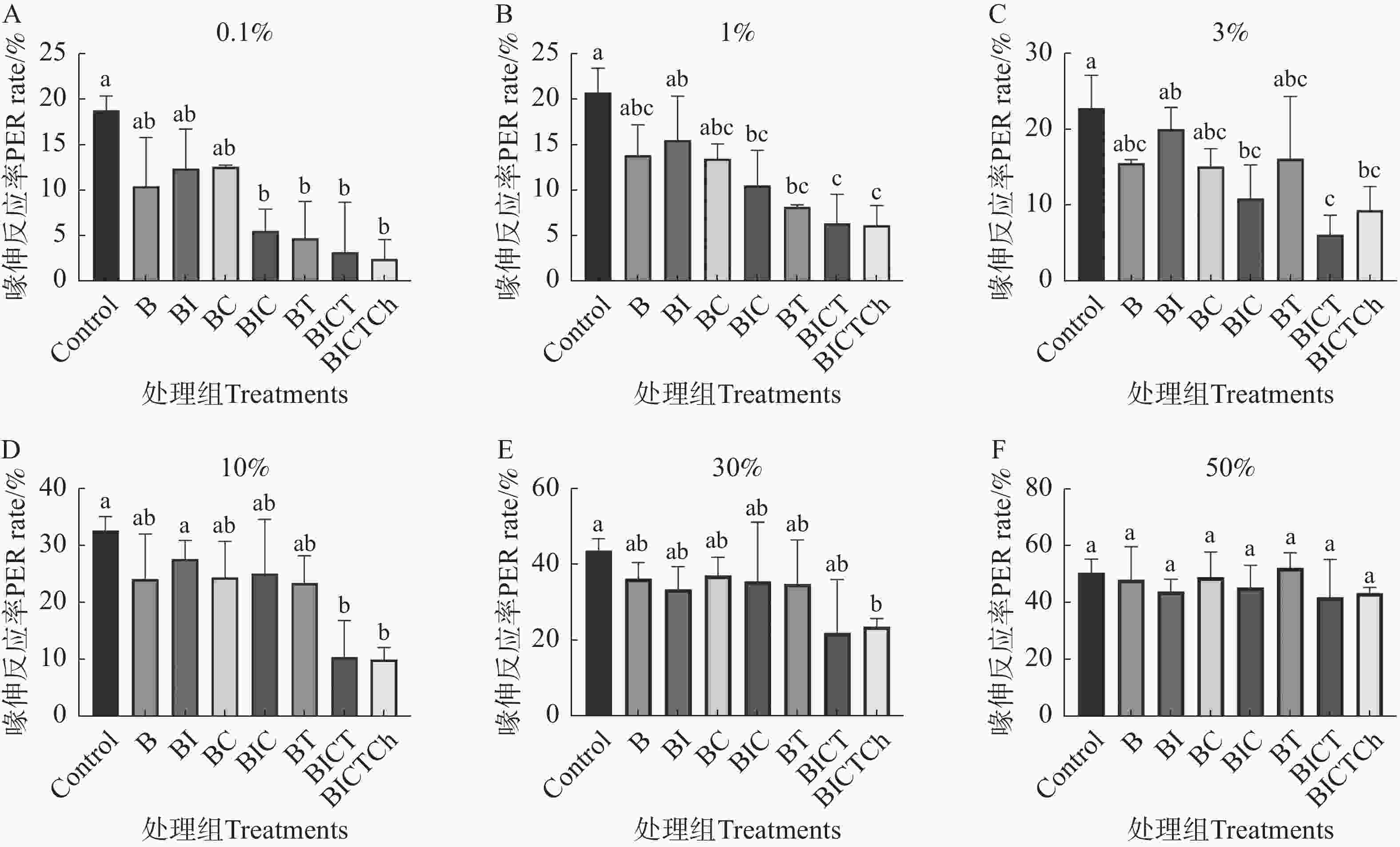
图 3 联苯菊酯及其混剂对中华蜜蜂工蜂蔗糖溶液敏感性的影响
Figure 3. Effects of bifenthrin and its mixtures on the sensitivity of sucrose solution of Apis cerana cerana workers
图4展示了不同处理组中华蜜蜂工蜂对不同蔗糖溶液浓度的敏感性。数据表明,同一处理组中,随着蔗糖溶液浓度的增加,工蜂对蔗糖溶液刺激的喙伸反应率也明显提高。
-
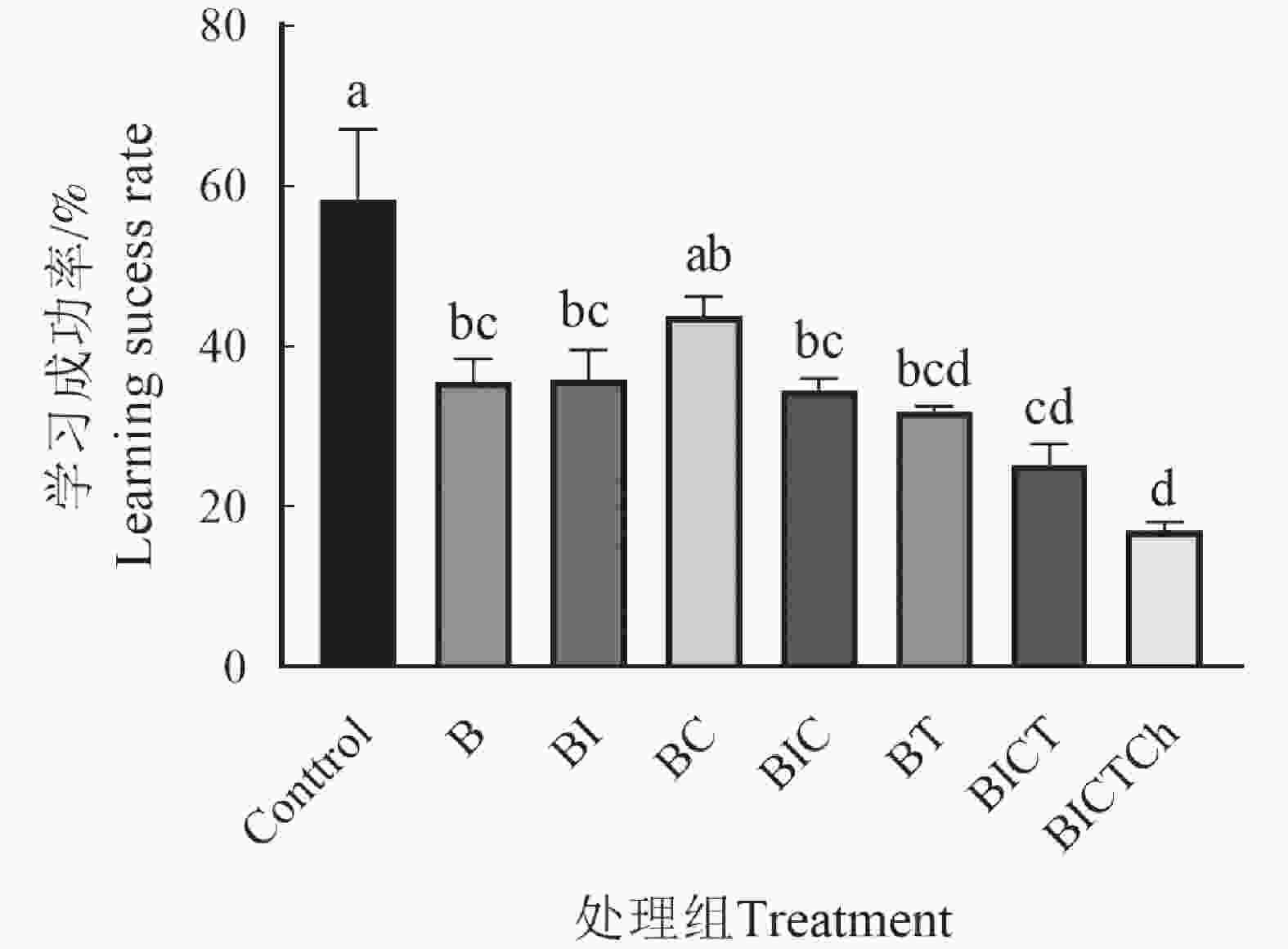
不同处理组的中华蜜蜂工蜂在训练过程中,对条件刺激的喙伸反应率反映了中华蜜蜂工蜂学习能力的高低[24]。对照组工蜂的学习成功率要明显高于农药影响下的工蜂,其中多种类农药混合处理组工蜂在训练中的表现情况最差。各处理组工蜂在学习训练中的成功率如图5所示,实验结果显示在多次训练中,对照组学习成功率呈上升趋势,说明该组工蜂的学习能力较强。相反,农药处理组的各组间差距明显,说明蜂粮中残留剂量的农药对中华蜜蜂工蜂的学习能力有影响,且随着农药混合种类的增加,对工蜂学习能力的影响也随之增大。
-
联苯菊酯是拟除虫菊酯类杀虫剂的典型代表,主要通过干扰电位依赖的Na+通道闸门开闭,延长受害昆虫神经Na+通道的开放时间,使其过度兴奋、惊厥,最后麻痹而死[25]。联苯菊酯在农作物上使用广泛,不仅在果蔬产品中经常检测到其残留[26],在蜂粮中也具有较高的残留量[13-14]。本研究根据Xiao等[14]报道的蜂粮内联苯菊酯及其多种药剂的残留量,测定了中华蜜蜂工蜂长期暴露于环境剂量的这些药剂,对其生存率和学习能力的影响。实验结果表明,联苯菊酯、吡虫啉、毒死蜱、多菌灵、戊唑醇同时存在蜂粮中时,对中华蜜蜂工蜂造成的死亡率显著高于对照。吡虫啉属于新烟碱类杀虫剂,通过作用于烟碱型乙酰胆碱受体,干扰昆虫的神经系统[27]。在蜂粮中,检测到吡虫啉的频次也是较高的。实验过程中,配置蜂粮内吡虫啉残留剂量浓度的蔗糖溶液,饲喂中华蜜蜂工蜂,未能饲养到第10天就全部死亡,说明残留剂量的吡虫啉对中华蜜蜂的生存具有重大威胁。为了进行中华蜜蜂工蜂学习能力的实验,把吡虫啉残留剂量的浓度缩小一半,才得以进行后续的实验。毒死蜱为有机磷类杀虫剂,是一种胆碱酯酶抑制剂[28]。多菌灵是一种广谱性杀菌剂,在中国蜂粮中的检出率为77.1% [29]。戊唑醇属于三唑类杀菌剂,前期研究表明,戊唑醇对新烟碱类杀虫剂有协同增效的作用[30]。农药的混合物普遍存在于开花作物及附近的野花上[31],采集蜂从不同作物采集回巢的花粉和花蜜存储于同一巢脾,更使蜂粮中的农药种类叠加。本实验结果表明,蜂粮中含农药种类越多,对蜜蜂的危害越大。
蜜蜂对蜜源丰富程度的判断主要取决于蜜蜂对不同浓度糖的敏感程度,因此蜜蜂嗅觉的敏感性对于蜜蜂来说十分重要[32]。蜜蜂长期暴露于多种农药下,势必对其嗅觉行为产生一定的影响。本研究通过喙伸反应,测定了不同农药处理组中华蜜蜂工蜂对不同蔗糖浓度的敏感性,结果表明残留剂量的联苯菊酯及其混合药剂导致中华蜜蜂工蜂对蔗糖的敏感性大大降低。在低浓度蔗糖溶液的刺激下,对照组中华蜜蜂工蜂的表现要远优于农药影响下的中华蜜蜂工蜂。随着农药种类的增加,中华蜜蜂工蜂对低浓度蔗糖溶液的敏感性变弱,对高浓度蔗糖溶液的感知有略微变化,但总体上与对照组的差距不再过于明显。本研究表明,蜂粮中农药残留种类越多,对工蜂的嗅觉神经损伤越大,可能降低其对低糖蜜源植物的采集效率。
近年来研究表明,农药影响蜜蜂的学习能力[33]。本研究结果也表明,联苯菊酯及其混剂处理组中华蜜蜂工蜂PER正确应答率显著低于对照,很难甚至无法将气味与食物之间建立起联系。相比之下,对照组中华蜜蜂工蜂在PER实验中表现为学习能力较强,能够快速应对相应的情景,且在多次重复中的喙伸反应率呈上升趋势,可以很快将不同气味与蔗糖溶液或盐水建立起联系。此外,多种农药混剂处理组,中华蜜蜂工蜂的学习能力最弱。究其原因可能为联苯菊酯、吡虫啉、毒死蜱均为神经毒剂,如毒死蜱的神经靶标乙酰胆碱是蜜蜂学习和记忆的主要神经递质[34],中华蜜蜂长期暴露这些杀虫剂,可持续中断神经元信息的传递,从而影响其学习行为。综上所述,蜂粮中存在多种农药,即使残留剂量也会对蜜蜂的健康产生重大威胁。因此,在生产实践中毒性较高的杀虫剂施用应远离蜜源植物和放蜂区,减少多种农药的混用,以降低蜂群长期暴露多种农药残留的风险,保障蜂群健康。
联苯菊酯及其混剂对中蜂工蜂嗅觉和学习能力的影响
DOI: 10.15886/j.cnki.rdswxb.20250081
 CSTR: 32425.14.j.cnki.rdswxb.20250081
CSTR: 32425.14.j.cnki.rdswxb.20250081
Effects of bifenthrin and its mixtures on the olfactory sensitivity and learning ability of Apis cerana cerana workers
-
摘要: 蜂产品中的农药残留对蜜蜂健康的危害日益受到关注。喙伸反应(proboscis extension reflex,PER)适用于评价农药对蜜蜂行为的影响。本研究旨在明确中华蜜蜂工蜂长期经口暴露于蜂粮中残留剂量的联苯菊酯及其混剂对其嗅觉和学习能力的影响。结果表明,经口饲喂含残留剂量联苯菊酯及其混剂(单独或混合)的蜂粮10 d后,多种药剂处理组显著降低工蜂的存活率,但对其体重无显著性影响。处理组工蜂对低浓度蔗糖溶液(质量分数分别为0.1%、1.0%、3.0%和10.0%)的敏感性显著降低,学习能力也显著降低。因此,蜜蜂长期同时暴露于多种不同作用机制的杀虫剂和杀菌剂残留,对其存活和学习能力产生显著负面影响,进而威胁到蜂群的健康发展。Abstract: The issue of pesticide residues in bee products and their impact on bee health is receiving increasing attention. Previous studies have shown that observations of the proboscis extension reflex (PER) are suitable for evaluating the behavioral effects of pesticides on honey bees. In this context an attempt was made to clarify the long-term effects of exposure to bifenthrin and its mixtures in beebread on the olfactory and learning ability of Apis cerana cerana worker. The results showed that after 10 days of oral administration of bifenthrin and its mixtures, either alone or in combination, the survival rate of worker honey bees was significantly reduced in the groups treated with various pesticide mixtures, but there was no significant effect on their body weight. Moreover, the olfactory sensitivity of honey bees in the treatment groups to 0.1%, 1%, 3% and 10% sucrose solutions was significantly reduced, and their learning ability was also significantly decreased. Therefore, long-term exposure of honey bees to multiple insecticides and fungicides with different mechanisms of action has a significant impact on their survival and learning abilities, which in turn threatens the healthy development of honey bee colonies.
-
Key words:
- Apis cerana cerana /
- bifenthrin /
- pesticide residue /
- proboscis extension reflex /
- learning ability
-
-
[1] Potts S G, Imperatriz-fonseca V, Ngo H T, et al. Safeguarding pollinators and their values to human well-being [J]. Nature, 2016, 540(7632): 220−229. https://doi.org/10.1038/nature20588 doi: 10.1038/nature20588 [2] 刘朋飞, 吴杰, 李海燕, 等. 中国农业蜜蜂授粉的经济价值评估[J]. 中国农业科学, 2011, 44(24): 5117−5123. https://doi.org/10.3864/j.issn.0578-1752.2011.24.018 doi: 10.3864/j.issn.0578-1752.2011.24.018 [3] Klein A M, Vaissière B E, Cane J H, et al. Importance of pollinators in changing landscapes for world crops [J]. Proceedings of the Royal Society B: Biological Sciences, 2007, 274(1608): 303−313. https://doi.org/10.1098/rspb.2006.3721 doi: 10.1098/rspb.2006.3721 [4] Rundlöf M, Andersson G K S, Bommarco R, et al. Seed coating with a neonicotinoid insecticide negatively affects wild bees [J]. Nature, 2015, 521(7550): 77−80. https://doi.org/10.1038/nature14420 doi: 10.1038/nature14420 [5] Janousek W M, Douglas M R, Cannings S, et al. Recent and future declines of a historically widespread pollinator linked to climate, land cover, and pesticides [J]. Proceedings of the National Academy of Sciences of the United States of America, 2023, 120(5): e2211223120. https://doi.org/10.1073/pnas.2211223120 doi: 10.1073/pnas.2211223120 [6] Bargańska Ż, Ślebioda M, Namieśnik J. Honey bees and their products: bioindicators of environmental contamination [J]. Critical Reviews in Environmental Science and Technology, 2016, 46(3): 235−248. https://doi.org/10.1080/10643389.2015.1078220 doi: 10.1080/10643389.2015.1078220 [7] Kadlikova K, Vaclavikova M, Halesova T, et al. The investigation of honey bee pesticide poisoning incidents in Czechia [J]. Chemosphere, 2021, 263: 128056. https://doi.org/10.1016/j.chemosphere.2020.128056 doi: 10.1016/j.chemosphere.2020.128056 [8] Vázquez D E, Latorre-estivalis J M, Ons S, et al. Chronic exposure to glyphosate induces transcriptional changes in honey bee larva: a toxicogenomic study [J]. Environmental Pollution, 2020, 261: 114148. https://doi.org/10.1016/j.envpol.2020.114148 doi: 10.1016/j.envpol.2020.114148 [9] Daniele G, Giroud B, Jabot C, et al. Exposure assessment of honeybees through study of hive matrices: analysis of selected pesticide residues in honeybees, beebread, and beeswax from French beehives by LC-MS/MS [J]. Environmental Science and Pollution Research, 2018, 25(7): 6145−6153. https://doi.org/10.1007/s11356-017-9227-7 doi: 10.1007/s11356-017-9227-7 [10] Graham K K, Milbrath M O, Zhang Y J, et al. Pesticide risk to managed bees during blueberry pollination is primarily driven by off-farm exposures [J]. Scientific Reports, 2022, 12(1): 7189. https://doi.org/10.1038/s41598-022-11156-1 doi: 10.1038/s41598-022-11156-1 [11] Giroud B, Vauchez A, Vulliet E, et al. Trace level determination of pyrethroid and neonicotinoid insecticides in beebread using acetonitrile-based extraction followed by analysis with ultra-high-performance liquid chromatography–tandem mass spectrometry [J]. Journal of Chromatography A, 2013, 1316: 53−61. https://doi.org/10.1016/j.chroma.2013.09.088 doi: 10.1016/j.chroma.2013.09.088 [12] Villalba A, Cecchetto F, Vazquez N D, et al. Contaminant dynamics in honey bees and hive products of apiaries from environmentally contrasting Argentinean regions [J]. Environmental Research, 2024, 249: 118306. https://doi.org/10.1016/j.envres.2024.118306 doi: 10.1016/j.envres.2024.118306 [13] Tong Z, Duan J S, Wu Y C, et al. A survey of multiple pesticide residues in pollen and beebread collected in China [J]. Science of the Total Environment, 2018, 640-641: 1578−1586. https://doi.org/10.1016/j.scitotenv.2018.04.424 doi: 10.1016/j.scitotenv.2018.04.424 [14] Xiao J J, He Q B, Liu Q Q, et al. Analysis of honey bee exposure to multiple pesticide residues in the hive environment [J]. Science of the Total Environment, 2022, 805: 150292. https://doi.org/10.1016/j.scitotenv.2021.150292 doi: 10.1016/j.scitotenv.2021.150292 [15] Brittain C, Potts S G. The potential impacts of insecticides on the life-history traits of bees and the consequences for pollination [J]. Basic and Applied Ecology, 2011, 12(4): 321−331. https://doi.org/10.1016/j.baae.2010.12.004 doi: 10.1016/j.baae.2010.12.004 [16] Ke L, Chen X S, Dai P L, et al. Chronic larval exposure to thiacloprid impairs honeybee antennal selectivity, learning and memory performances [J]. Frontiers in Physiology, 2023, 14: 1114488. https://doi.org/10.3389/fphys.2023.1114488 doi: 10.3389/fphys.2023.1114488 [17] Stanley D A, Garratt M P D, Wickens J B, et al. Neonicotinoid pesticide exposure impairs crop pollination services provided by bumblebees [J]. Nature, 2015, 528(7583): 548−550. https://doi.org/10.1038/nature16167 doi: 10.1038/nature16167 [18] Wu X B, Li Z, Yang H Y, et al. The adverse impact on lifespan, immunity, and forage behavior of worker bees (Apis mellifera Linnaeus 1758) after exposure to flumethrin [J]. Science of the Total Environment, 2023, 858(Pt 3): 160146. https://doi.org/10.1016/j.scitotenv.2022.160146 [19] Wang Y H, Zhu Y C, Li W H. Comparative examination on synergistic toxicities of chlorpyrifos, acephate, or tetraconazole mixed with pyrethroid insecticides to honey bees (Apis mellifera L.) [J]. Environmental Science and Pollution Research, 2020, 27(7): 6971−6980. https://doi.org/10.1007/s11356-019-07214-3 doi: 10.1007/s11356-019-07214-3 [20] Han W S, Yang Y M, Gao J L, et al. Chronic toxicity and biochemical response of Apis cerana cerana (Hymenoptera: Apidae) exposed to acetamiprid and propiconazole alone or combined [J]. Ecotoxicology, 2019, 28(4): 399−411. https://doi.org/10.1007/s10646-019-02030-4 doi: 10.1007/s10646-019-02030-4 [21] Zhang W X, Liu Z G, Zhu M, et al. Molecular cloning, expression and oxidative stress response of the vitellogenin Gene (AccVg) from Apis cerana cerana [J]. Apidologie, 2017, 48(5): 599−611. https://doi.org/10.1007/s13592-017-0503-9 doi: 10.1007/s13592-017-0503-9 [22] El Hassani A K, Dacher M, Gauthier M, et al. Effects of sublethal doses of fipronil on the behavior of the honeybee (Apis mellifera)[J]. Pharmacology Biochemistry and Behavior, 2005, 82(1): 30−39. https://doi.org/10.1016/j.pbb.2005.07.008 doi: 10.1016/j.pbb.2005.07.008 [23] Smith B H, Burden C M. A proboscis extension response protocol for investigating behavioral plasticity in insects: application to basic, biomedical, and agricultural research [J]. Journal of Visualized Experiments, 2014(91): e51057. https://doi.org/10.3791/51057 doi: 10.3791/51057 [24] Li A R, Yin L H, Ke L, et al. Thiacloprid impairs honeybee worker learning and memory with inducing neuronal apoptosis and downregulating memory-related genes [J]. Science of the Total Environment, 2023, 885: 163820. https://doi.org/10.1016/j.scitotenv.2023.163820 doi: 10.1016/j.scitotenv.2023.163820 [25] Gammon D W, Liu Z W, Chandrasekaran A, et al. Pyrethroid neurotoxicity studies with bifenthrin indicate a mixed Type Ⅰ/Ⅱ mode of action [J]. Pest Management Science, 2019, 75(4): 1190−1197. https://doi.org/10.1002/ps.5300 doi: 10.1002/ps.5300 [26] 曾静, 乔雄梧. 我国近年蔬菜水果中农药残留超标状况浅析[J]. 农药学学报, 2023, 25(6): 1206−1221. https://doi.org/10.16801/j.issn.1008-7303.2023.0091 doi: 10.16801/j.issn.1008-7303.2023.0091 [27] Elbert A, Haas M, Springer B, et al. Applied aspects of neonicotinoid uses in crop protection [J]. Pest Management Science, 2008, 64(11): 1099−1105. https://doi.org/10.1002/ps.1616 doi: 10.1002/ps.1616 [28] Yang Z M, Xiao T X, Lu K. Contribution of UDP-glycosyltransferases to chlorpyrifos resistance in Nilaparvata lugens [J]. Pesticide Biochemistry and Physiology, 2023, 190: 105321. https://doi.org/10.1016/j.pestbp.2022.105321 doi: 10.1016/j.pestbp.2022.105321 [29] Tong Z, Wu Y C, Liu Q Q, et al. Multi-residue analysis of pesticide residues in crude pollens by UPLC-MS/MS [J]. Molecules, 2016, 21(12): 1652. https://doi.org/10.3390/molecules21121652 doi: 10.3390/molecules21121652 [30] 韩文素, 任承才, 高景林, 等. 常用杀菌剂对啶虫脒中华蜜蜂毒性潜在增效作用研究[J]. 生态毒理学报, 2017, 12(6): 273−280. https://doi.org/10.7524/AJE.1673-5897.20170930001 doi: 10.7524/AJE.1673-5897.20170930001 [31] David A, Botías C, Abdul-Sada A, et al. Widespread contamination of wildflower and bee-collected pollen with complex mixtures of neonicotinoids and fungicides commonly applied to crops [J]. Environment International, 2016, 88: 169−178. https://doi.org/10.1016/j.envint.2015.12.011 doi: 10.1016/j.envint.2015.12.011 [32] 宋怀磊, 周婷, 王强, 等. 亚致死剂量杀虫剂对意蜂工蜂嗅觉敏感性的影响[J]. 应用昆虫学报, 2011, 48(3): 611−615. [33] Siviter H, Koricheva J, Brown M J F, et al. Quantifying the impact of pesticides on learning and memory in bees [J]. Journal of Applied Ecology, 2018, 55(6): 2812−2821. https://doi.org/10.1111/1365-2664.13193 doi: 10.1111/1365-2664.13193 [34] Lozano V C, Armengaud C, Gauthier M. Memory impairment induced by cholinergic antagonists injected into the mushroom bodies of the honeybee [J]. Journal of Comparative Physiology A, 2001, 187(4): 249−254. https://doi.org/10.1007/s003590100196 doi: 10.1007/s003590100196 -




 下载:
下载: