-
植物寄生线虫(plant parasitic nematodes,PPNs)每年造成全球农作物经济损失高达1 570亿美元,其中,根结线虫属(Meloidogyne spp.)严重威胁番茄等重要经济作物的安全种植。南方根结线虫(Meloidogyne incognita)作为番茄根结线虫病的主要病原,通过侵染根系导致植株生长受阻甚至死亡,每年造成番茄产量损失可达22%~30%[1 − 3]。目前,根结线虫的防治方法包括生物防治、农业防治、物理防治、开发抗性作物和化学防治等[4 − 8],其中以化学药剂通过拌土、灌根的施药方法为主。2020年,中国杀线剂农药登记48种,仅化学杀线剂就多达 31 种,占杀线剂种类的 64.58%;其中,除了阿维菌素、噻唑磷、氟吡菌酰胺等少数产品之外,存在可供选择杀线剂种类较少、施药方法单一等问题,且不合理用药导致的环境安全和线虫抗药性也面临巨大挑战[9–10]。已有研究表明,当植物受到外界因素干扰,会造成萜类、酚类、黄酮类、生物碱和木质素类等与植物抗病和抗逆相关的次级代谢物质发生变化[11]。植物的诱导抗性是指植物在诱导子(生物或非生物)的刺激或作用下激活自身防御机制,产生获得性免疫功能,以避免或减少病原物对植物的伤害[12 − 14]。Hoysted 等[15]研究发现,蚜虫胁迫通过调控马铃薯根系分泌物组分抑制马铃薯白线虫(Globodera pallida)发育,进而影响线虫卵的孵化。Udalova等[16]发现外源纳米硒通过参与植物根和叶中PR-6基因的表达和增加蛋白酶抑制剂的活性,诱导番茄对根结线虫的系统抗性,减少线虫侵害,抑制线虫发育。根系在植物生长过程中产生无机离子或小分子有机物,用于调节根际环境从而使植物更好生存,这部分物质统称为根系分泌物[17]。根结线虫可以通过化学感受器,以根系分泌物为信号来定位寄主[18]。特定的根代谢物可作为引诱剂和驱避剂来影响线虫的行为[19]。茄科植物中的水杨酸甲酯是根结线虫二龄幼虫的强引诱剂[20–21]。山柰酚、槲皮素和杨梅素等黄酮类化合物对南方根结线虫具有驱避作用[22–23]。
本研究改变常见杀线剂传统的灌根、拌土等施药方法,采用叶面喷雾法,探索其对番茄根结线虫病的防治效果,并初步探究杀线剂叶面喷施处理后番茄根系分泌物及代谢物对南方根结线虫的抑杀效果。本研究打破传统杀线剂的施药方式,为杀线剂叶面喷施防治根结线虫病提供理论支持,有助于探索杀线“老药新用”的新路径。
-
南方根结线虫由海南大学热带农林学院植物线虫实验室分离鉴定,并在番茄(Solanum lycopersicum)上于28 ℃温室中通过单卵块扩繁。
-
试验用番茄品种为感病品种 ‘改良摇钱228番茄’,广州亚蔬园艺种苗有限公司生产。
-
95%噻唑磷原药,北京翰隆达科技发展有限公司生产;98%氟吡菌酰胺原药,北京伊诺凯科技有限公司生产;97%阿维菌素原药,海南省宝信生物科技有限公司生产;94%甲维盐原药,海南海道森科技有限公司生产。
-
杀线剂系列浓度溶液配置:称取甲维盐、阿维菌素、氟吡菌酰胺、噻唑磷原药各10 mg,溶于1 mL 二甲基甲酰胺(N,N-dimethyl formamide,DMF),然后用0.1%(v/v,下同)Tween-80溶液将杀线剂依次稀释为:6.25、12.5、25、50、100 mg·L−1。
供试二龄幼虫:洗净番茄病根,挑取卵囊,置于便携式线虫孵化装置[24]、28 ℃孵育,逐日收集根结线虫二龄幼虫(J2s)备用。
毒力测定:在12孔细胞板中依次加入0.5 mL药液和0.5 mL根结线虫J2s悬液(200条·mL−1),药液终浓度分别为3.125、6.25、12.5、25、50 mg·L−1,同时以有机溶剂0.1%Tween-80溶液(含5.0 mL·L−1 DMF)作为对照(CK),共21个处理,每个处理设置3个重复。置于28 ℃恒温箱中孵育,24 h后镜检统计线虫死亡情况,用细钢针(或睫毛针)反复触碰J2判断其死活,线虫缓慢扭动为存活,僵直不动为死亡,记录死虫数、活虫数,计算死亡率(1)和校正死亡率(2)[25 − 26]。
$$ 死亡率=\dfrac{\mathrm{死}\mathrm{亡}\mathrm{线}\mathrm{虫}\mathrm{数}}{\mathrm{线}\mathrm{虫}\mathrm{总}\mathrm{数}}\times 100\text{%} \text{,} $$ (1) $$ 校正死亡率=\frac{\mathrm{处}\mathrm{理}\mathrm{死}\mathrm{亡}\mathrm{率}-\mathrm{对}\mathrm{照}\mathrm{死}\mathrm{亡}\mathrm{率}}{1 - \mathrm{对}\mathrm{照}\mathrm{死}\mathrm{亡}\mathrm{率}}\times 100\text{%} 。 $$ (2) -
试验设计:待番茄长至3~4片真叶时,移栽到装有V无菌土﹕V基质=3﹕1的塑料花盆中(每盆1株)。定植14 d后进行药剂处理(单位:株)。OS(CK):0.1%Tween-80(含6.0 mL·L−1 DMF,5 mL叶面喷施);J20:20 mg·L−1 甲维盐(5 mL叶面喷施);J40:40 mg·L−1 甲维盐(5 mL叶面喷施);F20:20 mg·L−1 氟吡菌酰胺(5 mL叶面喷施);F40:40 mg·L−1 氟吡菌酰胺(5 mL叶面喷施);A20:20 mg·L−1 阿维菌素(5 mL叶面喷施);A40:40 mg·L−1 阿维菌素(5 mL叶面喷施);S30:30 mg·L−1 噻唑磷(5 mL叶面喷施);S60:60 mg·L−1 噻唑磷(5 mL叶面喷施);S30*:30 mg·L−1 噻唑磷(30 mL灌根);J30*:20 mg·L−1 甲维盐(30 mL灌根)。共设11个处理,每个处理3株,设3次重复,随机区组排列。施药后第3天接种线虫,接种量为300头·株-1,接虫7 d后进行第2次施药(S30*和J30*除外)。
结果统计:接种线虫30 d后测量植株根系鲜质量[27]。统计每株根结数、卵块数并按以下分级标准和公式计算相对繁殖指数(3)、每克根根结数(4)、相对防效(5)和病情指数(6)[28− 29]。
分级标准:
0级,根部无根结;
1级,根部有根结 1 ~ 3个;
2级,根部有根结 4 ~ 10个;
3级,根部有根结 11~ 30个;
4级,根部有根结 31 ~ 80个,少数根结上有再次根结;
5级,根部有根结80个及以上,多数根结相互连结成根结团块。
$$ 相对繁殖指数=\frac{\mathrm{处}\mathrm{理}\mathrm{产}\mathrm{生}\mathrm{卵}\mathrm{块}\mathrm{数}}{\mathrm{C}\mathrm{K}\mathrm{产}\mathrm{生}\mathrm{卵}\mathrm{块}\mathrm{数}} \text{,} $$ (3) $$ 每克根根结数=\frac{\mathrm{单}\mathrm{株}\mathrm{根}\mathrm{结}\mathrm{数}}{\mathrm{单}\mathrm{株}\mathrm{根}\mathrm{鲜}\mathrm{质}\mathrm{量}} \text{,} $$ (4) $$ \begin{split} & 相对防效=\\&\frac{\mathrm{C}\mathrm{K}\mathrm{每}\mathrm{克}\mathrm{根}\mathrm{根}\mathrm{结}\mathrm{数} - \mathrm{处}\mathrm{理}\mathrm{每}\mathrm{克}\mathrm{根}\mathrm{根}\mathrm{结}\mathrm{数}}{\mathrm{C}\mathrm{K}\mathrm{每}\mathrm{克}\mathrm{根}\mathrm{根}\mathrm{结}\mathrm{数}}\times 100\text{%} \text{,} \end{split} $$ (5) $$ 病情指数=\frac{\displaystyle\sum (\mathrm{各}\mathrm{级}\mathrm{植}\mathrm{株}\mathrm{数}\times \mathrm{级}\mathrm{数})}{\mathrm{调}\mathrm{查}\mathrm{总}\mathrm{株}\mathrm{数}\times \mathrm{最}\mathrm{高}\mathrm{级}\mathrm{数}}\times 100 。 $$ (6) -
番茄根系分泌物及代谢物的获得:选用3~4叶期的番茄苗,小心取出整个根系洗净,再用无菌水清洗 2~3次。将番茄苗整个根系放入盛有10 mL无菌水的离心管中,用封口膜封闭管口。分别配置氟吡菌酰胺、阿维菌素、噻唑磷梯度药液:5、10、20、40 mg·L−1,以0.1%Tween-80(含4.0 mL·L−1 DMF)作为对照(OS)。各取5 mL药液均匀喷施在番茄苗叶面上,每处理10株。置于光照恒温培养箱(光﹕暗=16 h﹕8 h,28 ℃)中培养72 h,收集各处理番茄根系浸泡液、用滤纸过滤杂质后真空冷冻干燥适量浓缩,按每克根浸泡液定容至5 mL后,过0.22 μm滤膜获得根系分泌物(root exudates, RE)。各处理番茄根加入适量无菌水、用冷冻研磨仪充分研磨后,5 000 r·min−1 离心5 min收集上清液、真空冷冻干燥浓缩上清液,按每克根的上清液定容至5 mL后,过0.22 μm滤膜获得根系代谢物(root metabolites, RM)。根系分泌物和根系代谢物均置于−80 ℃保存备用[30]。
对J2s的毒杀作用:分别取各处理收集的番茄根系分泌物(RE)和代谢物(RM)各1.5 mL和0.5 mL J2s悬浮液(200条·mL−1)加入到 12 孔培养板孔中混匀,共设置 24个处理,并分别以0.1%Tween-80(含4.0 mL·L−1 DMF)喷施番茄获得的OS-RE和OS-RM为对照,各处理设3次重复。将12孔培养板置于28 ℃培养箱中孵育,于72 h统计线虫死亡情况,并参照1.2.1计算校正死亡率。
对卵孵化的抑制作用:挑取番茄病根上的根结线虫卵囊,将卵囊置于1.0%次氯酸钠溶液中振荡1 min后10 000 r·min−1 离心,弃上清留底液,用灭菌水清洗3次,加水振荡后收集上清液得到单卵悬浮液[31 − 32]。取1.5 mL各处理收集的番茄根系分泌物(RE)和0.5 mL卵悬浮液(200粒·mL−1)加到 12 孔培养板中混匀,共12个处理,并以0.1%Tween-80(含4.0 mL·L−1 DMF)获得的OS-RE为对照,各处理设3次重复。置于28 ℃的培养箱中孵化,每2 d 在体视显微镜(Leica体视显微镜SAPO)下观察孵化情况1次,避免污染,第12天统计每孔孵化幼虫数和未孵化卵数,计算孵化率(7)、孵化抑制率(8)[33 − 34]。
$$ 孵化率=\frac{\mathrm{孵}\mathrm{化}\mathrm{总}\mathrm{虫}\mathrm{数}}{\mathrm{孵}\mathrm{化}\mathrm{总}\mathrm{虫}\mathrm{数}+\mathrm{未}\mathrm{孵}\mathrm{化}\mathrm{单}\mathrm{卵}\mathrm{数}}\times100\text{%}\ , $$ (7) $$ 孵化抑制率 = \frac{\mathrm{C}\mathrm{K}\mathrm{孵}\mathrm{化}\mathrm{率} - \mathrm{处}\mathrm{理}\mathrm{孵}\mathrm{化}\mathrm{率}}{\mathrm{C}\mathrm{K}\mathrm{孵}\mathrm{化}\mathrm{率}}\times 100\text{%}。 $$ (8) -
番茄根系分泌物及代谢物的获得:参照1.2.3,分别将噻唑磷、氟吡菌酰胺、阿维菌素母液稀释为20、40 mg·L−1,以0.1%Tween-80(含4.0 mL·L−1 DMF)作为对照(OS),在叶面喷施处理后的6 d内逐日收集番茄根系分泌物与代谢物。
对J2s的致死作用:3种药剂处理6 d内逐日收集的番茄根系分泌物(RE)、代谢物(RM)各1.5 mL和0.5mL J2s悬浮液(200条·mL−1)加入到 12 孔培养板孔中混匀,共36×2个处理,并分别以0.1% Tween-80(4.0 mL·L−1DMF)获得的OS-RE和OS-RM为对照,每处理设3次重复。置于28 ℃培养箱中孵育,72 h后观察统计线虫死亡情况,并参照1.2.1计算校正死亡率。
-
使用SPSS 26.0统计分析软件用于单因素方差分析(ANOVA)、Duncan法进行多重比较和差异显著性检验,显著性水平设置P<0.05。通过概率回归模型进行毒力分析。利用graphpad8.3软件作图,图表中数据均为平均值±标准误。
-
处理24 h后,4种药剂对南方根结线虫J2s的生物活性均较高(表1)。氟吡菌酰胺杀线活性最好,其LC50、LC99值分别为1.003、19.121 mg·L−1,阿维菌素次之,分别为1.693、20.565 mg·L−1,甲维盐和噻唑磷稍差,但噻唑磷毒力方程的斜率最大,说明J2s对噻唑磷的质量浓度变化表现最敏感,噻唑磷在一定浓度变化区间即可快速提升J2s的致死率。
表 1 4种杀线剂对南方根结线虫J2s的毒力
Table 1. Toxicity of nematicides against the second-stage juveniles of Meloidogyne incognita
药剂
Nematicide斜率±标准误差
Slope±SELC50(95%CL)/
(mg·L−1)LC99(95%CL)/
(mg·L−1)自由度
dfP值
P value卡方值
Chi-square甲维盐(J)
Emamectin benzoate2.315±0.174 2.490
(2.092~2.859 )25.235
(20.413~33.347 )13 0.692 10.018 阿维菌素(A)
Abamectin2.145±0.198 1.693
(1.277~2.076 )20.565
(16.293~28.461 )13 0.503 12.299 氟吡菌酰胺(F)
Fluopyram1.817±0.166 1.003
(0.592~1.410)19.121
(14.543~29.008)13 0.295 15.199 噻唑磷(S)
Fosthiazate3.145±0.169 4.654
(4.112~5.186)25.557
(20.400~34.719)13 0.014 26.646 -
噻唑磷、氟吡菌酰胺、阿维菌素叶面喷施处理对番茄根结线虫有一定的盆栽防效(表2)。与对照相比,噻唑磷、氟吡菌酰胺、阿维菌素叶面喷施处理减少了番茄根结的形成,各处理每克根根结数均比CK少,其中F40、S60显著降低番茄的每克根根结数;同时,药剂处理增加番茄根系鲜质量。药剂叶面喷施处理或灌根处理后,线虫繁殖指数均小于1,说明施药处理均能降低线虫的繁殖量。各药剂叶面喷施处理的相对防效虽不及灌根处理效果明显,但F40和S60叶面喷施处理的相对防效仍分别高达43.98%和41.94%,显著高于其他低剂量叶面喷施处理。甲维盐叶面喷施处理无明显防治效果,因此在后续试验中未做测试。
表 2 杀线剂叶面喷施处理对番茄根结线虫的盆栽药效
Table 2. Control effect of foliar application of nematicides on Meloidogyne incognita in tomato in pots
处理
Treatment根系鲜质量增长率/%
Growth rate of
fresh root weight/%每克根结数/(个·g−1)
The number of root
knot per gram root/
(number·g−1)相对繁殖指数
Relative reproduction
index病情指数
Disease index相对防效/%
Control efficiency/%CK (10.66±4.53)abc — (86.11±6.73)ab — J20 (21.42±4.18)b (11.74±3.91)a (0.58±0.33)a (88.89±7.70)a (−10.15±36.73)e J40 (19.67±2.21)b (11.36±2.08)ab (0.53±0.33)ab (87.22±7.52)ab (−6.55±19.52)e F20 (12.45±4.32)b (8.31±3.46)cd (0.53±0.59)abcd (78.89±8.39)abcd (22.04±32.45)bcd F40 (−3.29±5.28)c (5.97±2.58)d (0.48±0.38)d (68.89±7.70)d (43.98±24.15)b A20 (5.25±4.90)bc (9.84±3.22)abc (0.56±0.29)abcd (79.44±5.89)abcd (7.66±30.24)de A40 (14.23±6.55)b (8.71±2.33)bcd (0.71±0.65)a (83.89±3.47)abc (18.32±21.82)cd S30 (−4.55±6.06)c (8.60±3.01)bcd (0.43±0.29)bcd (76.11±3.47)bcd (19.29±28.25)cd S60 (5.70±4.55)bc (6.19±2.74)d (0.71±0.65)cd (72.22±1.92)cd (41.94±25.69)bc J20* (50.69±5.38)a (1.60±1.10)e (0.15±0.25)bc (51.67±4.41)e (84.99±10.37)a S30* (17.77±5.87)b (0.23±0.21)e (0.43±0.35)c (16.67±8.82)f (97.88±1.94)a 注:CK.0.1%Tween-80(含6.0 mL·L−1 DMF,叶面喷施);J20.20 mg·L−1甲维盐(叶面喷施);J40.40 mg·L−1甲维盐(叶面喷施);F20.20 mg·L−1氟吡菌酰胺(叶面喷施);F40.40 mg·L−1氟吡菌酰胺(叶面喷施);A20.20 mg·L−1阿维菌素(叶面喷施);A40.40 mg·L−1阿维菌素(叶面喷施);S30.30 mg·L−1噻唑磷(叶面喷施);S60.60 mg·L−1噻唑磷(叶面喷施);J20*.20 mg·L−1甲维盐(灌根);S30*.30 mg·L−1噻唑磷(灌根)。每个数值代表平均值 ± 标准差(n = 10),列中的每个字母代表显著差异程度:P<0.05。
Note: CK.0.1%Tween-80(Containing 6.0 mg·L−1 DMF, foliar application); J20.20 mg·L−1 Emamectin benzoate(Foliar application); J40.40 mg·L−1 Emamectin benzoate(Foliar application); F20.20 mg·L−1 Flupyram(Foliar application); F40. 40 mg·L−1 Flupyram(Foliar application); A20.20 mg·L−1 Abamectin(Foliar application); A40.40 mg·L−1 Abamectin(Foliar application); S30.30 mg·L−1 Fosthiazate(Foliar application); S60.60 mg·L−1 Fosthiazate(Foliar application); J20*.20 mg·L−1 Emamectin benzoate(Root irrigation); S30*.30 mg·L−1 Fosthiazate(Root irrigation). Each value represents mean ± standard deviation(n = 10), and each letter in the column represents the degree of significant difference: P<0.05. -
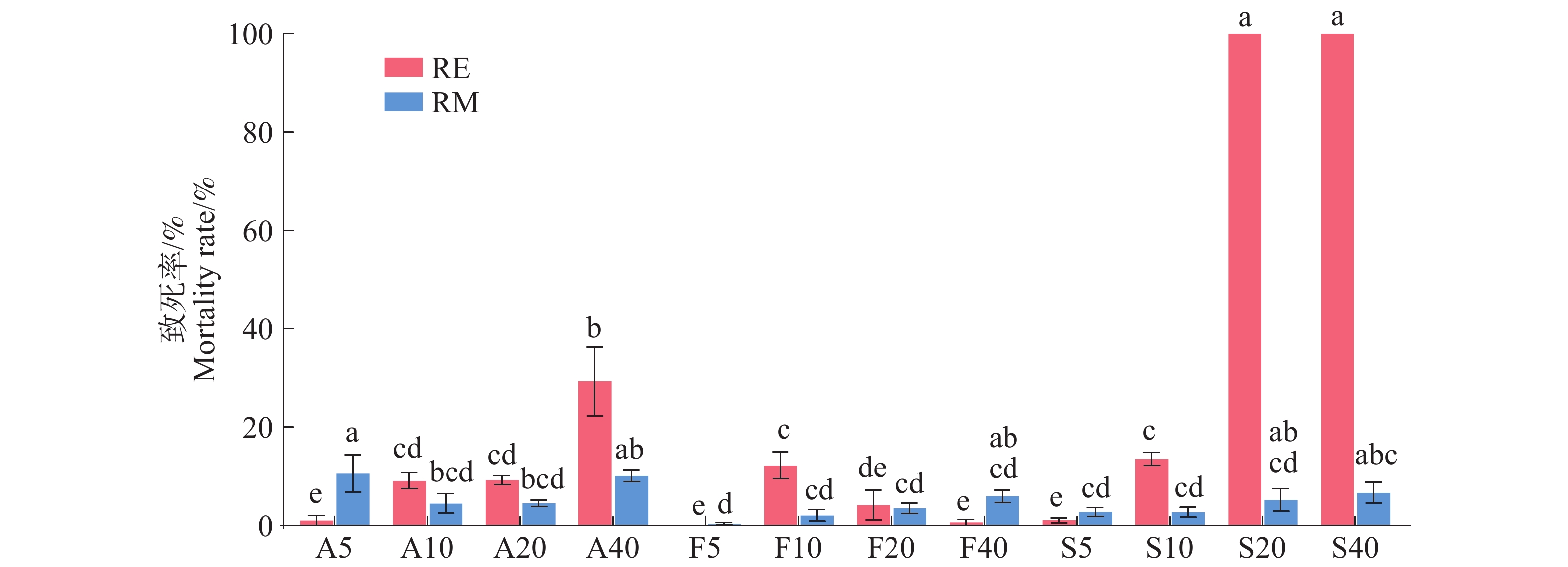
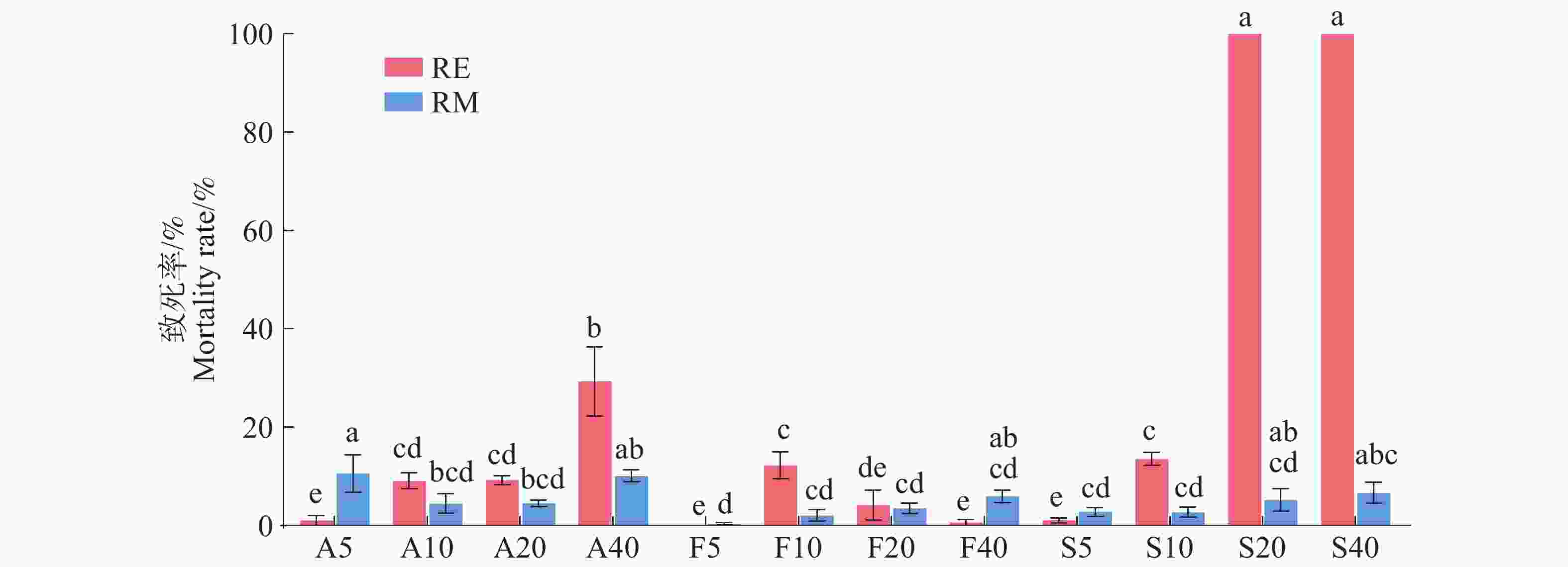
20、40 mg·L−1阿维菌素、噻唑磷叶面喷雾3 d后得到的RE对南方根结线虫有一定的致死效果(图1)。与对照组相比,阿维菌素随着处理质量浓度的增加RE对J2s的致死率提高,A40-RE致死率达到29.3%;而阿维菌素处理获得的RM对J2s的致死效果较差,且不稳定20、40 mg·L−1处理获得的RE对J2s的致死效果最好,随着处理质量浓度的提高而增加,S10-RE致死率为13.55%S20-RE和S40-RE致死率均高达100%,但噻唑磷处理的RM对J2s效果较差;氟吡菌酰胺处理获得的RE及RM均对J2s无明显致死效果。
-
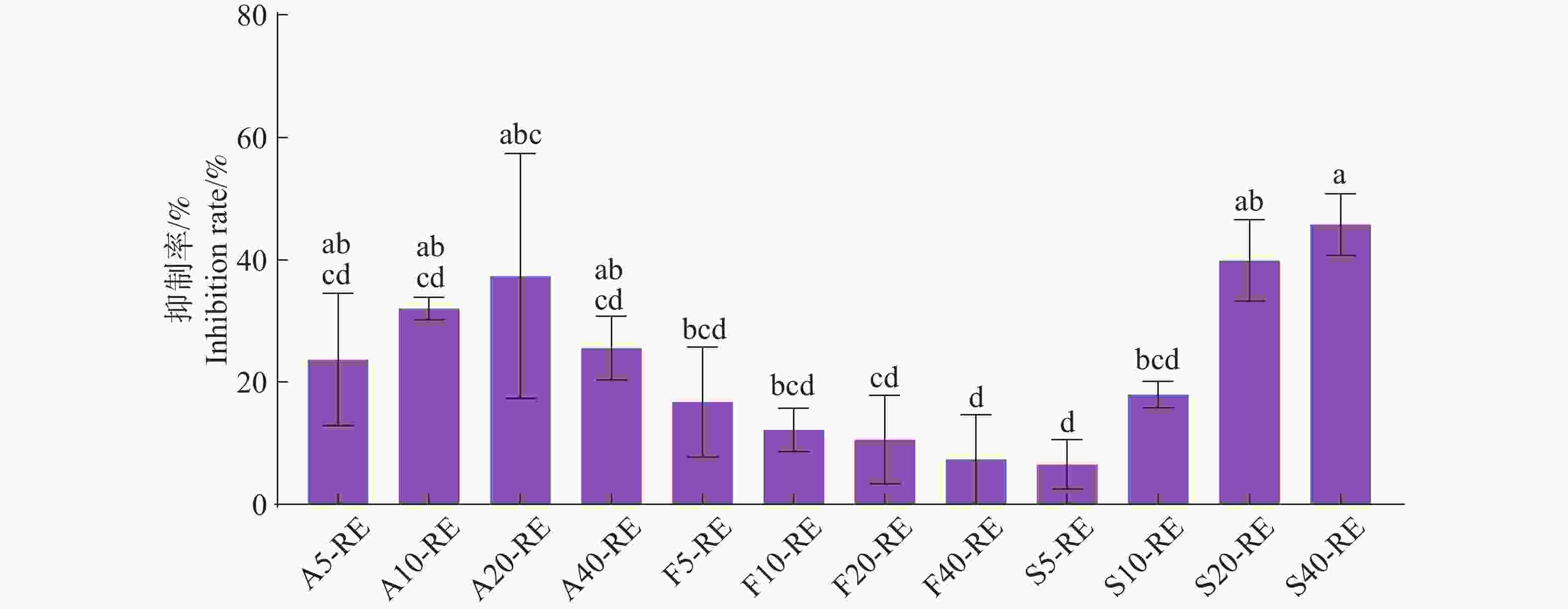
叶面喷施杀线剂后,番茄RE对线虫卵孵化的抑制作用表现不同(图2)。噻唑磷RE的抑制效果最好,S20-RE和S40-RE处理对卵孵化的抑制率分别达39.90%和45.78%;阿维菌素A20-RE抑制率达到峰值37.34%,而A40-RE则下降至25.56%;氟吡菌酰胺RE效果最差。
-
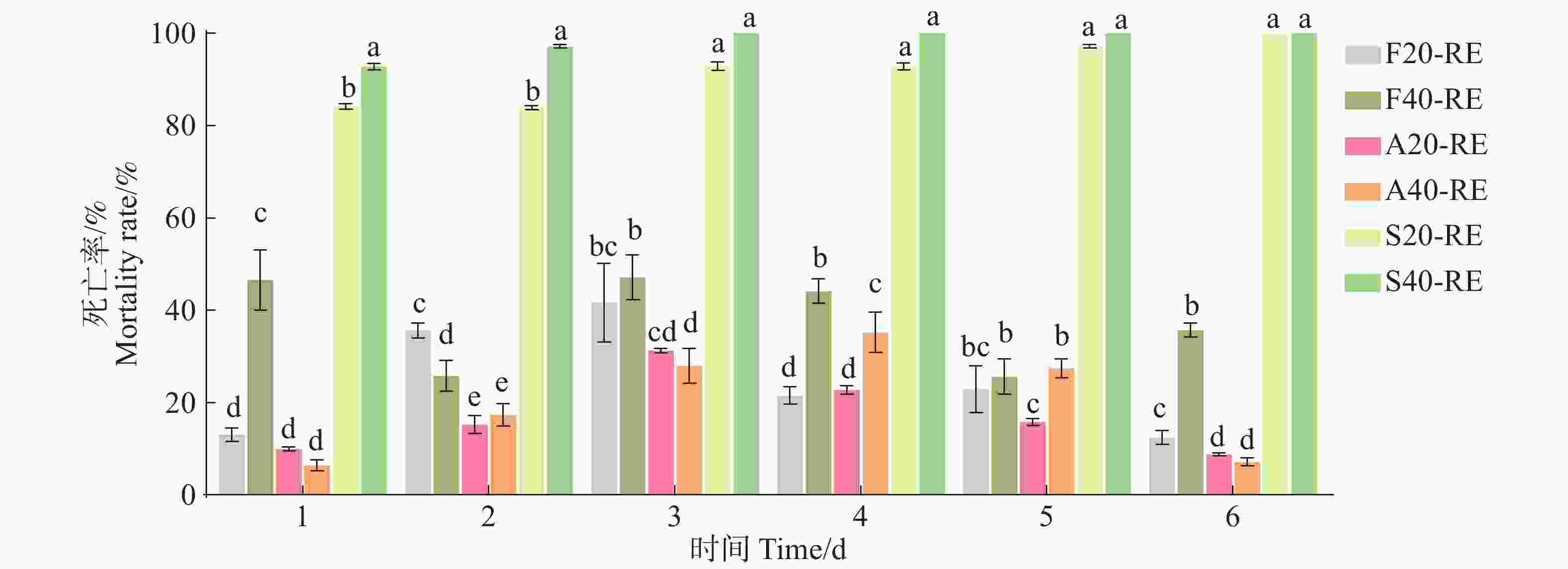
番茄喷施杀线剂后不同时段提取的RE对J2s的致死效果差异显著(图3)。噻唑磷处理组对J2s的致死效果显著高于阿维菌素和氟吡菌酰胺,S20-RE对J2s的致死率随着RE获取时间的延长而上升,至第6天达100%,而S40-RE在第3天致死率就达100%。F40-RE在第3天达到峰值,为47.12%,A40-RE在第4天达到峰值,仅为35.21%,两者均显著低于噻唑磷。
-
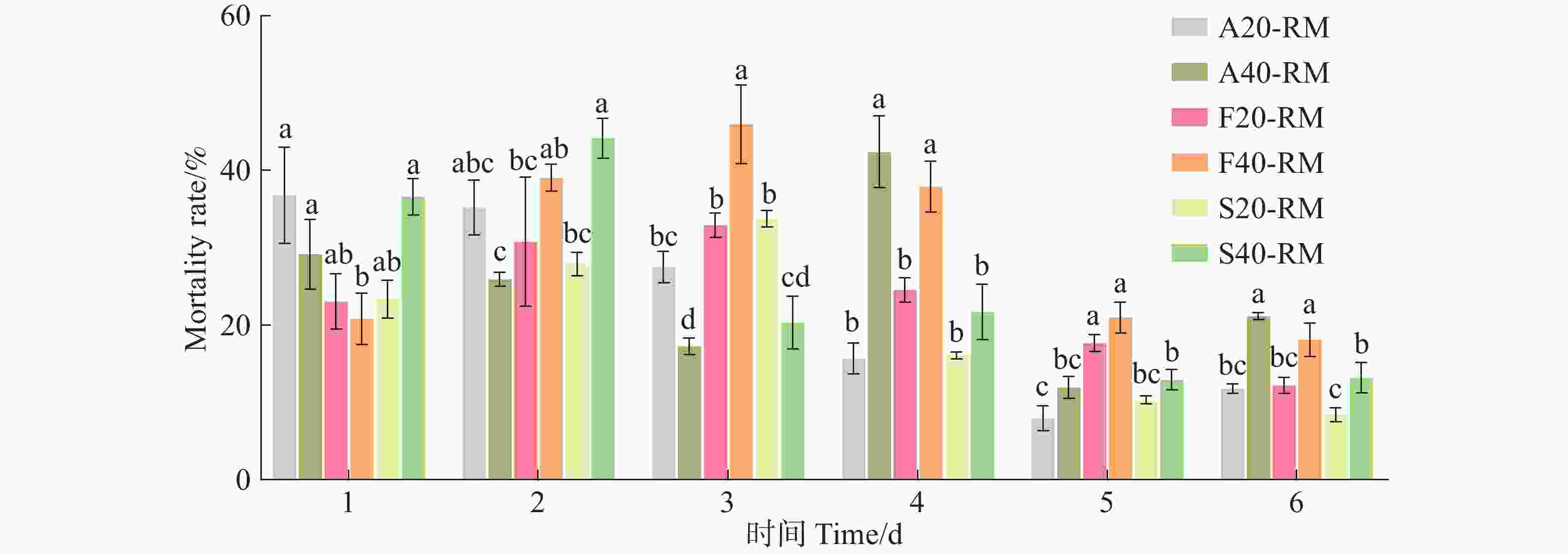
喷施杀线剂后不同时段提取的RM对J2s的致死效果不同(图4)。阿维菌素处理组RM对J2s致死效果整体呈现随着时间延长而下降;氟吡菌酰胺处理组RM整体呈现先增后减的趋势,且F40-RM在第3天达峰值45.97%;噻唑磷S40-RM在第2天达最高44.15%,随后呈下降趋势。
-
根结线虫是世界十大重要植物寄生线虫之首[2],不仅难以防治而且易与其他植物病原体相互作用,形成复合侵染[35]。目前根结线虫主要仍以噻唑磷、氟吡菌酰胺等化学药剂防治为主,通过拌土、灌根进行施药[6,9]。有研究者发现,噻唑磷可在番茄体内进行内吸输导,通过根部施药可兼治地上部害虫如蚜虫、叶螨、蓟马等[36 − 37];氟吡菌酰胺具有优异的内吸输导性,通过叶或根吸收后在植物体内输导达到抑菌效果[38]。在本研究中,氟吡菌酰胺、噻唑磷叶面喷施处理对番茄根结线虫病均具有一定防治效果,同时,叶面喷施处理获得的根系分泌物(RE)对J2s和卵孵化均有较好的抑杀效果,推测与氟吡菌酰胺和噻唑磷从番茄茎叶向根部输导有关。
当植物受到外界因素干扰时,会引起植物产生抗性相关次级代谢物质,可作为引诱剂和驱避剂来影响线虫行为[11,19]。蚜虫取食马铃薯后,其根系分泌会抑制马铃薯白线虫(Globodera pallida)卵的孵化,在暴露于受更多蚜虫侵染的马铃薯植株根系分泌物的孢囊中,Gpa-nep-1的上调显著减弱[15]。氟吡菌酰胺处理大豆幼苗后,出现多个与系统抗性相关的基因差异表达,这表明氟吡菌酰胺除了已知的杀线虫活性外,存在诱导大豆系统抗性的可能[39]。纳米硒喷施番茄植株叶面后,根系分泌物能够抑制根结线虫卵的孵化,且对根结线虫具有显著的盆栽防效[3]。本研究发现噻唑磷叶面喷施处理得到的RE对J2s具有极高的致死率,推测除了药剂的内吸性之外,噻唑磷可能诱导番茄合成了毒性代谢物(如黄酮类),从而对南方根结线虫起到杀伤作用。而噻唑磷处理诱导的根系代谢物(RM)对J2s的作用不佳,推测与采用水溶性提取方法导致非水溶性活性物质提取失败有关。因此,后续将完善RM的提取方法,并开展探索噻唑磷叶面喷施处理诱导番茄抗根结线虫的机制。
Foliar application of nematicides in the control of root-knot nematodes infecting tomato in pots
-
摘要: 根结线虫(Meloidogyne spp.)是全球最常见的植物寄生线虫之一,严重威胁农业生产,化学药剂根围施药仍是其目前主要的防治手段。本研究采用叶面喷施杀线剂的方法探索其对番茄根结线虫的盆栽防效,以及根系分泌物(RE)和根系代谢物(RM)对二龄幼虫(J2s)和卵孵化的抑杀效果。结果表明,氟吡菌酰胺、噻唑磷、阿维菌素叶面喷施对番茄根结线虫病具有一定的盆栽防效;整体上根系分泌物较根系代谢物对J2s、卵孵化的抑杀效果好,其中,噻唑磷叶面喷施处理获得的RE对J2s表现出极强的抑杀作用,在施药后第1天致死率就达到84.10%。研究结果初步证明了叶面喷施杀线剂防治根结线虫的可行性,可为热带设施农业减少土壤施药、“老药新用”提供创新策略。Abstract: Root-knot nematodes (Meloidogyne spp.) are one of the most important plant parasitic nematodes worldwide, which seriously threatens agricultural production. Application of nematicides around the root-zone is still the main control method. Tomato plants in pots were foliar sprayed with nematicides to explore the pot control efficacy of the nematicides against root-knot nematodes in tomato and the inhibitory effects of root exudates (RE) and root metabolites (RM) on the second-stage juveniles (J2s) and egg hatching. The results showed that foliar application of fluopyram, fosthiazate, and abamectin had certain pot control efficacy against root-knot nematodes in tomato. On the whole, RE had better inhibitory effect on J2s and egg hatching than RM. RE obtained by foliar application of fosthiazate showed extremely high inhibitory effect on J2s, with a mortality rate of 84.10% on the first day after application. The results preliminarily proved the feasibility of foliar application of nematicides for the control of root-knot nematodes, which might provide an innovative strategy for reducing soil application and "reusing old nematicides" in tropical facility agriculture.
-
Key words:
- Meloidogyne incognita /
- nematicide /
- foliar application /
- root exudates /
- root metabolites
-
图 2 经杀线剂叶面喷施处理的番茄根系分泌物对南方根结线虫卵孵化的抑制作用(12 d)
RE.根系分泌物;A5.5 mg·L−1阿维菌素;F5.5 mg·L−1氟吡菌酰胺;S5.5 mg·L−1噻唑磷,依此类推。
Fig. 2 Inhibition effect of root exudates of tomato sprayed with nematicides on the eggs hatching of Meloidogyne incognita (12 d)
RE.Root exudates; A5.5 mg·L−1 Avermectin; F5.5 mg·L−1 Flupyram; S5.5 mg·L−1 Fosthiazate, and so on.
图 3 杀线剂叶面喷施处理诱导番茄不同时段根系分泌物对南方根结线虫J2s的致死效果
RE.根系分泌物;A20.20 mg·L−1阿维菌素;F20.20 mg·L−1氟吡菌酰胺;S20.20 mg·L−1噻唑磷,依此类推。
Fig. 3 Lethal effects of tomato root exudates induced by foliar application of nematicides leaf different time on J2s of Meloidogyne incognita
RM.Root metabolites; A20.20 mg·L−1 Avermectin; F20.20 mg·L−1 Flupyram; S20.20 mg·L−1 Fosthiazate, and so on.
图 4 杀线剂叶面喷施处理诱导番茄不同时段根系代谢物对南方根结线虫J2s的致死效果
RM.根系代谢物;A20:20 mg·L−1阿维菌素;F20.20 mg·L−1氟吡菌酰胺;S20.20 mg·L−1噻唑磷,依此类推。
Fig. 4 Lethal effects of tomato root metabolites induced by foliar application of nematicides at different time on J2s of Meloidogyne incognita
RM. Root metabolites; A20.20 mg·L−1 Avermectin;F20.20 mg·L−1 Flupyram; S20.20 mg·L−1 Fosthiazate, and so on.
表 1 4种杀线剂对南方根结线虫J2s的毒力
Table 1 Toxicity of nematicides against the second-stage juveniles of Meloidogyne incognita
药剂
Nematicide斜率±标准误差
Slope±SELC50(95%CL)/
(mg·L−1)LC99(95%CL)/
(mg·L−1)自由度
dfP值
P value卡方值
Chi-square甲维盐(J)
Emamectin benzoate2.315±0.174 2.490
(2.092~2.859 )25.235
(20.413~33.347 )13 0.692 10.018 阿维菌素(A)
Abamectin2.145±0.198 1.693
(1.277~2.076 )20.565
(16.293~28.461 )13 0.503 12.299 氟吡菌酰胺(F)
Fluopyram1.817±0.166 1.003
(0.592~1.410)19.121
(14.543~29.008)13 0.295 15.199 噻唑磷(S)
Fosthiazate3.145±0.169 4.654
(4.112~5.186)25.557
(20.400~34.719)13 0.014 26.646 表 2 杀线剂叶面喷施处理对番茄根结线虫的盆栽药效
Table 2 Control effect of foliar application of nematicides on Meloidogyne incognita in tomato in pots
处理
Treatment根系鲜质量增长率/%
Growth rate of
fresh root weight/%每克根结数/(个·g−1)
The number of root
knot per gram root/
(number·g−1)相对繁殖指数
Relative reproduction
index病情指数
Disease index相对防效/%
Control efficiency/%CK (10.66±4.53)abc — (86.11±6.73)ab — J20 (21.42±4.18)b (11.74±3.91)a (0.58±0.33)a (88.89±7.70)a (−10.15±36.73)e J40 (19.67±2.21)b (11.36±2.08)ab (0.53±0.33)ab (87.22±7.52)ab (−6.55±19.52)e F20 (12.45±4.32)b (8.31±3.46)cd (0.53±0.59)abcd (78.89±8.39)abcd (22.04±32.45)bcd F40 (−3.29±5.28)c (5.97±2.58)d (0.48±0.38)d (68.89±7.70)d (43.98±24.15)b A20 (5.25±4.90)bc (9.84±3.22)abc (0.56±0.29)abcd (79.44±5.89)abcd (7.66±30.24)de A40 (14.23±6.55)b (8.71±2.33)bcd (0.71±0.65)a (83.89±3.47)abc (18.32±21.82)cd S30 (−4.55±6.06)c (8.60±3.01)bcd (0.43±0.29)bcd (76.11±3.47)bcd (19.29±28.25)cd S60 (5.70±4.55)bc (6.19±2.74)d (0.71±0.65)cd (72.22±1.92)cd (41.94±25.69)bc J20* (50.69±5.38)a (1.60±1.10)e (0.15±0.25)bc (51.67±4.41)e (84.99±10.37)a S30* (17.77±5.87)b (0.23±0.21)e (0.43±0.35)c (16.67±8.82)f (97.88±1.94)a 注:CK.0.1%Tween-80(含6.0 mL·L−1 DMF,叶面喷施);J20.20 mg·L−1甲维盐(叶面喷施);J40.40 mg·L−1甲维盐(叶面喷施);F20.20 mg·L−1氟吡菌酰胺(叶面喷施);F40.40 mg·L−1氟吡菌酰胺(叶面喷施);A20.20 mg·L−1阿维菌素(叶面喷施);A40.40 mg·L−1阿维菌素(叶面喷施);S30.30 mg·L−1噻唑磷(叶面喷施);S60.60 mg·L−1噻唑磷(叶面喷施);J20*.20 mg·L−1甲维盐(灌根);S30*.30 mg·L−1噻唑磷(灌根)。每个数值代表平均值 ± 标准差(n = 10),列中的每个字母代表显著差异程度:P<0.05。
Note: CK.0.1%Tween-80(Containing 6.0 mg·L−1 DMF, foliar application); J20.20 mg·L−1 Emamectin benzoate(Foliar application); J40.40 mg·L−1 Emamectin benzoate(Foliar application); F20.20 mg·L−1 Flupyram(Foliar application); F40. 40 mg·L−1 Flupyram(Foliar application); A20.20 mg·L−1 Abamectin(Foliar application); A40.40 mg·L−1 Abamectin(Foliar application); S30.30 mg·L−1 Fosthiazate(Foliar application); S60.60 mg·L−1 Fosthiazate(Foliar application); J20*.20 mg·L−1 Emamectin benzoate(Root irrigation); S30*.30 mg·L−1 Fosthiazate(Root irrigation). Each value represents mean ± standard deviation(n = 10), and each letter in the column represents the degree of significant difference: P<0.05. -
[1] COYNE D L, CORTADA L, DALZELL J J, et al. Plant-parasitic nematodes and food security in sub-Saharan Africa[J]. Annual Review of Phytopathology, 2018, 56: 381 − 403. doi: 10.1146/annurev-phyto-080417-045833 [2] JONES J T, HAEGEMAN A, DANCHIN E G J, et al. Top 10 plant-parasitic nematodes in molecular plant pathology[J]. Molecular Plant Pathology, 2013, 14(9): 946 − 961. doi: 10.1111/mpp.12057 [3] DAOUSH A S M, HENDAWEY M H, YASEEN R, et al. Effect of biosynthesized nanoselenium on controlling tomato root-knot nematode Meloidogyne incognita[J]. Agronomy, 2023, 13(7): 1668. doi: 10.3390/agronomy13071668 [4] WASWA S J, WACEKE J W, MWANGI M. Compatibility of velum® (synthetic nematicide) with endophytic Colletotrichum nigrum and commercial Trichoderma asperellum against root-knot nematodes on tree tomato[J]. International Journal of Plant & Soil Science, 2024, 36(11): 278 − 292. doi: 10.9734/ijpss/2024/v36i115143 [5] QIAO K, LIU Q C, ZHANG S A. Evaluation of fluazaindolizine, a new nematicide for management of Meloidogyne incognita in squash in calcareous soils[J]. Crop Protection, 2021, 143: 105469. doi: 10.1016/j.cropro.2020.105469 [6] BROWN C R, MOJTAHEDI H, JAMES S, et al. Development and evaluation of potato breeding lines with introgressed resistance to Columbia root-knot nematode (Meloidogyne chitwoodi)[J]. American Journal of Potato Research, 2006, 83(1): 1 − 8. doi: 10.1007/BF02869604 [7] NICO A I, JIMÉNEZ-DÍAZ R M, CASTILLO P. Control of root-knot nematodes by composted agro-industrial wastes in potting mixtures[J]. Crop Protection, 2004, 23(7): 581 − 587. doi: 10.1016/j.cropro.2003.11.005 [8] TALAVERA M, VERDEJO-LUCAS S, ORNAT C, et al. Crop rotations with Mi gene resistant and susceptible tomato cultivars for management of root-knot nematodes in plastic houses[J]. Crop Protection, 2009, 28(8): 662 − 667. doi: 10.1016/j.cropro.2009.03.015 [9] 刘晓艳, 闵勇, 饶犇, 等. 杀线虫剂产品研究进展[J]. 中国生物防治学报, 2021, 37(3): 592 − 597. doi: 10.16409/j.cnki.2095-039x.2021.01.004 [10] 张玉龙, 邹俊杰, 唐艳梅. 根结线虫防治技术研究[J]. 现代农村科技, 2023(7): 52 − 53. doi: 10.3969/j.issn.1674-5329.2023.07.035 [11] CAO W H, LIU J, ZHOU Q Y, et al. Expression of tobacco ethylene receptor NTHK1 alters plant responses to salt stress[J]. Plant, Cell & Environment, 2006, 29(7): 1210 − 1219. doi: 10.1111/j.1365-3040.2006.01501.x [12] RYALS J A, NEUENSCHWANDER U H, WILLITS M G, et al. Systemic acquired resistance[J]. The Plant Cell, 1996, 8(10): 1809. doi: 10.1105/tpc.8.10.1809 [13] VALLAD G E, GOODMAN R M. Systemic acquired resistance and induced systemic resistance in conventional agriculture[J]. Crop Science, 2004, 44(6): 1920 − 1934. doi: 10.2135/cropsci2004.1920 [14] DA ROCHA A B, HAMMERSCHMIDT R. History and perspectives on the use of disease resistance inducers in horticultural crops[J]. HortTechnology, 2005, 15(3): 518 − 529. doi: 10.21273/HORTTECH.15.3.0518 [15] HOYSTED G A, BELL C A, LILLEY C J, et al. Aphid colonization affects potato root exudate composition and the hatching of a soil borne pathogen[J]. Frontiers in Plant Science, 2018, 9: 1278. doi: 10.3389/fpls.2018.01278 [16] UDALOVA Z V, FOLMANIS G E, KHASANOV F K, et al. Selenium nanoparticles-an inducer of tomato resistance to the root-knot nematode Meloidogyne incognita (kofoid et white, 1919) chitwood 1949[J]. Doklady Biochemistry and Biophysics, 2018, 482(1): 264 − 267. doi: 10.1134/S1607672918050095 [17] 罗永清, 赵学勇, 李美霞. 植物根系分泌物生态效应及其影响因素研究综述[J]. 应用生态学报, 2012, 23(12): 3496 − 3504. doi: 10.13287/j.1001-9332.2012.0443 [18] BIRD D M. Signaling between nematodes and plants[J]. Current Opinion in Plant Biology, 2004, 7(4): 372 − 376. doi: 10.1016/j.pbi.2004.05.005 [19] REYNOLDS A M, DUTTA T K, CURTIS R H C, et al. Chemotaxis can take plant-parasitic nematodes to the source of a chemo-attractant via the shortest possible routes[J]. Journal of the Royal Society Interface, 2011, 8(57): 568 − 577. doi: 10.1098/rsif.2010.0417 [20] KIHIKA R, MURUNGI L K, COYNE D, et al. Parasitic nematode Meloidogyne incognita interactions with different Capsicum annum cultivars reveal the chemical constituents modulating root herbivory[J]. Scientific Reports, 2017, 7(1): 2903. doi: 10.1038/s41598-017-02379-8 [21] MURUNGI L K, KIRWA H, COYNE D, et al. Identification of key root volatiles signaling preference of tomato over spinach by the root knot nematode Meloidogyne incognita[J]. Journal of Agricultural and Food Chemistry, 2018, 66(28): 7328 − 7336. doi: 10.1021/acs.jafc.8b03257 [22] SIKDER M M, VESTERGÅRD M. Impacts of root metabolites on soil nematodes[J]. Frontiers in Plant Science, 2020, 10: 1792. doi: 10.3389/fpls.2019.01792 [23] KIRWA H K, MURUNGI L K, BECK J J, et al. Elicitation of differential responses in the root-knot nematode Meloidogyne incognita to tomato root exudate cytokinin, flavonoids, and alkaloids[J]. Journal of Agricultural and Food Chemistry, 2018, 66(43): 11291 − 11300. doi: 10.1021/acs.jafc.8b05101 [24] 丁晓帆, 邵雨, 范瑞琦, 等. 一种便携式线虫孵化装置: 中国, 211064709U[P]. 2020-07-24. https://pss-system.cponline.cnipa.gov.cn/documents/detail?prevPageTit=changgui. [25] 王曦茁, 汪来发, 孟繁丽, 等. 淡紫拟青霉航天诱变菌株对南方根结线虫的致病力[J]. 林业科学研究, 2016, 29(2): 216 − 220. doi: 10.3969/j.issn.1001-1498.2016.02.010 [26] 李秋捷, 陆秀红, 黄金玲, 等. 不同药剂对南方根结线虫的室内毒力测定[J]. 浙江农业科学, 2018, 59(8): 1432 − 1433. doi: 10.16178/j.issn.0528-9017.20180832 [27] 刘勇鹏. 不同杀线虫剂对日光温室番茄根结线虫病防效研究[D]. 郑州: 河南农业大学, 2018. [28] 高倩圆, 胡飞龙, 祝红红, 等. 蓖麻提取物和淡紫拟青霉对南方根结线虫的防治作用[J]. 生态学杂志, 2011, 30(10): 2250 − 2256. doi: 10.13292/j.1000-4890.2011.0299 [29] 席先梅, 白全江, 李玉民, 等. 41.7%氟吡菌酰胺悬浮剂不同施药时期对黄瓜根结线虫的防治效果[J]. 植物保护, 2021, 47(5): 314 − 319. doi: 10.16688/j.zwbh.2020291 [30] 肖靖秀, 郑毅, 汤利. 小麦− 蚕豆间作对根系分泌低分子量有机酸的影响[J]. 应用生态学报, 2014, 25(6): 1739 − 1744. doi: 10.13287/j.1001-9332.20140415.003 [31] AKHTAR H, ANITA S, PRABHAT KUMAR S. Studies on the management of root-knot nematode, Meloidogyne incognita-wilt fungus, Fusarium oxysporum disease complex of green gram, Vigna radiata cv ML-1108[J]. Journal of Zhejiang University Science B, 2005, 6(8): 736 − 742. doi: 10.1007/BF02842432 [32] 陆秀红, 刘志明, 黄金玲, 等. 白花曼陀罗叶提取物对南方根结线虫生长发育的影响[J]. 广西农业生物科学, 2006, 25(2): 136 − 139. [33] GIANNAKOU I O, KARPOUZAS D G, ANASTASIADES I, et al. Factors affecting the efficacy of non-fumigant nematicides for controlling root-knot nematodes[J]. Pest Management Science, 2005, 61(10): 961 − 972. doi: 10.1002/ps.1081 [34] 漆永红, 曹素芳, 吕和平, 等. 不同药剂对南方根结线虫卵孵化及2龄幼虫活性的影响[J]. 西北农业学报, 2011, 20(9): 184 − 189. doi: 10.3969/j.issn.1004-1389.2011.09.037 [35] LI D, JI J, YUAN Y J, et al. Toxicity comparison of nanopolystyrene with three metal oxide nanoparticles in nematode Caenorhabditis elegans[J]. Chemosphere, 2020, 245: 125625. doi: 10.1016/j.chemosphere.2019.125625 [36] 李翠英. 福气多[J]. 湖南农业, 2011(7): 16. [37] LIN S K, ZHOU Y, WU J Y Z, et al. Dissipation and residue of fosthiazate in tomato and cherry tomato and a risk assessment of dietary intake[J]. Environmental Science and Pollution Research, 2022, 29(6): 9248 − 9256. doi: 10.1007/s11356-021-16305-z [38] CHAWLA S, PATEL D J, PATEL S H, et al. Behaviour and risk assessment of fluopyram and its metabolite in cucumber (Cucumis sativus) fruit and in soil[J]. Environmental Science and Pollution Research, 2018, 25(12): 11626 − 11634. doi: 10.1007/s11356-018-1439-y [39] ROCHA L F, SUBEDI A, PIMENTEL M F, et al. Fluopyram activates systemic resistance in soybean[J]. Frontiers in Plant Science, 2022, 13: 1020167. doi: 10.3389/fpls.2022.1020167 -




 下载:
下载: