-
沉香是沉香属(Aquilaria)或拟沉香属(Gyrinops)植物茎干在受到损伤后,分泌树脂并逐渐形成的树脂化木材,具有极高的药用价值,被誉为“药中黄金”和“众香之首”,在传统药物、香水、化妆品、熏香和精油中均具有广泛的应用[1]。研究表明,沉香中富含倍半萜、色酮类和芳香族类等多种次生代谢物,其中2−(2−苯乙基)色酮和倍半萜是其特征成分和主要药理活性成分[2-3]。沉香提取物中具有多种生物活性,包括神经活性、细胞毒性、抗菌、抗炎、和抗氧化活性等[4-6]。白木香(Aquilaria sinensis)是中国本土所产沉香的唯一来源植物[7],主要分布在中国华南地区[8]。白木香只有遭受自然因素(雷击、虫噬、真菌感染等)或人为因素(砍伤、钻孔、打钉等)胁迫后才会产生沉香[9]。在受到外界胁迫时,白木香会启动防御反应系统,激活倍半萜和色酮等次生代谢途径并合成相关代谢产物[10]。值得注意的是,这些次生代谢产物的跨膜转运和区隔化储存过程不仅决定了沉香的化学组成谱,更直接影响其品质。因此,阐明沉香倍半萜和色酮类次生代谢物的转运机制,对于揭示沉香形成机制及提升其品质具有重要的理论意义和应用价值。
ABC(ATP-Binding Cassette)转运蛋白是迄今发现的最大转运蛋白家族之一,在动物、植物和微生物中普遍存在[11]。该蛋白具有高度保守的核苷酸结合结构域(NBD)和包含5或6个跨膜螺旋的跨膜结构域(TMD)[12]。ABC转运蛋白主要以氨基酸、脂质体、多糖、多肽、生物碱和药物等为底物,通过ATP水解为能量,完成对底物的跨膜运输[13]。大多数ABC转运蛋白是膜蛋白,可在细胞膜上运输各种分子,按照其转运功能分为摄取型和外排型两类[14]。植物中共发现8个ABC转运蛋白亚家族:ABC-A、ABC-B、ABC-C、ABC-D、ABC-E、ABC-F、ABC-G和ABC-I[15]。ABC-G是植物中最大的ABC蛋白家族,相关研究表明ABC-G转运蛋白能广泛参与植物重金属、抗菌化合物、脱落酸,以及萜类、黄酮类、木脂素类等次生代谢物的转运[16]。
目前,关于沉香特征性成分形成的研究集中于解析沉香特征性成分的合成及调控方面,而关于特征性成分转运的机制研究较少,相关转运蛋白及其调控机制研究也未见报道。本研究从白木香中克隆了ABC-G转运蛋白编码基因AsABCG1,通过对其理化性质、结构域、蛋白二级结构和三级结构、启动子区的顺式调控元件等方面进行分析,并利用实时荧光定量PCR(qRT-PCR)技术对AsABCG1基因的表达变化趋势进行了分析,为进一步研究AsABCG1基因在白木香次生代谢物转运过程中的功能奠定基础。
-
本次实验所用的白木香材料来源于中国热带农业科学院热带生物技术研究所基地,选取生长一致的3年生白木香进行胁迫处理。对于机械伤害处理,利用电钻对白木香茎干钻孔处理(图1-A);茉莉酸甲酯处理,使用溶解于体积分数为0.1%乙醇溶液的180 μmol·L−1茉莉酸甲酯浸湿纸巾包裹白木香茎干(图1-B)。每个处理3个生物学重复,并于处理后0、3、6、24、72、120 h后分别取样,立即放于液氮冷冻研磨,并于−80 ℃冷冻保存,以供后续实验使用。
-
采用诺维公司RNA提取试剂盒并按照说明书方法提取白木香茎干总RNA,提取后利用琼脂糖凝胶电泳评估其质量。RNA样本质量经检测条带正确后,使用RNA反转录试剂盒进行反转录,合成cDNA后置于−80 ℃保存。
-
结香剂处理能够激活白木香茎干次生代谢物合成并促进沉香的形成。先前研究中对白木香茎干进行结香剂处理并在0、3、6、9 d对处理后的白木香进行采样,之后对采取的白木香样品进行转录组测序得到白木香转录组数据[17]。基于转录组注释数据和FPKM的表达值分析,筛选出一条结香剂处理差异表达基因,将其命名为AsABCG1。通过软件SPSS v20.0分析差异表达基因与6种已知2−(2−苯乙基)色酮类化合物含量的皮尔逊相关系数。根据AsABCG1的CDS序列,使用软件CE Design v1.01设计其特异性引物(表1)。以逆转录获得的cDNA为模板进行PCR扩增,得到与目的基因大小一致的条带后,使用Agarose Gel DNA Recovery Kit [中科瑞泰(北京)生物科技有限公司]对扩增产物进行纯化。将纯化后的目的基因构建到PMD-19T载体上,并转入大肠杆菌感受态DH5α中,经菌液PCR鉴定为阳性后提取质粒,然后送测序。序列正确的质粒冻存于−20 °C冰箱供后续实验。
表 1 本实验中使用的引物
Table 1. The primers used in this experiment
引物名称 Primer 引物序列(5′—3′)
Sequence (5′—3′)AsABCG1-F GAACCTTGGGATTGAGAAGACGA AsABCG1-R GCAACTAGTTTGCCCATACTAAACCAGACTCT qAsABCG1-F ATGGGATGGACATAGAGGATTTG qAsABCG1-R GGAAGAATCCTCCCACCAATATC AsGADPH-F CTGGTATGGCATTCCGTGTA AsGADPH-R AACCACATCCTCTTCGGTGTA -
用Expasy在线软件(Expasy-SIB Swiss Institute of Bioinformatics)对AsABCG1蛋白的理化性质、跨膜结构、信号肽、磷酸位点进行预测,利用NPS@:SOPMA(ibcp.fr)在线预测蛋白二级结构,使用SWISS-MODEL(expasy.org)在线预测蛋白三级结构;运用PlantCARE(ugent.be)在线软件查找启动子区顺式作用元件;使用DNAMAN软件对不同物种的蛋白序列进行对比分析,通过MEGA v10.0软件建立系统发育树。
-
依据荧光定量试剂盒说明书中的方法,设计用于检测AsABCG1基因表达的荧光定量引物和内参基因的荧光定量引物(表1)。根据说明书中反应体系进行加样,并在实时荧光定量PCR仪上进行扩增,设置程序为二步法。对每种处理条件的样品均进行3次生物学重复实验,并采用2−ΔΔCt法计算并分析该基因的相对表达水平。
-
根据课题组梅文莉等专利结香技术处理的白木香转录组数据库[18],共筛选出10个差异表达的ABC转运蛋白基因。利用软件TBtools v2.056 分析其FPKM值并绘制表达量热图(图2-A),结果显示, evm.model.Scaffold2.763 基因的表达在结香剂处理后上调最为明显,将其命名为 AsABCG1。将色酮类化合物含量与ABC基因表达进行相关性分析(图2-B),结果显示,10个具有差异表达的AsABC基因中5个与色酮类具有不同程度的正相关性,另外5个则具有不同程度的负相关性,而AsABCG1与几种主要的色酮类化合物均表现出较高的正相关性,说明AsABCG1可能参与沉香色酮等代谢物的积累。
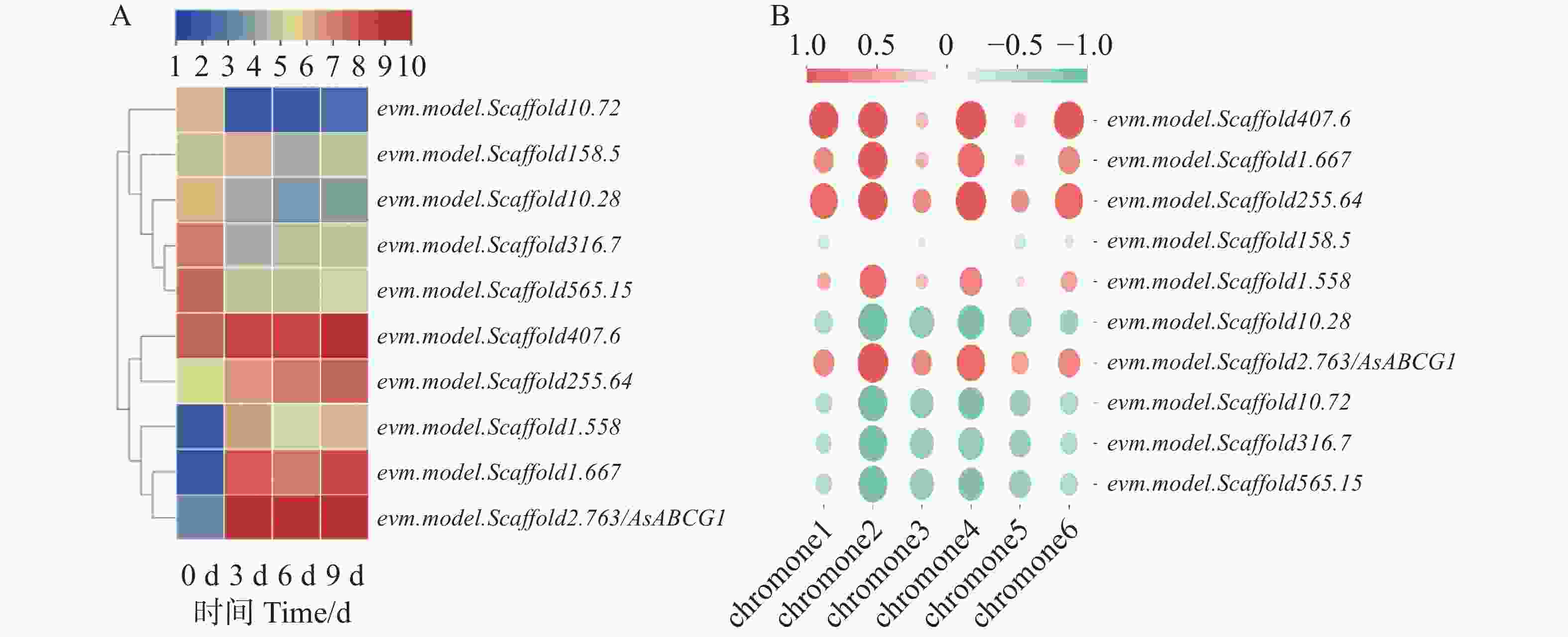
图 2 结香剂处理后AsABC基因的表达及色酮含量相关性分析
Figure 2. Correlation analysis of AsABC gene expression and chromone content after treatment with agarwood inducer
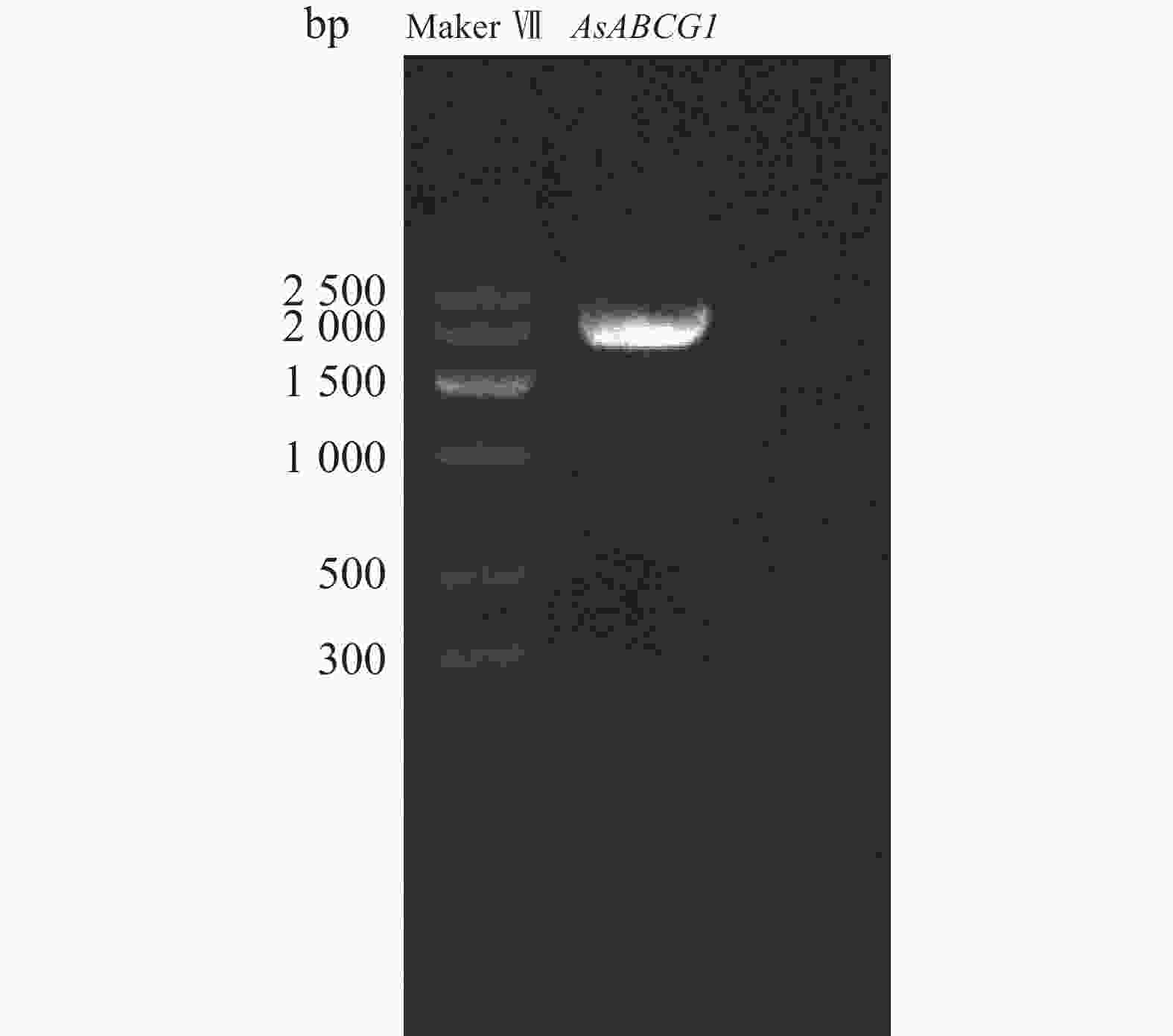
根据白木香转录组中的序列设计 AsABCG1 基因的特异性引物并进行PCR扩增,经琼脂糖凝胶电泳检测显示获得一条清晰的条带(图3)。测序结果表明,该基因的 CDS序列全长为1 986 bp,编码一个包含661个氨基酸的蛋白质。
-
AsABCG1蛋白(分子式:C
3327 H5222 N872O931S38)分子质量约为73.56 kDa,理论等电点(pI)值为8.64;脂肪系数为96.07,不稳定系数为40.98。电荷分析显示该蛋白含有56个负电荷残基(Asp + Glu)和62个正电荷残基(Arg + Lys)。平均亲水性系数为0.139,结合其多肽链存在显著的非亲水性区域,表明AsABCG1属于疏水蛋白(图4-A)。TMHMM server v2.0跨膜结构在线预测表明编码该蛋白的661个氨基酸中共包含6个跨膜结构域,确认为跨膜蛋白(图4-B)。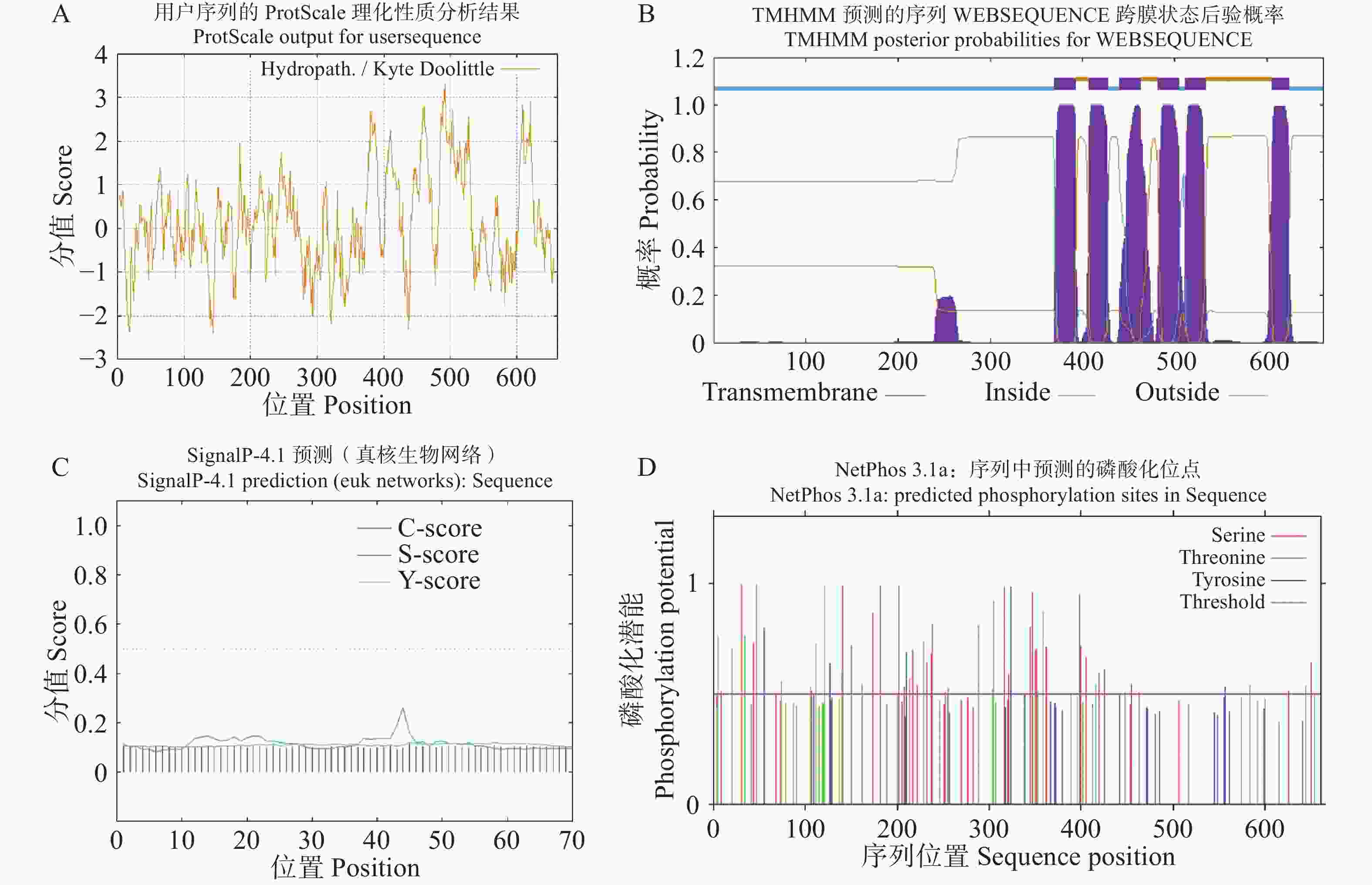
图 4 AsABCG1蛋白理化性质及结构分析
Figure 4. Physicochemical properties and structural analysis of AsABCG1 protein
信号肽在线预测显示AsABCG1蛋白C-score、S-score和Y-score分值都较低,且不存在信号肽剪切位点,为非分泌性蛋白(图4-C)。此外,NetPhos v3.0预测揭示AsABCG1存在较多的潜在磷酸化位点,其中丝氨酸(Ser)最多共有33个,苏氨酸(Thr)为21个,酪氨酸(Tyr)为6个(图4-D)。
-
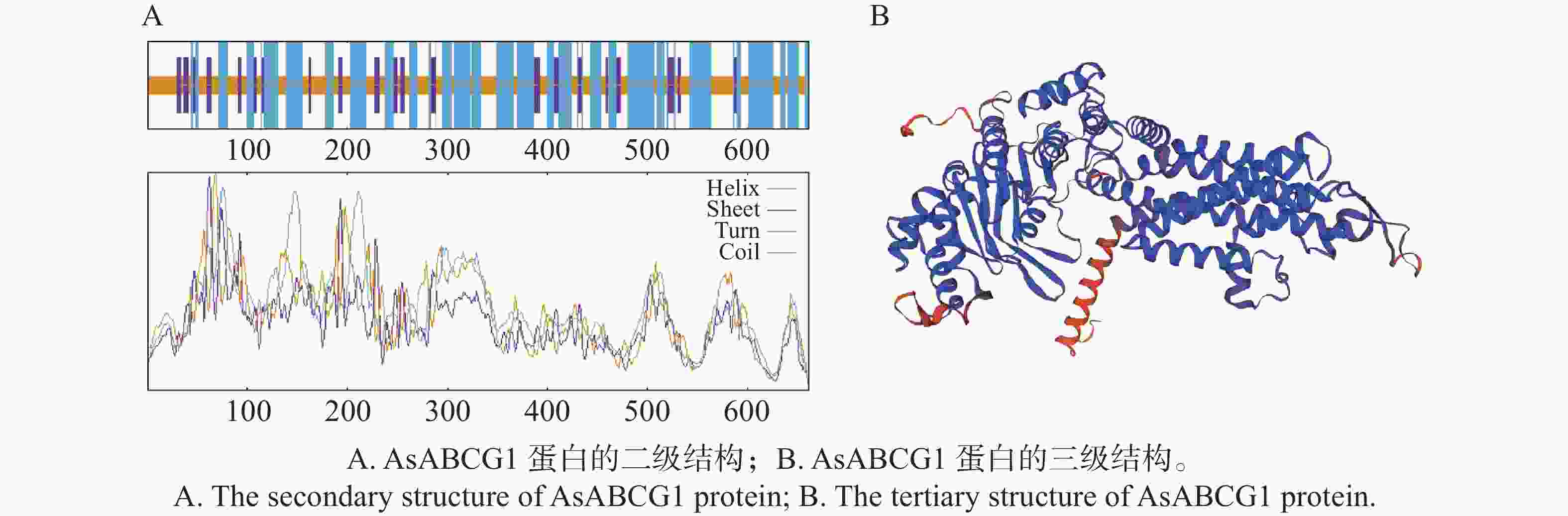
蛋白二级结构有α−螺旋、β−折叠、无规则卷曲和延伸链等。SOPMA在线预测AsABCG1蛋白二级结构(图5-A)结果显示,其结构主要为α−螺旋(48.26%)、无规则卷曲(39.49%)另还有较少的延伸链(12.25%)。α−螺旋是蛋白质二级结构的主要形式,主要由其精确的原子级结构决定,具有高度的规律性和稳定性,能够构成跨膜通道并转运蛋白;无规卷曲是由主链骨架无规律排列形成的构象,能够介导分子识别与结合、构成催化位点、作为翻译后修饰和调控的位点;延伸链指的是构成 β−折叠的肽链构象,也称为β−构象,为蛋白质提供了独特的刚性、平坦和抗拉伸的结构基元。AsABCG1中α−螺旋为其主要结构,结合该结构的功能,可进一步证实该蛋白属于跨膜蛋白。
使用SWISS-MODLE预测三级结构(图5-B),结果表明,该结构与已知榴莲中ABC-G基因家族成员(LOC111308351)的GMQE值为0.81。证实了AsABCG1属于ABC-G亚家族成员,且该结构中存在较多的α−螺旋,这也印证了二级结构的预测结果。二级结构和三级结构的预测结果均表明,AsABG1符合ABC转运蛋白的结构特征。
-
从NCBI中下载与AsABCG1同源性较高的氨基酸序列,并做同源性对比(图6)。结果显示AsABCG1具有典型的植物ABC转运蛋白结构特征,包含2个保守结构域(MotifA和MotifB)。AsABCG1与木槿(Hibiscus syriacus)HsABCG、陆地棉(Gossypium hirsutum)GhABCG、榴莲(Durio zibethinus)DzABCG、可可树(Theobroma cacao)TcABCG、哥伦比亚锦葵(Herrania umbratica)HuABCG中ABC蛋白同源性分别为69.39%、69.77%、69.77%、69.24%、69.20%。
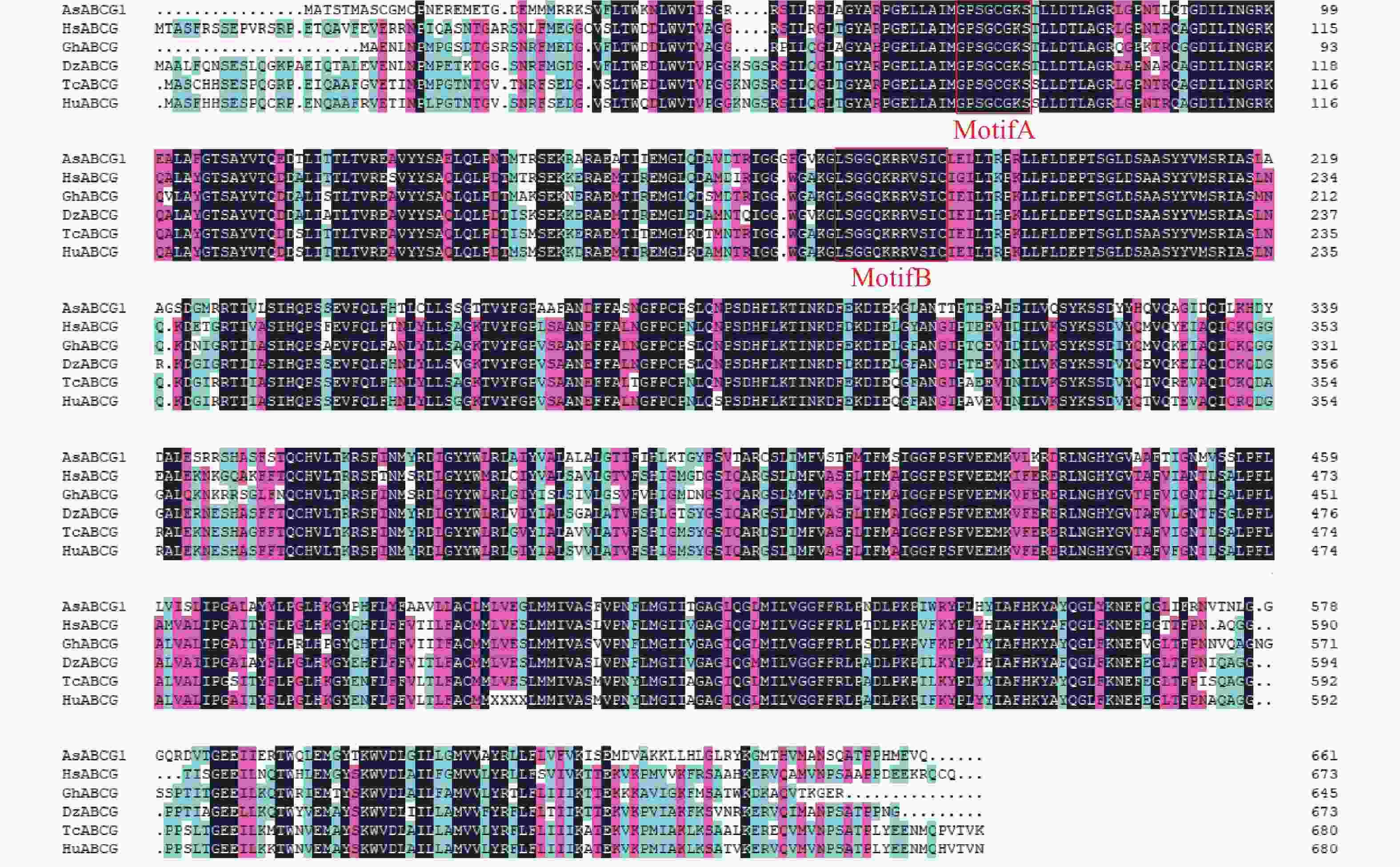
图 6 AsABCG1 与其他植物ABCG多序列比对
Figure 6. Comparison of sequences between AsABCG1 and other plant ABCG proteins
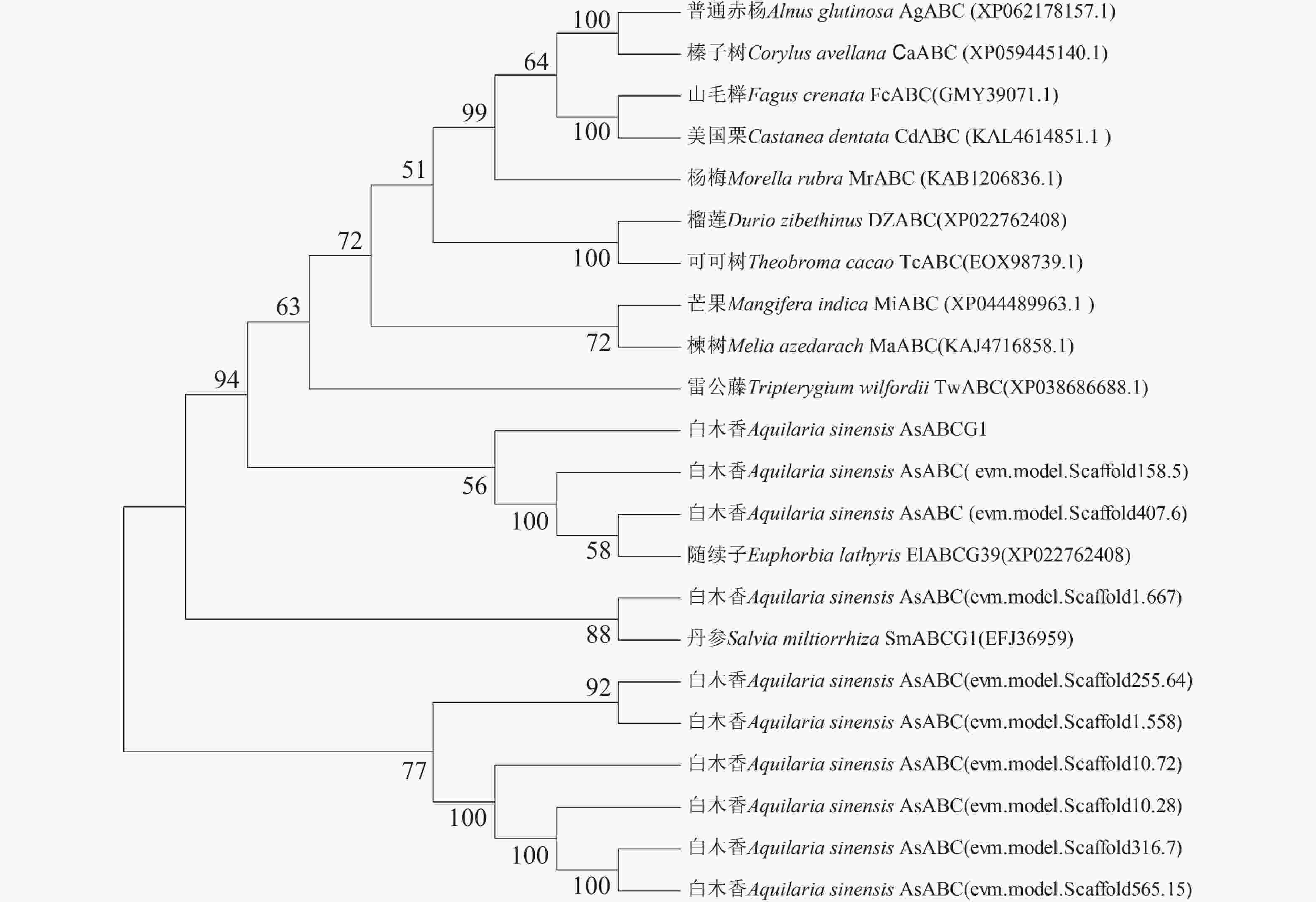
将10个具有差异表达的AsABC蛋白与其他植物中的ABC蛋白氨基酸序列进行系统发育树构建(图7),结果表明,有4个AsABC蛋白(AsABCG1、em.model.Scafold158.5、ev.model.Scafold407.6和evm.model.Scafold1.667)属于ABC-G亚家族,该家族成员在调控植物次生代谢物转运过程中具有重要的作用。
-
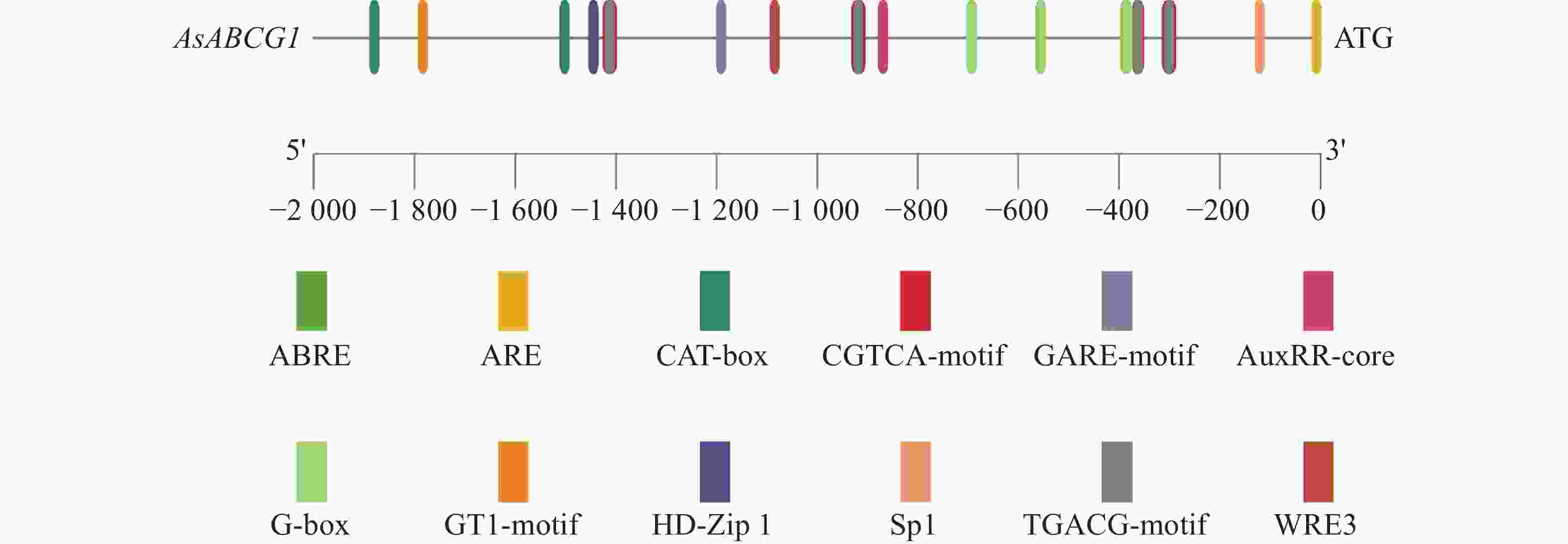
用PlantCARE对AsABCG1基因启动子区进行分析,结果(图8)显示,该区域存在多种参与植物表达调控的顺式作用元件,包括参与光响应调控(G-box cis-acting element)G-box;参与茉莉酸(jasmonic acid response element)TGACG-motif、生长素 (auxin response element)AuxRR-core、赤霉素(gibberellin response element)GARE-motif、脱落酸(abscisic acid response element)ABRE 等多种激素调控;参与胁迫响应如厌氧诱导反应(anaerobic response element)ARE、机械损伤响应元件(wound responsive element 3)WRE3及参与植物生长发育等相关元件。以上结果表明,AsABCG1基因的表达可能受到这些因素的调控。
-
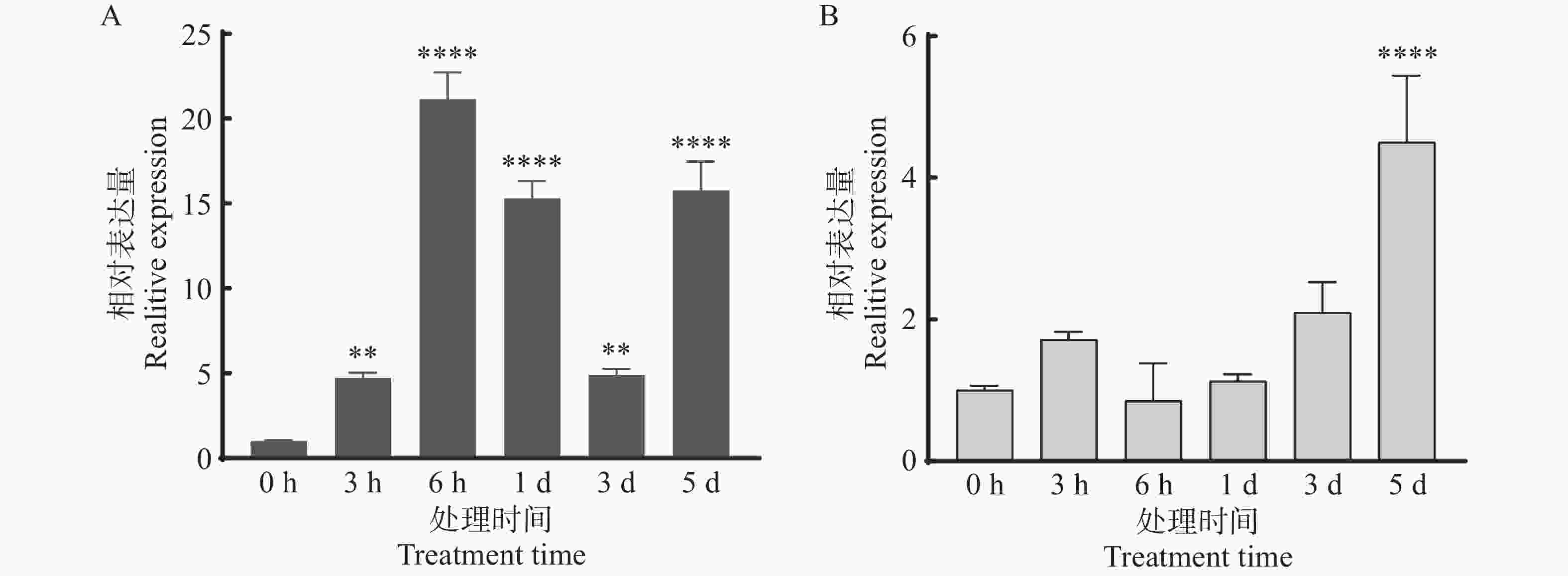
采用RT-qPCR技术分析了AsABCG1在茉莉酸甲酯和机械伤害处理下的表达模式,结果显示,AsABCG1基因对2种处理均表现出显著的应答反应。在茉莉酸甲酯处理下(图9-A),AsABCG1的表达在各时间点均明显上调,其中在处理6 h后表达量达到最高,为对照组的21.1倍。而在机械伤害处理中,基因表达量在处理5 d后才达到峰值,为对照组的4.5倍(图9-B)。上述结果表明,AsABCG1可能参与了茉莉酸信号通路和机械伤害应答的生理过程。
-
ABC转运蛋白参与植物体内多种次生代谢产物的运输,在促进次生代谢物积累中起着关键作用,现已成为植物次生代谢工程领域的研究热点之一[18]。本研究基于课题组的白木香转录组数据,克隆出一条编码ABC转运蛋白的基因AsABCG1。并对其理化性质、蛋白结构及基因表达量进行分析,旨在阐明ABC转运蛋白对白木香中次生代谢物的转运机制,为揭示沉香特征性成分积累机制和提高人工诱导沉香中特征性成分含量奠定基础。
近些年来,关于ABC转运蛋白对植物次生代谢产物转运功能的研究,已有了很大的进展。有研究表明,ABC转运蛋白能够参与萜类化合物的转运,例如,丹参中SmABCG1参与二萜类化合物丹参酮的转运[19];ElABCG39是续随子(Euphorbia lathyrism)大环二萜类化合物的关键转运蛋白[20];青蒿(Artemisia annua)AaPDR3具有转运半萜类化合物β−石竹烯的功能。此外,ABC转运蛋白也参与黄酮类化合物的转运,例如,拟南芥中AtABCC1、AtABCC2、AtABCC14参与花青素的转运[21];佛手(Citrus medica)中CmABCB19、CmABCC10参与蜜橘黄素、橙皮素、柚皮苷等黄酮类次生代谢物的转运[22]。倍半萜类和2−(2−苯乙基)色酮类化合物是沉香中的特征性成分和主要生物活性成分,其中2−(2−苯乙基)色酮类化合物与黄酮类化合物结构相似[23]。据此推测ABC转运蛋白在沉香倍半萜和2−(2−苯乙基)色酮类化合物的转运和积累过程中发挥重要的调控作用。蛋白结构预测结果表明,AsABCG1为跨膜蛋白,具有ABC转运蛋白的基本特征;在结香剂处理下,该基因表达与色酮类化合物积累正相关,表明AsABCG1可能参与沉香色酮类等次生代谢物的转运。
通常健康的白木香树不会产生沉香,只能在损伤后诱导才能形成[24]。研究表明,伤害处理和茉莉酸甲酯处理可诱导沉香中倍半萜和2−(2−苯乙基)色酮类化合物产生并促进次生代谢物形成[25−28]。本研究发现AsABCG1启动子存在多个茉莉酸和防御胁迫相关响应元件,进一步表达分析显示茉莉酸甲酯处理和伤害处理均可显著诱导AsABCG1基因的表达,说明AsABCG1参与了白木香伤害和茉莉酸信号转导,可能介导倍半萜和2−(2−苯乙基)色酮类化合物的转运。本研究不仅为沉香属植物研究提供了一个新的候选基因,也为深入揭示AsABCG1在沉香特征性成分转运与积累中的功能奠定了重要基础。后续将对该基因是否参与次生代谢物的转运等功能进行验证,并进一步解析其表达调控机制,以系统阐明ABC转运蛋白在沉香特征性成分转运过程中的功能及调控网络。相关研究结果有望为开发新型结香诱导技术、提升沉香特征性成分的积累水平提供理论依据和技术支撑。在此基础上可对该基因是否具有转运次生代谢物等功能进行验证,以期探究ABC转运蛋白对调控沉香特征性成分转运的分子机制并进一步揭示沉香特征性成分的转运和调控机制。
白木香AsABCG1基因的克隆与表达分析
DOI: 10.15886/j.cnki.rdswxb.20250126
 CSTR: 32425.14.j.cnki.rdswxb.20250126
CSTR: 32425.14.j.cnki.rdswxb.20250126
Cloning and expression analysis of AsABCG1 gene in Aquilaria sinensis
-
摘要: 沉香是一种传统的名贵药材与天然香料,因蕴藏丰富的次生代谢产物而极具价值。ABC转运蛋白是一类广泛分布于生物体的跨膜蛋白,在植物次生代谢产物的运输与积累中起着关键作用。为探究ABC转运蛋白在沉香次生代谢物转运过程中的功能,通过分析白木香(Aquilaria sinensis)转录组数据,鉴定出一个编码ABC转运蛋白的基因AsABCG1,该基因编码区全长为1 986 bp,编码一个由661个氨基酸组成的蛋白,AsABCG1具有典型的植物ABC转运蛋白结构特征,包含两个保守结构域MotifA和MotifB。AsABCG1启动子区含有茉莉酸、生长素、赤霉素、脱落酸等多种激素响应元件及厌氧诱导、机械损伤等胁迫响应元件。实时荧光定量PCR(RT-qPCR)分析表明,茉莉酸甲酯和机械伤害处理均能够显著诱导白木香茎干中AsABCG1的表达。本研究为后续阐明AsABCG1基因在白木香防御胁迫响应和次生代谢物积累中的功能奠定了基础。Abstract: Agarwood is a traditional precious medicinal material and a natural aromatic material, which is highly valuable due to its rich secondary metabolites. ABC transporters are a type of transmembrane proteins widely distributed in organisms and play a crucial role in the transport and accumulation of secondary metabolites in plants. To deeply explore the function of ABC transporters in the transport process of secondary metabolites in agarwood, a gene encoding an ABC transporter AsABCG1; was identified by analyzing the transcriptome data of Aquilaria sinensis. The coding sequence (CDS) length of this gene is 1986 bp, encoding a protein consisting of 661 amino acids. AsABCG1 has typical structural characteristics of plant ABC transporters, including two conserved domains, Motif A and Motif B. The promoter region of AsABCG1 contains various hormone response elements such as jasmonic acid, auxin, gibberellin, abscisic acid, as well as stress response elements such as anaerobic induction and mechanical injury. The real-time fluorescence quantitative PCR (RT-qPCR) analysis showed that methyl jasmonic acid and mechanical injury treatments could significantly induce the expression of AsABCG1 in the stems of A. sinensis. All these findings laid the foundation for further elucidating the function of the AsABCG1 gene in the defense response to stress and the accumulation of secondary metabolites in A. sinensis.
-
Key words:
- Aquilaria sinensis /
- ABC transporter protein /
- AsABCG1 /
- expression analysis /
- secondary metabolite
-
图 2 结香剂处理后AsABC基因的表达及色酮含量相关性分析
注:chromone1,2−[2−(3−甲氧基−4−羟基)苯乙基]色酮;chromone2,6−羟基−2−[2−(4−甲氧基)苯乙基]色酮;chromone3,6−羟基−2−2(苯乙基)色酮;chromone4,2−[2−(4−甲氧基)苯乙基]色酮;chromone5,2−(2−苯乙基)色酮;chromone6,6−羟基−2−[2−(3−甲氧基−4−羟基)苯乙基]色酮。
Fig. 2 Correlation analysis of AsABC gene expression and chromone content after treatment with agarwood inducer
Note: chromone1, 2−[2−(3−methoxyl−4−hydroxy)phenylethyl]chromone; chromone2, 6−hydroxy−2−[2−(4−methoxyl)phenylethyl]chromone; chromone3, 6−hydroxy−2−(2−phenylethyl)chromone; chromone4, 2−[2−(4−methoxyl)phenylethyl]chromone; chromone5, 2−(2−phenylethyl)chromone; chromone6, 6−hydroxy−2−[2−(3−methoxy−4−hydroxy)phenylethyl]chromone.
图 4 AsABCG1蛋白理化性质及结构分析
A. AsABCG1 亲水与疏水性;B. AsABCG1 信号肽;C. AsABCG1 跨膜结构;D. AsABCG1 磷酸化位点。
Fig. 4 Physicochemical properties and structural analysis of AsABCG1 protein
A. AsABCG1 hydrophilicity and hydrophobicity; B. AsABCG1 signal peptide; C. AsABCG1 transmembrane structure; D. AsABCG1 phosphorylation sites.
图 5 AsABCG1蛋白结构预测
注:蓝色,α−螺旋;紫色,延伸链;橙色,无规则卷曲;越接近蓝色表示该部分结构与已知植物相似度高,越接近橙色表示相似度越低。
Fig. 5 Prediction of the structure of the AsABCG1 protein
Note: blue, α-helix; purple, extended chain; orange, random coil; The closer to blue, the higher the similarity of this part of the structure to the reported plants; the closer to orange, the lower the similarity.
表 1 本实验中使用的引物
Table 1 The primers used in this experiment
引物名称 Primer 引物序列(5′—3′)
Sequence (5′—3′)AsABCG1-F GAACCTTGGGATTGAGAAGACGA AsABCG1-R GCAACTAGTTTGCCCATACTAAACCAGACTCT qAsABCG1-F ATGGGATGGACATAGAGGATTTG qAsABCG1-R GGAAGAATCCTCCCACCAATATC AsGADPH-F CTGGTATGGCATTCCGTGTA AsGADPH-R AACCACATCCTCTTCGGTGTA -
[1] 李慧婷, 王露露, 王雅丽, 等. 白木香6个不同种质所结沉香的GC-MS分析[J]. 热带作物学报, 2024, 45(8): 1727−1741. https://doi.org/10.3969/j.issn.1000-2561.2024.08.022 doi: 10.3969/j.issn.1000-2561.2024.08.022 [2] Zhou H, Li X Y, Fang H B, et al. Five new sesquiterpenoids from agarwood of Aquilaria sinensis [J]. Beilstein Journal of Organic Chemistry, 2023, 19: 998−1007. https://doi.org/10.3762/bjoc.19.75 doi: 10.3762/bjoc.19.75 [3] Zhang H, Ma J L, Chang C, et al. Gastroprotective 2-(2-phenylethyl) chromone-sesquiterpene hybrids from the resinous wood of Aquilaria sinensis (Lour.) Gilg [J]. Bioorganic Chemistry, 2023, 133: 106396. https://doi.org/10.1016/j.bioorg.2023.106396 doi: 10.1016/j.bioorg.2023.106396 [4] Xia L L, Li W, Wang H, et al. LC-MS guided identification of dimeric 2-(2-phenylethyl) chromones and sesquiterpene-2-(2-phenylethyl) chromone conjugates from agarwood of Aquilaria crassna and their cytotoxicity [J]. Fitoterapia, 2019, 138: 104349. https://doi.org/10.1016/j.fitote.2019.104349 doi: 10.1016/j.fitote.2019.104349 [5] Li C G, Pan L, Han Z Z, et al. Antioxidative 2-(2-phenylethyl) chromones in Chinese eaglewood from Aquilaria sinensis [J]. Journal of Asian Natural Products Research, 2020, 22(7): 639−646. https://doi.org/10.1080/10286020.2019.1607841 doi: 10.1080/10286020.2019.1607841 [6] Wei S Y, Hu D B, Xia M Y, et al. Sesquiterpenoids and 2-(2-phenylethyl) chromone derivatives from the resinous heartwood of Aquilaria sinensis [J]. Natural Products and Bioprospecting, 2021, 11(5): 545−555. https://doi.org/10.1007/s13659-021-00313-0 doi: 10.1007/s13659-021-00313-0 [7] Wang Z F, Cao H L. The complete mitochondrial genome sequence of Aquilaria sinensis [J]. Mitochondrial DNA Part B, 2021, 6(2): 381−383. https://doi.org/10.1080/23802359.2020.1869609 doi: 10.1080/23802359.2020.1869609 [8] Chen Y, Wu K L, Xu J R, et al. Development and application of SSR markers for Aquilaria sinensis on the basis of whole-genome resequencing data [J]. Plants, 2025, 14(9): 1323. https://doi.org/10.3390/plants14091323 doi: 10.3390/plants14091323 [9] 黄兴, 梅文莉, 王昊, 等. 白木香AsCYP131基因的克隆及表达分析[J]. 热带作物学报, 2025, 46(5): 1076−1083. https://doi.org/10.3969/j.issn.1000-2561.2025.05.006 doi: 10.3969/j.issn.1000-2561.2025.05.006 [10] Naziz P S, Das R, Sen S. The scent of stress: evidence from the unique fragrance of agarwood [J]. Frontiers in Plant Science, 2019, 10: 840. https://doi.org/10.3389/fpls.2019.00840 doi: 10.3389/fpls.2019.00840 [11] Alam A, Locher K P. Structure and mechanism of human ABC transporters [J]. Annual Review of Biophysics, 2023, 52: 275−300. https://doi.org/10.1146/annurev-biophys-111622-091232 doi: 10.1146/annurev-biophys-111622-091232 [12] Locher K P. Mechanistic diversity in ATP-binding cassette (ABC) transporters [J]. Nature Structural & Molecular Biology, 2016, 23(6): 487−493. https://doi.org/10.1038/nsmb.3216 doi: 10.1038/nsmb.3216 [13] Dhara A, Raichaudhuri A. ABCG transporter proteins with beneficial activity on plants [J]. Phytochemistry, 2021, 184: 112663. https://doi.org/10.1016/j.phytochem.2021.112663 doi: 10.1016/j.phytochem.2021.112663 [14] Lewinson O, Orelle C, Seeger M A. Structures of ABC transporters: handle with care [J]. FEBS Letters, 2020, 594(23): 3799−3814. https://doi.org/10.1002/1873-3468.13966 doi: 10.1002/1873-3468.13966 [15] Yan L, Zhang J H, Chen H Y, et al. Genome-wide analysis of ATP-binding cassette transporter provides insight to genes related to bioactive metabolite transportation in Salvia miltiorrhiza [J]. BMC Genomics, 2021, 22(1): 315. https://doi.org/10.1186/s12864-021-07623-0 doi: 10.1186/s12864-021-07623-0 [16] Ichino T, Yazaki K. Modes of secretion of plant lipophilic metabolites via ABCG transporter-dependent transport and vesicle-mediated trafficking [J]. Current Opinion in Plant Biology, 2022, 66: 102184. https://doi.org/10.1016/j.pbi.2022.102184 doi: 10.1016/j.pbi.2022.102184 [17] LI R S, ZHU J H, GUO D, et al. Genome-wide identification and expression analysis of terpene synthase gene family in Aquilaria sinensis [J]. Plant Physiology and Biochemistry, 2021, 164: 185−194. https://doi.org/10.1016/j.plaphy.2021.04.028 doi: 10.1016/j.plaphy.2021.04.028 [18] 梅文莉, 戴好富, 王辉, 等. 一种生产沉香的方法: 中国, 201310150138.5[P]. 2013-04-26. https://d.wanfangdata.com.cn/patent/Ch1QYXRlbnROZXdTb2xyOVMyMDI2MDEyNzE1NTEzORIpWkxfQ04yMDEzMTAxNTAxMzguNV9DTjEwMzIyOTY3N0JfMjAxNDA1MTQaCDgzbGlxemIy. [19] How S S, Nathan S, Lam S D, et al. ATP-binding cassette (ABC) transporters: structures and roles in bacterial pathogenesis [J]. Journal of Zhejiang University-SCIENCE B, 2025, 26(1): 58−75. https://doi.org/10.1631/jzus.B2300641 doi: 10.1631/jzus.B2300641 [20] Li Y J, Chen J F, Zhi J Y, et al. The ABC transporter SmABCG1 mediates tanshinones export from the peridermic cells of Salvia miltiorrhiza root [J]. Journal of Integrative Plant Biology, 2025, 67(1): 135−149. https://doi.org/10.1111/jipb.13806 doi: 10.1111/jipb.13806 [21] Lin G Y, Li P R, Li L W, et al. Discovery of ElABCG39: a key player in ingenol transmembrane efflux identified through genome-wide analysis of ABC transporters in Euphorbia lathyris L. [J]. Plant Cell Reports, 2024, 43(11): 274. https://doi.org/10.1007/s00299-024-03361-1 doi: 10.1007/s00299-024-03361-1 [22] Dean J V, Willis M, Shaban L. Transport of acylated anthocyanins by the Arabidopsis ATP-binding cassette transporters AtABCC1, AtABCC2, and AtABCC14 [J]. Physiologia Plantarum, 2022, 174(5): e13780. https://doi.org/10.1111/ppl.13780 doi: 10.1111/ppl.13780 [23] Zhang M, Zhao Y Y, Nan T G, et al. Genome-wide analysis of Citrus medica ABC transporters reveals the regulation of fruit development by CmABCB19 and CmABCC10 [J]. Plant Physiology and Biochemistry, 2024, 215: 109027. https://doi.org/10.1016/j.plaphy.2024.109027 doi: 10.1016/j.plaphy.2024.109027 [24] 王昊, 丁旭坡, 曾军, 等. 沉香种质资源、品质评价与形成机制研究进展[J]. 中国科学: 生命科学, 2024, 54(10): 1885−1906. https://doi.org/10.1360/SSV-2023-0291 doi: 10.1360/SSV-2023-0291 [25] Ding X P, Mei W L, Lin Q, et al. Genome sequence of the agarwood tree Aquilaria sinensis (Lour.) Spreng: the first chromosome-level draft genome in the Thymelaeceae family [J]. GigaScience, 2020, 9(3): giaa013. https://doi.org/10.1093/gigascience/giaa013 doi: 10.1093/gigascience/giaa013 [26] Xu J R, Du R Y, Wang Y, et al. Wound-induced temporal reprogramming of gene expression during agarwood formation in Aquilaria sinensis [J]. Plants, 2023, 12(16): 2901. https://doi.org/10.3390/plants12162901 doi: 10.3390/plants12162901 [27] 张鹏, 徐谙为, 杨光大, 等. 物理伤害诱导白木香应激反应的生理特征[J]. 热带作物学报, 2021, 42(12): 3521−3528. https://doi.org/10.3969/j.issn.1000-2561.2021.12.019 doi: 10.3969/j.issn.1000-2561.2021.12.019 [28] Xu Y H, Sun P W, Tang X L, et al. Genome-wide analysis of WRKY transcription factors in Aquilaria sinensis (Lour.) Gilg [J]. Scientific Reports, 2020, 10(1): 3018. https://doi.org/10.1038/s41598-020-59597-w doi: 10.1038/s41598-020-59597-w -




 下载:
下载: