-
大豆(Glycine max)含有丰富的蛋白质、油脂,是全球第一大油料作物,在国民经济中地位重要[1]。大豆是高营养的植物蛋白原料。在日常生活生产中容易获得,不仅可以加工为食用油,也可以供养殖业作为饲料使用,是中国重要的粮食、油料和饲料作物。中国大豆产业供需落差大,依赖国外进口。根源在于国内大豆的单产相对不足。航天诱变开辟了一条高速、高效、自主创新的路径,来培育能够应对当前挑战的新品种,从根本上保障国家大豆供给和产业安全。本研究以4个品种大豆航天诱变一代(SP1)种子为材料,系统研究叶片光合色素以及叶片显微结构的变异规律,通过初步评估本次太空诱变的效果,为后续世代筛选出可遗传的优良变异指明方向、奠定基础,作为后续重点观察对象,并为选育速生抗逆大豆新种质提供理论支撑。
航天育种也被称为太空诱变育种[2],是选育新品种的新育种途径[3]。该技术能够产生自然界较难获得的新性状和基因[4]。航天诱变突变广,频率高。航天诱变育种较常规途径可以显著缩短育种时间,并能产生一些特殊的变异类型。在许多育种领域中得到了应用,并取得不错的成果。大豆航天育种虽开展较晚,但也积累了可以借鉴的经验。刘鑫磊等[5]发现空间诱变可使大豆光合性状产生丰富变异;吕爽等[6]研究发现2个株系经航天诱变与射线复合处理,大多表形性状均产生变异;张勇等[7]通过搭载F2种子选育出大豆新品种‘克山1号’。航天诱变对创造新变异有独特作用[6,9]。中国大豆航天育种与其他作物相比起步较晚[7]。于上个世纪九十年代初首先开展。仅获得不多的有价值突变体,并没有经正式审定推广的新品种。后续又进行了多次大豆航天搭载研究,以“神舟4号”和“实践八号”卫星进行的两次搭载最具代表性。且育成了一批有特色的突变体,并经过国家或省级审定。航天诱变不仅直接培育出了众多优良品种,更重要的是它提供了一个巨大的“突变体库”。本研究测定航天诱变后大豆的光合色素和叶片显微结构,探究航天诱变对大豆生长及生理特性的影响,旨在为大豆种质创新与新品种选育提供基础的种质材料与数据支撑,同时也为航天诱变育种技术在大豆遗传改良领域的推广应用提供科学参考。
-
供试验使用的大豆品种有4种,分别为‘德顺34’、‘德顺14’、‘东创19’、‘东农219’。‘德顺34’蛋白质含量41.58%,脂肪含量20.04%,平均产量
3326.5 kg·km−2。‘德顺14’蛋白质含量39.86%,脂肪含量19.9%,平均产量3 075.0 kg·km−2。‘东创19’蛋白质含量41.14%,脂肪含量21.09%,平均产量2 821.4 kg·km-2,‘东农219’蛋白质含量39.07%,脂肪含量20.74%,平均产量3299.9 kg·km−2。以上品种均为经审定、亚有限结荚习性、生育期为110 d左右的优良品种,由黑龙江省讷河市德顺种业有限责任公司提供。 -
将4个品种大豆种子随机分成两组:试验组与对照组,每个组分3个小区,每个小区为200粒种子。试验组的大豆种子于2024-09-27日搭载“实践十九号”卫星,运行14 d后,2024-10-11日返回地面。随后将搭载处理的种子置于4 °C冰箱保存,保持种子的干燥。将每组种子于2024-11-29日播种于海南大学儋州校区农科基地中,试验地土壤为红壤,中等肥力。生理生化试验在海南大学儋州校区橡胶研究所,于2024年11月至2025年7月进行。
-
每组大豆材料选择5株,分别取上部第一完全展开叶中部相同部位的叶片等量混合,采样时间为10:00。测定方法为80%丙酮研磨法(Arnon法)。将新鲜叶片剪碎混匀,称取0.1 g置于研钵中,用80%丙酮研磨至匀浆状,用80%丙酮定容至10 mL后离心,取上清液。用紫外可见分光光度计测定OD663、OD645、OD440 值,以80%丙酮作为空白对照。各指标均测定3次重复,各指标计算公式:
$$ \mathit{C} _{ \mathrm{叶绿素a}} \mathrm{=9.87} \mathit{OD} _{ \mathrm{663}} \mathrm{-0.99} \mathit{OD} _{ \mathrm{645}} \mathrm{,} $$ $$ \mathit{C} _{ \mathrm{叶绿素b}} \mathrm{=21.43} \mathit{OD} _{ \mathrm{645}} \mathrm{-4.65} \mathit{OD} _{ \mathrm{663}} \mathrm{,} $$ $$ \mathit{C} _{ \mathrm{总叶绿素}} \mathrm{=5.13} \mathit{OD} _{ \mathrm{663}} \mathrm{+20.44} \mathit{OD} _{ \mathrm{645}} \mathrm{,} $$ $$ \mathit{C} _{ \mathrm{类胡萝卜素}} \mathrm{=4.7} \mathit{OD} _{ \mathrm{440}} \mathrm{-0.27} \mathit{C} _{ \mathrm{总叶绿素}} \mathrm{,} $$ $$ \mathit{A} \mathrm= \mathit{C} \mathrm{\times } \mathit{V} \mathrm{/(} \mathit{W} \mathrm{\times 1000)。} $$ 式中:A为色素含量(mg·g−1);C为色素质量浓度(mg · L−1);V为提取液体积(mL);W为叶片鲜质量(g)
-
将2025年5月采集品种航天诱变和对照组生长状况良好的成熟叶片,沿中脉切取4 mm×4 mm的小块,固定于FAA(V50%乙醇:V冰醋酸:V甲醛=90:5:5)。24 h后各品种航天诱变和对照各取3片,经乙醇逐级脱水、二甲苯透明、浸蜡、石蜡包埋和切片。切片脱蜡复水后,经番红-固绿染色,用中性树胶封片。在光学显微镜下观察、拍照。测定叶片各显微结构参数。
-
试验数据采用Excel 2021与SPSS 26.0软件进行统计分析。
-
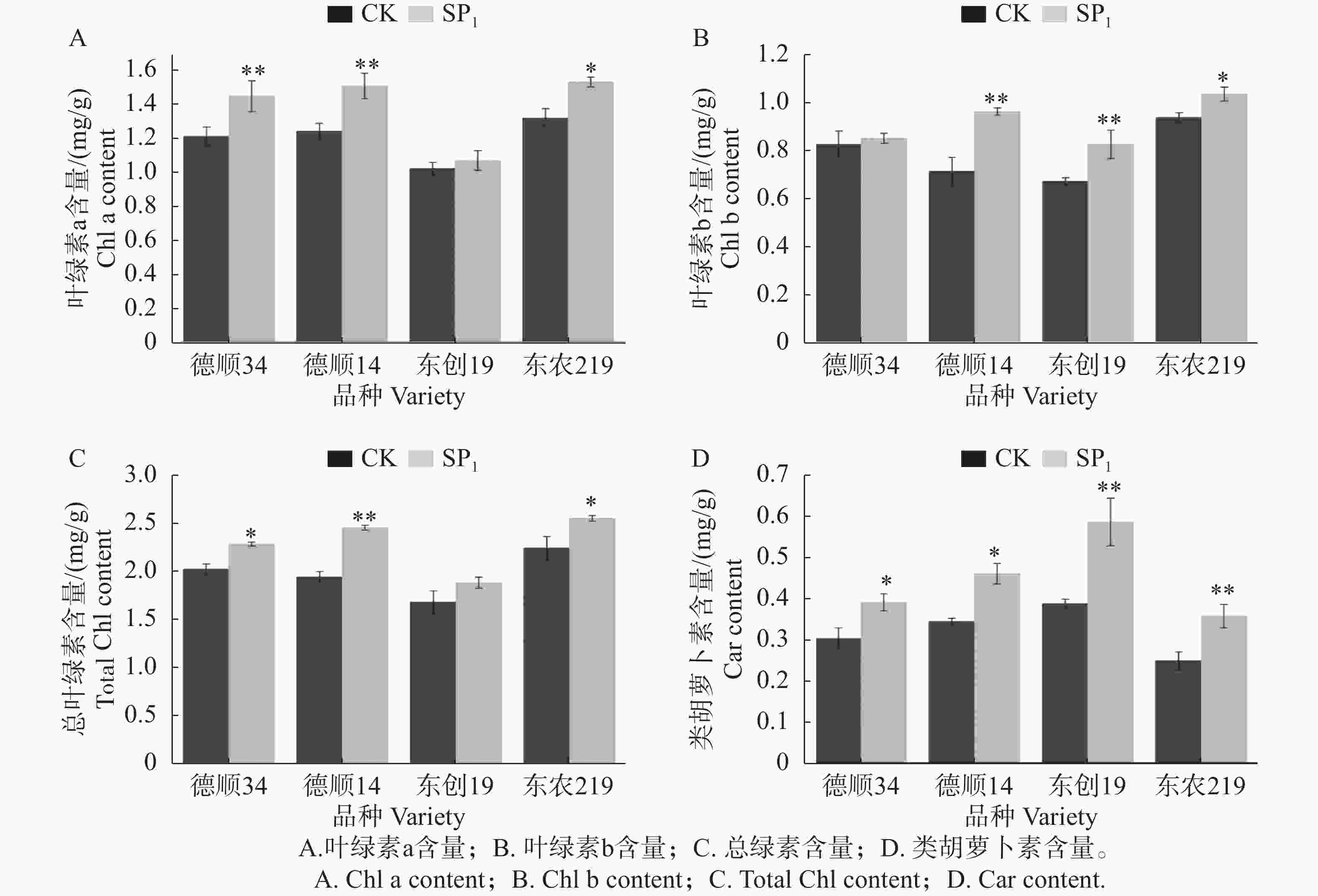
航天诱变后,‘德顺34’、‘德顺14’大豆叶片叶绿素a含量极显著高于对照,分别提高了 19.58%、21.49%,‘东农219’与对照相比有增加16.07%,差异达到显著水平,‘东创19’较对照略有上升,但差异未达显著水平。航天诱变提高了‘德顺14’、‘东创19’、‘东农219’叶绿素 b 含量,其中‘德顺14’、‘东创19’极显著高于对照,分别提高34.92%、22.92%,‘东农219’显著高于对照10.52%,‘德顺34’较对照略有提升,但差异不显著。航天诱变后,‘德顺34’、‘德顺14’、‘东农219’总叶绿素含量显著或极显著高于对照,分别比对照高12.91%、26.38%、13.77%,而‘东创19’总叶绿素含量无明显变化。与对照相比,航天诱变后,‘德顺34’、‘德顺14’、‘东创19’、‘东农219’类胡萝卜素含量显著提高,分别比对照高了28.93%、33.73%、51.40%、43.71%。其中,航天诱变后的‘德顺34’、‘德顺14’类胡萝卜素含量显著高于对照,‘东创19’、‘东农219’类胡萝卜素含量极显著高于对照。
-
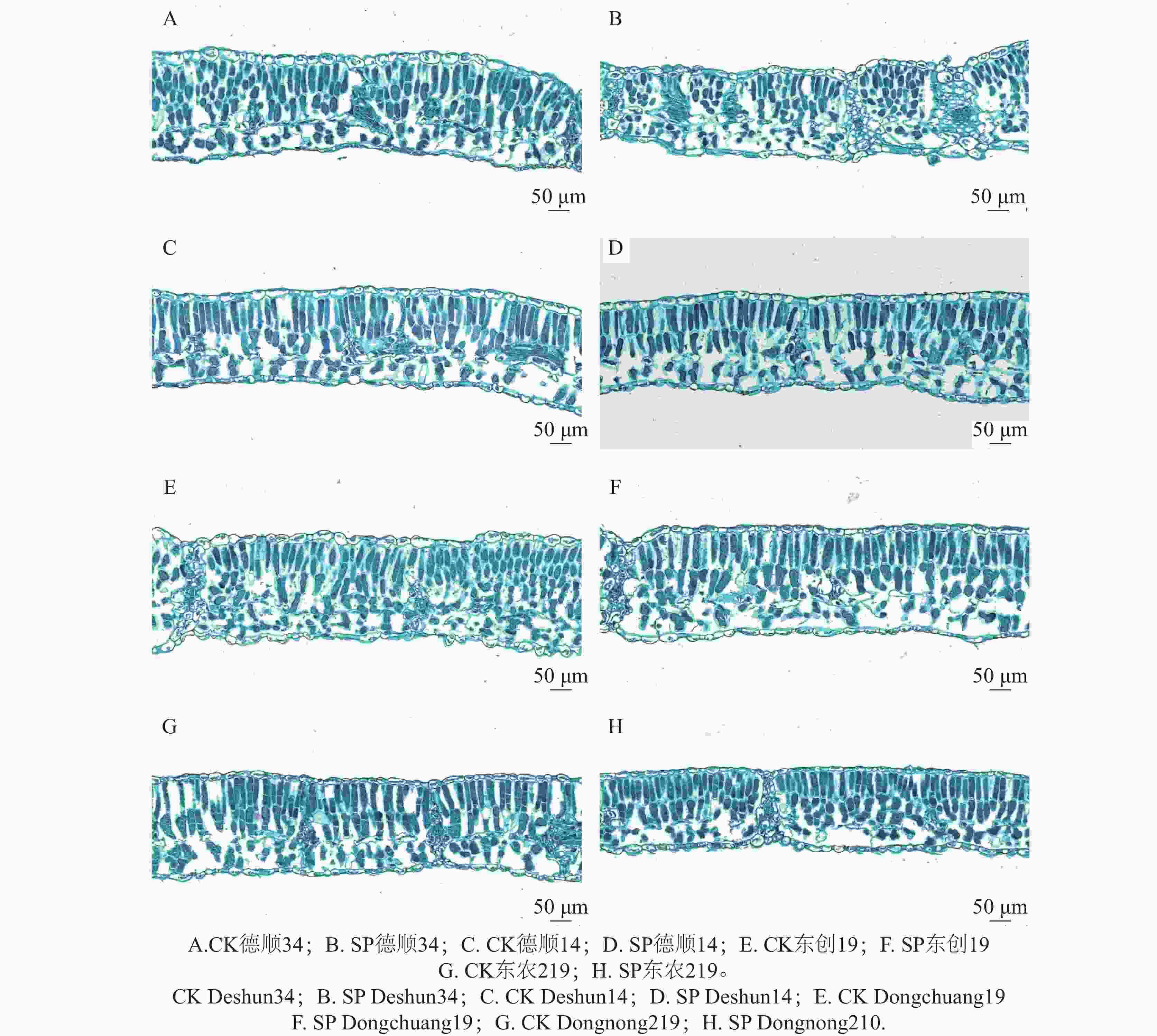
如图2可见,经过航天诱变后各品种大豆叶片细胞形态、排列方式较对照明显变化。‘德顺34’叶片的栅栏组织和海绵组织分界明显,细胞排列相对整齐,形态饱满,结构清晰。栅栏组织细胞呈近圆柱形,层数较为稳定,海绵组织细胞虽排列不规则但间隙发达。航天诱变后‘德顺34’叶片各部分细胞出现皱缩,结构模糊,栅栏组织和海绵组织的分界不明显,细胞排列混乱且分散。整体形态皱缩,细胞饱满度下降,与对照相比,细胞形态和排列方式发生了显著变化。‘德顺14’栅栏组织由4~5层短圆柱形细胞组成,细胞间隙较大,排列较规则。整体清晰,分界明确。经航天诱变后栅栏组织由2~3层圆柱状细胞组成,排列较整齐且间隙较小,细胞饱满,海绵组织细胞呈近椭圆形。‘东创19’细胞较大且排列较疏松;海绵组织排列不规则、形状不一,间隙发达;栅栏组织和海绵组织分界明显。经航天诱变后栅栏组织细胞结构清晰,呈长圆柱形,排列有序,间隙发达;海绵组织细胞形状多样,分布混乱。‘东农219’叶片上下表皮细胞呈近椭圆形,且饱满;栅栏组织和海绵组织均为近圆柱形细胞,排列整齐,间隙较小。经过航天诱变后叶片细胞皱缩,形态模糊,排列混乱且分散。
-
航天诱变改变了大豆叶片各显微结构参数。经过航天诱变后‘德顺14’叶片厚度极显著高于对照,比对照高了9.25%,而‘东农219’叶片厚度极显著低于对照13.99%,‘德顺34’叶片厚度显著低于对照4.70%,‘东创19’较对照无明显差异。航天诱变后‘东农219’叶片上表皮厚度极显著低于对照。而经过航天诱变的‘德顺34’上表皮厚度极显著高于对照,比对照高了23.89%,‘德顺14’上表皮厚度显著高于对照11.85%,‘东创19’较对照无明显差异。‘德顺34’经过航天诱变后叶片下表皮厚度极显著高于对照35.48%,而‘德顺14’、‘东农219’则显著低于对照,分别比对照13.24%、12.03%,‘东创19’较对照极显著降低20.45%。与对照相比,航天诱变极显著降低了‘德顺34’、‘东农219’叶片栅栏组织厚度,较对照分别极显著降低14.19%、7.57%。而‘德顺14’、‘东创19’叶片栅栏组织厚度较对照无明显差异。航天诱变后‘德顺34’、‘东创19’、‘东农219’叶片海绵组织厚度变薄,其中‘东农219’低于对照21.06%,且达到极显著水平,‘德顺14’海绵组织厚度较对照极显著提升30.95%。
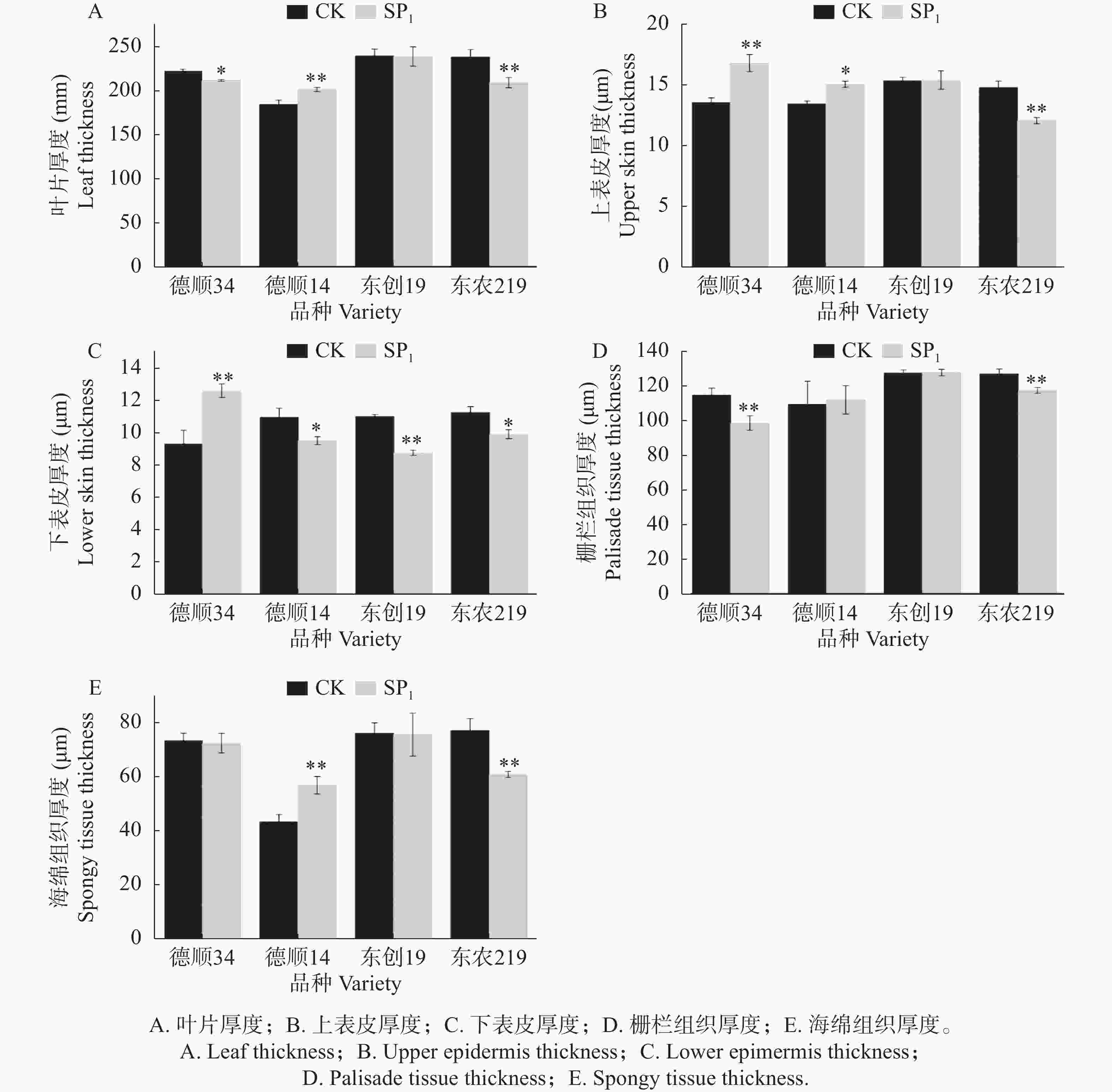
图 3 航天诱变对大豆叶片显微结构参数的影响
Figure 3. Effects of space mutagenesis on microstructural parameters of soybean leaves
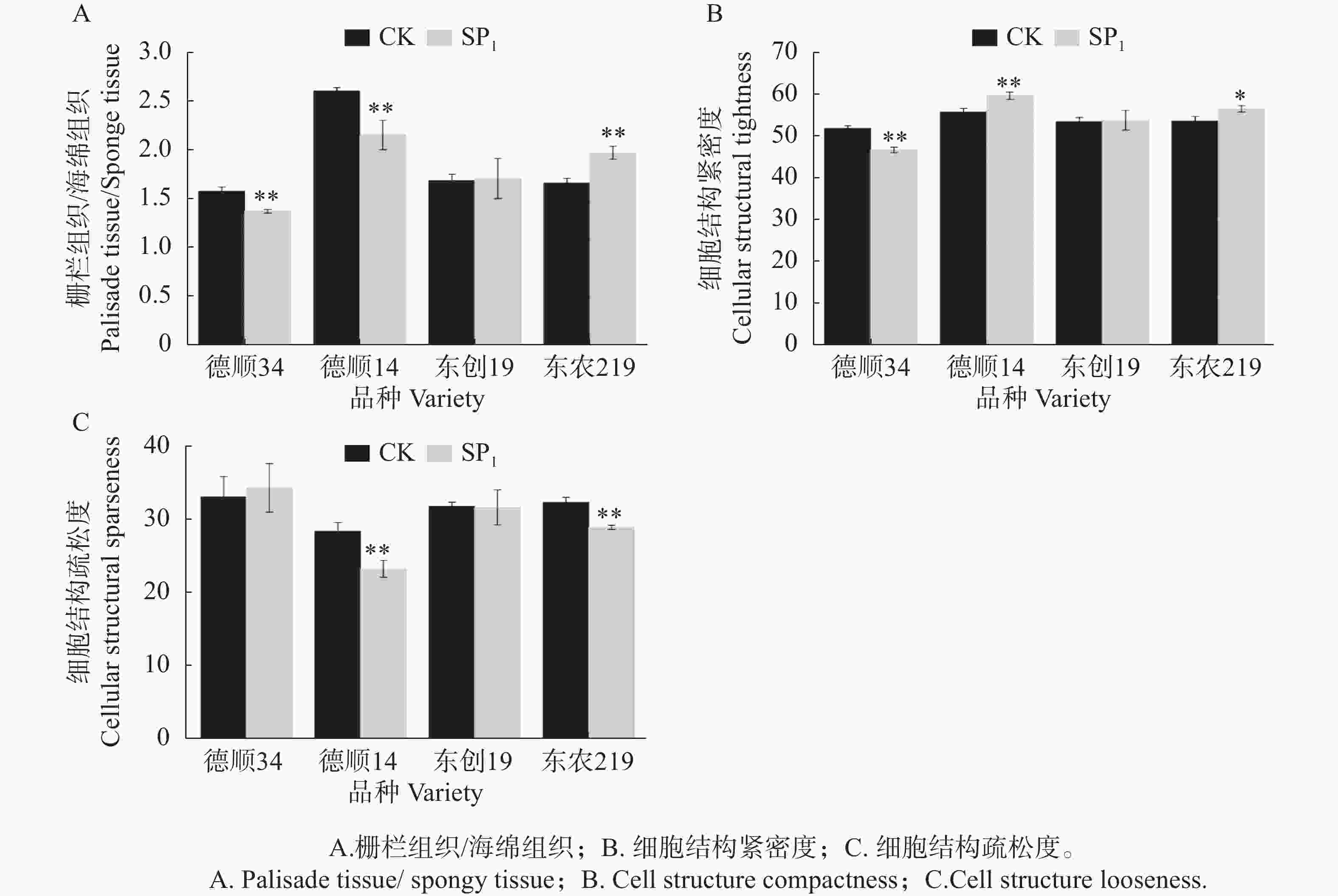
航天诱变后‘东农219’栅栏组织厚度/海绵组织厚度极显著高于对照,提高了18.52%,而‘德顺34’、‘德顺14’栅栏组织厚度/海绵组织厚度与对照相比极显著降低13.02%、17.31%,‘东创19’较对照无明显差异。与对照相比,航天诱变后各品种叶片细胞结构紧密度发生不同程度的变化,其中,‘德顺14’、‘东农219’分别比对照显著或极显著增加了6.55%、5.45%,而‘德顺34’较对照极显著降低9.96%,‘东创19’与对照相比差异不显著。航天诱变后,‘德顺14’、‘东农219’叶片细胞结构疏松度低于对照,分别比对照降低了18.17%、10.64%,差异达到极显著水平,‘东创19’较对照降低,未达显著水平。而‘德顺34’经航天诱变后叶片细胞结构疏松度增加,差异未达显著水平。
-
叶绿体其结构的完整性对色素含量的变化非常重要[10−11]。叶绿体对环境极敏感,导致光合色素合成也容易受到影响[12]。空间环境可能会改变植株叶绿体结构使光合色素含量降低[13]。本研究中航天诱变促进了大豆叶片色素的合成,为获得长势强壮和高产的植株奠定基础。
植物主要通过叶片感知外部环境,其结构特征反映植物的适应能力[14−15]。叶片对环境变化非常敏感[16]。所处环境的改变会引发叶片显微结构的变化[17]。冯鹏等[18]研究表明,航天诱变后紫花苜蓿叶片参数与对照相比均有增加。本研究中,经航天诱变后‘德顺14’叶片海绵组织厚度高于对照,而‘东农219’叶片海绵组织厚度低于对照,‘德顺34’、‘东农219’叶片栅栏组织厚度低于对照,可能是由于航天诱变对不同品种的诱变效果不同。植物抗逆性与叶片显微结构参数密切相关[19−20]。经过航天诱变的‘德顺34’、‘东农219’大豆叶片厚度显著降低,但‘德顺14’叶片厚度极显著增加,即有更强的贮水能力。细胞结构紧密度作为抗寒指标,通常用栅栏组织厚度与叶片厚度的比值表示[21−23],前人认为细胞结构紧密度与抗寒性呈正相关。本研究中,航天诱变后‘德顺14’、‘东农219’大豆叶片组织结构紧密度均有所提高,说明特殊的空间环境有利于增强植株抵御逆境的能力和抗寒性的提高,为选育抗逆性植株奠定了基础。
综上所述,航天诱变后‘德顺34’、‘德顺14’、‘东农219’总叶绿素含量显著高于对照12.91%~26.38%。航天诱变后,各品种类胡萝卜素含量显著高于对照 28.93%~51.40%。航天诱变后‘德顺34’叶片细胞皱缩、结构模糊,栅栏组织细胞和海绵组织细胞分布混乱,而‘德顺14’叶片细胞饱满,细胞排列整齐,胞间隙较小。航天诱变后,‘德顺14’大豆叶片厚度、海绵组织厚度、细胞结构紧密度极显著高于对照、‘东农219’栅栏组织厚度/海绵组织厚度极显著高于对照,增加量达18.52%,而‘德顺14’、‘东农219’细胞结构疏松度却低于对照,比对照降低了 10.64%~18.17%,‘德顺14’、‘东农219’的正向变异较为明显,可考虑作为后续重点研究对象。为后续选育新品种提供种质材料和理论依据。由于第一代性状稳定性差,需要在后世代大量定向选育,针对提高光合指标,抗逆性提高等以上这些方向切入,选育出大豆优良新品种。
Effects of space mutation on photosynthetic pigments and microstructure of Glycine max Leaves
-
摘要: 为探讨航天诱变对不同品种大豆叶片光合色素及叶片显微结构的影响,本研究以“实践十九号”卫星搭载的4种优良大豆种子为研究对象。经航天诱变处理后返回地面进行SP1代地面种植,未经搭载的大豆种子为CK,对其光合色素以及叶片显微结构参数进行了测定和分析,结果表明:航天诱变后‘德顺34’、‘德顺14’、‘东农219’叶片总叶绿素含量显著高于对照12.91%~26.38%,而‘东创19’较对照未达显著水平。航天诱变后各品种类胡萝卜素含量显著高于对照 28.93%~51.40%。航天诱变后大豆各品种叶片细胞发生明显变化,航天诱变后‘德顺14’叶片细胞饱满,细胞排列整齐,胞间隙较小,叶片厚度、海绵组织厚度、细胞结构紧密度极显著高于对照、‘东农219’栅栏组织厚度/海绵组织厚度极显著高于对照,增加量达18.52%。‘德顺14’、‘东农219’细胞结构疏松度低于对照,比对照降低了10.64%~18.17%。本研究为大豆种质改良和品种选育提供基础材料,为大豆航天诱变育种的深化及该技术在豆科作物遗传改良中的应用提供了基础与参考。Abstract: Seeds of four superior soybean varieties carried by the "Shijian-19" satellite were selected for experiment to explore the effects of space mutation on the photosynthetic pigments and microscopic structure of leaves in different soybean varieties. After space mutation treatment, the plants of SP1 generation of these four soybean varieties were planted on the ground. The soybean seeds that were not carried by the satellete were used as the control (CK). The photosynthetic pigments and microscopic structure parameters of the leaves of the soybean plants under space mutation treatment and the control were measured and analyzed. The results showed that the soybean varieties Deshun 34, Deshun 14, and Dongnong 219 under space mutation were 12.91% to 26.38% higher, significantly higher in total chlorophyll content than the control. After space mutation, the carotenoid content of each variety was 28.93% to 51.40% higher, significantly higher than that of the control. After space mutation, the cell morphology, arrangement, and thickness of the leaves of each soybean variety changed significantly. The leaf cells of Deshun 14 were plump, arranged neatly, and had small intercellular spaces. After space mutation, the leaf thickness, spongy tissue thickness, and cell structure compactness of Deshun 14 soybeans were highly significantly higher than those of the control, and the palisade tissue thickness/spongy tissue thickness of Dongnong 219 was highly significantly higher than that of the control, with an increase of 18.52%. However, the cell structure looseness of Deshun 14 and Dongnong 219 was lower than that of the control, decreasing by 10.64% to 18.17%. This experiment provides basic materials for soybean germplasm improvement and variety selection, and offers a foundation and reference for further soybean space mutation breeding and the application of space mutagenesis in the genetic improvement of leguminous crops.
-
Key words:
- Glycine max /
- space mutagenesis /
- photosynthetic pigment /
- leaf microstructure
-
-
[1] 郑伟, 郭泰, 王志新, 等. 大豆航天育种研究进展[J]. 辐射研究与辐射工艺学报, 2015, 33(5): 1−9. https://doi.org/10.11889/j.1000-3436.2015.rrj.33.050101 doi: 10.11889/j.1000-3436.2015.rrj.33.050101 [2] 周世奇, 罗琳, 程立锐, 等. 烟草航天诱变突变体叶形遗传分析及基因定位[J]. 分子植物育种, 2021, 19(2): 584−590. https://doi.org/10.13271/j.mpb.019.000584 doi: 10.13271/j.mpb.019.000584 [3] 胡冰, 陈朝黎, 陈天笑, 等. 航天诱变对四种木本花卉容器苗生长与生理特性的影响[J]. 核农学报, 2023, 37(11): 2107−2116. https://doi.org/10.11869/j.issn.1000-8551.2023.11.2107 doi: 10.11869/j.issn.1000-8551.2023.11.2107 [4] 刘郎红, 赵云昊, 姜明亮. 航天诱变育种在园艺作物中的应用进展[J]. 2024(14): 135−141. https://doi.org/10.11937/bfyy.20240216 [5] 刘鑫磊, 马岩松, 栾晓燕, 等. 航天诱变对大豆品种光合性状的影响[J]. 大豆科学, 2011, 30(4): 606−608. [6] 吕爽, 郑伟, 郭泰, 等. 大豆航天搭载与60Co-γ辐射复合诱变效果分析[J]. 中国种业, 2012(2): 34−36. https://doi.org/10.3969/j.issn.1671-895X.2012.02.017 doi: 10.3969/j.issn.1671-895X.2012.02.017 [7] 张勇, 杨兴勇, 董全中, 等. 利用空间诱变技术选育大豆新品种克山1号[J]. 核农学报, 2013, 27(9): 1241−1246. https://doi.org/10.11869/hnxb.2013.09.1241 doi: 10.11869/hnxb.2013.09.1241 [8] 赵曦, 王广金, 李铁, 等. 大豆空间诱变突变体的RAPD分析[J]. 核农学报, 2014, 28(5): 772−776. https://doi.org/10.11869/j.issn.100-8551.2014.05.0772 doi: 10.11869/j.issn.100-8551.2014.05.0772 [9] 李卫东, 崔清宇, 马长华, 等. 我国中草药航天育种研究进展与展望[J]. 中国现代中药, 2020, 22(3): 447−451. https://doi.org/10.13313/j.issn.1673-4890.20190208001 doi: 10.13313/j.issn.1673-4890.20190208001 [10] 刘建福, 陈育才, 王文建, 等. 航天搭载对武夷名丛相关生理及生长特性的影响[J]. 植物学报, 2020, 55(5): 564−572. https://doi.org/10.11983/CBB20035 doi: 10.11983/CBB20035 [11] Szymańska R, Ślesak I, Orzechowska A, et al. Physiological and biochemical responses to high light and temperature stress in plants [J]. Environmental and Experimental Botany, 2017, 139: 165−177. https://doi.org/10.1016/j.envexpbot.2017.05.002 doi: 10.1016/j.envexpbot.2017.05.002 [12] 杨玉皎, 郭淑萍, 杨顺林, 等. 增强UV-B辐射对杧果叶片光合生理和超显微结构的影响[J]. 果树学报, 2021, 38(9): 1524−1539. https://doi.org/10.13925/j.cnki.gsxb.20200465 doi: 10.13925/j.cnki.gsxb.20200465 [13] 路超, 袁存权, 李云, 等. 3种木本植物种子航天诱变研究初报[J]. 核农学报, 2010, 24(6): 1152−1157. https://doi.org/10.11869/hnxb.2010.06.1152 doi: 10.11869/hnxb.2010.06.1152 [14] Hu Y, Yang L, Gao C, et al. A comparative study on the leaf anatomical structure of Camellia oleifera in a low-hot valley area in Guizhou Province, China [J]. PLoS One, 2022, 17(1): e0262509. https://doi.org/10.1371/journal.pone.0262509 doi: 10.1371/journal.pone.0262509 [15] Xia P G, Li Q Q, Liang Z S, et al. Spaceflight breeding could improve the volatile constituents of Andrographis paniculata [J]. Industrial Crops and Products, 2021, 171: 113967. https://doi.org/10.1016/j.indcrop.2021.113967 doi: 10.1016/j.indcrop.2021.113967 [16] 孙大元, 张景欣, 陈冠州, 等. 空间诱变选育抗稻瘟病水稻品种研究进展与展望[J]. 核农学报, 2017, 31(2): 271−279. https://doi.org/10.11869/j.issn.100-8551.2017.02.0271 doi: 10.11869/j.issn.100-8551.2017.02.0271 [17] 田晨霞, 张咏梅, 王凯, 等. 紫花苜蓿组织解剖结构对NaHCO3盐碱胁迫的响应[J]. 草业学报, 2014, 23(5): 133−142. https://doi.org/10.11686/cyxb20140515 doi: 10.11686/cyxb20140515 [18] 冯鹏. 紫花苜蓿种子含水量对卫星搭载诱变效应的影响[D]. 兰州: 甘肃农业大学, 2008. [19] 杨伟, 刘勇, 王良群, 等. 航天诱变处理对高粱产量以及品质的影响[J]. 农学学报, 2015, 5(8): 19−22. [20] 冯鹏, 孙力, 申晓慧, 等. 不同诱变处理对苜蓿叶片细胞显微和超微结构的影响[J]. 草业学报, 2018, 27(6): 72−80. https://doi.org/10.11686/cyxb2017285 doi: 10.11686/cyxb2017285 [21] 农玉琴, 陈远权, 李金婷, 等. 广西茶树品系叶片解剖结构特征与特性关系的研究[J]. 中国热带农业, 2020(5): 58−61. https://doi.org/10.3969/j.issn.1673-0658.2020.05.014 doi: 10.3969/j.issn.1673-0658.2020.05.014 [22] Suarez N. Comparative leaf anatomy and pressure-volume analysis in plants of Ipomoea pes-caprae experimenting saline and/or drought stress [J]. International Journal of Botany, 2011, 7(1): 53−62. https://doi.org/10.3923/ijb.2011.53.62 doi: 10.3923/ijb.2011.53.62 [23] 房用, 孟振农, 李秀芬, 等. 山东茶树叶片解剖结构分析[J]. 茶叶科学, 2004, 24(3): 190−196. https://doi.org/10.3969/j.issn.1000-369X.2004.03.008 doi: 10.3969/j.issn.1000-369X.2004.03.008 -

 点击查看大图
点击查看大图
计量
- 文章访问数: 95
- HTML全文浏览量: 84
- 被引次数: 0



 下载:
下载: