-
联合国政府间气候变化专门委员会(Intergovernmental Panel on Climate Change,IPCC)第6次报告指出,人类活动对大气环流的影响导致干旱、暴雨和旱涝交替等极端气候事件的发生频率增加,对自然生态系统产生了严重影响[1]。例如,在全球气候变暖背景下,频繁发生的高强度降水和洪涝灾害成为制约植物正常生长发育的主要水分胁迫因子[2]。同时,极端高温干旱致使全球多地湖泊和河流水位持续下降[3],进而威胁植物生长。此外,高强度降水和极端干旱的频发容易导致干湿交替现象出现,这些降水格局的变化将会影响土壤理化性质和微生物活性等,从而影响土壤有机碳的固存和植物生长[4]。鉴于植物在维持生态系统平衡和保障人类健康中的重要作用,探究极端气候胁迫对植物生长及土壤环境的影响十分必要。樟树(Cinnamomum camphora)因其生长速率快且病虫害少等特点,是热带和亚热带地区的一种重要绿化造林树种[5]。在生态功能上,樟树可以抑制粉尘、稳固土壤、防止风蚀及美化环境,具有较高的生态经济价值[6]。但樟树对环境的变化较为敏感,例如,在干旱胁迫下,香樟幼苗的水分生理机能衰退,光合能力以及对二氧化碳(CO2)的利用能力明显下降,从而抑制了体内有机物质的积累,进而影响樟树的生长[7]。然而,樟树对不同类型的胁迫表现出不同的响应策略,并与胁迫条件下的土壤养分含量密切相关。干旱通常促进根系在土壤中延伸,因为干旱胁迫会降低土壤碳含量、碳氮比和微生物生物量碳等土壤养分含量[8],使植物需要更长的根系来获取养分,而过湿的环境则可能有利于叶片生长[9]。此外,干湿交替条件下,土壤氮素矿化可能增加、减少或无显著变化[10],土壤有机质分解也可能增加或无显著变化[11]。面对不同的水分胁迫时,樟树展示出不同的生长反应。例如,干湿交替下樟树叶片营养物质也可能没有显著变化[9]。因此,以樟树为研究对象,探究极端水分胁迫对其生长和生长环境的影响具有重要的科学意义[12]。
植物与土壤微生物互利共生,在极端气候条件下,水分胁迫会通过直接影响植物的生理生态功能,进而间接影响根际微生物对养分的吸收和利用[13]。土壤微生物群落结构与功能的变化反过来影响土壤养分循环和植物生长[14]。例如,干旱胁迫通过改变植物–土壤反馈机制来影响土壤微生物功能和植物生长[15],同时减少了土壤中养分的有效迁移,从而减少了植物对养分的吸收[16]。此外,根际微生物能够协助宿主植物抵御干旱胁迫。例如,细菌能分泌更多的植物生长调节物质以增强宿主植物的耐旱性能,而真菌可将菌丝体延伸到植物根系外围,以获取额外的养分和水分,促进植物在水分匮乏条件下维持正常的代谢与生长活动[17]。与细菌相比,真菌由于独特的生理结构,对水分胁迫的耐受性更强[18]。研究表明,在长期干旱条件下,细菌群落的多样性和生物量显著下降,而真菌群落则相对稳定[19]。干旱胁迫后的复水过程会引起土壤水势的快速变化,导致微生物群落结构和生物量发生显著变化[20]。而在干湿交替条件下,细菌群落的活性增强,真菌群落则受到抑制[21]。此外,也有研究发现复水过程会导致总微生物活性数量增加[22]。同时,剧烈的水分渗透变化会诱导微生物细胞裂解,增强土壤的矿化作用,进而影响植物的生长[23]。
以往的研究主要集中在水分胁迫对樟树生理生态和光合特性的影响。然而,对水淹、干旱和干湿交替胁迫下土壤特性的变化,尤其是土壤微生物群落的响应特征研究相对缺乏。磷脂脂肪酸(phospholipid fatty acid,PLFA)作为微生物活细胞的一种标志物,随微生物细胞的死亡迅速分解,可有效反映土壤中活体微生物的状态,并能提供有关微生物群落结构与组成的信息[24]。在极端水分胁迫条件下,樟树幼苗的土壤微生物生物量变化,以及这些变化对樟树幼苗生长及土壤理化性质的影响有待进一步探究。本研究通过对不同胁迫环境下樟树土壤微生物磷脂脂肪酸含量的分析,揭示各类水分胁迫处理对樟树土壤微生物生物量的影响,从而为在全球极端气候变化背景下樟树的栽培管理与种植策略的制定提供科学依据。
-
本实验在南昌工程学院的遮雨棚下进行,所用土壤取自附近种植园的表层土壤,风干后混合均匀装于底部带孔的花盆中。2017年5月初,选取80株长势均匀的一年生樟树幼苗预培养,每盆种植1株幼苗。实验开始前将所有土壤预先浇灌至田间持水量水平。为保证实验期间幼苗维持正常生长,每周每盆施200 mL可溶性营养肥(施可得园艺肥料有限公司,中国武汉)。
-
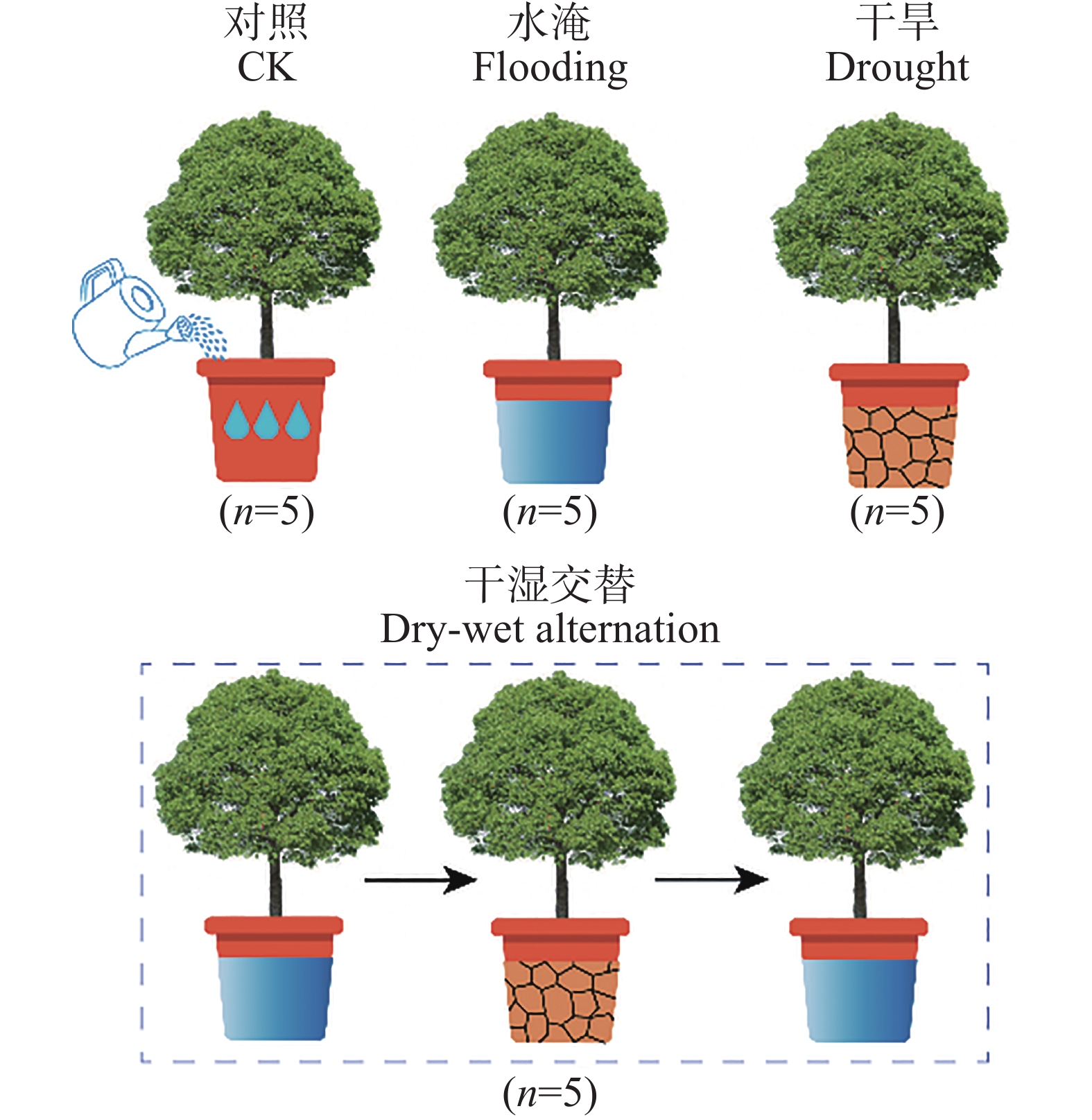
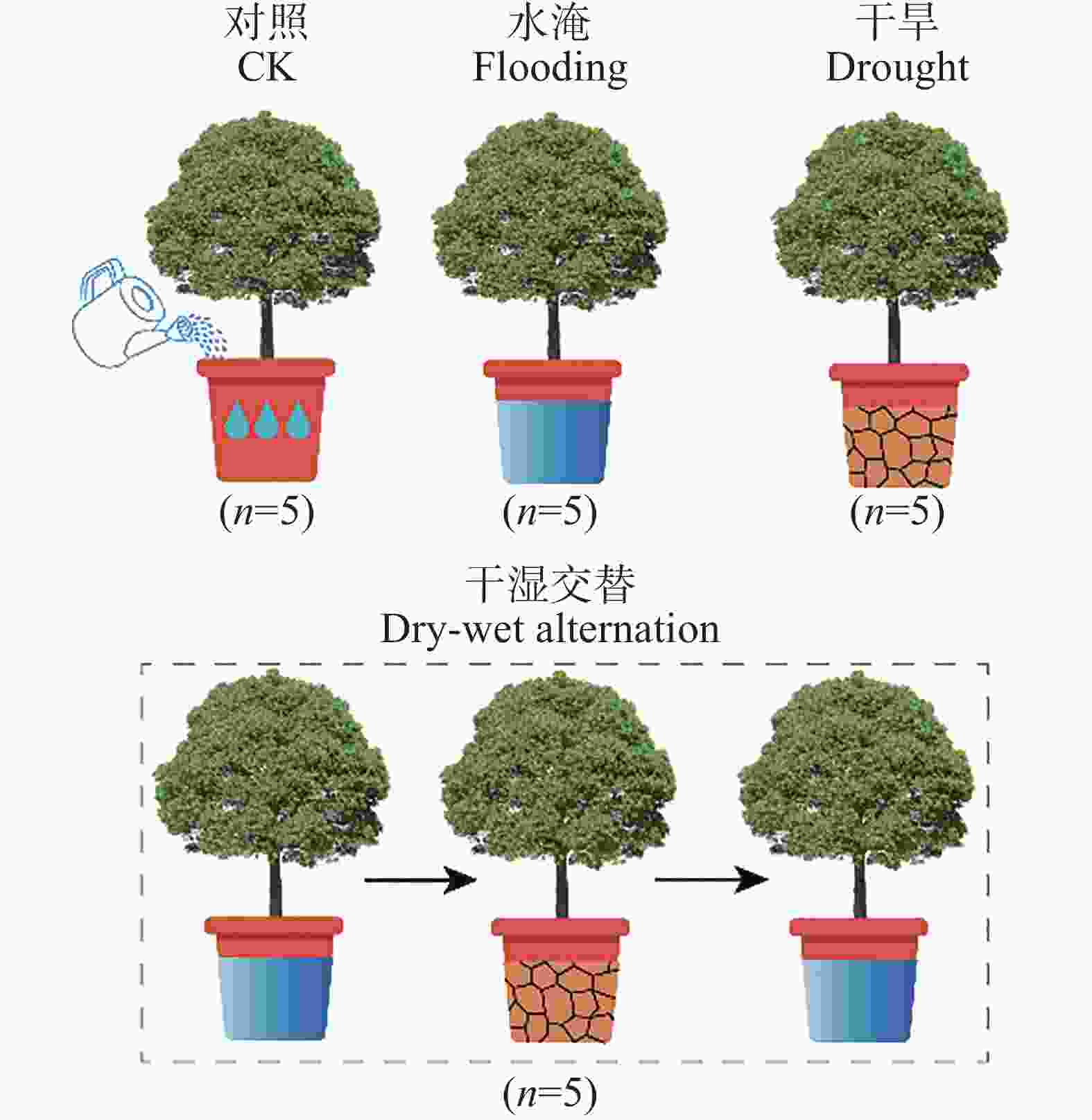
2017−09−19,选取25盆生长良好、长势均匀的幼苗(实验第0天),设计4种不同的水分处理(图1)。1)对照:选取10盆幼苗置于遮雨棚中,土壤湿度维持在田间持水量水平;2)干旱胁迫:选取5盆幼苗置于遮雨棚中,实验开始后不再进行浇水;3)水淹胁迫:选取5盆幼苗置于水桶中,保持桶内水面高于土壤表面5 cm,模拟水淹胁迫;4)干湿交替:选取5盆幼苗置于大棚中。首先,淹水处理幼苗(与水淹胁迫相同),气孔导度下降到接近0 mol·m−2·s−1(第11天)时将幼苗从水桶中移出,进行干旱处理,当气孔导度因干旱胁迫下降到0 mol·m−2·s−1时(第36天),再进行1次淹水处理直到实验结束(第40天)。实验进行至第40天时,收割各处理的樟树幼苗,并对每个处理组的5盆土壤进行破坏性取样,将土壤混匀并去除石块和残渣,一部分放4 ℃冰箱保存,另一部分风干后过筛。
-
土壤pH的测定:土水比1∶2.5,用pH计测定。土壤有机碳(soil organic carbon, SOC):采用重铬酸钾外氧化加热法进行测定。土壤总氮(total nitrogen, TN):采用硫酸–过氧化氢消煮法。
-
采用磷脂脂肪酸法(PLFA)测定土壤微生物群落结构,参照Bligh等[25]的方法进行测定,用V氯仿∶V甲醇∶V柠檬酸缓冲液=1∶2∶0.8提取冻干土壤样品中的总脂质,将极性脂质与糖基脂质和中性脂质分离,经甲基化转化为脂肪酸甲酯,用气相色谱仪测定。
选取磷脂脂肪酸分子(表1)指示微生物类群[26]。其中18:1 ω7c作为指示厌氧菌的功能菌[27−28]。单不饱和脂肪酸包括16:1 ω7c、18:1 ω7c、18:1 ω9、16:1 ω5[29]。
表 1 特征脂肪酸对不同种类微生物的指征
Table 1. Indications of specific fatty acids for different microorganisms
微生物类群Microbial community 磷脂脂肪酸分子PLFAs 细菌Bacteria 15:0, 15:0 iso, 15:0 anteiso, 16:0 iso, 16:0 anteiso, 17:0 iso, 17:0 anteiso,
16:1 ω7c, 18:0, 18:1 ω7c革兰氏阳性菌Gram positive bacteria 15:0 iso, 15:0 anteiso, 16:0 iso, 16:0 anteiso, 17:0 iso, 17:0 anteiso 革兰氏阴性菌Gram negative bacteria 16:1 ω7c, 18:1 ω7c 真菌Fungi 16:1 ω5c, 18:2 ω6c, 18:1 ω9c 放线菌Actinomycete 16:0 10-methyl -
真菌和细菌磷脂脂肪酸之比(F/B)用来指示微生物群落结构[30 − 32]。通过PLFA生物标记的丰富度指数(SR)、香农–威纳多样性指数(H)、Simpson 优势度指数(D)和Pielou均匀度指数(J)4个生态学参数评估土壤微生物群落多样性状况[33]。具体计算方法如下:
$$ H=-\mathrm{\Sigma }Pi\mathrm{l}\mathrm{n}Pi \text{,} $$ $$ D=\mathrm{ }1-\mathrm{\Sigma }P{i}^{2} , $$ $$ J=H/\mathrm{l}\mathrm{n}S , $$ $$ SR=\mathrm{ }(S-1)/\mathrm{l}\mathrm{n}N 。 $$ 式中,Pi=Ni/N;Ni表示第i种磷脂脂肪酸含量,i=1,2,3······;N表示每个样品中所有磷脂脂肪酸的含量总和;S表示每个样品中出现的磷脂脂肪酸种类数。
-
采用Excel 2021对实验数据进行整理,所有的统计分析和画图都在R 4.0.3下完成。使用单因素方差分析(One-way ANOVA)分析各处理下的土壤理化性质、微生物磷脂脂肪酸含量,显著性水平P<0.05。
-
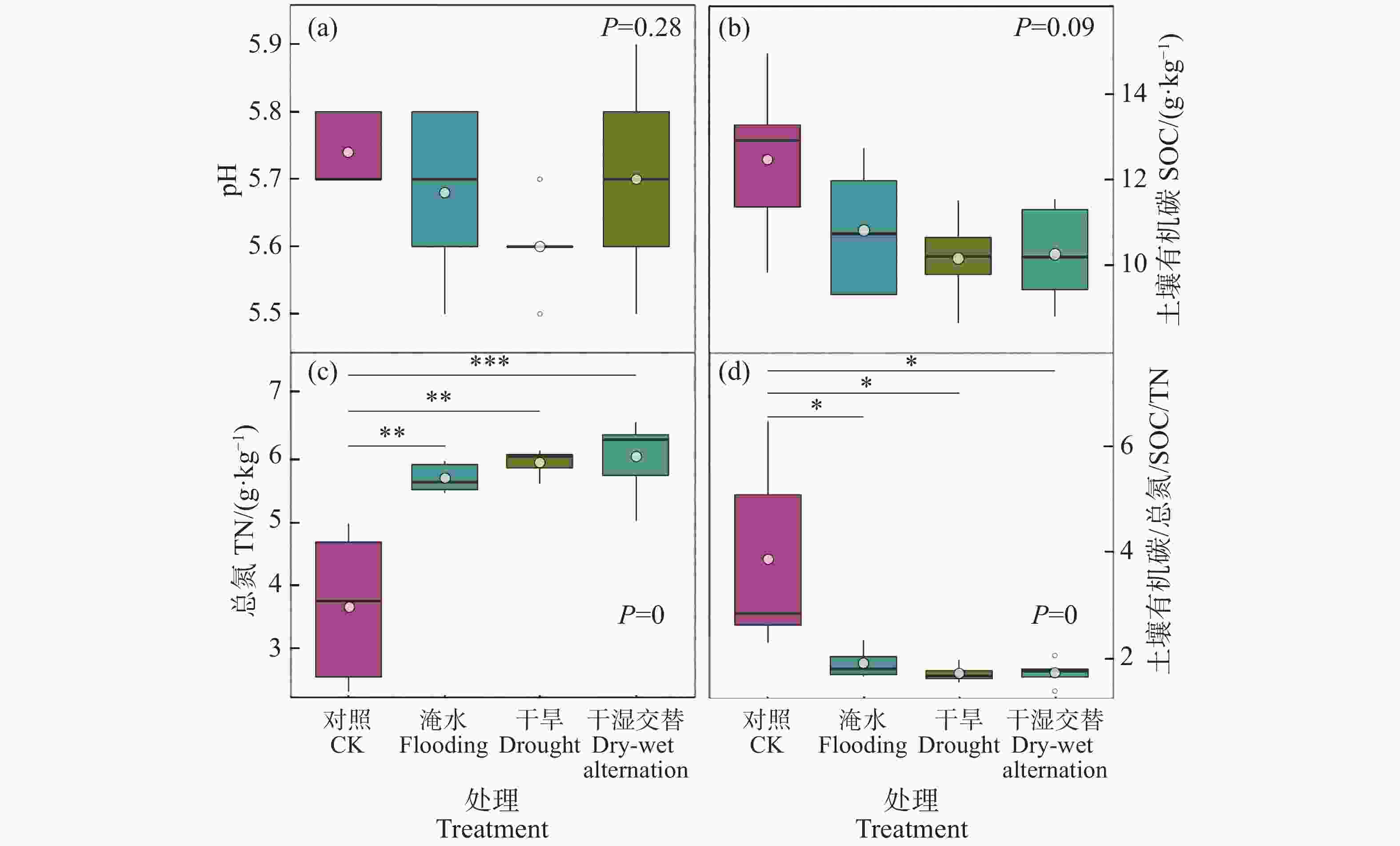
对照组的樟树总平均生物量为41 g·株−1,水淹、干旱及干湿交替胁迫的生物量分别下降了26%、42%和42%[9]。土壤pH与SOC在各处理之间没有显著差异(图2−a、2−b),但干旱胁迫、水淹胁迫和干湿交替处理下的SOC含量均比对照组低(图2−b)。干旱胁迫、水淹胁迫和干湿交替处理下的TN含量显著高于对照组(图2−c)。土壤碳氮比(C/N)在干旱胁迫、水淹胁迫和干湿交替处理下显著低于对照组(图2−d)。
-
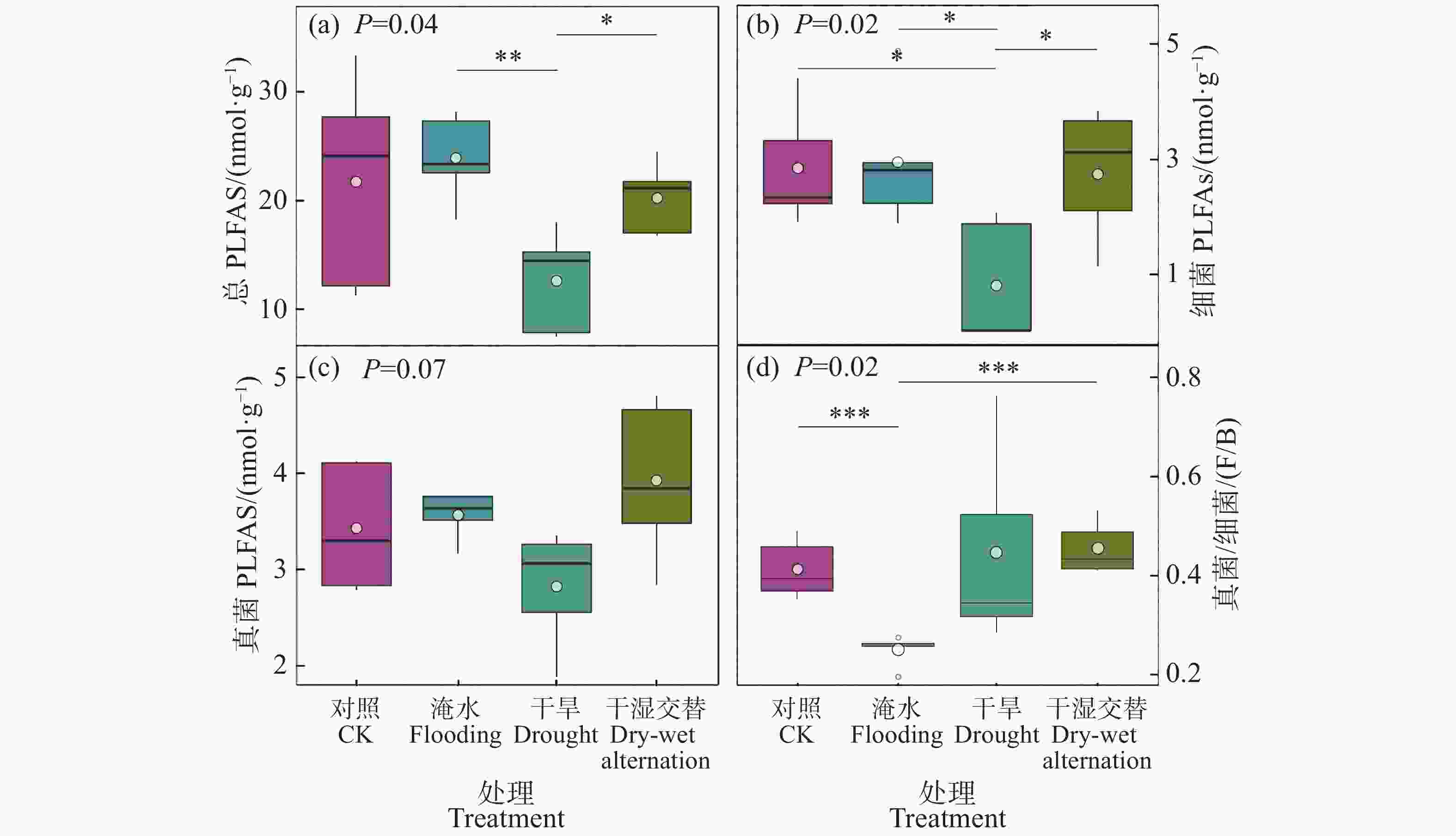
总微生物生物量在干旱胁迫下显著低于水淹胁迫和干湿交替胁迫(图3−a)。进一步分析细菌生物量和真菌生物量发现,干旱胁迫下细菌生物量显著低于其他处理(图3−b);真菌生物量在各处理之间无显著差异(图3−c);水淹胁迫下真菌/细菌(F/B)显著低于对照组和干湿交替处理组(图3−d)。
-
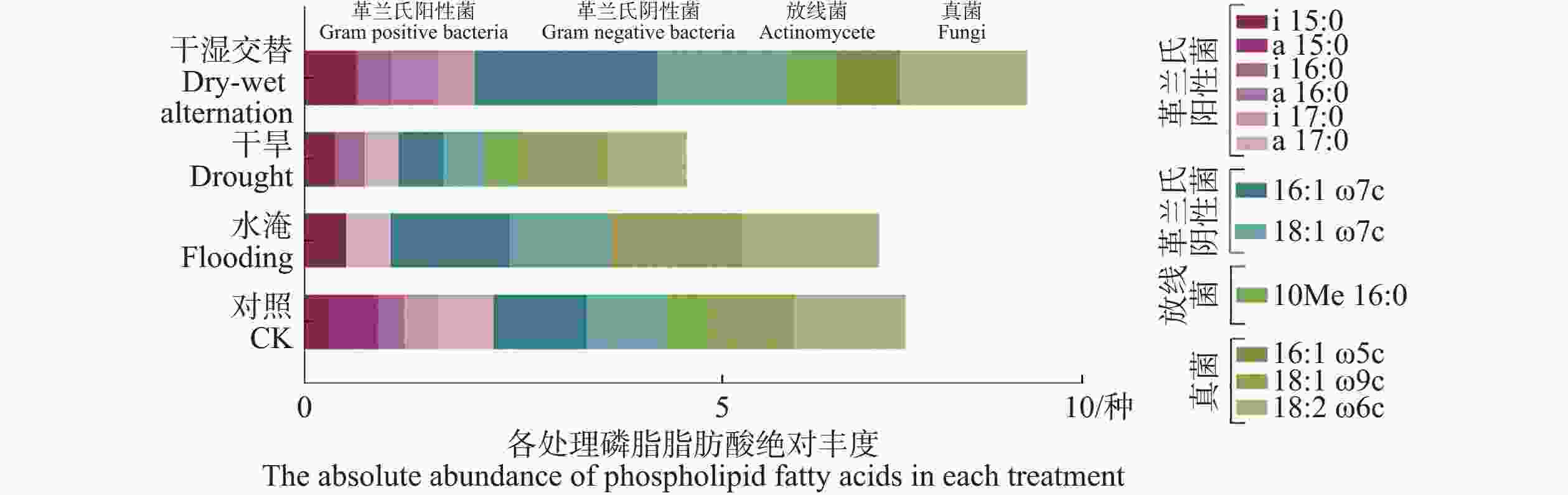
由图4可看出,干湿交替胁迫下微生物生物量丰度的增加主要是由于革兰氏阴性细菌含量的增加。水淹胁迫下,革兰氏阳性菌丰度减少,而革兰氏阴性细菌和真菌丰度增加。干旱胁迫下微生物生物量丰度减少。
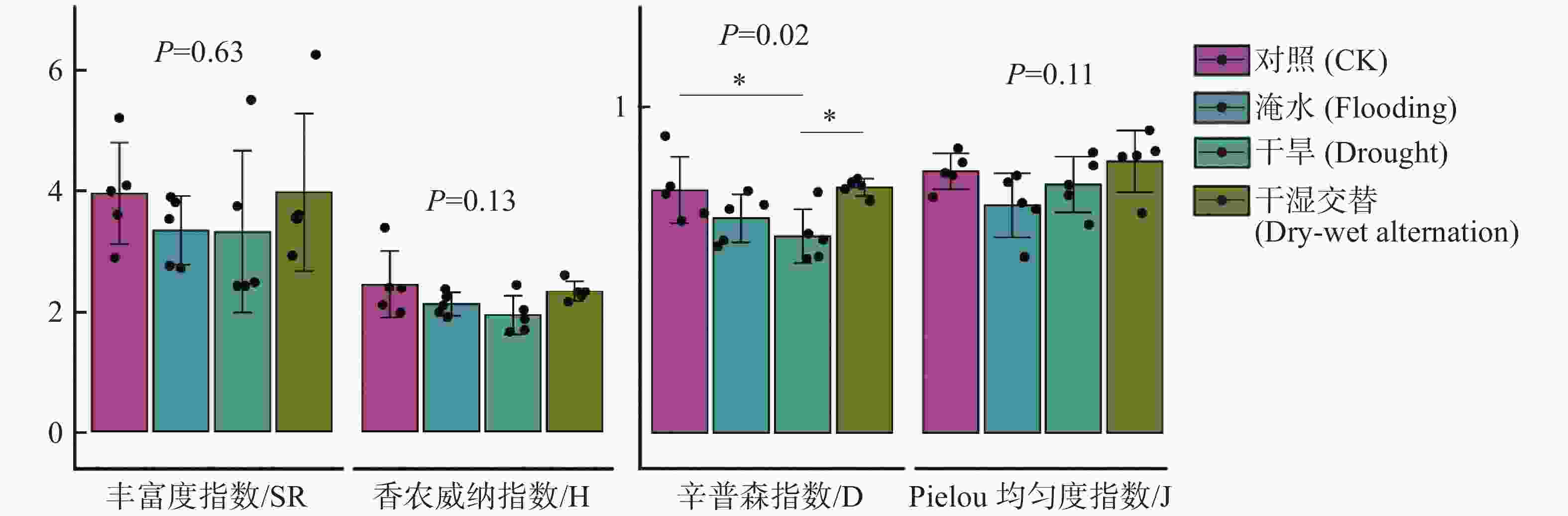
各微生物多样性参数中,Simpson指数在干旱胁迫下显著低于对照和干湿交替处理;各处理在丰富度指数、香农–威纳指数和Pielou均匀度指数上,均无显著性差异(图5)。
由表2可知,16:1 ω5c只在干湿交替胁迫下出现;16:1 ω7c在干湿交替胁迫下显著高于干旱胁迫;18:1 ω7c在干旱胁迫下,显著低于其他处理组;18:1 ω9c在各处理下均无显著差异,且在干湿交替胁迫下没有出现。
表 2 不同胁迫对单不饱和磷脂脂肪酸含量的影响
Table 2. Effects of different stresses on the content of monounsaturated phospholipid fatty acids
PLFAs指标 处理 Treatment 对照 CK 淹水 Flooding 干旱 Drought 干湿交替 Dry-wet alternation 16:1 ω5c NA NA NA 0.74(−) 16:1 ω7c 1.12(0.15)ab 1.44(0.25)ab 0.54(0.12)b 2.17(0.57)a 18:1 ω7c 0.96(0.26)a 1.21(0.26)a 0.46(0.26)b 1.59(0.26)a 18:1 ω9c 1.13(0.19)a 1.61(0.45)a 1.00(0.12)a NA 注:表中值为平均值(标准误差),单因素方差分析(ANOVA),不同字母表示有显著差异,相同字母无显著差异。(−)表示该处理下所有重复中只出现一次对应PLFA,NA表示该处理下无对应PLFA出现。
Note:The data in the table are the average values (standard error) and subjected to one-way analysis of variance (ANOVA). Different letters in the same row indicate significant differences. (−) indicates only one corresponding PLFA in all replicates under this treatment;NA indicates no corresponding PLFA under this treatment. -
在本研究中,与对照组相比,胁迫处理下的樟树总生物量显著降低[9]。土壤中的氮磷元素与植物体内的养分循环过程密切相关[34−35],是维持植物体生长发育的必需元素[36]。水分胁迫使根系养分吸收能力发生变化,对土壤氮素的需求减少,樟树生长受限,导致在不同胁迫处理下土壤TN含量显著增加,这与先前的研究结果相吻合[35]。而SOC含量在各胁迫处理下均低于对照组(P=0.09)。一方面,樟树生长受到抑制导致向地下输入的光合碳含量减少[37];另一方面,在水淹胁迫下,土壤中的可溶性有机质被水溶解而损失,降低了土壤中的有机碳含量,不利于土壤碳的固定和储存[38−39]。
-
本研究表明,干旱胁迫下,总微生物生物量显著低于水淹胁迫和干湿交替胁迫,低于对照组但不显著。因为干旱下土壤水分匮乏,导致微生物细胞内部产生较高的渗透压,进而引发微生物细胞损伤甚至死亡,从而降低了微生物生物量[40]。进一步将总微生物生物量分类发现,相比真菌生物量,细菌生物量在各胁迫下含量发生显著变化。有研究表明,与细菌相比,真菌拥有独特的水分调控机制,能够通过菌丝体内部水分的有效再分配来应对水分胁迫所带来的生理挑战[41],因此更加能适应水分的波动[42]。此外,细菌在土壤环境中的运动和对营养物质的获取,在很大程度上取决于土壤中水分的有效流动性,因而与真菌相比,细菌对于水分条件变化更为敏感[43]。这一结论凸显出水分条件对不同类型的土壤微生物群落结构和功能响应的差异化影响。
在水淹和干湿交替处理下,革兰氏阴性细菌丰度增加。这可能是因为在水淹条件下土壤环境转变为低氧或无氧状态,有利于厌氧微生物的繁殖[44],本实验结果显示,厌氧细菌标志物18:1 ω7c特征脂肪酸在水淹及干湿交替处理组中的浓度显著高于对照组和干旱胁迫组。尽管真菌相比细菌被认为在对抗水分胁迫方面具备一定的优势,但有研究发现,真菌占据多重水分生态位,并且部分真菌类群对水分的变化极为敏感[45]。本研究同样发现在水淹胁迫下,代表真菌的18:1 ω9c特征脂肪酸含量高于对照组与干旱胁迫处理组,使得水淹胁迫下的真菌丰度提升。而干湿交替则是因为磷脂脂肪酸的种类增多,使其丰度提升。此外,放线菌在本次研究中的分布表现出明显的环境偏好,除了在淹水胁迫下没有出现,其他处理组均检测到放线菌的存在,可能是因为放线菌耐受干旱的能力较强且喜欢偏干燥的环境[46],因此在水淹条件下未能检测到。真菌/细菌比在淹水处理下显著低于对照组,也证实可能是淹水导致土壤中溶解氧含量减少,厌氧细菌的含量在水淹胁迫下增加,导致微生物群落结构发生改变[47]。
在表征微生物多样性的各生态学参数中,Simpson指数在干旱胁迫下显著低于对照组和干湿交替胁迫。表明干旱胁迫下微生物群落种类较少,进而导致微生物群落多样性下降。但干湿交替处理下的各多样性参数相比其他处理都较高,若干种单不饱和特征脂肪酸在干湿交替处理下的含量也相对较高,外界胁迫越大微生物能够合成更多单不饱和脂肪酸[48],对干湿交替下微生物多样性有一定促进作用[49]。
土壤水分的变化会引起植物养分、土壤理化性质和土壤微生物之间关系的变化[50]。本研究结果显示,在水淹处理下,革兰氏阴性细菌16:1 ω7c和18:1 ω7c丰度增加,可能促进了碳循环相关的细菌对有机质的利用[51]。有研究表明,长期水淹可以增加土壤微生物的活性,从而促进微生物对有机质的转化[52]。在干湿交替处理下,一方面,干旱期间积累的有机质和死亡的微生物被存活的微生物重新利用,微生物群落进入快速生长和繁殖阶段[22],这一过程导致不饱和磷脂脂肪酸的含量和种类增加,增强了细菌群体的代谢活动,从而促进了微生物对碳基质的降解和消耗[53]。此外,较低的土壤碳氮比可能导致更多的氮元素可供微生物利用,微生物的快速增长对碳源的需求随之加大,从而增强了碳的矿化作用[22];另一方面,干旱复水能显著提高土壤中CO2的释放速率[54],从而导致SOC含量减少。而干旱处理下,虽然微生物生物量与多样性显著降低,但在面对极度缺水的情况下,微生物会更为高效地利用土壤中的有机物质,来应对突然改变的环境[53],从而造成SOC的减少。综合来看,土壤水分的不同处理方式通过调节微生物活动和养分循环过程,影响SOC动态。
-
本研究基于盆栽控制实验,发现干旱胁迫抑制樟树幼苗的生长和土壤有机碳的固存潜力,并改变土壤微生物群落结构。相比之下,淹水胁迫和干湿交替虽然在一定程度上促进土壤微生物多样性的增加,但这两类水分胁迫条件下土壤有机碳含量相较于对照组均下降,且樟树的生物量也显著减少。综上所述,相较于水淹和干湿交替胁迫,干旱胁迫对樟树与土壤微生物的综合影响最为显著。因此,在樟树遭受极端气候事件的恢复阶段,应考虑增强微生物–植物的耦合作用,提升植物适应极端气候的能力,同时维系土壤生态系统的稳定和功能,从而提高树木对极端环境的适应性和恢复力。
土壤理化性质和微生物群落组成对极端水分胁迫的响应
DOI: 10.15886/j.cnki.rdswxb.20240119
 CSTR: 32425.14.j.cnki.rdswxb.20240119
CSTR: 32425.14.j.cnki.rdswxb.20240119
Response of soil physio-chemical properties and microbial community composition to extreme water stress based on a pot experiment of Cinnamomum camphora seedlings
-
摘要: 极端气候引起降水格局变化并导致暴雨、干旱及干湿交替事件频繁发生,是影响植物生长和土壤群落稳定的重要环境因素。为探究极端气候胁迫对植物生长及土壤环境的影响,通过设置对照组、淹水、干旱和干湿交替胁迫模拟降水格局变化,测定樟树(Cinnamomum camphora)盆栽土壤理化性质(pH、土壤有机碳、土壤总氮)和微生物生物量,研究樟树土壤系统对水分胁迫的响应。结果表明,相比对照组,3种胁迫处理显著增加土壤总氮含量(P<0.001)。土壤总微生物生物量和细菌生物量在淹水和干湿交替胁迫下显著高于干旱胁迫,而真菌生物量在几种胁迫下较为稳定。干旱胁迫下的微生物Simpson指数显著低于其他处理。综上分析,在极端水分胁迫后,樟树生长受到负面影响,土壤微生物受到碳底物限制更强;相比水淹和干湿交替,干旱胁迫对樟树土壤理化和微生物群落的影响更大。樟树在遭受极端气候事件后可以考虑增强微生物–植物的耦合作用,以提升植物适应极端气候的能力,从而维系土壤生态系统的稳定和功能并助力植物生长恢复。Abstract: Extreme climate-driven alterations in precipitation patterns lead to frequent heavy rainfall, drought, and dry-wet alternation events, and hence significantly impact plant growth and soil community stability. Cinnamomum camphora, a crucial economic species for greening, is particularly sensitive to these environmental changes. Understanding the influence of altered precipitation patterns on the growth of C. camphora and its associated soil systems holds significant implications for cultivation, management and planting strategies in the context of global extreme climate change. A pot experiment was designed to simulate precipitation patterns to cultivate C. camphora seedlings to determine the soil physicochemical properties (pH, soil organic carbon, and soil total nitrogen) and microbial biomass in the pot soil. The seedlings were treated with stress of flooding, drought, or wet-dry alternation, with no stress as a control. Results indicated that the three stress treatments notably increased soil total nitrogen content (P<0.001 as against the control. Soil total phospholipid fatty acids and bacterial biomass were significantly higher in the stress treatment of flooding or dry-wet alternation compared to the drought stress, whereas fungal biomass remained relatively stable under stress conditions. Additionally, the microbial Simpson index was significantly lower under the drought stress treatment compared to the other treatments. In conclusion under extreme stress events the growth of C. camphora was inhibited, and the soil microorganisms become more constrained by carbon substrates. The drought stress had a more pronounced impact on soil physiochemical properties and microbial communities compared to the stress treatments of flooding and dry-wet alternation. Under the extreme climate events the coupling of microorganisms and plants should be enhanced to improve the ability of plants to adapt to extreme climate, thereby preserving the stability and functionality of the soil ecosystem and benefiting plant recovery.
-
Key words:
- Cinnamomum camphora /
- drought stress /
- flooding stress /
- dry-wet alternation /
- phospholipid fatty acid
-
图 2 各处理下土壤pH(a)、有机碳(b)、总氮(c)和碳氮比(C/N)(d)
单因素方差分析,星号表示不同组别间存在显著差异。“***”代表P<0.001,“**”代表P<0.01,“*”代表P<0.05。
Fig. 2 Soil pH (a), soil organic carbon (b), total nitrogen (c), and C/N (d) in each treatment
One-way analysis of variance (ANOVA) was performed;asterisks indicate significant differences among different groups. ***:P < 0.001;**:P < 0.01;* P < 0.05.
图 3 各处理下土壤总微生物生物量(a)、细菌生物量(b)、真菌生物量(c)、真菌/细菌比(d)
单因素方差分析,星号表示不同组别间存在显著差异。“***”代表P<0.001,“**”代表P<0.01,“*”代表P<0.05。
Fig. 3 Total soil microbial biomass (a), bacterial biomass (b), fungal biomass (c), and fungal/bacterial ratio (d) of each treatment
One-way analysis of variance (ANOVA) was perfomred;asterisks indicate significant differences among different groups. ***:P < 0.001;**:P < 0.01;*:P < 0.05.
表 1 特征脂肪酸对不同种类微生物的指征
Table 1 Indications of specific fatty acids for different microorganisms
微生物类群Microbial community 磷脂脂肪酸分子PLFAs 细菌Bacteria 15:0, 15:0 iso, 15:0 anteiso, 16:0 iso, 16:0 anteiso, 17:0 iso, 17:0 anteiso,
16:1 ω7c, 18:0, 18:1 ω7c革兰氏阳性菌Gram positive bacteria 15:0 iso, 15:0 anteiso, 16:0 iso, 16:0 anteiso, 17:0 iso, 17:0 anteiso 革兰氏阴性菌Gram negative bacteria 16:1 ω7c, 18:1 ω7c 真菌Fungi 16:1 ω5c, 18:2 ω6c, 18:1 ω9c 放线菌Actinomycete 16:0 10-methyl 表 2 不同胁迫对单不饱和磷脂脂肪酸含量的影响
Table 2 Effects of different stresses on the content of monounsaturated phospholipid fatty acids
PLFAs指标 处理 Treatment 对照 CK 淹水 Flooding 干旱 Drought 干湿交替 Dry-wet alternation 16:1 ω5c NA NA NA 0.74(−) 16:1 ω7c 1.12(0.15)ab 1.44(0.25)ab 0.54(0.12)b 2.17(0.57)a 18:1 ω7c 0.96(0.26)a 1.21(0.26)a 0.46(0.26)b 1.59(0.26)a 18:1 ω9c 1.13(0.19)a 1.61(0.45)a 1.00(0.12)a NA 注:表中值为平均值(标准误差),单因素方差分析(ANOVA),不同字母表示有显著差异,相同字母无显著差异。(−)表示该处理下所有重复中只出现一次对应PLFA,NA表示该处理下无对应PLFA出现。
Note:The data in the table are the average values (standard error) and subjected to one-way analysis of variance (ANOVA). Different letters in the same row indicate significant differences. (−) indicates only one corresponding PLFA in all replicates under this treatment;NA indicates no corresponding PLFA under this treatment. -
[1] Intergovernmental Panel on Climate Change (IPCC). Climate Change 2022: impacts, adaptation and vulnerability[M]. Cambridge: Cambridge University Press, 2023: 1 − 3056. [2] 胡俊靖, 陈卫军, 郭子武, 等. 水分胁迫对竹子生理特性影响的研究进展[J]. 西南林业大学学报, 2015, 35(1): 91 − 95. doi: 10.11929/j.issn.2095-1914.2015.01.018 [3] 张颖娴, 孙劭, 刘远, 等. 2021年全球重大天气气候事件及其成因[J]. 气象, 2022, 48(4): 459 − 469. doi: 10.7519/j.issn.1000-0526.2022.032201 [4] HARRISON-KIRK T, BEARE M H, MEENKEN E D, et al. Soil organic matter and texture affect responses to dry/wet cycles: changes in soil organic matter fractions and relationships with C and N mineralisation[J]. Soil Biology and Biochemistry, 2014, 74: 50 − 60. doi: 10.1016/j.soilbio.2014.02.021 [5] 夏银华, 章新平, 戴军杰, 等. 亚热带季风区樟树蒸腾与气象因子之间的时滞效应[J]. 水土保持学报, 2021, 35(5): 194 − 203. doi: 10.13870/j.cnki.stbcxb.2021.05.027 [6] 王卓敏, 郑欣颖, 薛立. 樟树幼苗对干旱胁迫和种植密度的生理响应[J]. 生态学杂志, 2017, 36(6): 1495 − 1502. doi: 10.13292/j.1000-4890.201706.033 [7] 胡义, 胡庭兴, 胡红玲, 等. 干旱胁迫对香樟幼树生长及光合特性的影响[J]. 应用与环境生物学报, 2014, 20(4): 675 − 682. doi: 10.3724/SP.J.1145.2013.12019 [8] WANG C T, SUN Y, CHEN H Y H, et al. Meta-analysis shows non-uniform responses of above- and belowground productivity to drought[J]. Science of The Total Environment, 2021, 782: 146901. doi: 10.1016/j.scitotenv.2021.146901 [9] ZHAO Y J, WANG D F, DUAN H L. Effects of drought and flooding on growth and physiology of Cinnamomum camphora seedlings[J]. Forests, 2023, 14(7): 1343. doi: 10.3390/f14071343 [10] 李梦寻, 王冬梅, 任远, 等. 不同干湿交替频率对土壤速效养分、水溶性有机碳的影响[J]. 生态学报, 2018, 38(5): 1542 − 1549. doi: 10.5846/stxb201702190268 [11] 张素, 熊东红, 校亮, 等. 干湿交替对土壤性质影响的研究[J]. 土壤通报, 2017, 48(3): 762 − 768. doi: 10.19336/j.cnki.trtb.2017.03.35 [12] 夏银华, 章新平, 戴军杰, 等. 亚热带季风区樟树的水分利用特征[J]. 水土保持学报, 2022, 36(6): 195 − 205. doi: 10.13870/j.cnki.stbcxb.2022.06.025 [13] 刘方春, 邢尚军, 马海林, 等. 持续干旱对樱桃根际土壤细菌数量及结构多样性影响[J]. 生态学报, 2014, 34(3): 642 − 649. doi: 10.5846/stxb201211061552 [14] KOHLER J, KNAPP B A, WALDHUBER S, et al. Effects of elevated CO2, water stress, and inoculation with Glomus intraradices or Pseudomonas mendocina on lettuce dry matter and rhizosphere microbial and functional diversity under growth chamber conditions[J]. Journal of Soils and Sediments, 2010, 10(8): 1585 − 1597. doi: 10.1007/s11368-010-0259-6 [15] KAISERMANN A, DE VRIES F T, GRIFFITHS R I, et al. Legacy effects of drought on plant-soil feedbacks and plan-plant interactions[J]. New Phytologist, 2017, 215(4): 1413 − 1424. doi: 10.1111/nph.14661 [16] HE M Z, DIJKSTRA F A. Drought effect on plant nitrogen and phosphorus: a meta-analysis[J]. New Phytologist, 2014, 204(4): 924 − 931. doi: 10.1111/nph.12952 [17] 庞志强, 余迪求. 干旱胁迫下的植物根系-微生物互作体系及其应用[J]. 植物生理学报, 2020, 56(2): 109 − 126. doi: 10.13592/j.cnki.ppj.2019.0383 [18] JIA Y Y, VAN DER HEIJDEN M G A, WAGG C, et al. Symbiotic soil fungi enhance resistance and resilience of an experimental grassland to drought and nitrogen deposition[J]. Journal of Ecology, 2021, 109(9): 3171 − 3181. doi: 10.1111/1365-2745.13521 [19] PREECE C, VERBRUGGEN E, LIU L, et al. Effects of past and current drought on the composition and diversity of soil microbial communities[J]. Soil Biology and Biochemistry, 2019, 131: 28 − 39. doi: 10.1016/j.soilbio.2018.12.022 [20] FIERER N, SCHIMEL J P. Effects of drying–rewetting frequency on soil carbon and nitrogen transformations[J]. Soil Biology and Biochemistry, 2002, 34(6): 777 − 787. doi: 10.1016/S0038-0717(02)00007-X [21] STEENWERTH K L, JACKSON L E, CALDERÓN F J, et al. Response of microbial community composition and activity in agricultural and grassland soils after a simulated rainfall[J]. Soil Biology and Biochemistry, 2005, 37(12): 2249 − 2262. doi: 10.1016/j.soilbio.2005.02.038 [22] 谢志煌, 高志颖, 郭丽丽, 等. 土壤微生物活性和生物量对干湿交替的响应[J]. 土壤与作物, 2020, 9(4): 348 − 354. doi: 10.11689/j.issn.2095-2961.2020.04.003 [23] AUSTIN A T, YAHDJIAN L, STARK J M, et al. Water pulses and biogeochemical cycles in arid and semiarid ecosystems[J]. Oecologia, 2004, 141(2): 221 − 235. doi: 10.1007/s00442-004-1519-1 [24] 孙嘉鸿, 郭彤, 董彦民, 等. 冻融循环对金川泥炭沼泽土壤微生物量及群落结构的影响[J]. 生态学报, 2022, 42(7): 2763 − 2773. doi: 10.5846/stxb202101290314 [25] BLIGH E G, DYER W J. A rapid method of total lipid extraction and purification[J]. Canadian Journal of Biochemistry and Physiology, 1959, 37(8): 911 − 917. doi: 10.1139/o59-099 [26] WU J P, LIU W F, FAN H B, et al. Asynchronous responses of soil microbial community and understory plant community to simulated nitrogen deposition in a subtropical forest[J]. Ecology and Evolution, 2013, 3(11): 3895 − 3905. doi: 10.1002/ece3.750 [27] 陈振翔, 于鑫, 夏明芳, 等. 磷脂脂肪酸分析方法在微生物生态学中的应用[J]. 生态学杂志, 2005, 24(7): 828 − 832. doi: 10.3321/j.issn:1000-4890.2005.07.022 [28] 张秋芳, 刘波, 林营志, 等. 土壤微生物群落磷脂脂肪酸PLFA生物标记多样性[J]. 生态学报, 2009, 29(8): 4127 − 4137. doi: 10.3321/j.issn:1000-0933.2009.08.014 [29] 马书琴, 王小丹, 王荷, 等. 藏北高寒草地土壤磷脂脂肪酸指纹特征及其与土壤化学性质的关系[J]. 生态环境学报, 2017, 26(9): 1480 − 1487. doi: 10.16258/j.cnki.1674-5906.2017.09.004 [30] 曹志平, 李德鹏, 韩雪梅. 土壤食物网中的真菌/细菌比率及测定方法[J]. 生态学报, 2011, 31(16): 4741 − 4748. doi: 10.20103/j.stxb.2011.16.028 [31] CAMENZIND T, PHILIPP GRENZ K, LEHMANN J, et al. Soil fungal mycelia have unexpectedly flexible stoichiometric C: N and C: P ratios[J]. Ecology Letters, 2021, 24(2): 208 − 218. doi: 10.1111/ele.13632 [32] 庞丹波, 吴梦瑶, 赵娅茹, 等. 贺兰山东坡不同海拔土壤微生物群落特征及其影响因素[J]. 应用生态学报, 2023, 34(7): 1957 − 1967. doi: 10.13287/j.1001-9332.202307.031 [33] 马鑫茹, 郑旭理, 郑春颖, 等. 毛竹扩张对常绿阔叶林土壤微生物群落的影响[J]. 应用生态学报, 2022, 33(4): 1091 − 1098. doi: 10.13287/j.1001-9332.202204.030 [34] 蒋文伟, 周国模, 余树全, 等. 安吉山地主要森林类型土壤养分状况的研究[J]. 水土保持学报, 2004, 18(4): 73 − 76. doi: 10.3321/j.issn:1009-2242.2004.04.019 [35] 马朋, 李昌晓, 任庆水, 等. 模拟水淹-干旱胁迫对水杉幼树实生土壤营养元素含量的影响[J]. 生态学报, 2015, 35(23): 7763 − 7773. doi: 10.5846/stxb201405110966 [36] 文旻, 胡启武, 阳文静, 等. 氮、磷添加对鄱阳湖典型苔草湿地土壤养分和植物生物量的影响[J]. 生态学杂志, 2021, 40(6): 1669 − 1676. doi: 10.13292/j.1000-4890.202106.035 [37] ZANG U, GOISSER M, GRAMS T E E, et al. Fate of recently fixed carbon in European beech (Fagus sylvatica) saplings during drought and subsequent recovery[J]. Tree Physiology, 2014, 34(1): 29 − 38. doi: 10.1093/treephys/tpt110 [38] 杨予静, 李昌晓, 张晔, 等. 水淹-干旱交替胁迫对湿地松幼苗盆栽土壤营养元素含量的影响[J]. 林业科学, 2013, 49(2): 61 − 71. doi: 10.11707/j.1001-7488.20130210 [39] YIN S, BAI J H, WANG W, et al. Effects of soil moisture on carbon mineralization in floodplain wetlands with different flooding frequencies[J]. Journal of Hydrology, 2019, 574: 1074 − 1084. doi: 10.1016/j.jhydrol.2019.05.007 [40] 朱义族, 李雅颖, 韩继刚, 等. 水分条件变化对土壤微生物的影响及其响应机制研究进展[J]. 应用生态学报, 2019, 30(12): 4323 − 4332. doi: 10.13287/j.1001-9332.201912.031 [41] BARNARD R L, OSBORNE C A, FIRESTONE M K. Responses of soil bacterial and fungal communities to extreme desiccation and rewetting[J]. The ISME Journal, 2013, 7(11): 2229 − 2241. doi: 10.1038/ismej.2013.104 [42] DE VRIES F T, GRIFFITHS R I, BAILEY M, et al. Soil bacterial networks are less stable under drought than fungal networks[J]. Nature Communications, 2018, 9(1): 3033. doi: 10.1038/s41467-018-05516-7 [43] EVANS S E, WALLENSTEIN M D. Soil microbial community response to drying and rewetting stress: does historical precipitation regime matter?[J]. Biogeochemistry, 2012, 109(1/3): 101 − 116. doi: 10.1007/s10533-011-9638-3 [44] YANG C M, YANG L Z, YAN T M. Chemical and microbiological parameters of paddy soil quality as affected by different nutrient and water regimes[J]. Pedosphere, 2005, 15(3): 369 − 378. [45] DE VRIES F T, LIIRI M E, BJØRNLUND L, et al. Land use alters the resistance and resilience of soil food webs to drought[J]. Nature Climate Change, 2012, 2(4): 276 − 280. doi: 10.1038/nclimate1368 [46] 左易灵, 贺学礼, 王少杰, 等. 磷脂脂肪酸(PLFA)法检测蒙古沙冬青根围土壤微生物群落结构[J]. 环境科学, 2016, 37(7): 2705 − 2713. doi: 10.13227/j.hjkx.2016.07.038 [47] 牛佳, 周小奇, 蒋娜, 等. 若尔盖高寒湿地干湿土壤条件下微生物群落结构特征[J]. 生态学报, 2011, 31(2): 474 − 482. doi: 10.20103/j.stxb.2011.02.019 [48] GUCKERT J B, ANTWORTH C P, NICHOLS P D, et al. Phospholipid, ester-linked fatty acid profiles as reproducible assays for changes in prokaryotic community structure of estuarine sediments[J]. FEMS Microbiology Letters, 1985, 31(3): 147 − 158. doi: 10.1016/0378-1097(85)90016-3 [49] 张斌, 李利, 张美俊, 等. 干旱对燕麦早期根际土壤微生物群落功能多样性的影响[J]. 山西农业大学学报(自然科学版), 2022, 42(5): 9 − 16. doi: 10.13842/j.cnki.issn1671-8151.202207002 [50] 张乃莉, 郭继勋, 王晓宇, 等. 土壤微生物对气候变暖和大气N沉降的响应[J]. 植物生态学报, 2007, 31(2): 252 − 261. doi: 10.17521/cjpe.2007.0029 [51] 滕怡敏, 李丛笑, 张天昱, 等. 不同水淹梯度下河漫滩湿地土壤有机碳特征及其影响因子[J]. 环境科学学报, 2023, 43(8): 362 − 371. doi: 10.13671/j.hjkxxb.2023.0041 [52] GENG Y Q, WANG D M, YANG W B. Effects of different inundation periods on soil enzyme activity in riparian zones in Lijiang[J]. CATENA, 2017, 149: 19 − 27. doi: 10.1016/j.catena.2016.08.004 [53] 张梦瑶, 高永恒, 谢青琰. 干湿交替对土壤有机碳矿化影响的研究进展[J]. 世界科技研究与发展, 2017, 39(1): 17 − 23. doi: 10.16507/j.issn.1006-6055.2017.02.001 [54] XU X K, LUO X B. Effect of wetting intensity on soil GHG fluxes and microbial biomass under a temperate forest floor during dry season[J]. Geoderma, 2012, 170: 118 − 126. doi: 10.1016/j.geoderma.2011.11.016 -




 下载:
下载: