-
寄生植物通过寄生结构——吸器(haustorium)侵入寄主的根、茎、叶或芽等器官,从而与寄主植物建立寄生关系[1]。全球寄生植物约占被子植物总数的1.6%,涵盖22科270属约
4750 种植物,中国寄生植物共有722种,隶属12科50属[2]。根据是否具有光合作用能力,寄生植物可划分为两类:半寄生植物与全寄生植物。其中,半寄生植物具有光合作用能力,而全寄生植物则完全丧失光合作用活性,完全依赖吸器从寄主中获得所有的还原碳[1]。半寄生植物约占寄生植物总数的80%[3],其体内含有叶绿素具备一定的光合能力,但光合产物尚不足以维持生长,须从寄主中摄取大量的水分和矿质养分[4]。根据寄主部位及依赖程度的不同,半寄生植物可分为3种基本功能类型:根半寄生植物,通过根部与寄主相连,其地上部分形态与非寄生植物通常无明显差异;该类群可进一步分为兼性半寄生和专性半寄生两类[1],前者如变色直草果(Triphysaria versicolor)、独脚金(Striga asiatica)、檀香(Santalum album)等,可不完全依赖寄主完成生命周期;后者如小鼻花(Rhinanthus minor)、甘肃马先蒿(Pedicularis kansuensis)、百蕊草(Thesium chinense)等,必须连接寄主才能完成生活史。茎半寄生植物由于根系的退化或缺失,寄生于寄主植物茎部,均为专性寄生植物,代表物种包括广寄生(Taxillus chinensis)、槲寄生(Viscum coloratum)、无根藤(Cassytha filiformis)等。
半寄生植物在生态系统中扮演着独特而复杂的角色,在影响层面,大多数半寄生植物对寄主植物的产生消极作用,不仅抑制寄主生长、降低其种子质量及产量,还可能传播病原体[7],削弱寄主应对环境胁迫的能力[6],进而对农林业经济造成严重损失。在生态功能方面,半寄生植物亦展现出多重积极效应,例如从寄主获取养分以调节群落中的竞争关系、释放富含营养的高质量凋落物、促进生态系统中的养分循环、为动物提供住所和食物、增加群落生物多样性等[7]。目前,国内外对半寄生植物与寄主间的寄生关系的研究,主要集中于以下几个维度:半寄生植物吸器形成发育过程、形态解剖结构、对寄主植物的选择偏好性、对寄主植物的影响、在不同环境下的生存策略。近年来,随着生物信息学技术的发展,相关研究也更多地集中在分子机制和基因组学等前沿领域。
本文系统梳理了半寄生植物与寄主间寄生关系的国内外研究进展,在总结相关成果的基础上,重点对比了根半寄生植物与茎半寄生植物的吸器形成方式、寄生策略上的异同,旨在丰富对半寄生植物的认识、揭示其寄生策略的多样性,并展望未来研究可聚焦的关键方向,以期为深入理解半寄生植物的生理生态机制及其在生态系统中的作用提供理论依据与新的研究视角。
-
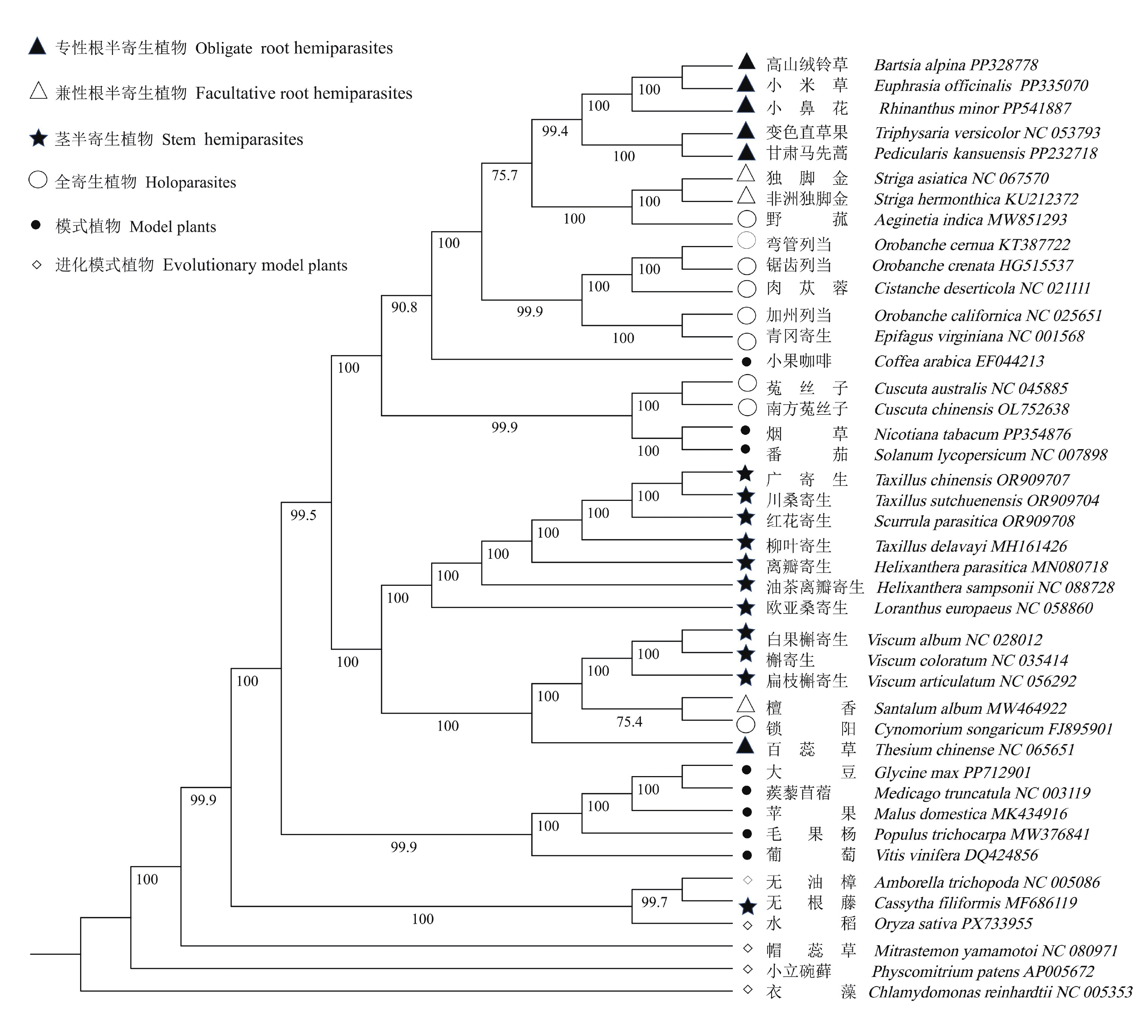
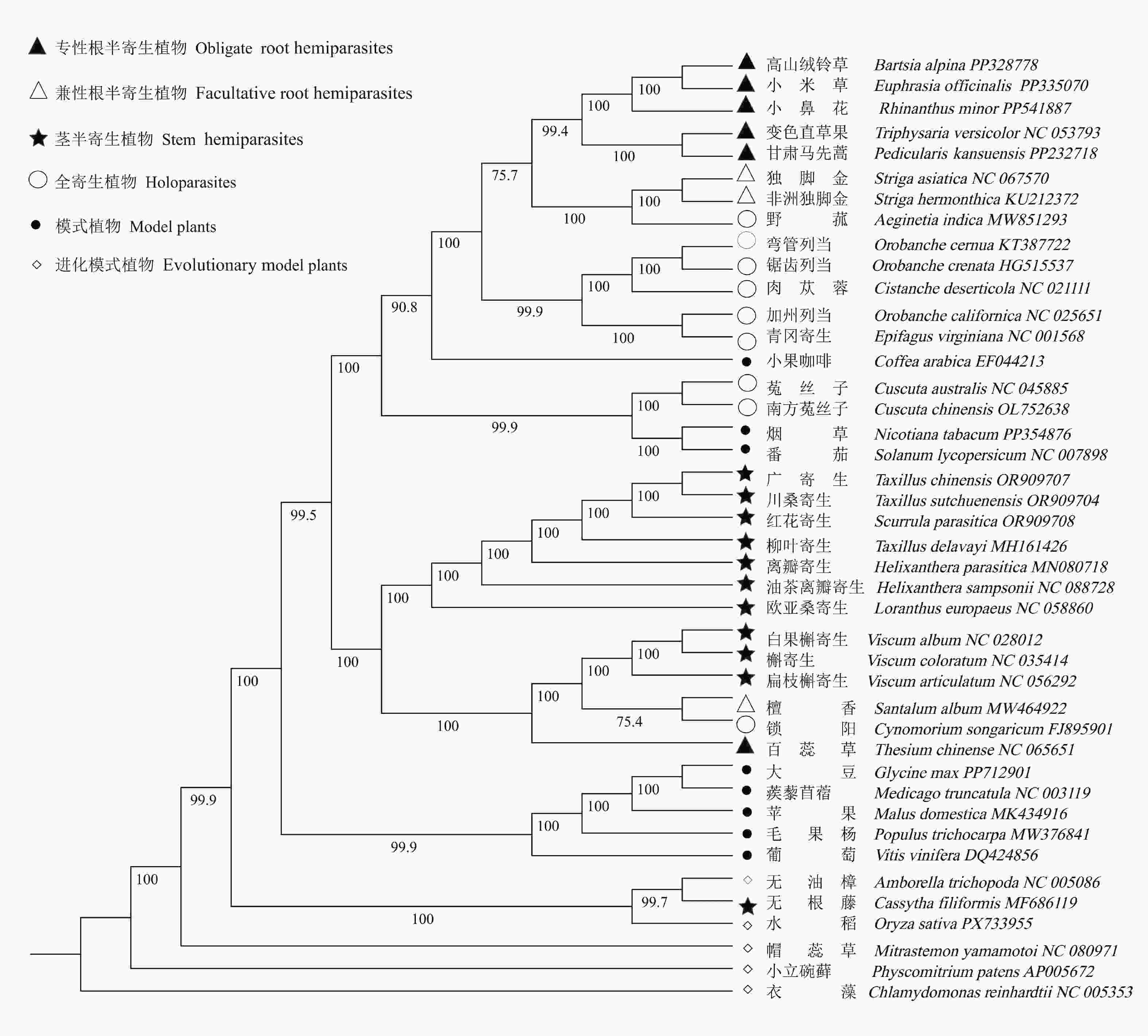
寄生植物在被子植物中经历了12~13次独立起源,从自养类群逐步演化出半寄生植物,并进一步衍生出完全丧失光合作用能力的全寄生植物[8]。半寄生植物因寄生部位(根或茎)及依赖程度(兼性或专性)存在显著差异,形成了多样化的寄生策略。吸器作为寄生关系的核心结构,其形成机制(包括诱导、发育等)在半寄生植物不同类群间呈现显著差异,这种差异可能是半寄生植物在各自的进化过程中适应不同寄生策略的结果。系统发育分析显示,根半寄生植物与茎半寄生植物在进化上形成了明显的分支,兼性与专性寄生习性在多个支系中独立出现(图1),这表明了寄生生活方式的复杂演化历史。为阐明半寄生植物的进化位置,本研究选取模式进化植物衣藻(Chlamydomonas reinhardtii)作为外类群,并纳入代表性全寄生植物进行比较。
基于此,本研究从种子萌发、吸器诱导因子及吸器发育过程3个方面,系统阐述半寄生植物吸器的形成机制,并在此过程中对比根半寄生与茎半寄生植物的异同,以期为理解寄生策略的进化适应提供机制层面的解释。
-
吸器形成的首要条件是种子萌发[9],在此阶段,根半寄生植物与茎半寄生植物的种子存在明显的差异。前者的种子萌发具有严格的寄主依赖性,种子微小且休眠期长,需感知到寄主根系分泌的特定萌发刺激物才能打破休眠[10]。相比之下,大多数茎半寄生植物种子无休眠期,胚成熟立即萌发,其幼苗为异养生长,依靠感知寄主释放的挥发性物质寻找寄生,并迅速通过吸器与寄主茎干建立寄生关系[11]。在环境恶劣或无合适寄主的情况下,部分寄生植物的种子可维持长期休眠;此外,一些半寄生植物种子可以经过鸟类或袋鼠肠道消化提高萌发率。
-
吸器形成通常需要受到化学/物理信号的诱导[1],诱导吸器的化合物被称为吸器诱导因子(haustorium-inducing factors,HIFs)。根半寄生植物的相关研究历史较长,1966年,从寄主棉花(Gossypium hirsutum)根分泌物中分离出来一种独脚金种子强力催芽剂——独脚金内酯(Strigol),被确认为可诱导独脚金种子萌发的天然倍半萜内酯[1]。在随后的研究中,从根系分泌物中鉴定出了20多种与其化学结构相似的寄生植物种子萌发刺激物,统称为独脚金内酯家族(SLs)[12]。Nelson[13]进一步阐明,SLs由寄主在磷饥饿时大量分泌,经KAI2d受体(一种独脚金内酯受体)被种子感知,启动下游ABA降解与胚根伸长。1986年,从寄主高粱(Sorghum bicolor)根提取物中鉴定出的2,6-二甲氧基-对苯醌(DMBQ),成为首个被报道的“吸器诱导因子”[14],主要诱导吸器发育,对种子萌发无显著作用。后续研究扩展了此类因子,包括由寄主木质素解聚衍生而来的酚酸(如丁香酸、香草酸和香豆酸)及其经寄生植物自身过氧化物酶氧化后生成的醌类物质,以及黄酮类化合物等[1]。木质素在寄生关系中扮演着矛盾的双重角色。一方面,寄主木质素的降解产物(如由S型木质素衍生的丁香酸)被证实是强效的HIFs[15],寄生植物自身在响应这些信号时,会主动在根尖沉积木质素,促进其吸器的形成[16]。另一方面,寄主木质素也被证实是抵御寄生植物的物理屏障,当田野菟丝子(Cuscuta campestris)试图附着时,抗性番茄的茎皮层细胞会迅速局部木质化,形成一道坚硬的物理屏障,阻止菟丝子的吸器穿透并建立连接[17];在向日葵(Helianthus annuus)中过表达 HaWRKY29,并直接激活 HaLAC17 表达,诱导了木质素在寄生部位的异常沉积,破坏了列当吸器与向日葵根部维管束的连接,导致列当坏死,寄生失败[18]。木质素在寄生关系中扮演矛盾的双重角色:既是寄主构筑的物理防御屏障,也是寄生植物感知并利用的进攻信号。寄生植物自身也含有这些酚类物质,但为何不自我诱导?近期的一项研究从分子层面揭示了寄生植物如何化解这一矛盾,实现“自我识别”。Xiang等[19]发现,松蒿(Phtheirospermum japonicum)通过尿苷二磷酸-葡萄糖基转移酶UGT72B1,将自身产生的酚类HIFs进行糖基化修饰,使其失活,从而避免在自身或亲缘植物上形成吸器。
吸器诱导因子还可通过启动信号转导级联反应,导致寄生植物根中ROS的积累进而促进吸器的形成。对檀香根部施加DMBQ显著促进吸器发育,同时SaRac1[与激活呼吸爆发氧化酶蛋白Rboh互作进而产生ROS]受到DMBQ的显著诱导,这暗示着SaRac1可能通过ROS生成参与了檀香吸器发育过程[20],通过寄主诱导基因沉默技术(host-Induced gene silencing,HIGS),培育转基因杨树(Populus alba × P. glandulosa),靶向并下调寄生植物中的SaRac1,与野生型或空载体对照组相比,檀香吸器发育受到显著抑制,证实了SaRac1与SaRbohA相互作用协同增强ROS的产生,促进吸器形成[21]。
此外,细胞分裂素、生长素等植物激素也被证实可以诱导根半寄生植物吸器形成。其作用机制可以分为两类:1)细胞分裂素(cytokinin,CKs)可直接启动吸器发生。寄主拟南芥(Arabidopsis thaliana)根系分泌物中的CKs激活独脚金中细胞分裂素受体,激活DMBQ下游相同的转录途径,上调原吸器形成相关基因(ShGH3、ShLBD16)[22]。2)吸器诱导因子触发内源生长素合成。松蒿经DMBQ处理3~6 h后,根表皮生长素生物合成基因YUCCA3显著上调,沉默YUCCA3后,松蒿吸器形成减少[23];此现象与对变色直草果外源施加生长素增加吸器形成的结果一致[24]。
相较于根半寄生植物,关于茎半寄生植物吸器形成诱导机制的研究相对有限,但现有成果已初步揭示其独特的调控模式。在分子层面,广寄生的蛋白质组学分析表明,其吸器形成受多途径协同调控:苯丙素代谢途径通过关键蛋白促进木质素积累,从而驱动吸器形态建成;吸器中显著富集了与内源生长素、茉莉酸、脱落酸以及生长素信号通路相关的基因,在吸器发育20 d后检测到生长素含量的显著提升[25];在环境信号层面,白果槲寄生(Viscum album)等主要依赖物理接触与远红光等环境信号来启动吸器形成,该机制不依赖于独脚金内酯,可能是茎半寄生植物为适应空中寄生生态位而演化出的关键策略[9]。
-
吸器发育是一个连续的生物学过程,可清晰地划分为起始、入侵与传导3个阶段,各阶段伴随特定结构的形成与功能分化。在起始阶段,与寄主接触后,吸器顶端表皮细胞分化为细胞质致密、细胞核增大的侵入细胞(栅栏细胞),共同构成了寄生--寄主界面的肿胀结构;在入侵阶段,侵入细胞定向延伸,穿透寄主组织并最终抵达其木质部导管。传导阶段,吸器中央的细胞则分化为导管分子或管状细胞,通过形成“木质部桥”(吸器)与寄主木质部建立水力连通,完成寄生关系的建立[1]。除木质部连接外,一些半寄生植物,例如锯齿列当(Orobanche crenata)和独脚金在寄主韧皮部形成发育吸器细胞以连接寄主的维管组织[26-27],甚至在锯齿列当与寄主连接的界面上也观察到通过胞间连丝的共质体连续性[1]。
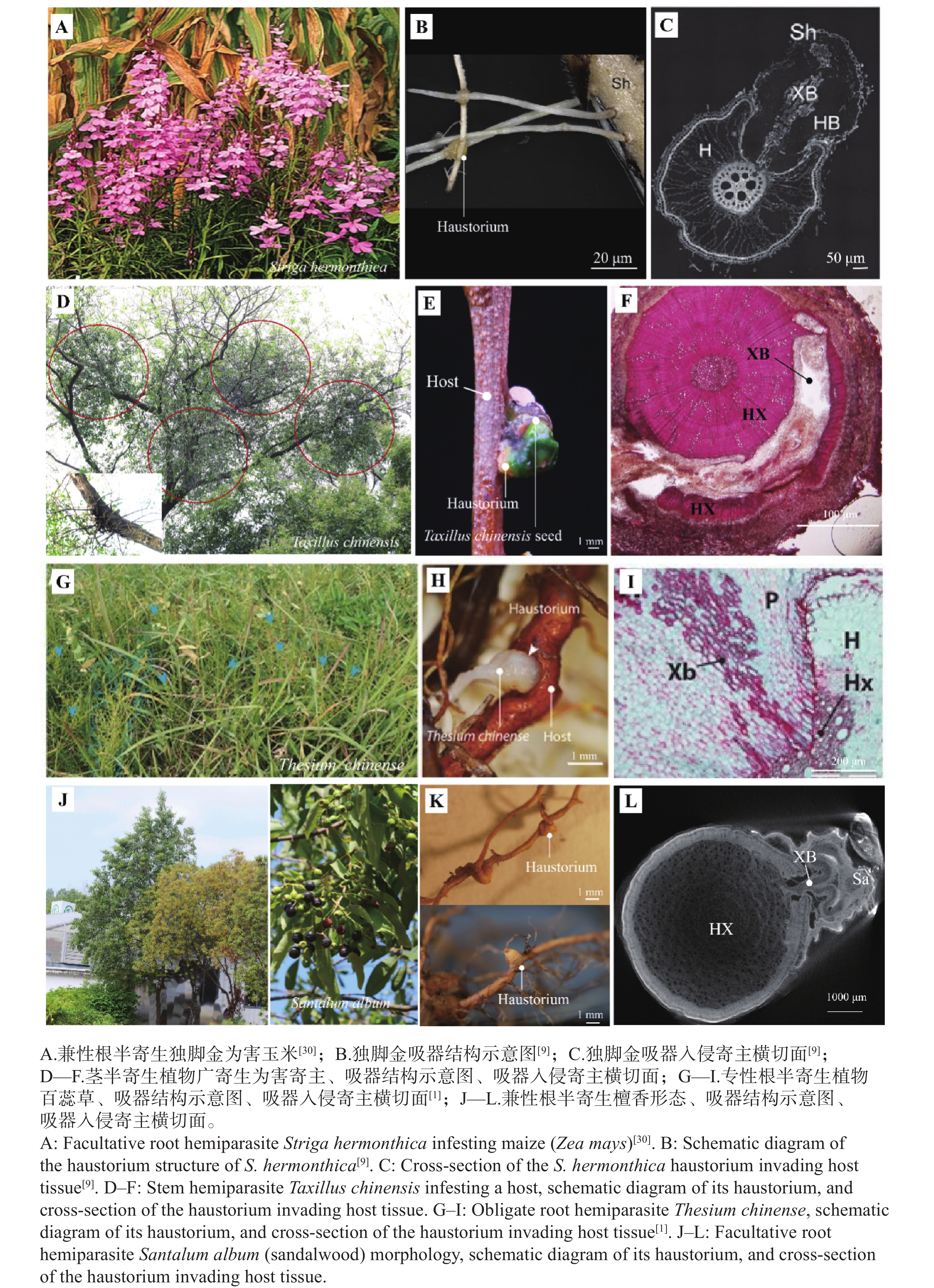
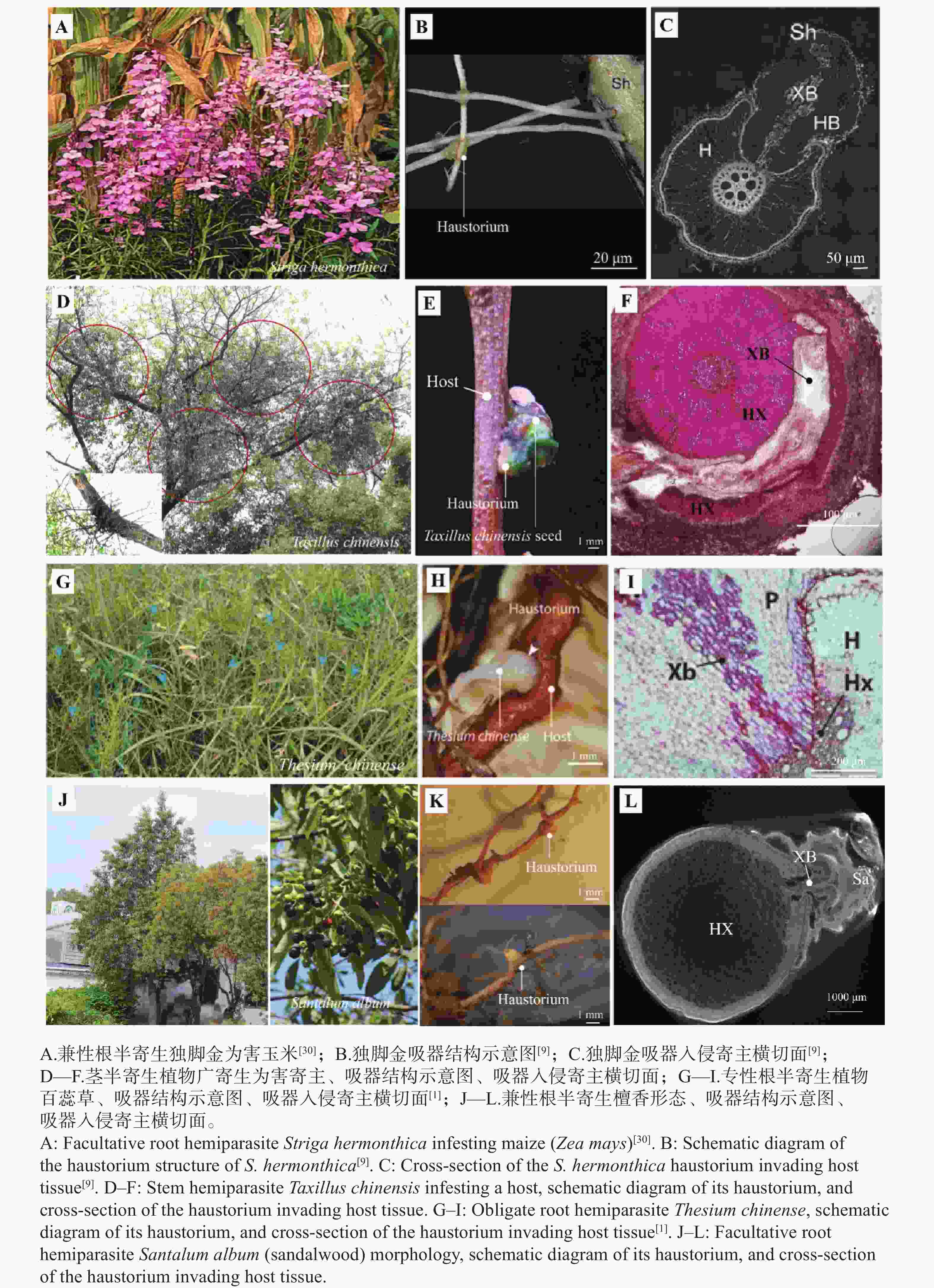
有研究指出,光合作用能力低甚至为零的寄生植物通常会直接从寄主韧皮部摄取养分,全寄生植物如菟丝子(Cuscuta chinensis)和鞭寄生(Hydnora africana)等,由于缺乏功能性叶绿素,无法进行有效光合作用,完全依赖寄主植物提供营养,这些植物通过吸器穿透寄主组织,建立与寄主韧皮部的连接,从中获取糖类、氨基酸等可溶性养分,被称作韧皮部取食者,而其他专门与寄主木质部相连的被成为木质部取食者[28]。但不管光合能力如何,所有寄生植物都与其寄主的木质部建立了功能联系[29](图2)。
-
半寄生植物的吸器解剖结构及物质摄取效率存在明显的种间差异,反映出不同的寄生策略。以独脚金和小鼻花为代表的一年生根半寄生植物,具备高效的溶质摄取能力,其木质部导管与寄主管腔直接连通,形成连续的质外体通道[28],溶质转移主要由寄主与寄生植物间的水势梯度驱动,属于被动运输过程。这类半寄生植物通过维持高蒸腾速率、气孔异常开放[31]以及积累甘露醇等渗透调节物质,使其水势持续低于寄主。相比之下,多年生根半寄生植物则采取相对保守的寄生策略[32],其溶质转移主要通过细胞壁途径或接触薄壁组织实现[29],依赖于主动跨膜运输机制,因其对水势梯度的要求较低,其蒸腾速率与非寄生植物相当,通常很少超过其寄主[31]。
与根半寄生植物不同,茎半寄生植物多寄生于乔木或灌木树种,不仅从寄主木质部取养分和水分,更能占据林冠层的优势位置以获取更充足的光合有效辐射[29]。其溶质转移机制呈现出高度的整合性与可塑性,涉及管腔连通、细胞壁渗透和薄壁细胞传输等多种途径,不同物种、个体乃至单个吸器中各机制的占比存在差异[31]。尽管槲寄生的水势通常低于寄主,但其水势动态多与寄主协同变化,气孔行为也更为常规,不呈现根半寄生植物那样的异常开放模式[33]。
-
寄生植物通过吸器与寄主进行物质交流,除水分和矿质养分外,半寄生植物还能从寄主中转移蛋白质、mRNA和代谢物等大分子,甚至包括病毒和植原体等病原体[34]。Péron等[35]利用羧基荧光素二乙酸酯(CFDA)示踪发现,在寄生-寄主界面上有直接的韧皮部连接,并从寄生植物种分离出3个编码蔗糖转运蛋白的寄主基因,证实寄生植物可通过韧皮部获取寄主植物的光合产物。此外,半寄生植物也能通过吸器向寄主植物传递生长素、脱落酸等激素,调节寄主植物在不同环境条件下的生理响应[36]。以檀香与寄主降香黄檀(Dalbergia odorifera)为例,两者之间存在着氮素的双向传递,且寄主的固氮作用能显著提高它们之间的氮素传递量[37]。
寄生植物能通过基因水平转移(horizontal gene transfer,HGT)完成信息的交换,2010年,寄生植物和寄主间存在核基因的水平转移被首次证明[38];近年来,越来越多的功能性基因转移事件被报道。例如,一个在十字花科中起源的类异胡豆苷合成酶(strictosidine synthase-like, SSL)基因被发现分别转移到分枝列当和南方菟丝子(Cuscuta australis)中,该基因在这两种寄生植物的不同发育阶段和不同组织样品中都具有比较高的转录水平,尤其在营养生长阶段和吸器中的表达量显著提高,这不仅证明了寄生植物和其寄主之间存在着水平基因转移,更证明了该基因在新的寄主背景中仍然执行着重要的功能[39]。
-
寄生植物对寄主的选择偏好性对于揭示其生态策略与进化机制具有核心理论价值,是理解寄生植物与寄主间协同进化过程的关键窗口。阐明偏好性机制能为防控寄生植物提供直接思路,例如通过培育非偏好寄主品种或干扰其化学信号识别以实现精准防控,同时也有助于预测其在农林生态系统中的扩散范围与危害风险。偏好性主要受寄主营养状况(氮、磷含量等)、次生代谢物(防御性生物碱等)及根茎物理结构等因素驱动。
-
多数寄生植物具有较广的寄主范围,这可能与不同的寄主能够提供不同类型的资源有关。半寄生植物在寄生范围方面亦存在显著差异,一些半寄生植物能够寄生数十乃至数百种不同科属的寄主,例如,Castilleja indivisa可以寄生100多科不同科的寄生植物[32]。虽然茎半寄生植物的寄主范围通常小于根寄生植物,但仍有物种具有广泛的寄主范围,例如五蕊寄生(Dendrophthoe falcata)约有400种寄主[40]。因此,完全限定于单一寄主物种的寄生植物极为罕见,多数仍局限于若干亲缘关系较近的寄主[41]。
-
有假说认为,植物寄生是在水分和养分有限的干旱环境中进化而来的[42],在此背景下,氮作为植物生长发育的关键限制性养分,其获取效率可能直接驱动了寄主选择策略的形成于分化。已有研究证实,半寄生植物的寄主选择存在明显的氮偏好性。例如,槲寄生被认为有选择性地寄生在含氮量高的寄主物种上(豆科、禾本科等)上[43];沙漠槲寄生(Phoradendron californicu)在豆科寄主Acacia greggii上的生长速度是在单子圆柏(Juniperus monosperma)的7倍,木质部汁液氮含量是后者的3.5倍[44];寄生在豆科寄主红车轴草(Trifolium pratense)上的小鼻花其株高相较于无寄主处理组提升了一个数量级[45]。然而,半寄生植物主要与寄主的木质部和/或韧皮部连接,这些部位的氮含量非常低。目前,半寄生植物因含氮量高的植物中的何种物质进行了选择,尚未明确。此外,半寄生植物表现出根据不同寄主调整其养分吸收策略的能力,白果槲寄生的营养物质及化学元素组成受寄主种类的影响显著,其生长在木瓜(Chaenomeles sinensis)上时,体内碳水化合物、粗脂肪、粗灰分、镁、钙、钠、铁、锌等元素含量显著高于生长在其他寄主上的个体;而生长在东北杏(Prunus mandshurica)上时,其体内钾、铜和磷的含量则相对更高[46]。
-
寄生植物能够从寄主处获取并积累次生代谢产物,这一特性对其自身的生态适应性的提升具有重要意义,不仅可以增强其对食草动物的抗性,减少取食伤害,还能增加对传粉者的吸引力。以Castilleja indivisa为例,该植物能够寄生在白羽扇豆(Clyde albus)上,而白羽扇豆存在高生物碱和低生物碱两种基因型。研究发现,当C. indivisa寄生在高生物碱型寄主上时,其组织内会大量富集来自寄主的生物碱,进而显著降低了昆虫对其的取食量;与此同时,这类植株的花朵更大,蜂类访花率更高,最终种子产量提升了15%~20%。由此可见,C. indivisa通过选择性寄生在化学防御能力较强的寄主上,直接获得了生存与繁殖上的双重优势[47];在“Phragmanthera austroarabica-Acacia gerrardii”寄生系统中也发现了类似现象,P. austroarabica不仅积累了高达寄主3倍的钾离子,还能特异性地富集寄主特有的防御性酚类与异黄酮,这些次生代谢物在寄生植物组织内积累后,有效增强了其对后续昆虫取食的抵御作用[48]。
-
寄主植物的根、茎结构也会影响半寄生植物 的寄主选择,半寄生植物更倾向于选择维管系统易被接触和穿透的寄主,例如,甘肃马先蒿对禾本科的偏好主要与禾本科植物根部构型特点相关:在土壤压实的环境下,禾本科植物通常会形成大量水平分布的纤维状小根,这种根部结构增加了其被根半寄生植物识别和攻击的概率[49]。与之相反,部分植物会通过结构防御寄主抵御寄生植物的入侵:滨菊(Leucanthemum vulgare)可通过诱导自身组织木质化,将小鼻花吸器包裹,阻止根寄生植物穿透其根中柱[50];水稻(Oryza sativa)通过内皮层细胞壁加厚并木质化,使独脚金吸器进入皮层后即被“封死”,阻断吸器推进,无法穿越内皮层到达中柱[51]。这可能暗示着寄主木质化程度更高,其抵御寄生植物入侵的能力越强。
-
半寄生植物通过吸器从寄主植物中摄取水分、矿质养分(如氮、磷、钾、钙、镁)及碳源,并将其大量积累于自身组织,同时消耗寄主的非结构性碳水化合物储备,从而影响寄主的生理过程,包括水分吸收、光合作用及矿质养分,常导致寄主植物生长减缓、生物量降低、叶片形态改变、花期与种子成熟期提前,并削弱其应对其他环境胁迫的能力。尽管半寄生植物很少直接导致寄主死亡,但其对寄主生理功能的长期影响是深远的,大部分寄生植物会抑制寄主植物的生长,但也有一些寄生植物寄生在寄主植物之后,对寄主植物产生促进效应或不显著的生态学效应。
-
半寄生植物通常会显著抑制寄主的光合与蒸腾作用,其典型表现为降低寄主的净光合速率、气孔导度,并改变其光合结构的功能[52]。无根藤(Cassytha filiformis)侵染降低了寄主荆豆(Ulex europaeus)和金雀花(Cytisus scopariu)的最大电子传递速率和光系统II效率,从而诱发了寄主植物的慢性光抑制[52];云杉矮槲寄生(Arceuthobium sichuanense)侵染青杄(Picea wilsonii)后显著降低寄主净光合速率、蒸腾速率及水分利用效率,改变寄主对环境因子的响应顺序[53]。
-
半寄生植物虽然具备一定的光合能力,但其碳源主要依赖于与对寄主有机碳的摄取。放射性14CO2标记实验已在多种根半寄生组合中证实,有机碳可从寄主向半寄生植物流动:在寄主高粱(Sorghum bicolor)上的非洲独脚金(S. hermonthica)和独脚金,高δ13C值检测结果表明,寄主碳在两种独脚金成熟叶片生物量中的占比分别高达28%和35%[54]。先前的研究采用相同方法评估了多种半寄生植物的碳收支,发现寄主同化物贡献了寄生生物量的20%~80%,具体比例因物种种类和发育阶段而异[55]。P. austroarabica通过维持远低于寄主金合欢的水势和渗透势,通过1.7倍于寄主的气孔导度和1.4倍于寄主的蒸腾速率,高效地摄取寄主的水分和矿质养分,使其体内钾离子浓度积累到寄主的3倍[48]。
-
半寄生植物通常具有比寄主更高的蒸腾速率和更低的水分利用效率,其根本动力来源于半寄生植物与寄主之间显著的水势梯度——半寄生植物通过维持比寄主更低(更负)的叶片水势,确保水分沿木质部从寄主单向流向自身[31]。在“小鼻花-大麦(Hordeum vulgare)”寄生系统中,小鼻花寄生后,其吸收水分、沉积和蒸腾作用显著增加,大部分水分以木质部汁液的形式从寄主体内摄取,消耗寄主最初吸收的总水分的20%左右[6]。如果在水分供应充足,养分不受限制的条件下,松槲寄生(Pine mistletoes)与寄主可以长期共存,但在干旱时期水分有限,半寄生植物的高耗水量和低水分利用效率可能会加剧寄主的干旱胁迫,导致寄主气孔关闭以节约水分,对寄主的生长产生负面影响[56]。
-
半寄生植物由于不需要在根部进行投资,其摄取水分和养分的成本可能远低于它们的寄主,但它们通常具有更高的蒸腾速率和气孔导度通常比寄主高,但叶面积却比寄主小,导致水分利用效率低。人们提出各种假设来解释这种模式:1)“氮寄生”假说认为槲寄生受到氮获取的强烈限制,因此,它们以非常高的蒸腾速率工作,以便在寄主木质部流中获得足够的氮[44];2)“碳寄生”假说认为槲寄生较高的蒸腾速率可能不仅受到对碳的需求的驱动,而且还受到通过寄主木质部以氨基酸形式获得大量碳的能力的驱动,即槲寄生中的部分碳实际上以氨基酸的形式从寄主木质部向寄生转移[45];3)磷寄生”假说则认为寄生的高蒸腾作用可能有助于在磷有限的地点从寄主中获取磷[57]。
最新的研究为“氮寄生”假说提供了依据:Zhang等[58]对中国西南地区4个地点的11种槲寄生和104种寄主的11种营养元素、2种同位素比值和2种叶片形态特征进行了测定,结果表明,槲寄生的磷、钾、硼含量显著高于寄主,氮同位素比(δ13N)显著高于寄主,碳同位素比(δ13C)显著低于寄主;且随着寄主氮浓度的增加,槲寄生的δ13C及与寄主的δ13C差值均增大(δ13C通常为寄生吸收强度的表现),表明寄生与寄主在有选择地竞争氮元素。此外,槲寄生异养性的计算方法仍存在争议,此后仍需要做更多的工作来证伪“磷寄生假说”和“碳寄生假说”。而Zhang的研究为“氮寄生假说”提供了强有力的野外证据,但其并未证伪“碳寄生”与“磷寄生”假说,二者可能在特定物种或磷极度匮乏的生境中起主导作用,未来需结合控制实验与多元素计量学方法,明确不同养分需求在驱动半寄生植物水分耗散中的相对权重。
-
部分研究发现,寄主植物被半寄生植物侵染后,其光合速率反而升高,可合成更多有机物,为半寄生植物提供充足养分。例如,Acacia ampliceps、白龙树(Sesbania Formosa)为寄主的檀香,其光合速率显著高于以非豆科植物为寄主或无寄主的个体,这可能与豆科植物能为檀香提供更多的氮源有关[59]。在一些根寄生植物-寄主系统中,与未被侵染的寄主相比,被侵染的寄主可能表现出更高的光合速率和养分吸收能力[32, 61],虽然这种对光合作用的积极影响并没有反映在寄主的生长中,仅使寄主的相对生长速率出现短暂的增加。有研究表明,寄主光合能力的增强可能是为了补偿被寄生植物摄取的有机化合物[62]。
在养分适宜的环境中,半寄生植物对寄主植物影响不显著。例如,柔毛槲寄生(Phoradendron villous)对沼生栎(Quercus palustris)的生长及存活无明显影响[63];另有研究显示,移除欧洲赤松(Pinus sylvestris)上的槲寄生后,寄主氮的可利用性、碳摄取量、氮富集程度及寄主的生长速率均较为移除槲寄生的寄主有所提升[64]。
综上,寄生植物对寄主的影响是复杂多变的(表1),其净效应取决于具体的物种组合、环境条件以及评估的生理指标。要全面解析其内在机制,必须对更多样的半寄生植物-寄主系统在不同环境梯度下进行深入研究。
专性根半寄生植物
Obligate root hemiparasites兼性根半寄生植物
Facultative root hemiparasites茎半寄生植物
Stem hemiparasites主要负面影响
Negative impacts资源竞争:强烈抑制寄主生长与生物量;大量掠夺水分与矿质养分(如氮、磷)。
生理胁迫:降低寄主光合与蒸腾效率,削弱其抗逆能力。
结构损害:吸器入侵可能破坏寄主维管组织资源竞争:强烈抑制寄主生长与生物量;大量掠夺水分与矿质养分(如氮、磷)。
生理胁迫:降低寄主光合与蒸腾效率,削弱其抗逆能力。
结构损害:吸器入侵可能破坏寄主维管组织1. 资源竞争:夺取寄主水分、矿质及部分光合产物;干旱时加剧寄主水分胁迫。
2. 结构损害:常导致寄主枝条枯死(“枝条自弃”)。
3. 传播病害:可能作为病毒、植原体等病原的传播媒介主要正面影响
Positive impacts生态系统层面:
1.调节群落:抑制优势种,促进物种共存与多样性。
2.促进循环:释放高质量凋落物,加速养分循环生理层面:
1. 双向互利:与特定寄主(如豆科)可能存在氮素等养分的双向交流。
2. 防御协同:可能传递抗虫信号,增强系统防御生态/系统层面:
1. 支持生物多样性:为鸟类、昆虫等提供独特食物与栖
息地。
资源输入:其富营养凋落物可局部提升土壤肥力主要作用机理与背景条件
Mechanism and context机理:建立高效吸器,维持极低水势,进行被动、单向的资源掠夺。
条件:其生态正面效应是强烈寄生压力下产生的间接结果,在资源匮乏的生态系统中尤为显著机理: 依赖程度可变,物质交换可能更复杂(如双向氮素传递)
条件:与高营养寄主(如豆科)连接时,可能实现互利;与低营养寄主连接时,表现为偏为害寄主或弱寄生机理:占据林冠优势位,既从寄主木质部获取资源,自身也进行光合作用;水力结构更安全。
条件:作为专性寄生生物,其存在本身就构成了特殊的生态位,正面效应是其长期与寄主及环境协同进化的系统性产物Table 1. Summary of positive and negative impacts of major hemiparasitic plant types on their hosts
-
在自然群落中,半寄生植物与寄主易受到干旱、温度变化、光照不足及食草动物取食等等多重环境胁迫。在此背景下,二者通过协同进化形成了一套动态的生存策略体系,其相互作用在资源竞争与信号互作中集中体现。
-
水分胁迫下,半寄生植物与寄主间的水分竞争尤为激烈,并展现出不同的水分生理策略。半寄生植物槲寄生在长期的干旱条件下,表现出“水力安全型”策略,在生理结构上表现出较寄主更小的水力导管直径、更小的导管面积指数以降低水分利用效率,表现出较寄主更厚的导管细胞壁、更大的导管密度等以增加水分运输安全,同时抗木质部栓塞性较寄主更强,以此优先保障水分运输的安全性[65]。与之相对,许多木本寄主植物则是表现出了“水力效率型”策略,表现出较寄主更低的叶片水势、膨压损失点,在生理结构上较寄主更小的水力导管直径、更小的气孔导度等以提高水分运输效率,表现出较寄主更强的耐旱性[65]。
值得注意的是,槲寄生具有更高的蒸腾速率却表现出较低的水分利用效率,这或许并非资源“浪费”,而是一种积极的生存权衡:其高蒸腾速率很可能是为了从稀薄的木质部汁液中摄取足量氮、磷等矿质养分,同时将有限的碳资源更多地分配给生长和繁殖,而非用于合成光合酶或构建庞大的根系。寄主植物通常通过提高脱落酸(ABA)水平、调整气孔开度、重新分配资源等生理调节机制应对半寄生植物的水分竞争[66]。例如,被小鼻花寄生后6~12 h,寄主大麦根系中ABA浓度提升2~4倍,以诱导气孔关闭、降低冠层蒸腾,试图逆转水势梯度[66]。但也存在例外情况,部分半寄生植物在干旱条件下维持高蒸腾速率、极低水势,其气孔对ABA不敏感且持续开放[67]。目前,关于寄生植物在干旱条件下应对寄生植物水分竞的生存策略研究还比较少,其内在机制有待深入研究。
-
在热带与高湿度生境中,水分与养分的稀缺性下降,光照与空间成为首要限制资源。槲寄生实施“空间与光资源抢占”策略:其种子多经鸟类消化道脱胶后散布于林冠高位枝条[65],吸器穿透木栓层后即永久锚固于次生木质部,直接占据林冠高位,在维持光合能力的同时,仍从寄主摄取半数以上的碳源[68]。针对槲寄生的资源抢占,寄主发展出多种结构性防御策略,形成长期共存但脆弱的平衡:一是瘤状体包裹,即寄主木栓形成层在吸器周围异常增殖,形成木质化瘤体,将吸器机械隔离于活跃输导组织之外,降低水分与氮流失;二是枝条自弃,对重度寄生枝实施程序性脱落,既减少碳汇损失,又避免寄生在林冠内水平扩散;脱落伤口快速形成保护性木栓层,降低二次感染概率[69]。
-
半寄生植物与寄主植物在自然界中易受食草动物和病原体等生物胁迫,其中虫害胁迫下的信号转导是一个新兴但快速发展的研究领域,近年研究表明,半寄生植物在虫害胁迫下不仅是资源获取者,更在植物间信号传递中扮演关键角色。以菟丝子为代表的旋花科寄生植物,在遭受蚜虫取食后,可通过跨界mRNA转运及激素信号调控,诱导寄主植物产生系统性抗虫响应[70]。具体而言,虫害胁迫显著增强了菟丝子与黄瓜(Cucumis sativus)之间的mRNA双向交流,并引发茉莉酸(JA)与水杨酸(SA)在寄主植物不同组织中的特异性积累,从而激活下游防御基因表达,提高寄主对虫害的抵抗能力[71]。
作者团队前期在对“檀香-降香黄檀”寄生系统应对黑肾卷群夜蛾(Plecoptera oculata,以降香黄檀为食的最常见的害虫之一)取食下的信号转导研究发现:经黑肾卷群夜蛾取食的降香黄檀释放出5种挥发物,均对黑肾卷群夜蛾取食起到一定抵御作用,由檀香释放的4种挥发物对随后的檀香粉蝶(Delias pasithoe)亦起到一定的抵御作用。同时,黑肾卷群夜蛾取食降香黄檀后,降香黄檀叶片中的JA、SA含量显著增加,寄主植物檀香中的JA相关含量显著增加,寄生-寄主植物系统中,与JA合成的相关基因表达显著上调,这表明该体系中的系统信号可以通过吸器转移,且寄主降香黄檀受到虫害胁迫后可以增强邻近寄生植物对檀香的食叶昆虫抗性[72]。
-
利用半寄生植物控制外来入侵植物是一种基于生态互作的生物调控策略。研究人员已利用半寄生植物(尤其是根半寄生植物)对寄主植物偏好性的特点,引入半寄生植物来抑制群落中的外来入侵种,保护乡土植物的物种多样性,加速群落的恢复。例如,根半寄生植物毛鼻花(Rhinanthus alectorolophus) 能在1~2 a消灭入侵植物拂子茅(Calamagrostis epigejos),其作用机制可能是以干扰其地下储藏和生长实现的[73];根半寄生植物田野山萝花(Melampyrum arvense)可减少入侵植物80%~90%的地下根茎生物量,并在4 a内将入侵植物Soligago gigantea、Symphyotrichum lanceolatum的地面覆盖率从90%降至8%~12%[74]。
-
对于独脚金、槲寄生、广寄生等危害较大的寄生植物,常使用除草剂处理或人工清除,但普遍存在着易复发、难以彻底清除的问题。随着分子生物技术的发展,半寄生植物的防治手段也逐渐从传统方法转向基于分子机制和寄主改良的精准防控策略。通过基因编辑( CRISPR-Cas9 技术等)敲除或抑制关键独脚金内酯转运蛋白基因,可减少寄主产生的吸器诱导因子:寄主通过基因突变(如高粱中的 lgs1 基因功能丧失),从寄生植物偏好的5-脱氧独脚金醇转变为偏好度较低的列当醇,从而显著降低寄生植物种子的萌发率[75];最新的研究表明:单独或联合敲除高梁中独脚金内酯转运蛋白 (SbSLT1 和 SbSLT2) 可以通过破坏独脚金内酯合成显著削弱独脚金萌发[76]。
此外,部分微生物也参与寄生植物的防治。内生真菌通过调控紫花针茅(Stipa purpurea )根系形态特征,增强紫花针茅根系和地上生物量以缓解甘肃马先蒿对其根系的寄生危害[77];丛枝菌根真菌通过抑制吸器连接和半寄生植物马先蒿(Pedicularis rex)的生长,显著减轻了对寄主的寄生效应[78];丛枝菌根真菌摩西球囊霉(Glomus mosseae)和根瘤菌(Rhizobium leguminosarum)共生,减轻了根半寄生植物马先蒿、三色马先蒿(P. tricolor)对豆科寄主白车轴草(Trifolium repens)的损害[79]。
-
半寄生植物是自然群落中的一种特殊的组成类群,其可直接影响寄主植物的生长发育且大部分半寄生植物对带来的影响是消极的,但在生态群落中又具有一定的积极意义。半寄生植物种类繁多,主要分布在热带和亚热带区域,在气候变化的背景下,寄生关系也将有所变化,对热带和亚热带地区的植物生态也可能带来威胁。因此,进行半寄生植物寄生机制、与寄主间寄主关系的研究,有助于推动半寄生植物的发展。半寄生植物与寄主之间的关系,未来可从以下4个方面深化研究:
1)聚焦半寄生植物吸器动态形成发育过程。半寄生植物吸器的形成发育是一个连续且快速的过程,部分根半寄生植物在受到吸器诱导因子的几个小时内就形成,而部分茎半寄生植物需长达数周的时间才能形成,且吸器与不同寄主建立连接的部位有所差异(木质部/韧皮部),这可能涉及到寄生植物在体内摄取的物质的差异。目前对于半寄生植物吸器解剖结构的分析已然良多,但对吸器形成的连续监测目前仍缺乏,需要对半寄生植物吸器的形成原因出判断与验证,可为半寄生植物的防治提出理论依据;对吸器与寄主的连接部位,有利于综合分析寄生植物对寄主植物水分、矿质养分、光合产物的影响途径,明确半寄生植物的寄生机制。
2)拓展半寄生植物寄主研究范围。目前,半寄生植物相关研究多集中于根半寄生植物与其多种寄主的寄生关系上,而茎半生植物由于其只能寄生于寄主茎部的局限性,其对于寄主的偏好性、与寄主间的物质、信息交流等,仍需通过更多的寄主互作进行探索。长期以来,半寄生植物与寄主间的寄生关系,更多地集中于寄生植物对寄主植物的生理影响,未来还需要关注寄生植物的特性对寄生植物的影响,阐明半寄生与寄主植物间的寄生关系,这可能面临着更大的空间维度和更长时间尺度的考验。
3)探索寄生关系的动态变化。在各种气候环境下,半寄生植物由于根系的退化需要一系列的生理调控,例如维持更高的蒸腾速率更低的水势从寄主中摄取足够的养分,而寄主则面临着气候胁迫与植物寄生的双重挑战,寄主将在水分调控、物质分配甚至生理结构上做出如何响应?目前对于寄生植物在干旱条件下应对寄生植物水分竞争的生存策略研究还比较少,特别是广寄生一类的茎半寄生植物,其根系基本完全退化,完全依靠吸器从寄主茎中摄取水分和养分,在气候变化中,广寄生与寄主植物将会做出何种响应,需要进一步从植物生理、结构上综合研究。
4)整合分子调控手段与抗寄生性状筛选,助力抗寄生物种育种进程。未来研究可进一步整合多组学数据与表型组学分析,系统解析寄主植物在寄生压力下的应答网络,挖掘关键抗性基因与调控元件。在此基础上,可利用CRISPR-Cas9、HIGS等基因编辑技术,精准调控寄主中与寄生识别、吸器形成抑制、防御信号激活相关的基因表达,创制具有稳定抗寄生性状的种质资源。同时,结合高通量表型筛选与人工智能辅助育种,建立寄主抗寄生性状的快速评价体系,实现从基因到表型的精准选育。此外,应重视田间生态适应性评估,确保抗性品种在复杂农田生态系统中的稳定表现。通过分子设计育种与传统育种的有机结合,有望培育出兼具抗寄生性与农艺性状优良的新品种,为可持续农业与林业生产提供种源保障。
半寄生植物作为寄生被子植物的重要组成部分,其与寄主之间的相互作用是一个复杂且动态的生态过程。
-
本文系统综述了半寄生植物吸器的形成机制、寄主选择偏好、半寄生植物与寄主间的相互作用及“半寄生植物-寄主植物”体系在环境变化下的适应策略以及对半寄生植物的应用与防治,揭示了其在生态系统中的双重角色——既是资源竞争者,也是生态调节者。当前研究虽已在分子机制、生理响应和生态效应等方面取得显著进展,但仍存在诸多未解之谜,如吸器发育的实时动态、寄生-寄主互作的环境可塑性等。未来研究应进一步整合多学科方法与技术,从微观机制到宏观生态多个层面深化对半寄生植物寄生关系的理解,并为基于生态原理的寄生植物管理与应用提供科学依据。
The parasitic relationship between hemiparasitic plants and host plants
DOI: 10.15886/j.cnki.rdswxb.20250150
- Received Date: 2025-10-22
- Accepted Date: 2026-01-06
- Rev Recd Date: 2025-12-30
-
Key words:
- Hemiparasitic plants /
- haustorium /
- parasitic relationship /
- survival strategy
Abstract: Hemiparasitic plants account for approximately 80% of parasitic species. Although they possess chlorophyll and retain a certain capacity for photosynthesis, these plants establish parasitic connections with their host plants via specialized structures called haustoria, which are attached to the host's stems or roots. Through these connections, hemiparasites extract substantial amounts of water and nutrients from their hosts to sustain their own growth. By imposing long-term nutrient stress on their hosts, hemiparasites not only severely inhibit host growth and development but also exacerbate the host's vulnerability to environmental changes, leading to significant economic losses in agriculture and forestry. A review was made to systematically elaborate on the parasitic relationship between hemiparasitic plants and their hosts, covering the formation, structure, and function of haustoria, host preferences, and the physiological impacts on hosts. This review also analyzes the survival strategies of hemiparasitic plants under changing environments, as well as their applications and control methods in ecosystems. Furthermore, the review discusses research trends in hemiparasitism and proposes future research directions, including focusing on the dynamic processes of haustorial development, expanding the scope of host studies, and elucidating the dynamics of parasitic relationships under environmental changes. Additionally, it highlights the integration of molecular regulation approaches and the screening of anti-parasitic traits to facilitate the breeding of parasitic-resistant species, aiming to provide valuable references for in-depth research into the physiological and ecological characteristics of hemiparasitic plants.
| Citation: | Liu Yunshan, Meng Sen, Qin Fangcuo, Lu Junkun. The parasitic relationship between hemiparasitic plants and host plants[J]. Journal of Tropical Biology. doi: 10.15886/j.cnki.rdswxb.20250150 |






 DownLoad:
DownLoad: