-
红树林湿地生态系统具有较高的生物多样性,是亚热带和热带海岸带独有的水域生态景观,是地球上生产力最高的海洋四大自然生态系统之一[1],也是世界上最濒危的生态系统之一[2]。近几十年,因沿海人类的活动产生大量环境污染物进入红树林湿地导致红树林湿地环境受到污染,特别是重金属(Hg,Cd,Ni,Pb,Cu,Cr,Zn)在红树林湿地的植物及动物群中大量累积,严重危害红树林的生态系统健康[3]。随着对红树林湿地环境保护意识的增强,红树林湿地重金属污染的相关研究受到普遍重视[4]。有研究表明,这些主要来自于外源河流和排污等的红树林沉积物是重金属的主要受纳场所,沉积物中重金属含量远高于水体中的;同时沉积物中的重金属会向水体释放,成为重金属污染的源头[5]。因此,红树林沉积物作为重金属的主要源和汇,其中重金属的形态转化与环境迁移及其生态毒性密切相关[6]。沉积物老化会对重金属进入沉积物中的物理化学行为等产生一系列影响[7],包括沉积物老化过程中伴随着形态变化,其变化过程主要是从有效态转变成非有效态,从而影响重金属的迁移转化规律[8]。笔者在海南东寨港红树林及其邻近区域选择了3个不同地理特征的区域,采用改进的BCR连续提取法研究红树林沉积物中重金属铅的赋存形态,分析在红树林沉积物老化过程中的老化时间、外源铅浓度以及沉积类型对铅赋存形态的影响,探索外源铅进入红树林沉积物后的环境化学行为。目前,国内外学者主要研究了沉积物老化过程对湖泊、河口和土壤等介质中重金属的影响[9],但对红树林沉积物涉及较少。因此,笔者研究在外源铅污染环境下,红树林沉积物中的重金属形态随时间迁移转化的规律,旨在对近岸海域生态环境污染的风险评估和治理提供参考。
HTML
-
东寨港红树林湿地位于海南岛东北角港湾内(110°32′~110°37′E,19°51′~20°01′N),通过北端北港岛两侧的潮汐通道连接琼州海峡,属热带季风气候[10]。该湿地中央呈半封闭式的漏斗状潟湖,港湾内海流平缓,入港的4条河流为港内带来大量的泥沙,形成深厚的沉积物[4]。2018年8月笔者在东寨港红树林湿地以海榄雌(Avicennia marina)为主的区域,选取3个不同地理特征的位置作为采样区域,其中区域A位于红树林低潮位处、B为高潮位处、C为红树林附近人为干扰较多的潮间带光滩。在3个采样点,分别用塑料铲随机选取5份表层沉积物(2~5 cm),密封于封口袋中,尽快带回实验室。在实验室分别将各采样点的5份样品充分混合后,风干,研磨,过2 mm筛备用。
-
采用综合法[11]测定沉积物的粒径,并采用Shepard的沉积物粒度三角图解法分类命名。沉积物的pH采用电位法测定,土水比为1∶5[12]。含水率和TOC分别根据国家标准(GB 17378.5-2007)[13]中的重量法和重铬酸钾容量法—外加热法测定。电导率根据环境标准(HJ 802-2016)[14]中的电极法,用电导率仪(DDSJ-308A,上海精密科学仪器有限公司)测定。沉积物中的总氮和总磷含量参照文献[12]中的凯氏定氮法和高氯酸—硫酸法进行测定。
-
采用硝酸铅水溶液作为外源铅添加到沉积物样品中。每种沉积物添加外源铅的浓度均按照0,25,250,500,1 000,2 000 mg·kg−1进行设置,每个浓度设置3个平行,每份样品为120 g沉积物,随后同时进行老化培养。老化培养期间,适时补充适量的去离子水以维持沉积物湿度。在老化培养30,60,120 d分别取样,室温风干,研磨过0.063 mm筛,装于塑封。参照改进的BCR法[15]测定铅的赋存形态:
(1)酸可提取态:沉积物干样过0.063 mm筛,定量取样品,于离心管中,加入相应的 0.11 mol·L−1醋酸溶液,室温振荡16 h。离心,取上清液,加入适量浓硝酸,4 ℃保存。超纯水清洗残渣,用于还原态的测量。
(2)可还原态:加入定量的盐酸羟胺(0.5 mol·L−1)于残渣,HNO3调整pH至1.5,振荡后离心,其后操作同步骤(1)。清洗残渣,用于氧化态的测量。
(3)可氧化态:往残渣中逐滴、缓慢加入H2O2(8.8 mol·L−1)溶液,室温下消解1 h,水浴(85 ℃)1 h。最后加热使溶液体积少于3 mL。凉置后,逐滴加入H2O2溶液,操作同上。冷却后,加入相应体积的 1.0 mol·L−1醋酸铵溶液(pH≈2)。其余操作与同步骤(1)。
(4)残渣态:差值法得到,即用全量减去前面3种形态的量。
-
采用微波消解/萃取仪(Touchwin4.0,奥谱勒仪器有限公司制造)消解沉积物中的重金属,后用火焰原子吸收光谱仪(AAS400,德国耶拿分析仪器股份有限公司)测定铅的含量。
-
实验数据采用SPSS 17.0作One-way ANOVA单因素方差分析,用Duncan做显著性检验,并用GraphPad 6.02进行绘图。
1.1. 研究区域与样品采集
1.2. 沉积物理化性质测定
1.3. 沉积物外源铅的老化实验设计
1.4. 铅含量的测定
1.5. 数据处理方法
-
从表1可见,沉积物A、B、C中pH、含水率、总有机碳、总氮/磷含量和电导率均差异显著(P<0.05),其中pH大小关系为A>C>B。沉积物C中的含水率、总有机碳、总氮/磷和电导率均为最大,沉积物C中含水率分别是沉积物A和B的1.5倍和1.9倍;沉积物C中总有机碳含量分别是A和B的3.2倍和2.8倍;沉积物C中总氮含量分别是A和B的1.9倍和2.7倍,沉积C的电导率也远高于A和B的。沉积物C的粒径分布与A和B的差异较大,C中黏土含量最高,分别是 A的3.9倍,B的2.0倍。整体来看,沉积物A与B的理化性质差别较小,与沉积物C的相差均较大。
沉积物编号
CodepH 含水率/%
Moisture
content总有机碳/%
Total organic
carbon总氮/
(g·kg−1)
Total N总磷/
(g·kg−1)
Total P电导率/
(μS·cm−1)
Conductivity粒径分布/% 粘土
Clay粉砂
Silt砂
SandA 7.40±0.04 26.9±0.03 2.65±0.03 0.42±0.01 0.53±0.05 2 115±12 9.05 86.84 4.11 B 6.03±0.06 21.7±0.02 3.02±0.01 0.29±0.03 0.33±0.04 2 195±15 17.66 78.16 4.18 C 7.03±0.02 41.6±0.02 8.44±0.02 0.79±0.04 0.63±0.02 9 870±7 34.9 54.57 10.53 Table 1. The physio-chemical properties of sediment samples
-
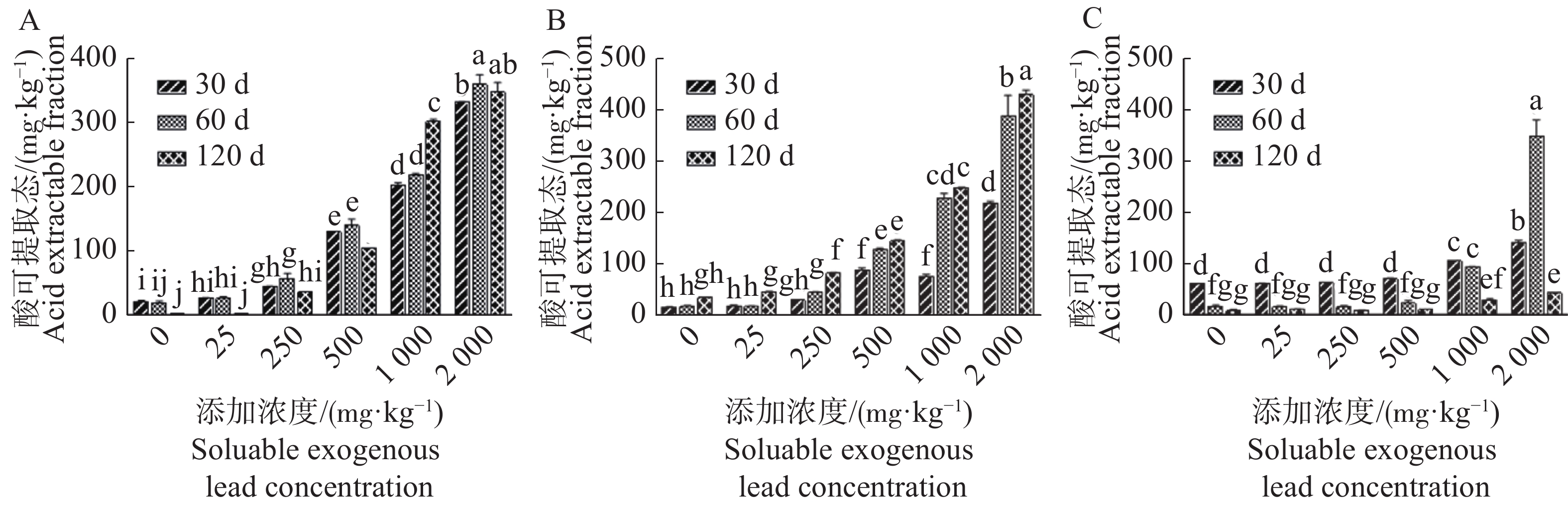
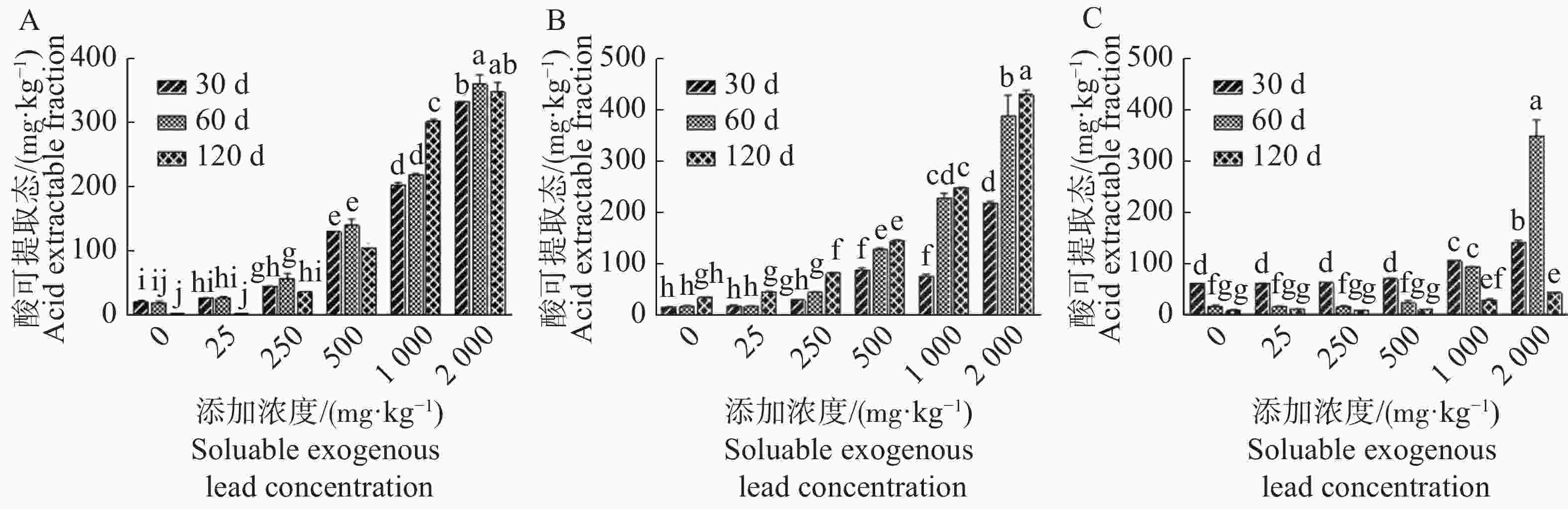
可溶性外源铅进入3种沉积物中,在不同老化时间(30,60,120 d),铅的各赋存形态变化趋势见图1~4。在A沉积物(图1A)中,同一添加浓度下(除 2 000 mg·kg−1外)老化30 d与60 d后,发现铅的酸可提取态含量无显著差异,但老化120 d后铅的酸可提取态含量在添加浓度为25,250,500 mg·kg−1较30 d和60 d显著降低(P<0.05),其中250 mg·kg−1浓度下老化120 d后酸可提取态的含量较60 d降幅最大,达到35.7%。B沉积物(图1B)中,同一添加浓度下(0,25,250 mg·kg−1),铅的酸可提取态含量在老化30 d与60 d时无显著差异,但老化120 d时较30 d和60 d差异显著(P<0.05),其中在250 mg·kg−1浓度下显著增加165.2%和80.3%(P<0.05);在500,1 000,2 000 mg·kg−1添加浓度下,同一处理老化30 d和60 d后铅的酸可提取态含量差异显著,但老化120 d后(除2 000 mg·kg−1)较60 d无显著差异。C沉积物(图1C)中,同一添加浓度(除1 000,2 000 mg·kg−1外)下,各处理沉积物铅的酸可提取态在老化30 d下较老化60,120 d显著增加,但老化60,120 d下无明显差异,当添加浓度为2 000 mg·kg−1时,酸可提取态在老化60 d含量最高,较30 d和120 d分别显著增加1.45倍和6.99倍(P<0.05,Duncan’s检验)。
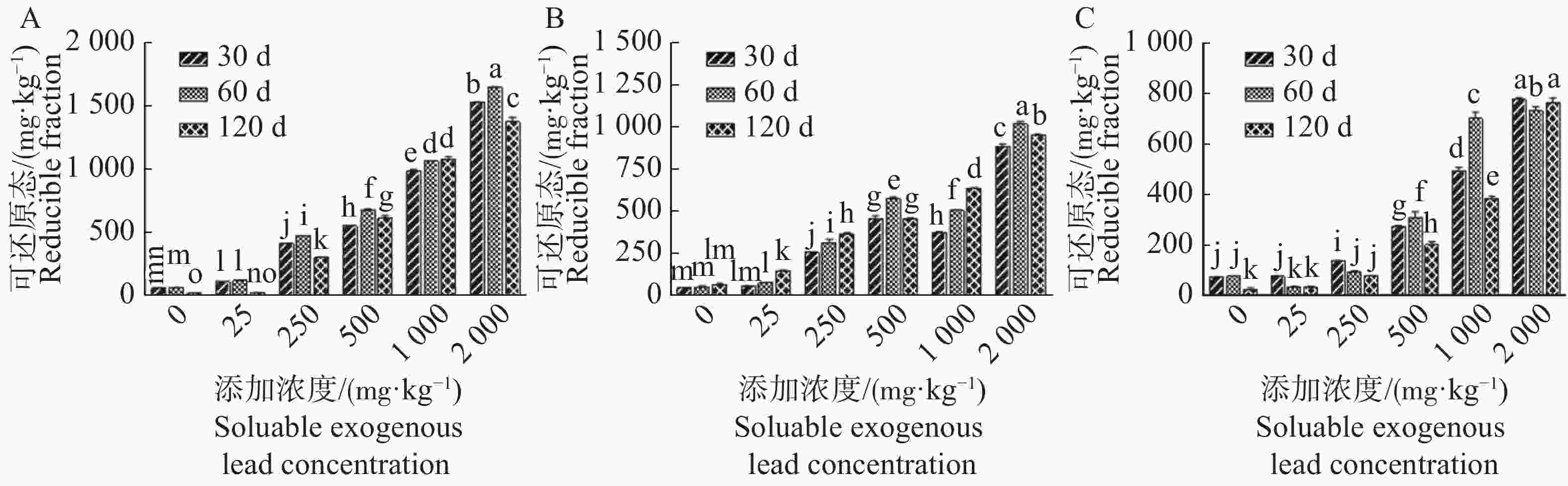
A和B沉积物中,同一添加浓度(0,25 mg·kg−1)下铅还原态含量在老化30 d和60 d下差异不大。随着添加浓度的增加(250,500,1 000,2 000 mg·kg−1),同一污染条件下铅还原态含量在老化30 d和60 d显著增加,但老化120 d下铅还原态含量在A和B沉积物中变化不同,其中A沉积物中铅还原态含量在老化120 d下较60 d均显著降低(除1 000 mg·kg−1下无差异外),B沉积物中在添加浓度为250 mg·kg−1和1 000 mg·kg−1下老化120 d后铅还原态含量较60 d显著增加,分别增加16.74%和26.22%,在添加浓度为500 mg·kg−1和2 000 mg·kg−1下老化120 d后铅还原态含量较60 d显著降低,分别降低25.32%和6.75%(图2A和B,P<0.05)。在沉积物C中,添加浓度为25 mg·kg−1和250 mg·kg−1下,老化60 d和老化120 d下铅可还原态含量差异不大,较老化30 d均显著降低。当添加浓度为500 mg·kg−1和1 000 mg·kg−1时,铅还原态含量在3个老化时间下差异较大(P<0.05),随老化时间的延长呈先增加后降低的趋势,其中在1 000 mg·kg−1时老化120 d较老化60 d显著降低45.17%,添加浓度至2 000 mg·kg−1时铅可还原态略有增加(图2C)。
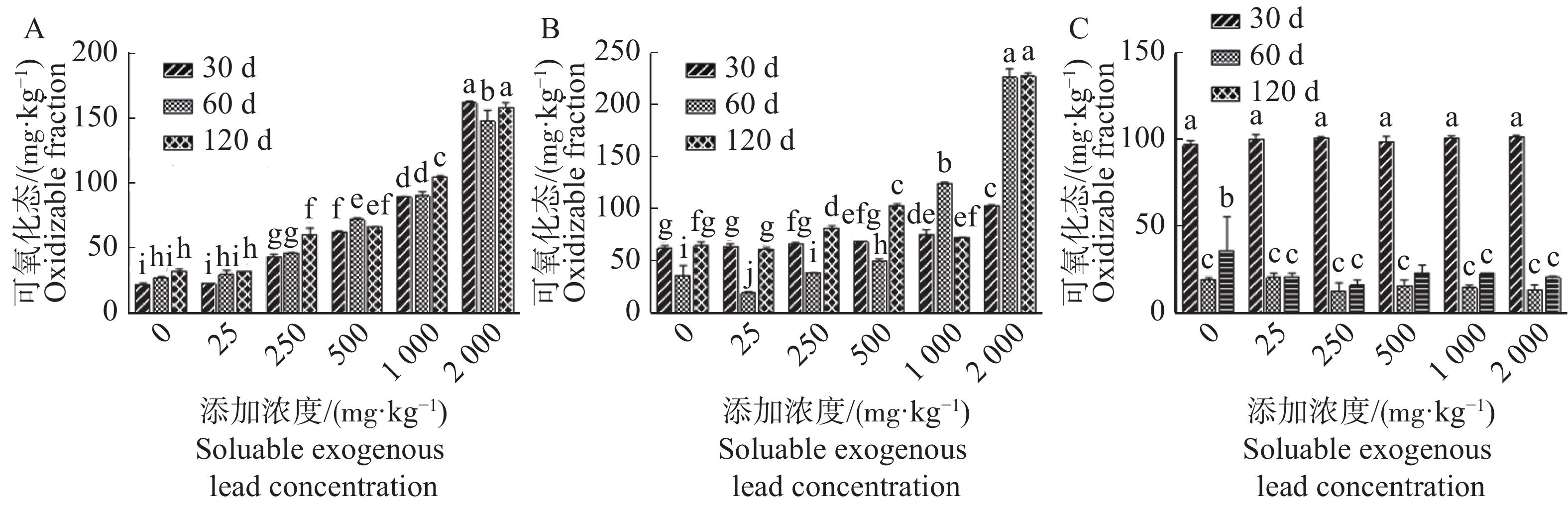
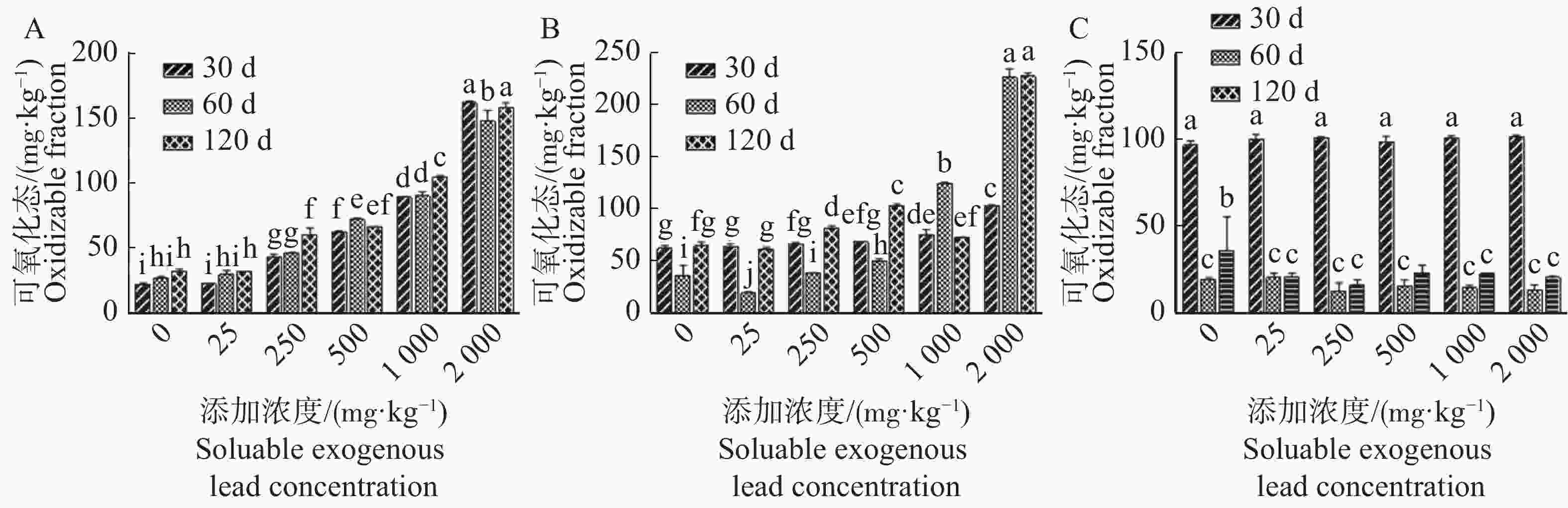
A沉积物中,当添加浓度为0,25,250 mg·kg−1时,老化30 d 和老化60 d后可氧化态含量无显著差异,但老化120 d较老化30 d沉积物可氧化态含量差异显著(P<0.05);当添加浓度至1 000 mg·kg−1和2 000 mg·kg−1时,老化120 d后沉积物可氧化态含量较老化60 d均显著增加,其中添加浓度至2 000 mg·kg−1时老化30 d 和120 d 可氧化态含量最高,分别高达161.79 mg·kg−1和158.23 mg·kg−1(图3A)。B沉积物中,除添加浓度为1 000 mg·kg−1和2 000 mg·kg−1外,其他各添加浓度下铅可氧化态含量随老化时间呈先降低后增加的趋势,且老化30 d 和60 d与老化60 d和120 d铅可氧化态含量均达显著差异(P<0.05);当添加浓度为1 000 mg·kg−1和2 000 mg·kg−1时,老化60 d铅可氧化态含量较老化30 d差异显著,但当添加浓度为2 000 mg·kg−1时老化120 d铅可氧化态含量较60 d无明显差异(图3B)。C沉积物中,同一添加浓度下老化30 d可氧化态含量较老化60 d和120d均达显著差异,但老化60 d较120 d后沉积物可氧化态含量无明显差异;不同添加浓度下相同老化时间铅可氧化态无显著差异(P<0.05)(图3C)。
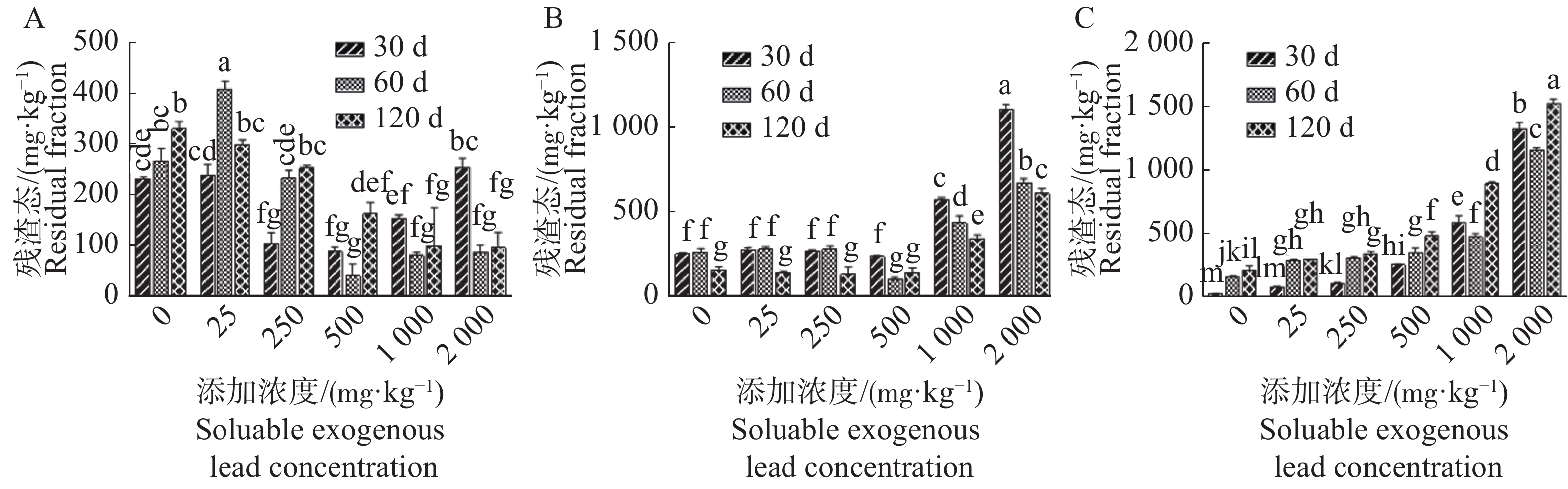
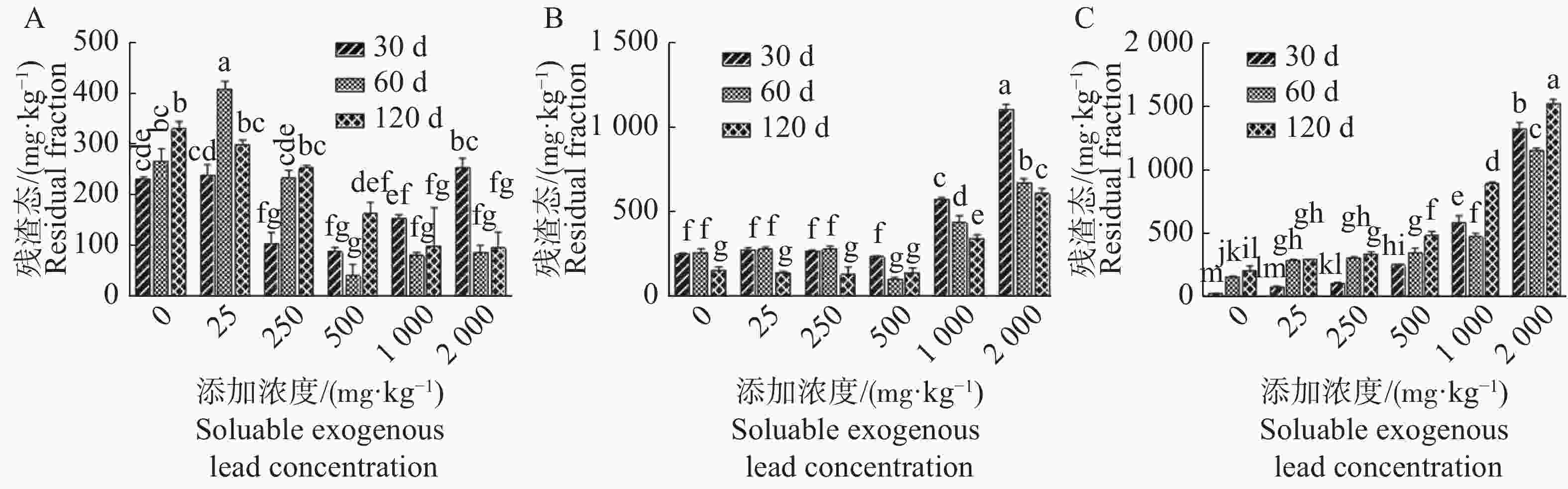
A沉积物中,同一添加浓度(除25 mg·kg−1和500 mg·kg−1外)下沉积物残渣态含量在老化60 d和老化120 d后无显著差异,残渣态含量在添加浓度25 mg·kg−1老化60 d后最高,达411 mg·kg−1。B沉积物中,当添加浓度为0,25,250 mg·kg−1时,沉积物残渣态含量在老化30 d和60 d时无显著差异,但老化120 d后沉积物残渣态含量较30 d和60 d显著降低;当添加浓度至1 000 mg·kg−1和2 000 mg·kg−1时,沉积物残渣态含量随老化时间延长逐渐降低,达显著差异。C沉积物中,当添加浓度为0,25 mg·kg−1和250 mg·kg−1时,老化60 d残渣态含量较老化120 d差异不显著,但老化30 d残渣态含量较老化60 d和120 d显著降低。当添加浓度为1 000 mg·kg−1和2 000 mg·kg-1时,残渣态含量随老化时间延长呈先降低后增加的趋势(P<0.05)(图4C)。
-
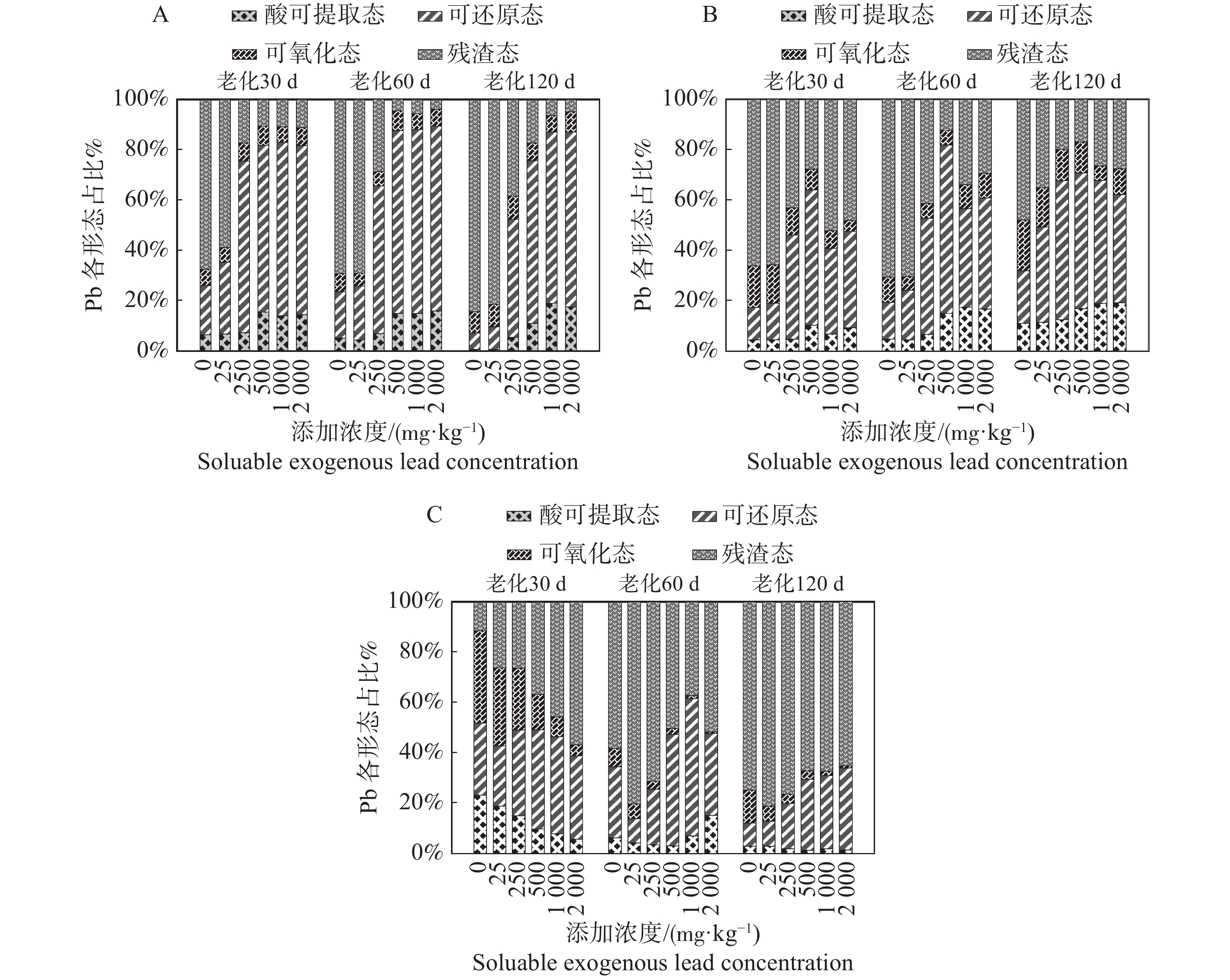
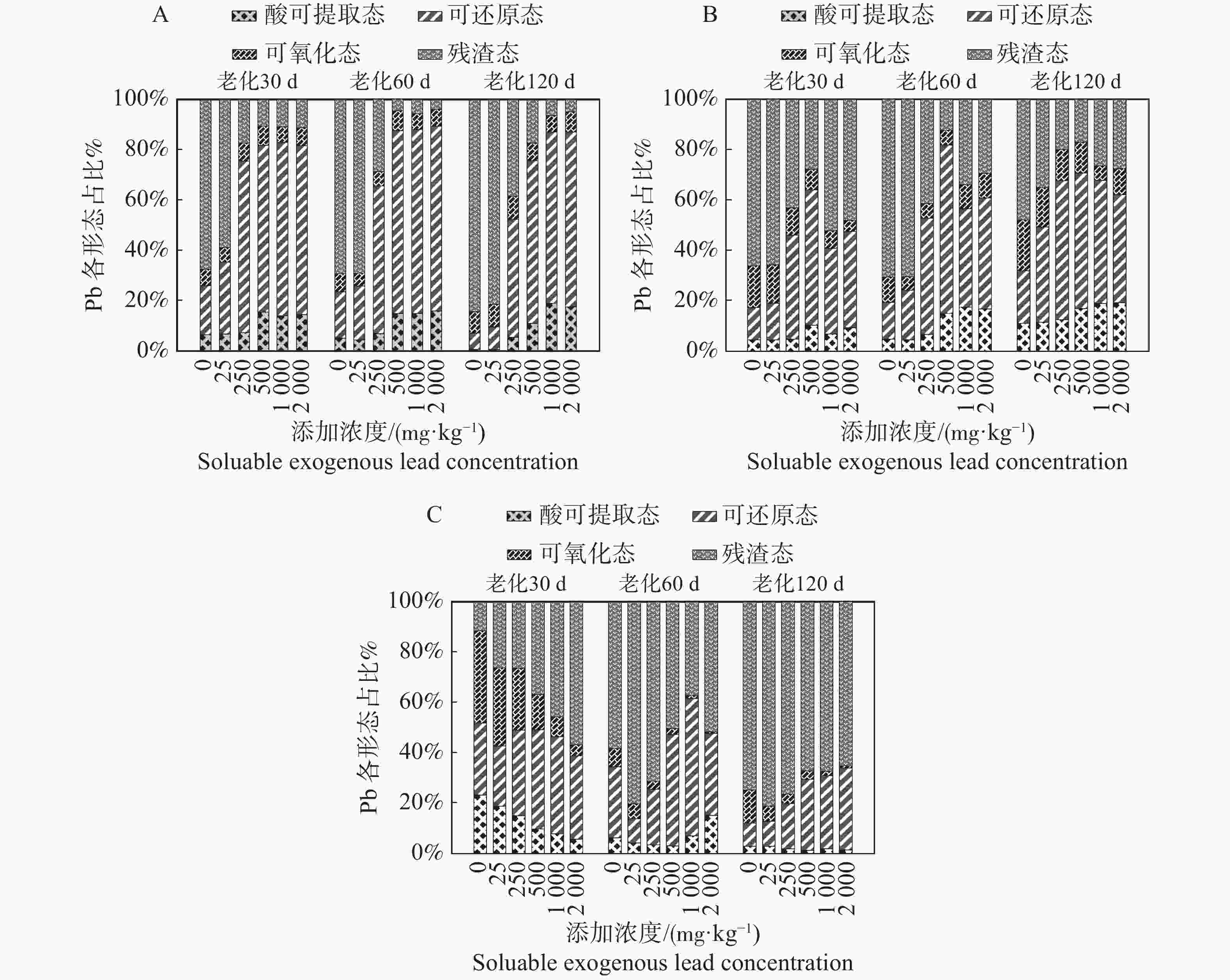
外源铅浓度的变化会影响沉积物中铅的赋存形态(图5)。沉积物A在外源铅低浓度0,25 mg·kg−1下,酸可提取态占的比例在3个老化时间都很低,而残渣态占的比例最大,为主要形态,其次是可还原态。其中,在老化时间为120 d时,可氧化态和可还原态占的比例相当。沉积物A在外源铅中浓度250,500 mg·kg−1下,3个老化时间段中,酸可提取态和可还原态所占的比例提高,其中可还原态取代残渣态成为占比最大的形态。沉积物A在外源铅高浓度1 000,2 000 mg·kg−1下,各形态的变化延续了中浓度的变化趋势,残渣态占的比例继续变小,可还原态占的比例保持着较高的水平。无论在哪种浓度水平下,可氧化态的占比都相差不大。
沉积物B在外源铅低浓度0,25 mg·kg−1下,酸可提取态在3个老化时间占有的比例都是最低的,其中在老化30 d和60 d占有的比例远低于在120 d占有的比例。残渣态为主要形态,占比最大,但老化120 d时,残渣态的比例相对较低。沉积物B在外源铅中浓度250,500 mg·kg−1下,可还原态占有的比例最大,为主要形态,而残渣态占有的比例下降,降为第2主要形态,氧化态占的比例下降,酸可提取态占的比例稍有提高。沉积物B在外源铅高浓度1 000,2 000 mg·kg−1下,残渣态占有的比例有所回升,在老化30 d时为主要形态,但在老化60 d和120 d时,可还原态依旧占有最大的比例,同时,酸可提取态占的比例也有提高,可氧化态的占比依旧不高。
沉积物C在老化30 d时,随着外源铅浓度的提高,酸可提取态和可氧化态占的比例依次下降,残渣态和可还原态占的比例依次上升。在低浓度中,各形态占比相当;在中浓度中,残渣态和可还原态为主要形态;在高浓度中,残渣态占的比例最大,氧化态占的比例最低。沉积物C在老化60 d和120 d时,在外源铅浓度0,25,250 mg·kg−1下,残渣态为主要形态,占比最大,其次是可还原态,可氧化态和酸可提取态占比都很低。沉积物C在老化60 d和120 d时,在外源铅浓度500,1 000,2 000 mg·kg−1下,可还原态占比提升,残渣态占比下降,残渣态依旧为主要形态,但在老化60 d时,可还原态与残渣态的占比相当;酸可提取态在老化60 d时的占比大于老化120 d的占比,但它同可氧化态一样,占的比例相对都很低。
-
在3种红树林沉积物中,铅的4种形态所占比例有较大差异。在沉积物A中所占比例大小顺序为:可还原态(50.00%)>残渣态(32.70%)>酸可提取态(10.23%)>可氧化态(7.07%);在沉积物B中所占比例大小顺序为:残渣态(40.74%)>可还原态(37.95%)>酸可提取态(11.07%)>可氧化态(10.23%);在沉积物C中所占比例大小顺序为:残渣态(54.44%)>可还原态(28.55%)>可氧化态(9.30%)>酸可提取态(7.70%)。3种沉积物中,可氧化态和酸可提取态所占的比例最低且相差不大,但残渣态和可还原态在各沉积物中相差可达21.74%和21.45%。经过120 d的老化,铅的形态分配在3种沉积物中不同。沉积物A的残渣态从30 d的29.30%升高到38.71%,沉积物B的残渣态从50.39%下降到28.97%,沉积物C的残渣态从33.74%升高到71.69%。
-
在3种红树林沉积物中,铅的4种形态所占比例有较大差异。在沉积物A中所占比例大小顺序为:可还原态(50.00%)>残渣态(32.70%)>酸可提取态(10.23%)>可氧化态(7.07%);在沉积物B中所占比例大小顺序为:残渣态(40.74%)>可还原态(37.95%)>酸可提取态(11.07%)>可氧化态(10.23%);在沉积物C中所占比例大小顺序为:残渣态(54.44%)>可还原态(28.55%)>可氧化态(9.30%)>酸可提取态(7.70%)。3种沉积物中,可氧化态和酸可提取态所占的比例最低且相差不大,但残渣态和可还原态在各沉积物中相差可达21.74%和21.45%。经过120 d的老化,铅的形态分配在3种沉积物中不同。沉积物A的残渣态从30 d的29.30%升高到38.71%,沉积物B的残渣态从50.39%下降到28.97%,沉积物C的残渣态从33.74%升高到71.69%。
2.1. 沉积物理化性质分析
2.2. 不同老化时间3种沉积物中铅的赋存形态
2.3. 添加不同浓度外源铅对沉积物中铅赋存形态的影响
2.4. 不同采样点沉积物中铅赋存形态的差异
2.5. 不同采样点沉积物中铅赋存形态的差异
-
在红树林沉积物120 d的老化过程中,老化时间、外源铅添加浓度以及沉积类型均可影响沉积物中铅的赋存形态。沉积物中铅的形态转化并不随时间呈单一的线性变化,这可能是受到沉积中生物和非生物相关因素的综合作用而呈现出较复杂的非线性变化[16]。随着沉积物老化时间从30,60 d增加到120 d,在沉积A与C中外源铅的赋存形态变化的基本趋势是酸可提取态和可还原态含量减低,残渣态含量增加。这与前人对外源铜和铅在土壤中的形态转化结果相类似[17]。但在沉积物B中铅的酸可提取态含量随老化时间延长而缓慢增加,推测这与沉积物B的弱酸性相关[18]。本研究结果显示,沉积物老化时间对铅的可还原态影响不大,这与有机肥对铅在土壤中形态分配的研究结果一致[19]。但也有研究显示[9]可还原态铅的比例随着沉积物老化时间的增加缓慢上升。老化时间对沉积物B和C中的铅的可氧化态的影响较为显著。在沉积物C中铅的可氧化态在老化前60 d显著降低,在老化60 d后缓慢上升。沉积物B和C相对沉积物A具有较高的有机碳含量,可以为铅稳定吸附提供充足的位点[20],进而影响到可氧化态的含量变化。残渣态铅含量随老化时间在沉积物C中增加,在沉积物B中下降,在A中的情况比较复杂。推测沉积物C中较高的残渣态铅含量与沉积物C粘土成分较高有关。在沉积物C的粒径分布中,粘土占有34.9%,约为沉积物B的2倍(粘土占17.66%),通常,粘粒含量高的土壤,其残渣态含量较高,因为带负电荷的黏粒可通过静电作用吸附阳离子[21];此外,粘粒具有较大的比表面积,可以为铅的附着提供位点[22]。
添加外源重金属浓度的高低会对重金属赋存形态的分布产生影响[23]。在沉积物A和B中,同等老化作用下随着外源铅浓度的增加,铅酸可提取态和可还原态铅占总量的比例增加,这可能与铅离子半径与钙离子半径的相似性有关,使得铅可以代替钙在碳酸盐晶格中形成混合碳酸盐相[24],从而使两者的形态含量增加。可氧化态铅占总量的比例变化趋势不明显,残渣态铅占总量的比例减少。沉积物B在1 000,2 000 mg·kg−1 铅污染条件下,随着外源铅浓度的增加,可还原态铅占总量的比例较少,残渣态铅占总量的比例反而增加。这可能是添加高浓度铅下延长了形态稳定需要的老化时间和进程[16]。通常,添加可溶性铅盐到土壤中,其流动性较强的组分所占比例较高[25]。本实验中,重金属铅以水溶性硝酸盐进入到沉积物之后,经过前30 d的快速动态吸附过程,较高污染浓度下的沉积物都是流动性较强的形态占的比例较大(沉积物C除外)。老化120 d后,在沉积物C中,残渣态铅占比逐渐增大,其他2种沉积物则减少。这是因为沉积物C位于受人为干扰较多的潮间带光滩,其含有的总有机碳含量高达8.44%,远大于沉积物A、B,后两者分别为2.54%和3.02%。而沉积物有机质是沉积物中可变电荷的主要来源,能够提供与金属发生金属-有机配合作用的丰富的羧基、羟基、氨基等官能团[7],一般总有机碳含量高的沉积物的有机质含量也高,可为铅提供更多的吸附位点[20]。另外,沉积物C中的电导率同样远高于沉积物A、B,沉积物矿物等表面的负电荷越多,对铅的吸附力越强[26]。
结果表明,外源铅进入红树林沉积物,经老化作用后,残渣态和可还原态是其主要赋存形态,可见老化过程在总体上降低了生物有效态铅的占比;老化浓度会影响铅赋存形态稳定所需的时间,并且沉积物中铅赋存形态还受到沉积理化特征的影响。本实验结果初步揭示了外源铅进入红树林沉积物后的环境行为,对红树林生态系统的重金属污染风险评估和近岸重金属污染的生物修复具有重要意义。
致谢:海南大学分析测试中心对本实验给予了大力支持和帮助!






 DownLoad:
DownLoad: