-
香蕉(Musa nana)为芭蕉科植物,是中国最重要的热带水果之一[1]。传统栽培品种如‘巴西蕉’植株高大,生育期长达12~13个月,易受台风侵袭,导致防风成本增加。相较之下,矮蕉株型矮小紧凑,抗风能力较强,生育期短,适宜密植,不仅能有效降低台风造成的损失,还可显著减轻劳动强度,减少物资投入[2]。此外,矮蕉果实成熟期相对较短,生长迅速,适合在有限空间内高密度种植,从而提升单位面积产量,是一种极具开发潜力的经济树种[3]。
土壤盐碱化不仅破坏土壤结构、降低养分利用效率,还通过渗透胁迫和离子毒害危害植物生长,对区域粮食安全与生态平衡构成威胁。目前,国内外对香蕉抗盐性的研究主要集中于巴西蕉和宝岛蕉,针对矮蕉的抗盐生理研究较少。海南省因其独特的地理条件,拥有丰富的矮蕉种质资源,研究潜力广阔,但目前相关研究鲜有报道。为此,本研究以海南矮蕉为材料,设置90、120、150和200 mmol·L-1的NaCl胁迫处理,测定盐胁迫下矮蕉幼苗的叶质膜透性、叶绿素、脯氨酸、可溶性蛋白、丙二醛(MDA)含量,以及超氧化物歧化酶(SOD)、过氧化物酶(POD)、过氧化氢酶(CAT)活性等耐盐生理指标,系统分析矮蕉幼苗的抗盐生理特性,旨在为海南矮蕉的耐盐品种选育及产业化栽培提供科学参考。
-
供试的矮蕉种植于海南大学儋州校区农科基地,通过组织培养获得小苗,苗高15~20 cm,处于五叶一心,且心叶未展开。
-
盐胁迫处理方案为以1/2 Hoagland培养液为基础,分别添加NaCl至以下浓度:0 mmol·L-1(CK)、90 mmol·L-1(T1)、120 mmol·L-1(T2)、150 mmol·L-1(T3)、200 mmol·L-1(T4)。每个处理设5株植株,3次重复。盐胁迫期间,定时定量加入NaCl溶液以维持设定浓度。分别于处理后的第0、4、8、12、16、20天采集叶片和根系样品,用于相关生理指标的测定。
-
参考《植物生理生化实验原理和技术》[4]对各项生理指标测定,其中,叶绿素含量通过紫外分光光度法测定(TU–1810,北京普析),叶质膜透性使用电导率仪测定(DDS–307A,上海仪电),脯氨酸含量利用酸性茚三酮测定,可溶性蛋白含量使用考马斯亮蓝法测定,MDA含量通过硫代巴比妥酸比色法测定,3种抗氧化酶(SOD、POD、CAT)活性分别使用氮蓝四唑光还原法、愈创木酚比色法和钼酸铵比色法测定。
-
用Excel2019进行数据统计,SPSS26进行显著性分析,Origin2021进行作图处理。
-
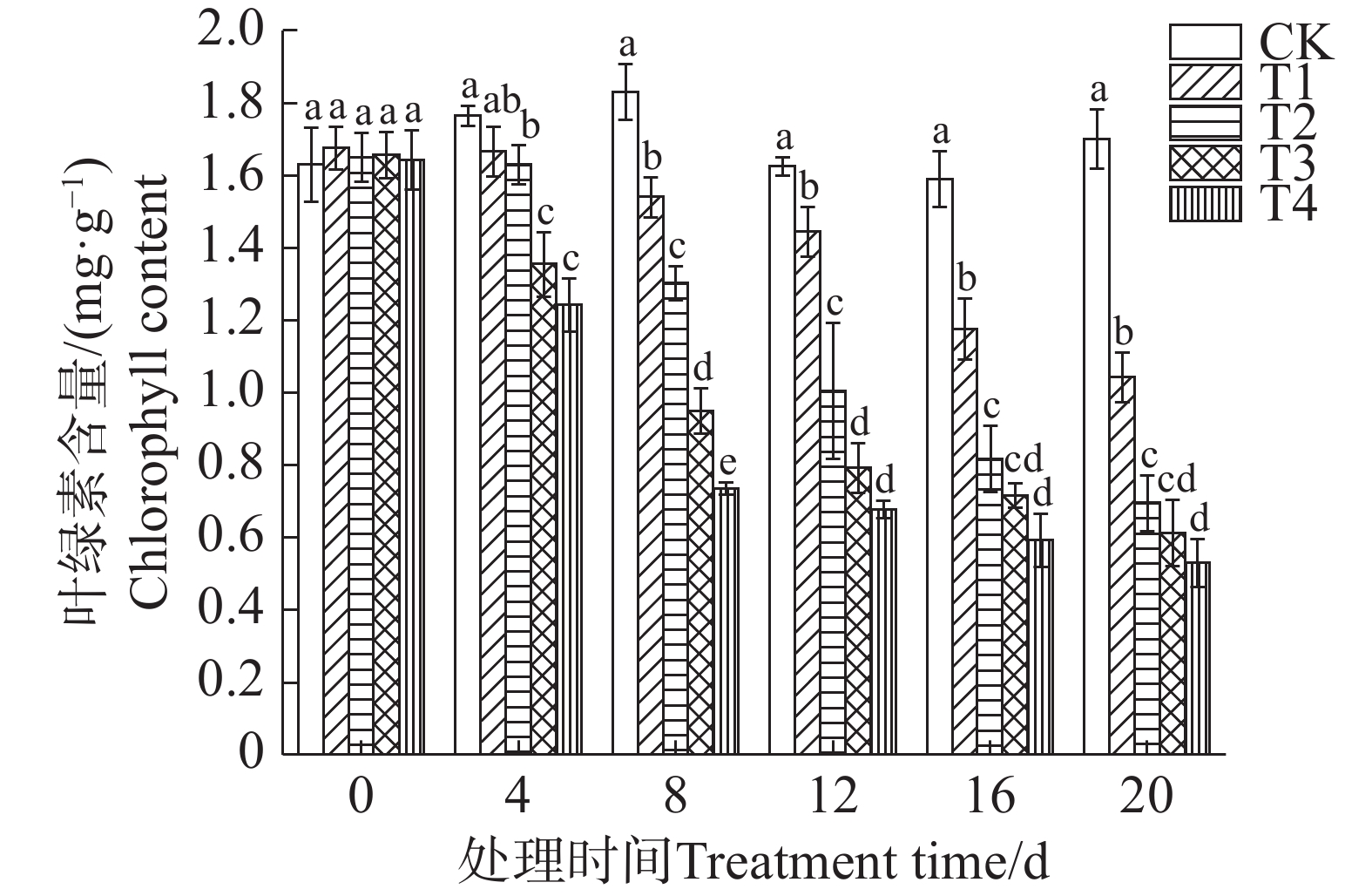
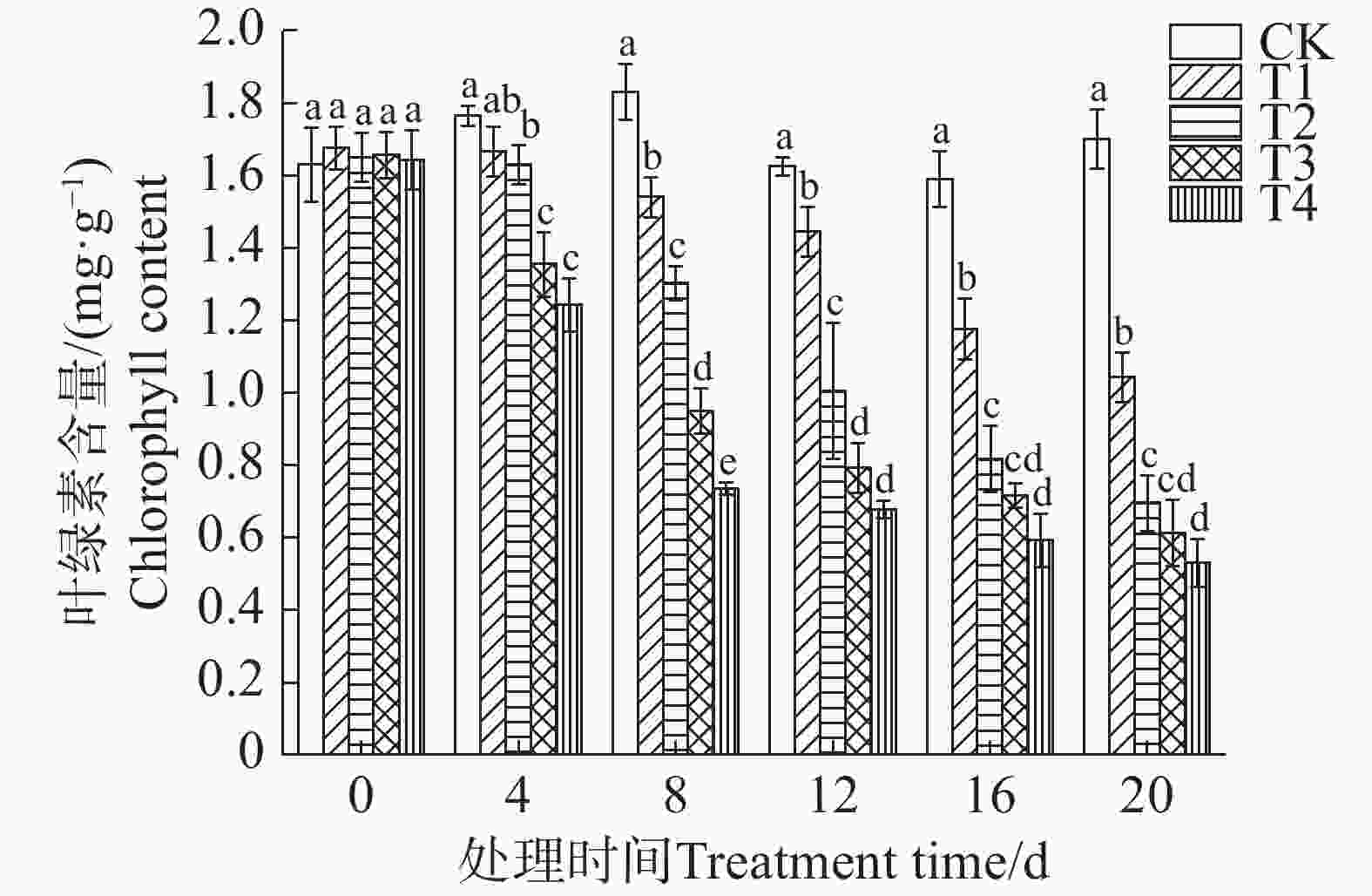
从图1可知,随着盐胁迫时间的延长,各处理的叶绿素含量均持续下降,且盐胁迫浓度越高,叶绿素降解越严重。第4天时,各处理间的叶绿素含量开始出现不同程度的下降,其中T3和T4处理下降尤为明显,表明矮蕉植株在盐胁迫初期对高盐浓度较为敏感,叶绿素降解机制被迅速激活。第4~12天,各处理组之间的差异不断增大,此阶段可能由于离子毒害与氧化应激的共同作用,加剧了叶绿体结构的损伤。第12~20天,T2~T4处理的叶绿素含量下降趋势逐渐放缓,部分原因可能是植株启动了某种耐盐适应机制,或剩余叶绿素已维持在相对稳定的低水平。第20天时,T1~T4处理的叶绿素含量分别下降了38.68%、59.11%、63.97%和68.85%。由此可见,盐胁迫显著降低了矮蕉幼苗的叶绿素含量,且下降程度随盐处理浓度的升高和胁迫时间的延长而加剧。
-
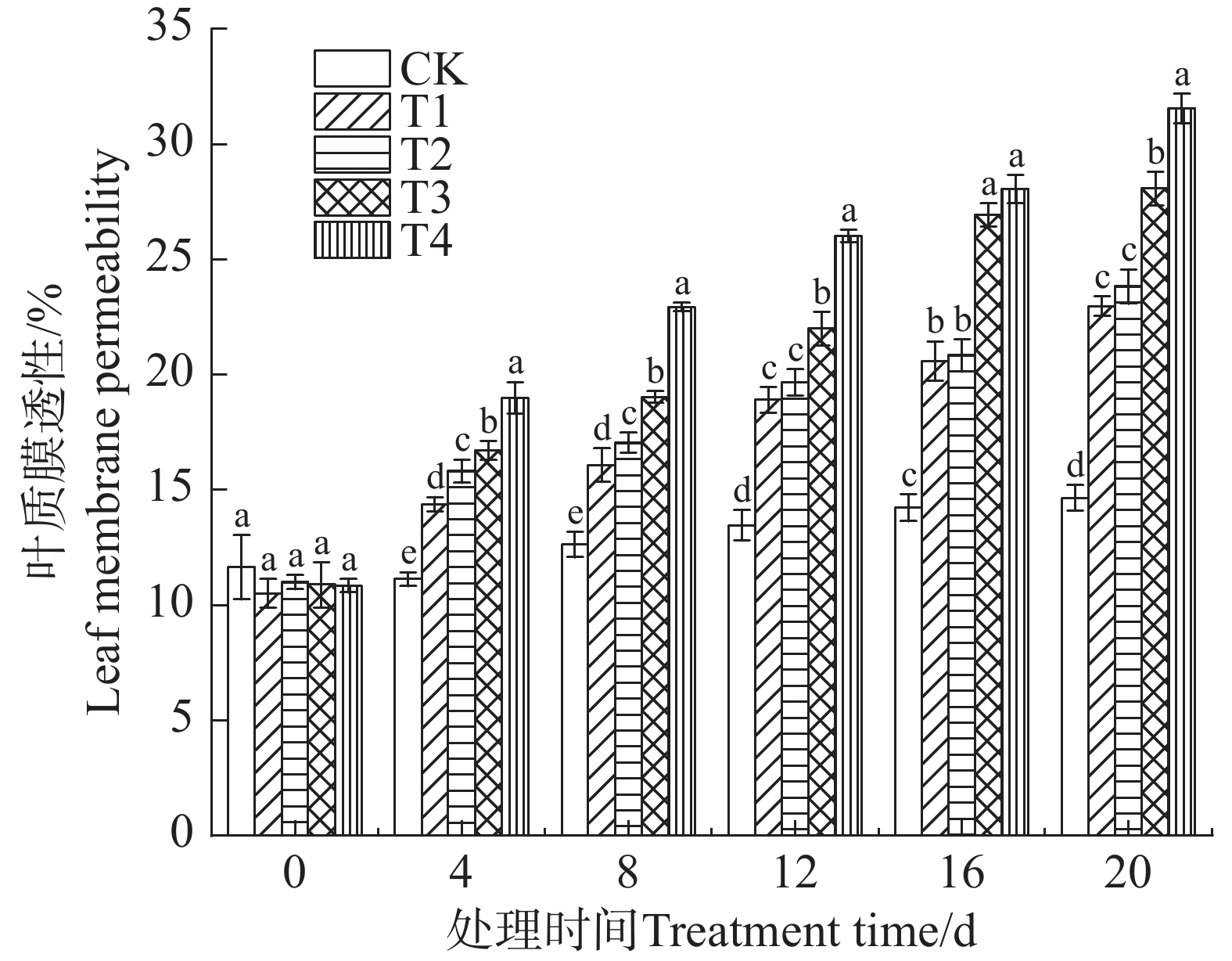
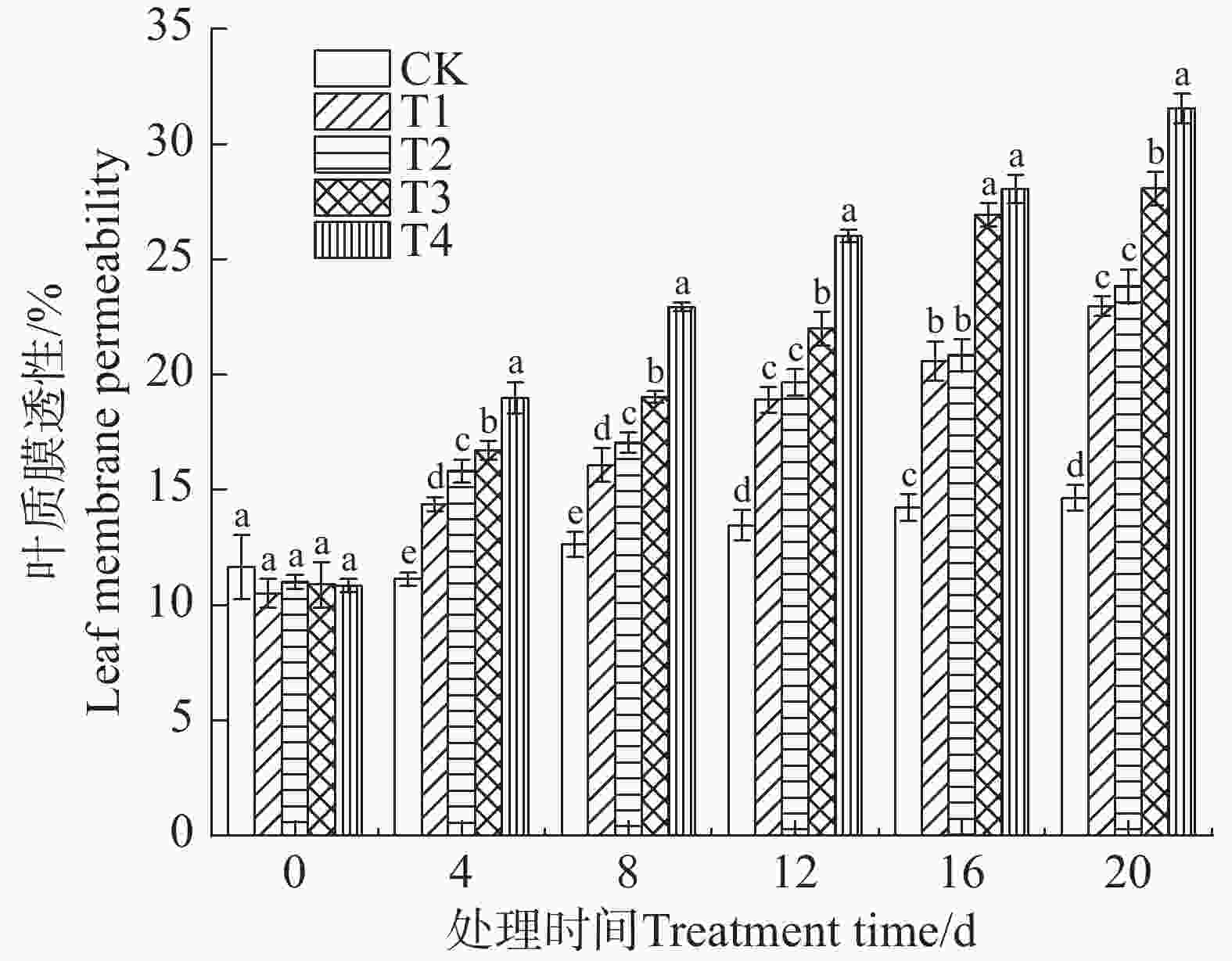
从图2可知,矮蕉幼苗的叶质膜透性呈上升趋势。盐胁迫第4天时,各处理组与CK组之间均出现差异,表明低浓度盐胁迫已对矮蕉叶质膜系统产生影响。随着盐胁迫时间的延长,矮蕉叶质膜透性持续上升,说明盐胁迫会导致其叶质膜系统逐渐功能丧失;盐胁迫浓度越高,叶质膜透性上升幅度越大。在较高浓度盐胁迫(T3、T4)下,处理第16天时叶质膜透性急剧上升,表明此时膜系统已发生较为严重的损伤。至第20天,T1~T4组的叶质膜透性分别增长56.79%、62.66%、91.60%和115.36%,膜系统损伤进一步加重。
-
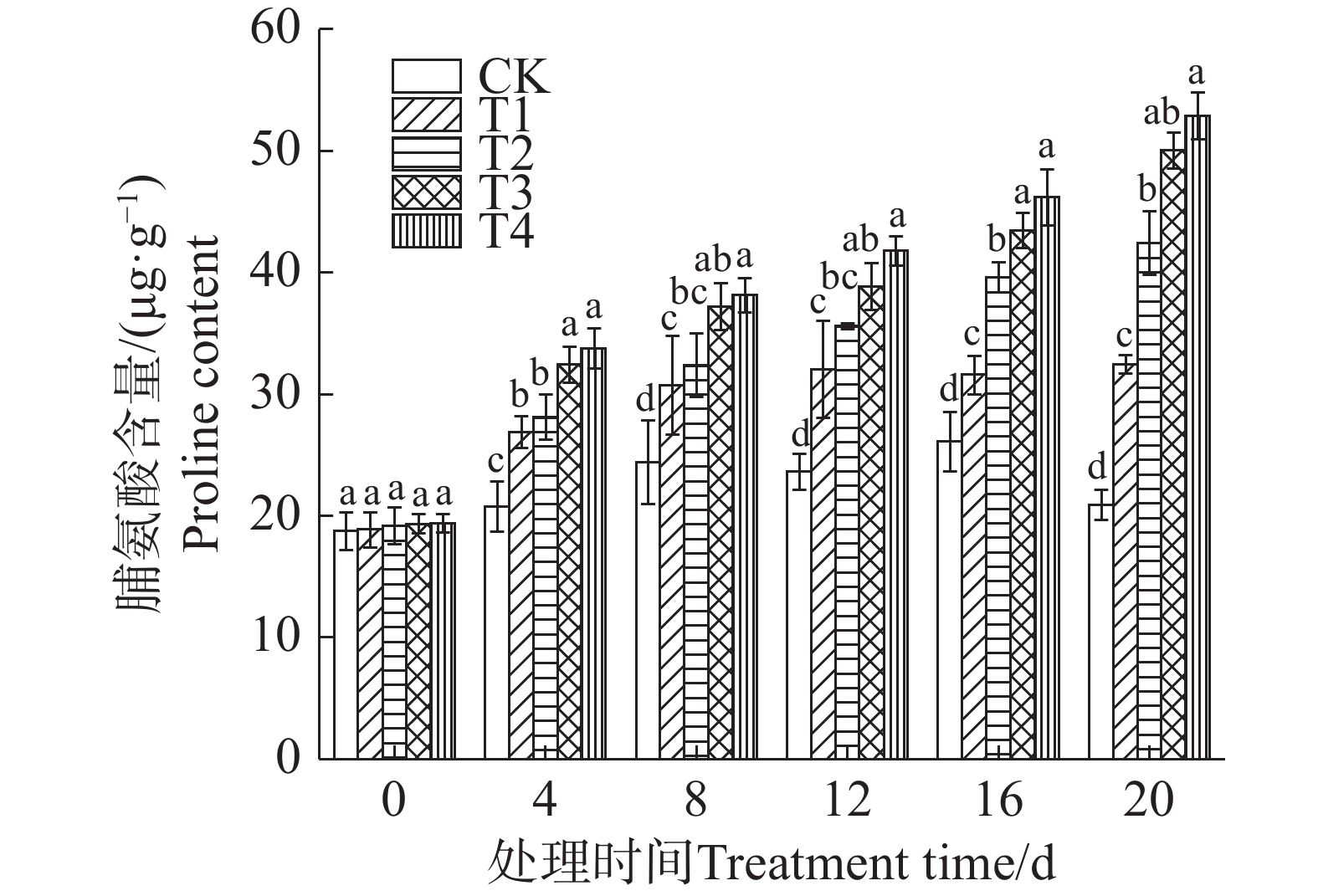
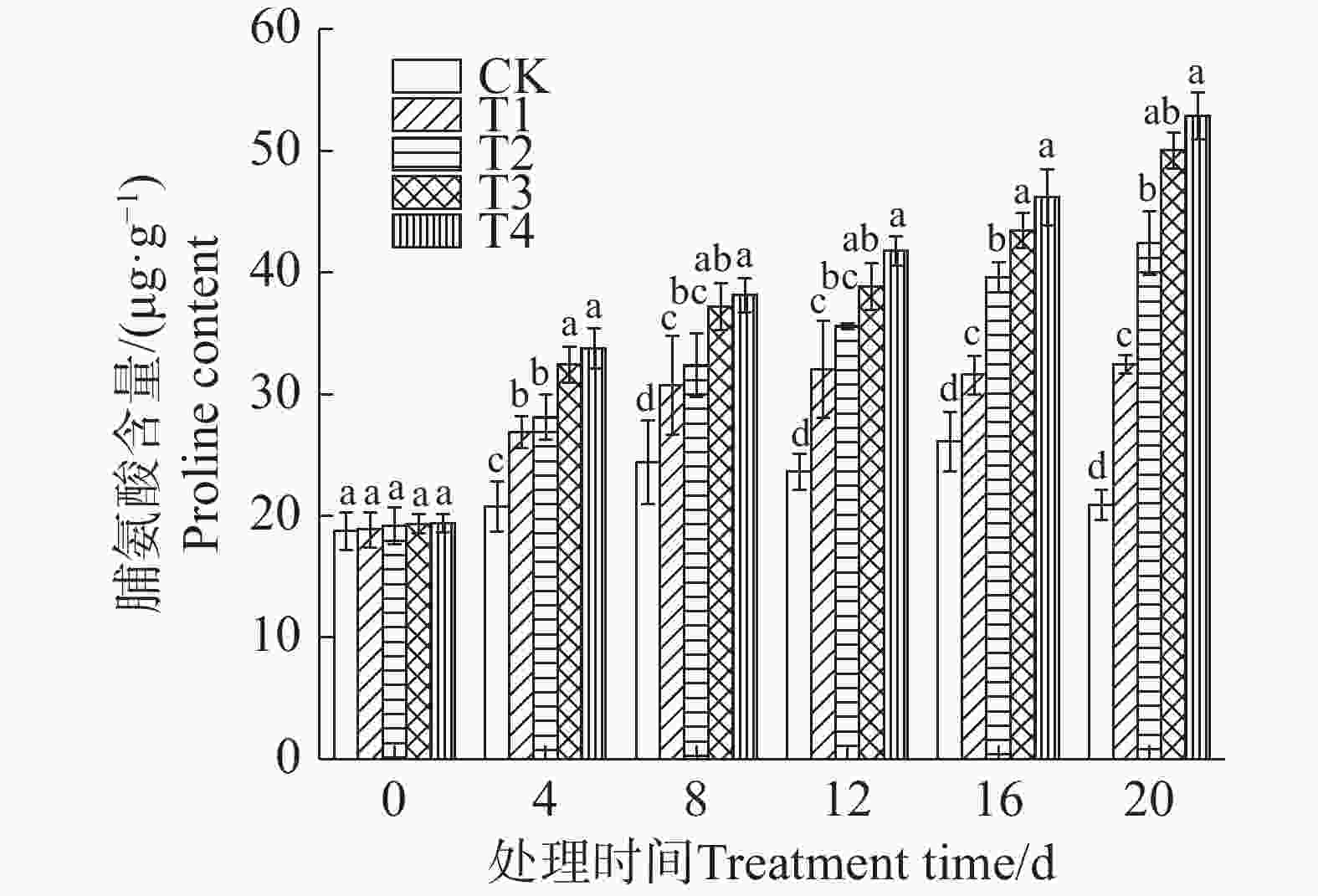
由图3可知,矮蕉幼苗的脯氨酸含量呈上升趋势,20 d时各盐胁迫处理组的脯氨酸含量达到最大值。表明盐胁迫处理能够诱导矮蕉幼苗脯氨酸的大量积累,且积累程度随着盐胁迫时间的延长而增长。在较低浓度盐胁迫(T1)条件下,脯氨酸含量在第8天后增长速度有所减缓,而在较高浓度盐胁迫(T3、T4)下,脯氨酸含量在整个实验期间均保持持续快速上升的趋势。第12~16天,较高浓度盐胁迫(T3、T4)的脯氨酸积累速率高于较低浓度处理,第20天时,T1~T4的脯氨酸含量分别增长55.19%、102.85%、139.17%、152.91%,表明在较高浓度盐胁迫下,植物需要积累更多的脯氨酸来维持渗透压以防止细胞过度失水。
-
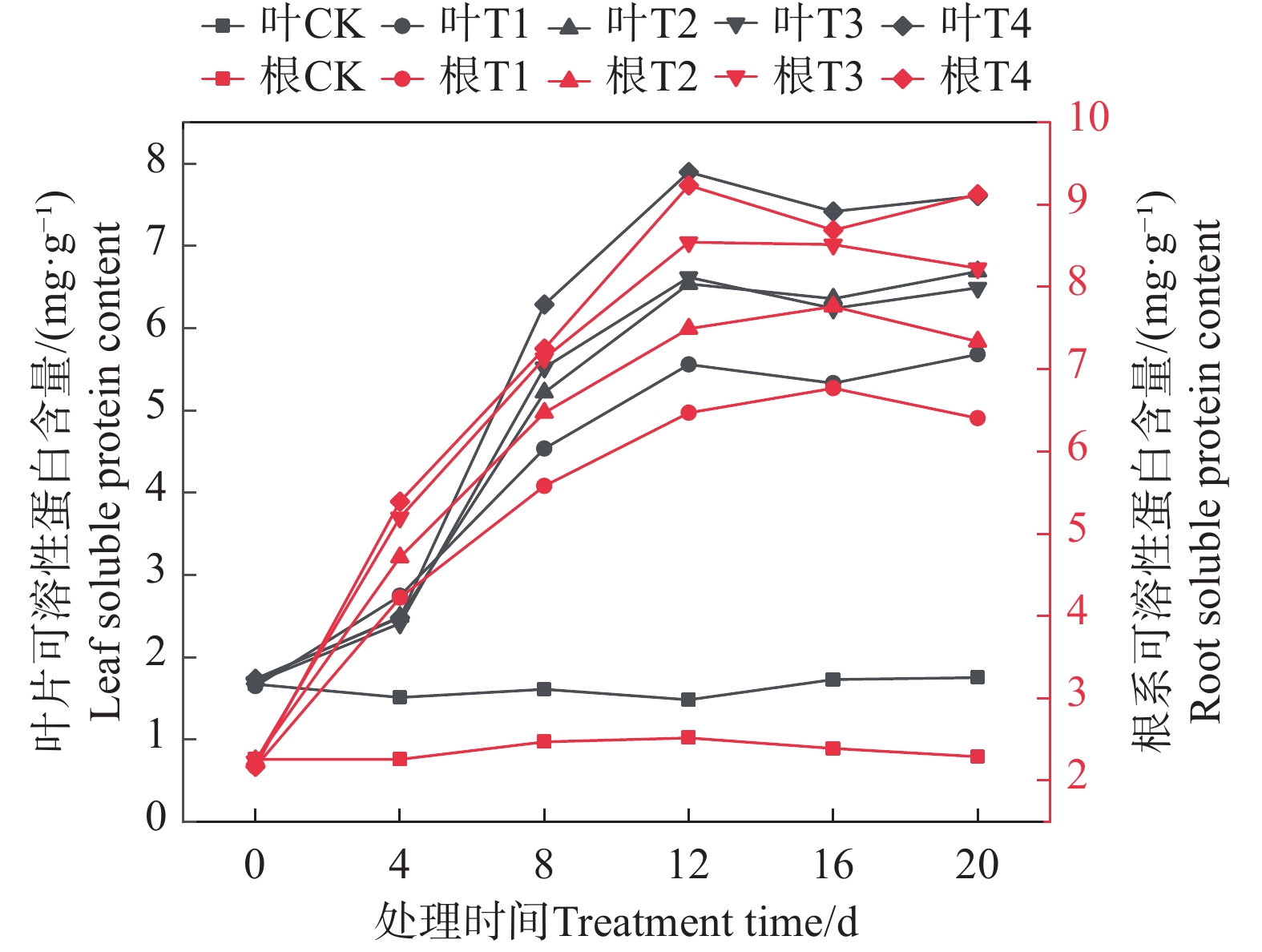
在本实验中,矮蕉幼苗叶片的可溶性蛋白含量变化趋势为先上升后下降(图4)。在0~12 d期间,不同浓度盐胁迫下,叶片可溶性蛋白含量持续升高,且盐胁迫浓度越高,蛋白含量增加越显著。第12天时,可溶性蛋白含量达到最大值,T1~T4处理组的可溶性蛋白含量分别增长了275.68%、342.11%、347.30%和433.56%。此后含量略有下降,但各盐胁迫处理组的可溶性蛋白含量仍高于第4天的水平。
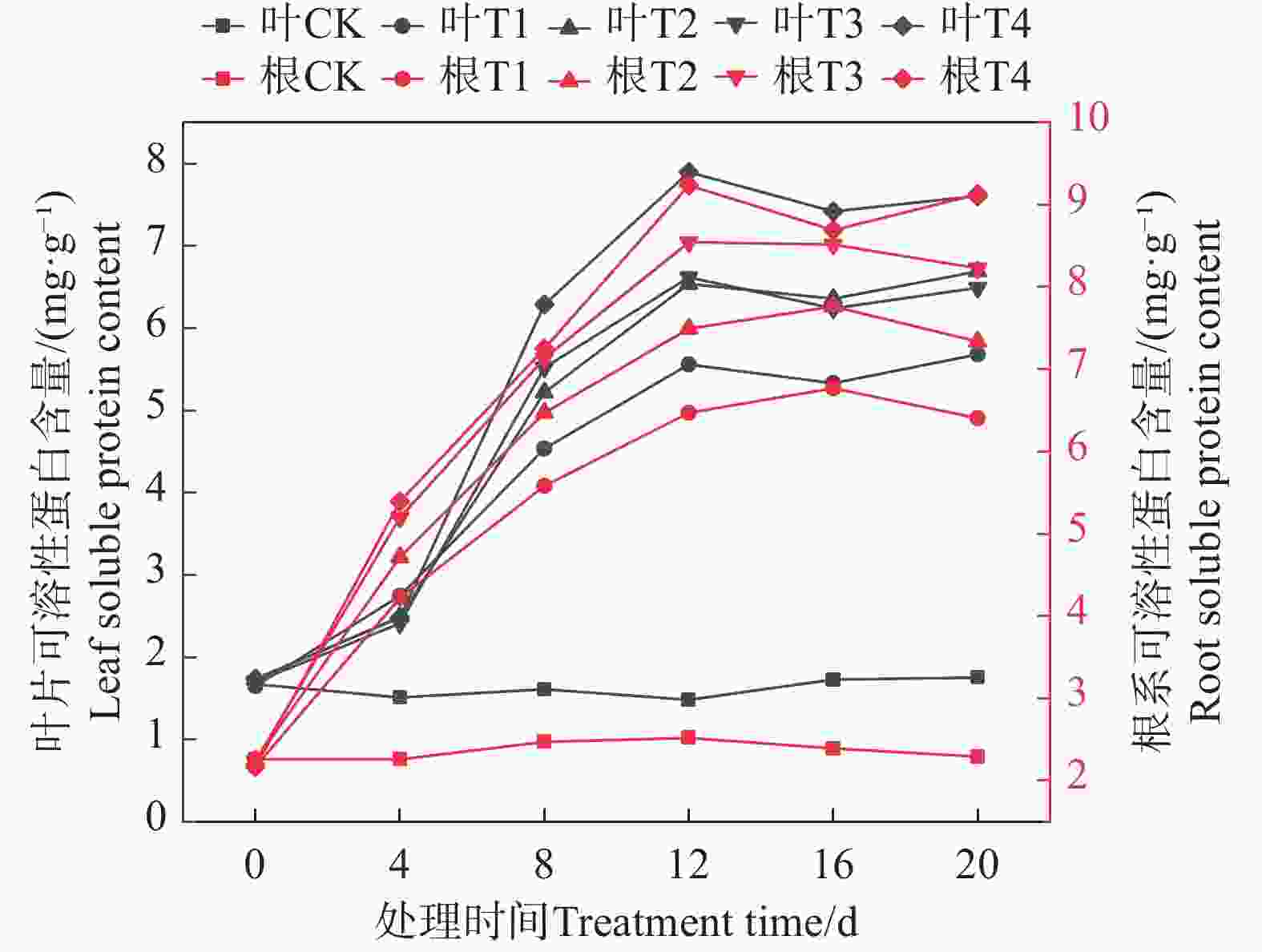
Figure 4. Effect of salt stress on soluble protein content in the leaves and roots of dwarf banana seedlings
矮蕉幼苗根系的可溶性蛋白含量变化趋势与叶片相似,也呈先上升后下降的趋势。在0~12天期间,根系可溶性蛋白含量不断上升,第12天时T1~T4处理组分别增长了186.43%、231.56%、278.17%和308.70%,达到最大值,之后略有下降,但仍维持在较高水平。
由此可见,矮蕉幼苗可通过积累细胞内的可溶性蛋白来抵抗盐胁迫,且积累量随盐胁迫浓度升高而增加。矮蕉幼苗能对盐胁迫迅速作出反应,大量积累可溶性蛋白并维持较高浓度。在盐胁迫下,根系的可溶性蛋白含量高于叶片,表明根系比叶片具有更强的可溶性蛋白积累能力,且对盐浓度变化更为敏感。
-
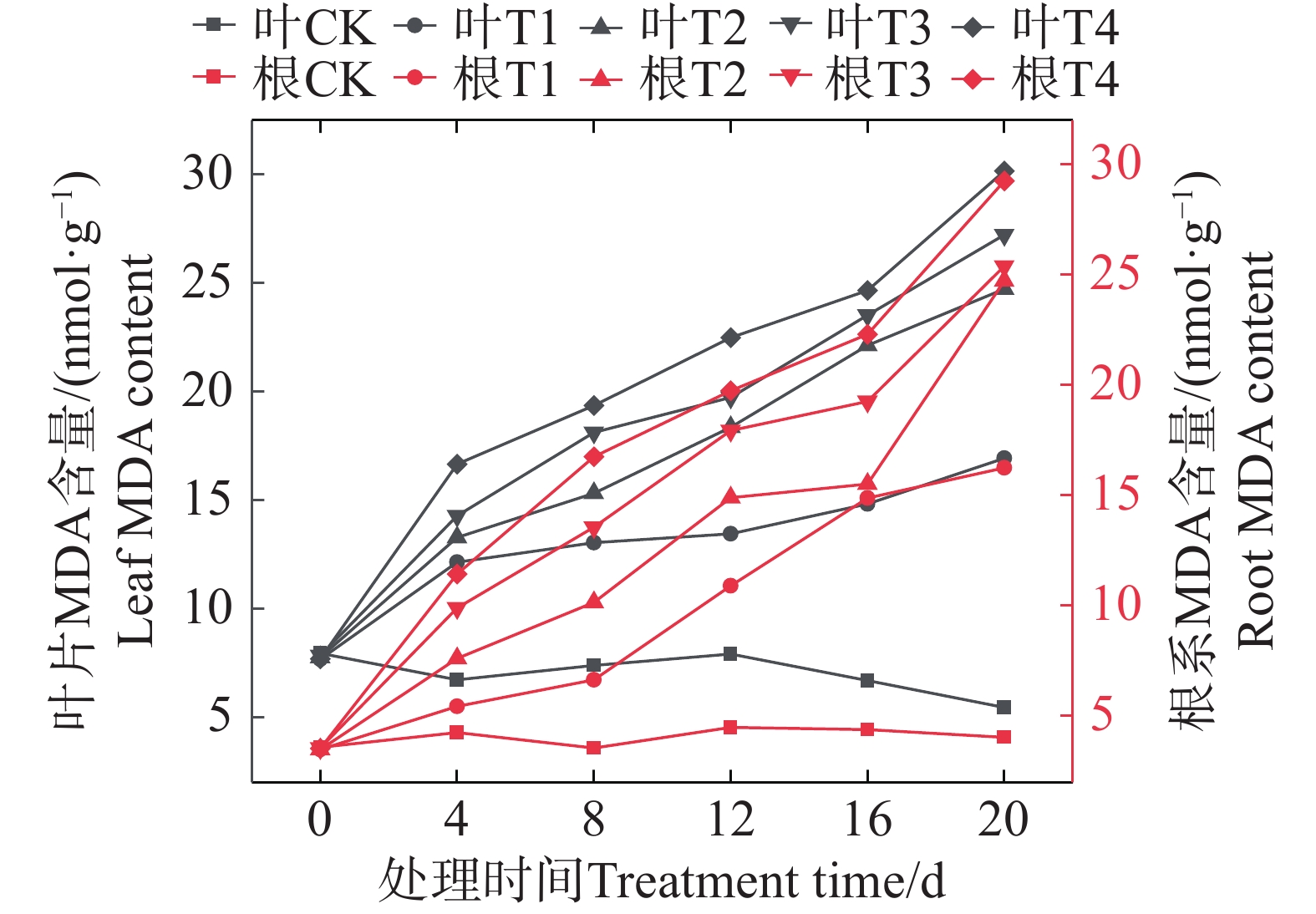
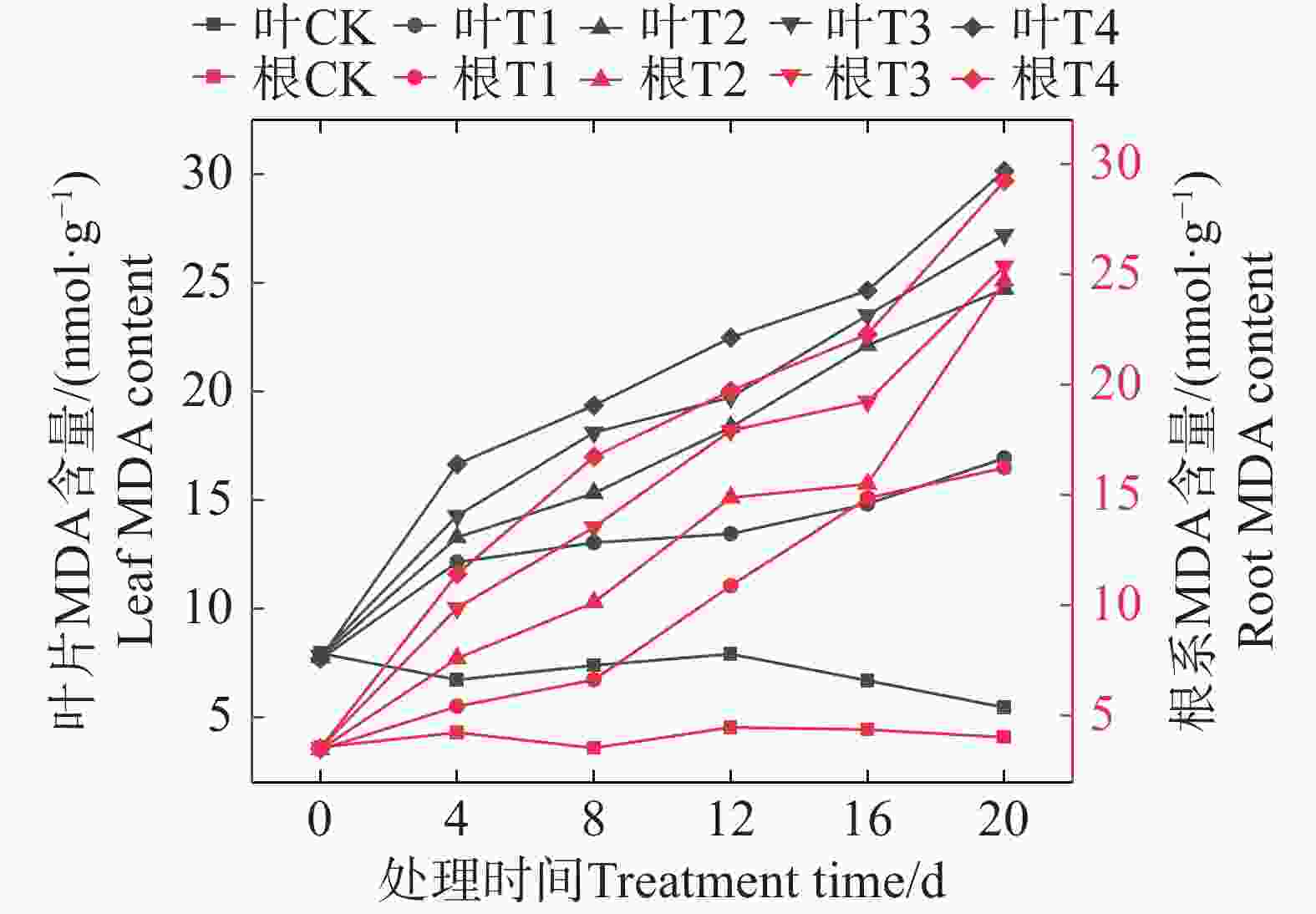
由图5可知,随着盐胁迫浓度增大,矮蕉幼苗叶片的MDA含量呈上升趋势。各盐胁迫处理在第20天时,叶片MDA含量达到最大值,相比对照组分别增加了211.07%、354.10%、400.18%和454.16%。其中,T4组的MDA含量最高,为30.18 nmol·g−1,较同期T1、T2、T3组分别高出78.14%、22.04%和10.79%。
在根系中,随着盐胁迫浓度增大,矮蕉幼苗根系的MDA含量总体也呈上升趋势。各胁迫处理在第20天时达到最大值,分别增加了302.23%、512.21%、528.79%和624.34%。其中,T4组含量最高,为29.26 nmol·g-1,较同期T1、T2、T3组分别高出80.08%、18.32%和15.19%。这表明矮蕉幼苗的膜系统损伤程度不断加剧,且高浓度盐胁迫会加速细胞膜脂过氧化,可能导致细胞膜严重损伤。相比之下,根系在盐胁迫下的相对损伤程度大于叶片,根系的响应启动更快,对盐浓度的敏感性也远高于叶片,不同处理间MDA含量的差异在根系中更为明显。
-
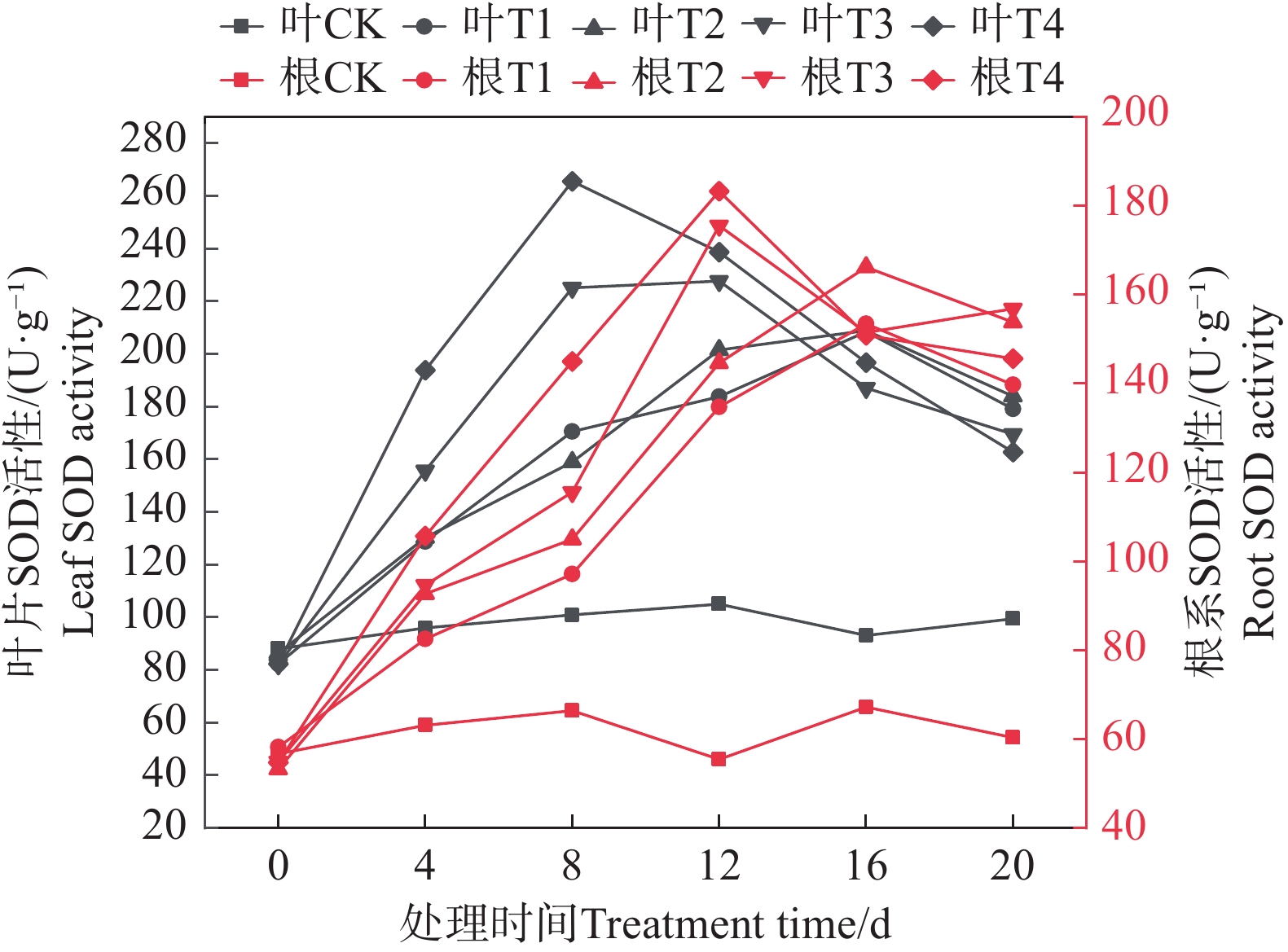
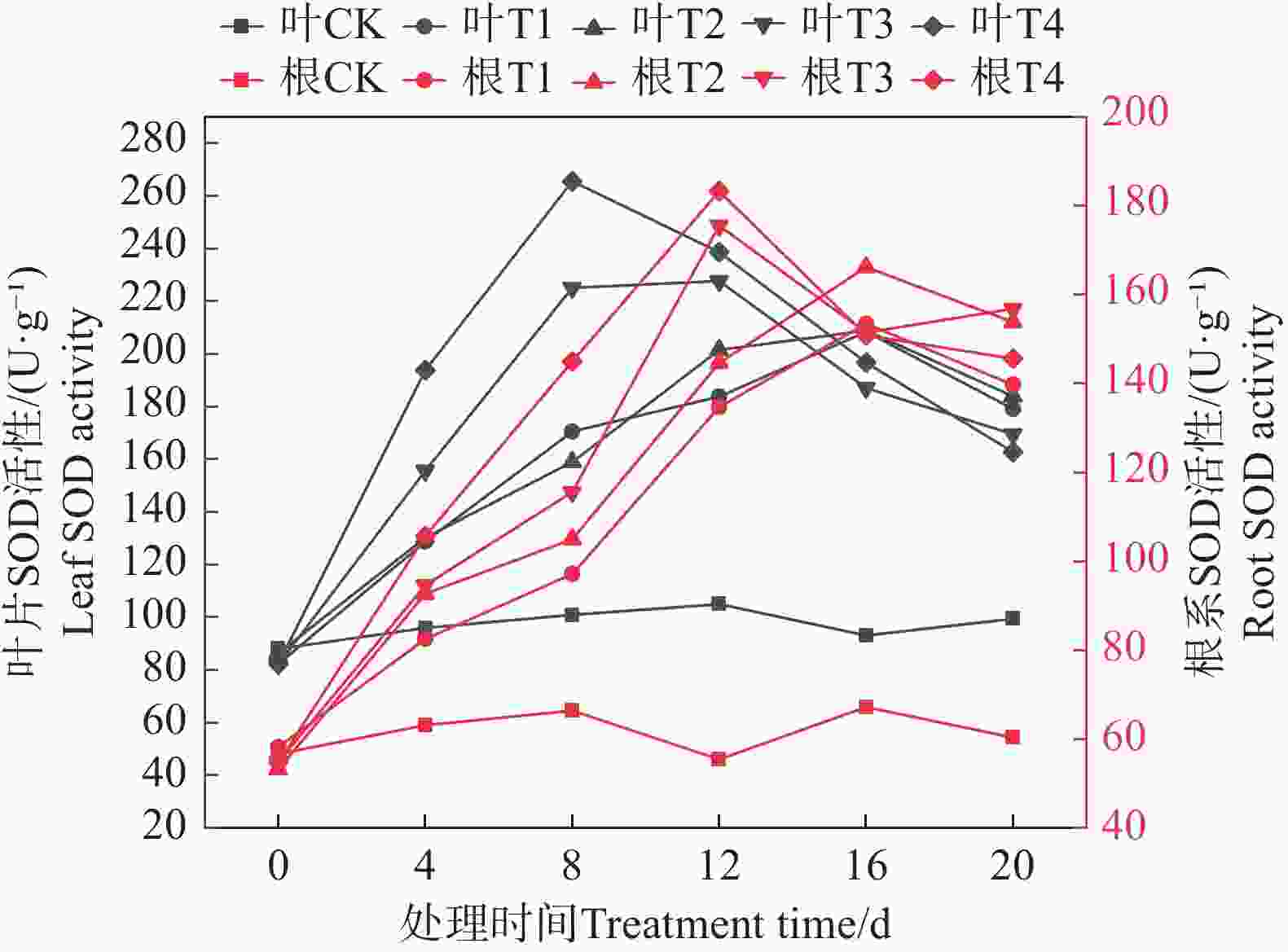
由图6可知,随着盐胁迫浓度的增大,矮蕉幼苗叶片的SOD活性总体呈先上升后下降的趋势。T1和T2处理在第16天时SOD活性达到最大值,分别为208.48 U·g−1和208.85 U·g−1;而T3和T4处理则在第8天时达到峰值,分别为225.19 U·g−1和265.66 U·g−1。矮蕉幼苗根系的SOD活性变化趋势与叶片相似,也表现为先上升后下降。T1和T2处理在第16天时达到最大值,分别为153.48 U·g−1和166.26 U·g−1;T3和T4处理则在第12天时达到峰值,分别为175.62 U·g−1和183.35 U·g−1。这表明盐胁迫可能诱导矮蕉幼苗提高SOD活性,且高浓度盐胁迫能更快激活其SOD活性以应对胁迫。在盐胁迫下,矮蕉幼苗根系SOD活性的相对激活强度高于叶片,且根系在达到峰值后活性维持时间更长;而叶片的响应速度更快,早期迅速激活,但也更早开始减弱。
-
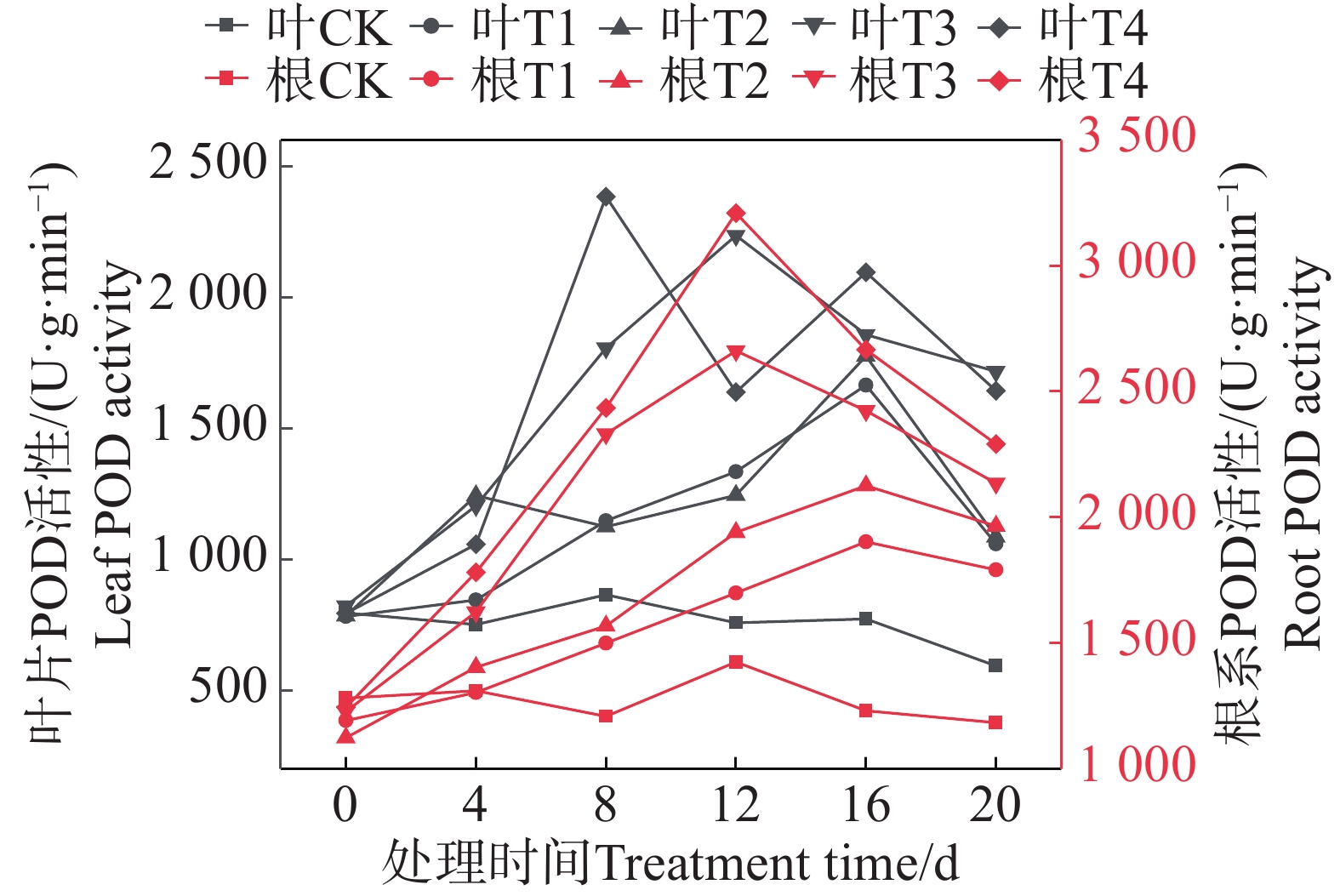
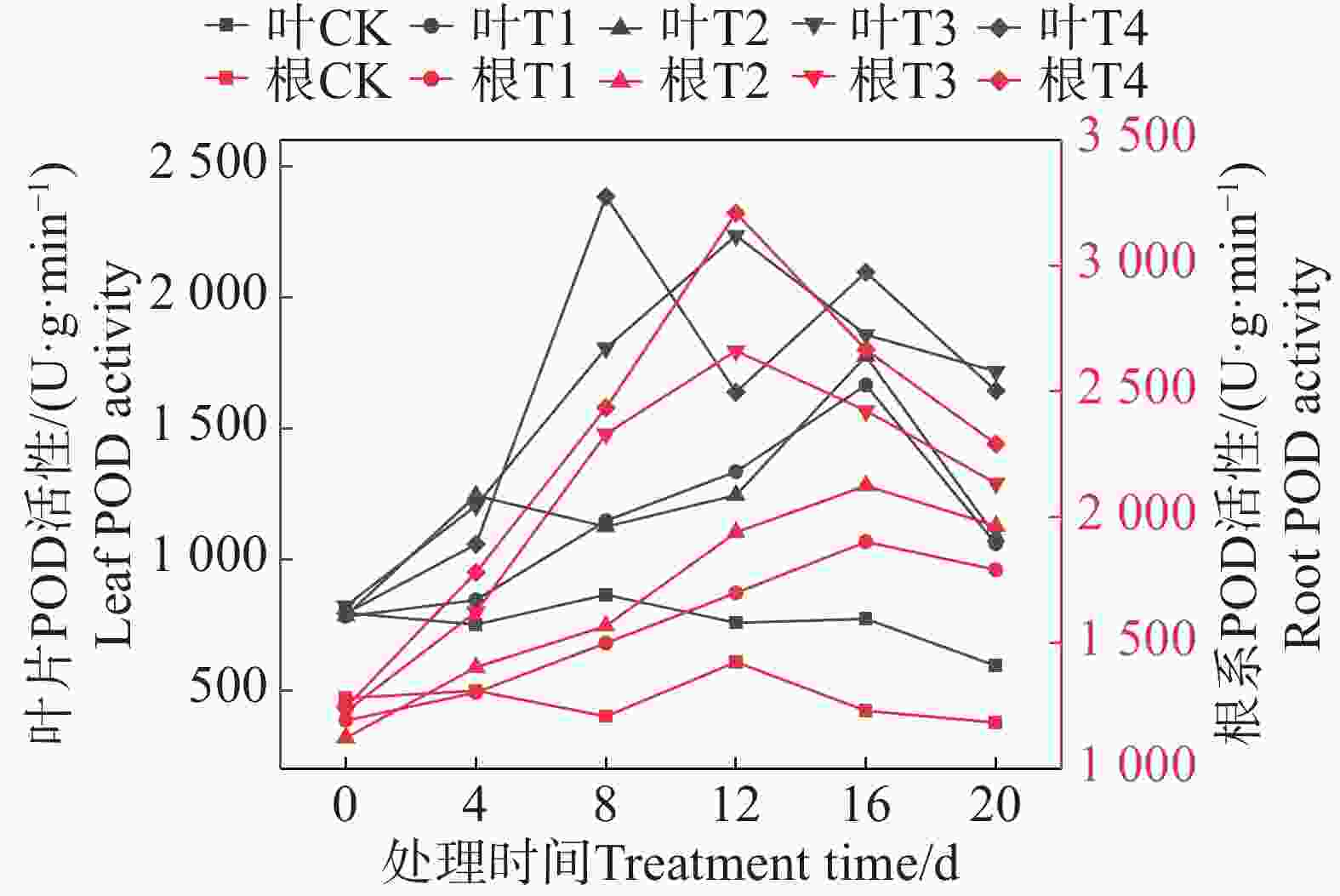
由图7可知,随着盐胁迫浓度增大,矮蕉幼苗叶片的POD活性呈先上升后下降的趋势。T1和T2处理在第16天达到最大值,分别为1 664.47 U·g−1·min−1和1 774.76 U·g−1·min−1;T3处理在第12天达到最大值(2 234.76 U·g−1·min−1);T4处理在第8天达到最大值(2 383.47 U·g−1·min−1)。
矮蕉幼苗根系的POD活性也随盐胁迫浓度增大呈先上升后下降的趋势。第16天时,T1和T2处理达到最大值,分别为1 902.35 U·g−1·min−1和2 124.80 U·g−1·min−1;T3和T4处理在第12天达到最大值,分别为2 662.05 U·g−1·min−1和3 209.07 U·g−1·min−1。这表明盐胁迫可能提高矮蕉幼苗的POD活性,且高浓度盐胁迫下,POD活性峰值出现的时间早于低浓度处理。相比之下,根系POD活性变化较为平缓,多呈单峰或平缓上升模式;而叶片POD活性波动更为剧烈,出现双峰现象。在后期,两者的POD活性均有所下降,但叶片活性回落更明显,根系回落相对较小。
-
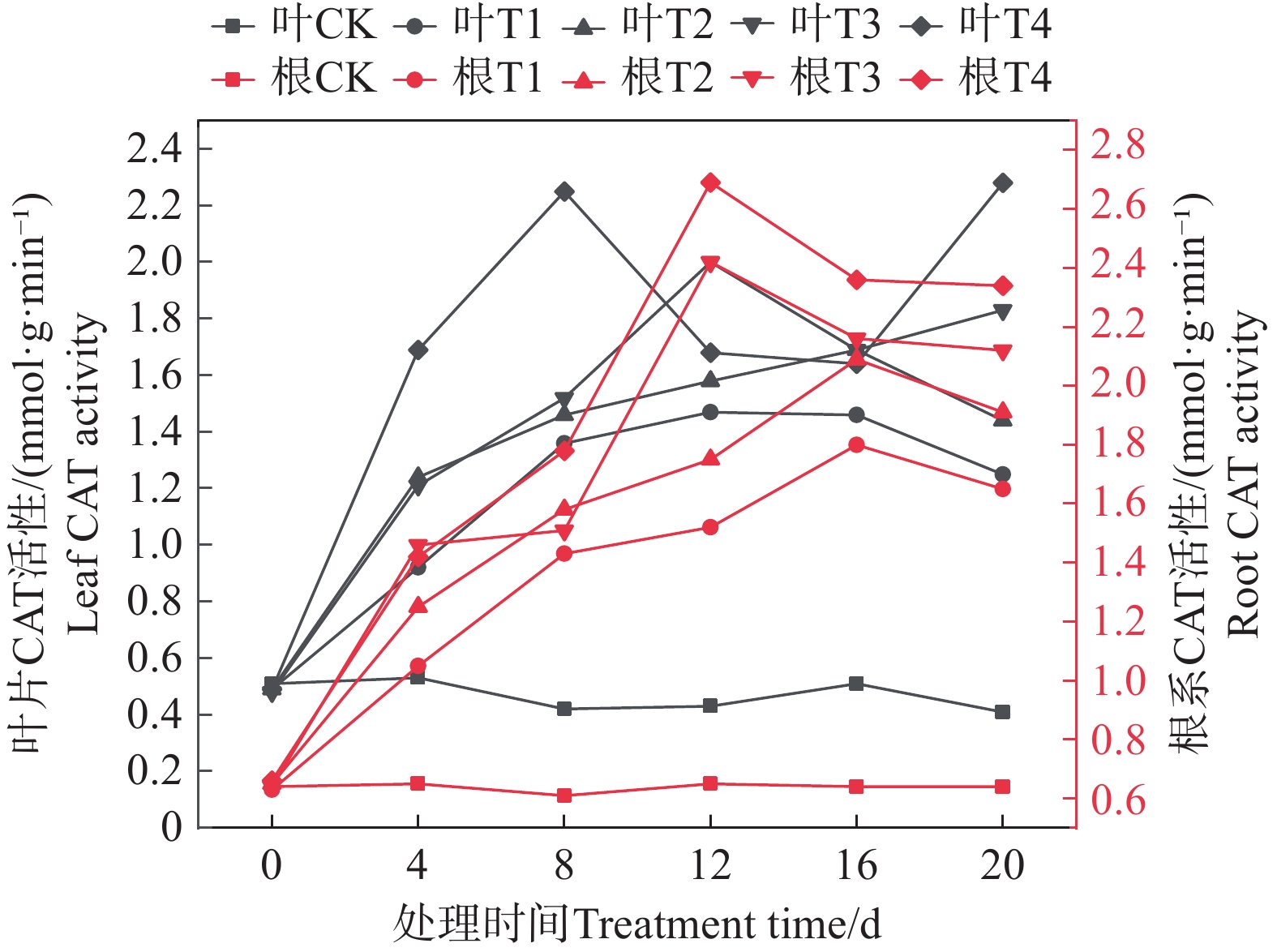
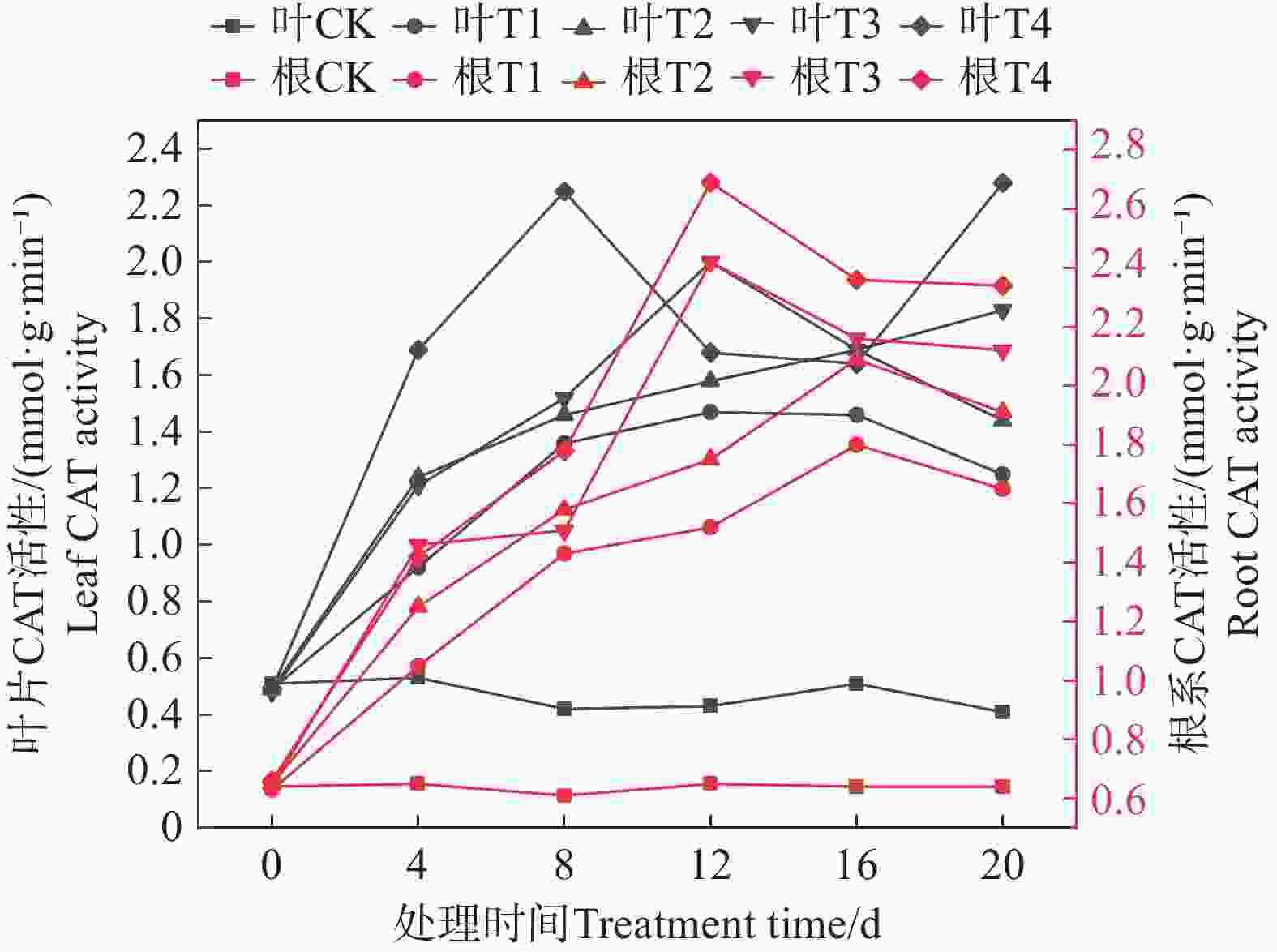
由图8可知,随着盐胁迫浓度的增加,矮蕉幼苗叶片的CAT活性变化趋势如下:除T4处理呈“上升−下降−上升”的趋势外,其余处理均表现为先上升后下降。其中,T1处理在第12天达到最大值,为1.47 mmol·g−1·min−1;T2处理在第16天达到最大值,为1.69 mmol·g−1·min−1;T3处理在第12天达到最大值,为2.00 mmol·g−1·min−1;T4处理则在第8天和第20天分别出现峰值,分别为2.25 mmol·g−1·min−1和2.28 mmol·g−1·min−1。
对于矮蕉幼苗根系的CAT活性,随着盐胁迫浓度的增大,各处理均呈现先上升后下降的趋势。T1和T2处理在第16天达到最大值,分别为1.80 mmol·g−1·min−1和2.09 mmol·g−1·min−1;T3和T4处理在第12天达到最大值,分别为2.42 mmol·g−1·min−1和2.69 mmol·g−1·min−1。结果表明,盐胁迫可能提高矮蕉幼苗的CAT活性,且高浓度盐胁迫更能刺激CAT活性达到较高峰值。在盐胁迫条件下,根系的CAT活性高于叶片,且上升速度更快。
-
叶绿素对植物的光合作用至关重要,其含量变化能够直接反映植物的光合能力。植物在受到盐胁迫时,叶绿素含量通常会不断下降[5]。本实验中,矮蕉幼苗在盐胁迫下的叶绿素含量持续减少,这与马铃薯(Solanum tuberosum)中的研究结果一致[6]。
细胞膜是植物细胞与环境进行物质交换的重要屏障[7],也是盐胁迫最敏感的作用靶点。本试验中,盐胁迫下矮蕉幼苗的叶质膜透性不断上升,这与桂花(Osmanthus fragrans)中的变化趋势一致[8]。
脯氨酸是一种渗透调节物质,能够降低细胞的渗透势,帮助细胞在盐胁迫下维持水分平衡,防止膜脂过氧化,从而保持细胞膜的完整性[9]。本实验中,盐胁迫下矮蕉幼苗的游离脯氨酸含量持续上升,这与大豆(Glycine max)在盐胁迫下的表现相同[10]。
可溶性蛋白可以增加细胞质浓度,降低细胞水势[11]。本实验中,矮蕉幼苗叶片和根系中的可溶性蛋白含量均呈先上升后下降的趋势,表明矮蕉幼苗能够通过积累可溶性蛋白来抵抗盐胁迫,这与甜瓜(Cucumis melo)中的变化规律一致[12]。
MDA是膜脂过氧化的产物,其含量可反映盐胁迫的强度及膜系统的损伤程度[13]。本研究结果表明,矮蕉幼苗叶片和根系的MDA含量均持续增加,这与番石榴(Psidium guajava)中的研究结果一致[14]。根系MDA含量的增幅显著高于叶片,说明根系可能承受了更严重的损伤,这可能是由于根系比叶片更早对盐胁迫作出反应。
盐胁迫会破坏植物体内活性氧(ROS)产生与清除之间的平衡。为应对氧化胁迫,植物激活了以SOD、POD、CAT为核心的抗氧化酶系统[15]。本实验中,矮蕉幼苗叶片和根系中的SOD、POD、CAT活性均呈先上升后下降的趋势,这与水稻(Oryza sativa)中的变化一致[16]。从时间进程上看,SOD是最早被激活的抗氧化酶,尤其是在高浓度盐胁迫下;POD和CAT活性的峰值出现时间晚于SOD,表明SOD作为第一道防线首先发挥作用,随后POD和CAT协同清除代谢过程中产生的H2O2。盐胁迫下,矮蕉幼苗根系的相对损伤程度大于叶片,不同处理之间MDA含量的差异在根系中更为明显。根系中的可溶性蛋白含量高于叶片,表现出更强的可溶性蛋白积累能力。根系SOD活性的相对激活强度大于叶片,且根系SOD活性在达到峰值后维持时间更长。根系POD活性的变化趋势相对平缓,多呈单峰或缓慢上升模式,而叶片POD活性波动更为剧烈,出现双峰现象。同时,根系的CAT活性高于叶片,且上升速度更快。根系的抗氧化酶活性整体高于叶片,且达到最大值所需时间更短,说明根系作为盐胁迫的感应器官,其抗氧化防御能力更强、反应更迅速。较高浓度的盐胁迫诱导出更强的抗氧化酶活性,但同时也导致MDA含量增加。SOD、POD、CAT活性在盐胁迫后期开始下降,这可能是由于矮蕉幼苗逐渐适应了盐胁迫,或者盐胁迫强度已超过其耐受极限,导致植株濒临死亡。
-
本研究以矮蕉幼苗为材料,通过胁迫处理,探究盐胁迫对其生理指标的影响。结果表明:随着盐胁迫浓度的升高和处理时间的延长,矮蕉幼苗的叶绿素含量逐渐下降;渗透调节物质脯氨酸和可溶性蛋白含量则逐渐上升;叶片质膜透性和丙二醛(MDA)含量持续升高;而抗氧化酶SOD、POD、CAT的活性呈先升高后降低的趋势。这表明,矮蕉幼苗在盐胁迫下,能够通过大量积累脯氨酸和可溶性蛋白等渗透调节物质,并提高SOD、POD、CAT等抗氧化酶活性,从而减轻盐胁迫造成的伤害。在盐胁迫条件下,根系因直接接触土壤中的盐分,最先感知渗透胁迫与离子毒害,因此能迅速启动相应的反应机制,包括积累渗透调节物质和抗氧化酶。根系的保护机制强于叶片,但MDA在根系中的积累也更为严重。研究结果可为海南矮蕉抗盐品种的选育及推广种植提供参考依据。
Effects of salt stress on physiological indices of young seedlings of dwarf banana in Hainan Province
DOI: 10.15886/j.cnki.rdswxb.20260049
- Received Date: 2026-03-16
- Accepted Date: 2026-04-04
- Rev Recd Date: 2026-04-03
-
Key words:
- Dwarf banana /
- salt stress /
- physiological index /
- antioxidant enzymes
Abstract: Seedlings of dwarf banan (Musa nana) in Hainan were treated with NaCl solutions at concentrations of 90, 120, 150, and 200 mmol·L-1 to analyze the effects of salt stress on their physiological indices. The leaves and roots of the seedlings were colleced to determine the leaf plasma membrane permeability, and their chlorophyll content, proline content, soluble protein content, malondialdehyde (MDA) content, and the activities of superoxide dismutase (SOD), peroxidase (POD), and catalase (CAT) at 4, 8, 12, 16, and 20 days after stress treatment, respectively. The results showed that with an increase in NaCl concentration and treatment duration, leaf plasma membrane permeability, proline content, and MDA content exhibited an upward trend. The soluble protein content and the activities of SOD, POD, and CAT initially increased and then decreased whereas chlorophyll content showed a continuous decline. These findings indicate that under salt stress conditions, dwarf banana seedlings can alleviate stress-induced damage to a certain extent through physiological regulation and the protective antioxidant enzyme system.
| Citation: | Wang Hao, Wei Junya, Liu Debing. Effects of salt stress on physiological indices of young seedlings of dwarf banana in Hainan Province[J]. Journal of Tropical Biology. doi: 10.15886/j.cnki.rdswxb.20260049 |






 DownLoad:
DownLoad: