-
油莎豆(Cyperus esculentus)隶属禾本目,又名油莎草、虎坚果,为莎草科莎草属的多年生草本C4植物[1-4]。油莎豆的产油率高和适应性广(如适合沙化、盐碱等边际土地种植不占用传统农业耕地)[5-6]使其成为替代进口大豆、减少食用油对外依赖的重要作物。同时,油莎豆也是迄今为止唯一已知在块茎中高水平积累油脂的新型油料作物,油脂含量占干质量的20%以上,其中,油酸含量占总脂肪酸的60%~75%,是研究营养组织高水平积累油脂的模式植物[7]。
植物油脂的生物合成可简化为“糖→乙酰-CoA→脂肪酸→三酰甘油(Triacylglycerol,TAG)”4步。首先,蔗糖经糖酵解在细胞质生成丙酮酸,丙酮酸通过丙酮酸转运体(PPT)进入质体,被丙酮酸脱氢酶复合体(PDHC)转化为乙酰-CoA;随后,乙酰-CoA羧化酶(ACC)和脂肪酸合酶(FAS)依次催化碳链延长,生成16:0-ACP与18:1-ACP。脂肪酸经硫酯酶(FATB/FATA)释放后,由长链酰基-CoA合成酶(LACS)重新酯化为酰基-CoA,并通过酰基转移酶DAGAT/PDAT途径在内质网(Endoplasmic Reticulum,ER)装配成三酰甘油,最终以油体形式储存[8]。在此过程中,多个转录因子通过激活或抑制功能基因的表达,精细调控油脂的生物合成[9]。目前,对植物油脂合成的认识多局限在种子中,非种子组织的研究较少。WRI1(WRINKLED1)基因是调控种子中油脂合成的关键转录因子[10],WRI2作为WRI1的旁系同源基因,在种子中,尚未有证据表明其参与油脂调控。但来源于牛油果(Persea americana)的PaWRI2在烟草(Nicotiana tabacum)中过表达后,能显著提高叶片中TAG含量,PaWRI2具有完整的AP2结构域且位于N端,但无C端的PEST基序[11]。与此类似,牛油果中果皮油脂合成与其他油料物的种子类似:脂肪酸合成基因普遍高表达LACS、WRI2-like及PDAT1基因显著高表达,并且该过程受到WRI家族转录因子的调控[12]。推测WRI2在植物营养组织油脂合成调控具有重要功能。本实验室的研究则表明,在拟南芥wri1-1突变体中表达来自油莎豆的CeWRI2基因,可恢复其种子油脂含量[13],因此,CeWRI2可能具备与拟南芥AtWRI1相似的油脂合成调控功能。尽管WRI2基因在不同物种非种子油脂合成中的具有重要的作用,但其具体的的分子作用尚不清楚。酵母双杂交技术(Yeast Two-Hybrid System,Y2H)是一种用于研究蛋白质-蛋白质相互作用的经典分子生物学技术[14]。在本研究中,选取油莎豆的CeWRI2转录因子作为诱饵,借助酵母双杂交技术对油莎豆块茎cDNA文库进行筛选,以期鉴定出与CeWRI2存在互作关系的蛋白,旨在阐明CeWRI2调控块茎油脂高效合成的分子机制。
-
本研究使用的油莎豆材料为‘热研3号’,样本取自中国热带农业科学院文昌试验基地(19°36′ N, 110°45′ E)。研究所用引物信息详见表1,所用载体为中国热带农业科学院热带生物技术研究所保存。
引物名称 Primer 引物序列 Sequence pNC-pGBKT7-CeWRI2-F AGTGGTCTCTGTCCAGTCCTATGGCGGCATCCAGC pNC-pGBKT7-CeWRI2-R GGTCTCAGCAGACCACAAGTTTCCTGGCAGTGGAATG AD-通用引物-F AATACCACTACAATGGATGATG AD-通用引物-R ATGGTGCACGATGCACAGT pNC-pGADT7-CeHB1-F AGTGGTCTCTGTCCAGTCCTATGAAGAGACTCAACAGCTCCGATTCCC pNC-pGADT7-CeHB1-R GGTCTCAGCAGACCACAAGTACTCCATTGCTGATCGGCGGAATAGT qPCR-CeWRI2-F AGTTCAGGAAGAGAAGGATGGT qPCR-CeWRI2-R GGTGAAGAAACAACATTTGTCCA qPCR-CeHB1-F TTTCGGCTCCCCCTCTTCTA qPCR-CeHB1-R ATAGTACCAAGCGAGCGACG CePDF2-F ACTTGAGCCGCAGGATTGTG CePDF2-R CCTCATTATCACGCAAAAGACG Table 1. Primer sequence information
-
pGBKT7-CeWRI2构建 根据油莎豆基因组数据库信息设计CeWRI2基因克隆引物,以本实验室保存的
1304 -SubN-CeWRI2重组质粒为模板,将扩增产物纯化后通过Nimble Cloning技术连接到pGBKT7载体上,转化大肠杆菌DH5α感受态,随后使用pGBKT7-CeWRI2-F、pGBKT7-CeWRI2-R引物(表1)对转化菌落进行PCR初筛,并对阳性克隆进行测序验证。 -
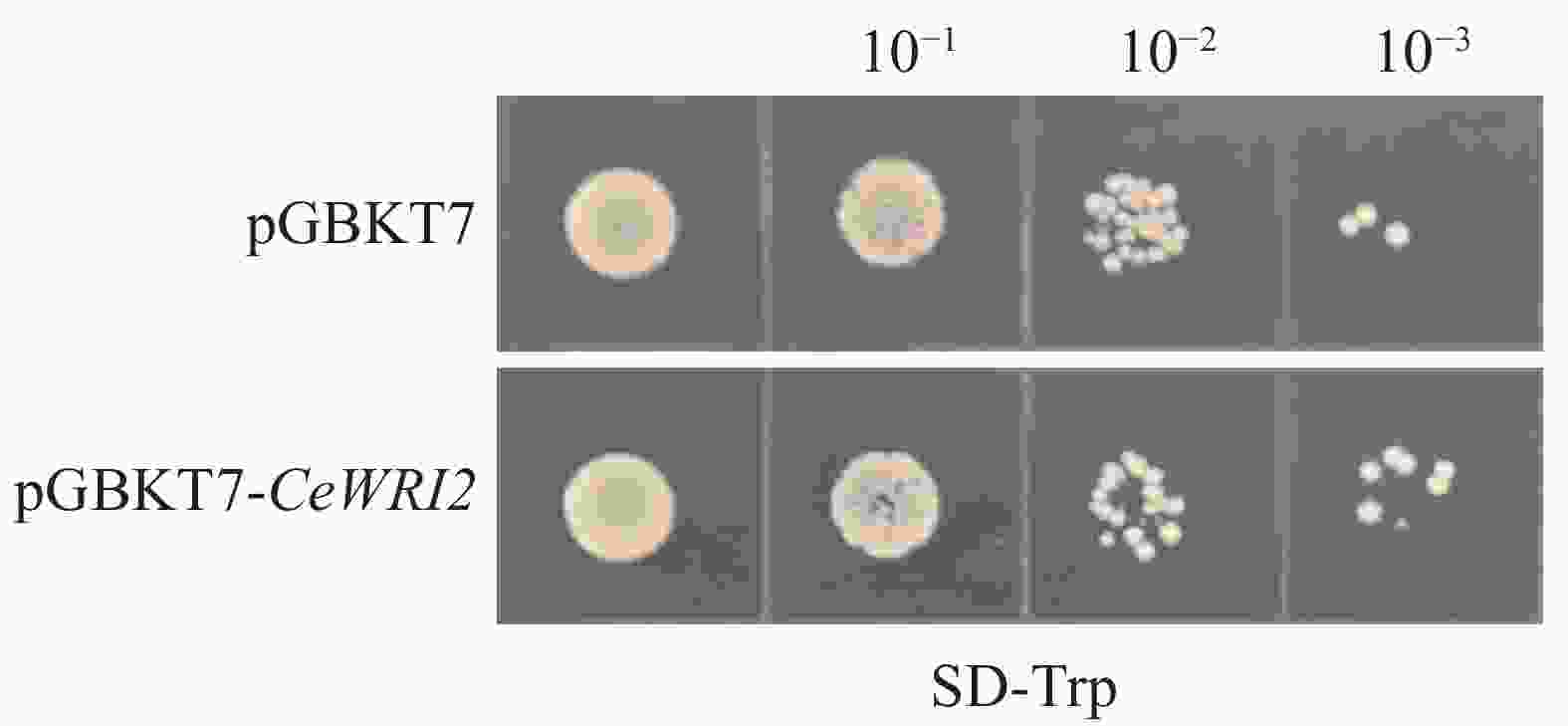
分别将pGBKT7空载质粒及pGBKT7-CeWRI2重组质粒转化至Y2H-Gold酵母感受态细胞中,涂布于SD/-Trp固体培养基上,28 ℃倒置培养2~3 d。随后分别挑取单克隆用无菌水稀释,将酵母菌液OD600值调整至0.6,随后进行梯度稀释(1︰1、1︰10、1︰100、1︰1 000)。每个稀释度取10 μL点接于SD/-Trp固体培养基,28℃倒置培养2~3 d,最终观察并记录菌落生长状况。
-
将pGADT7空载质粒与pGBKT7-CeWRI2重组质粒共转化至Y2H-Gold酵母感受态中,均匀涂布于SD/-Trp-Leu培养基,28℃培养2~3 d。挑取单克隆菌落重悬于无菌水,经梯度稀释后,分别取10 μL菌液点接至以下培养基:SD/-Trp-Leu、SD/-Trp-Leu-His-Ade及含有不同浓度(5、10、15、20、25 mmol·L−1)3-氨基-1,2,4-三氮唑(3-AT)的SD/-Trp-Leu-His-Ade培养基。以共转化pGBKT7-p53与pGADT7-largeT作为阳性对照,共转化pGBKT7-laminC与pGADT7-largeT作为阴性对照。所有平板置于28℃培养2~3 d后,观察并记录酵母菌落生长状况。
-
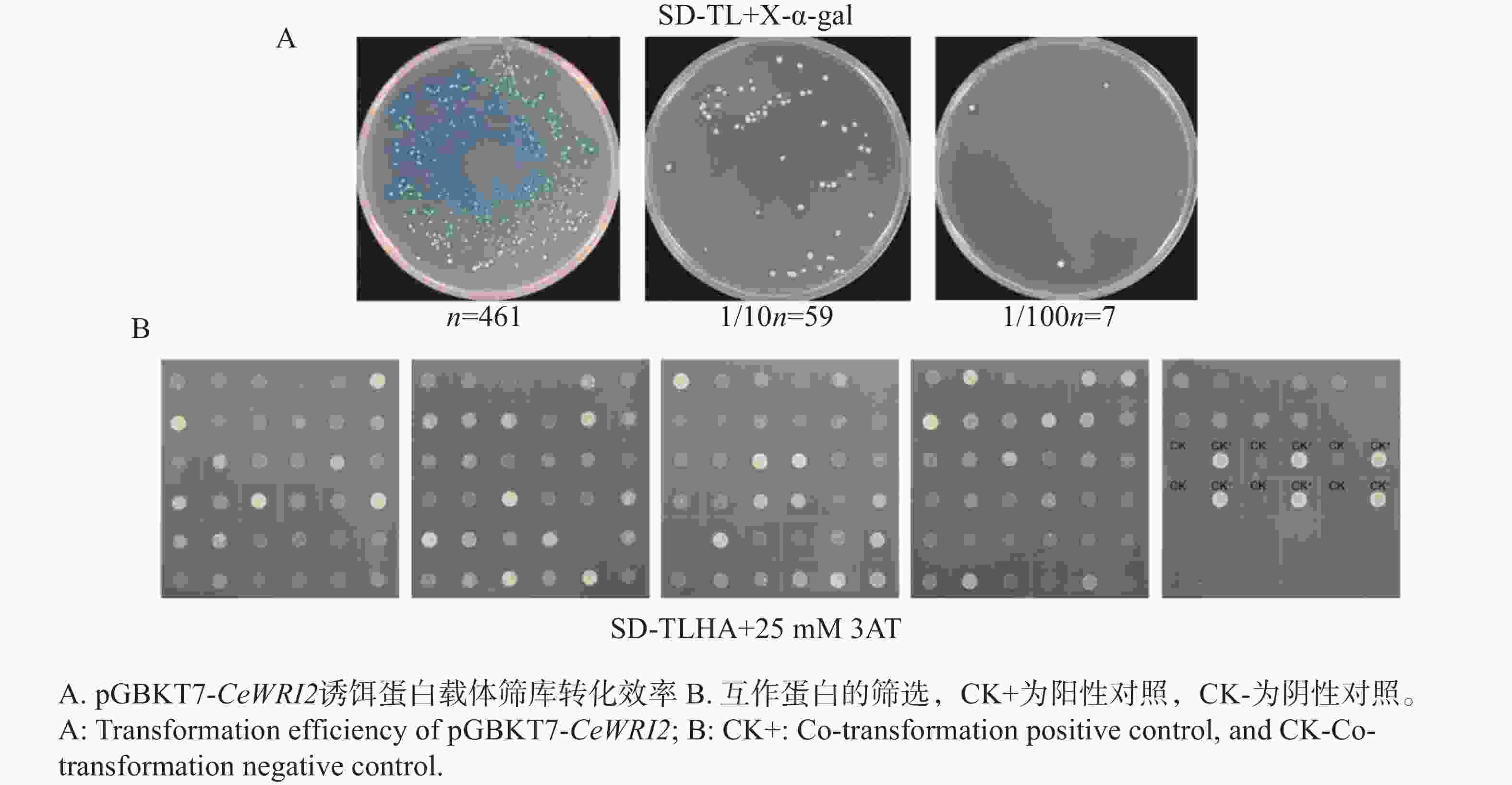
利用PEG/LiAc法,将油莎豆pGADT7-cDNA文库转入含有诱饵质粒pGBKT7-CeWRI2感受态中,吸取20 μL培养物,经梯度稀释后,涂布于SD/-Trp-Leu平板,用于检测文库的转化效率。其余涂SD/-Trp-Leu-His+25 mmol·L−1 3AT+X-α-gal平板,每块200 μL,共40块。挑取培养基上生长良好的菌落提取酵母质粒,转化TOP10感受态细胞,PCR验证后,擎科生物公司测序,获得与CeWRI2互作蛋白的编码基因序列。
-
根据测序结果,在油莎豆本地数据库中进行BLAST比对,获取同源性最高的编码序列。设计上下游引物CeHB1-F/R,使用Takara(R045A)高保真酶Prime STAR®Max DNA Polymerase,以cDNA为模板,扩增目标产物,通过1%(w)凝胶电泳检测PCR扩增产物,纯化回收后得到目的片段,构建pGADT7-CeHB1载体,转化DH5α大肠杆菌,擎科生物测序,确定获得候选的CeHB1基因序列。
-
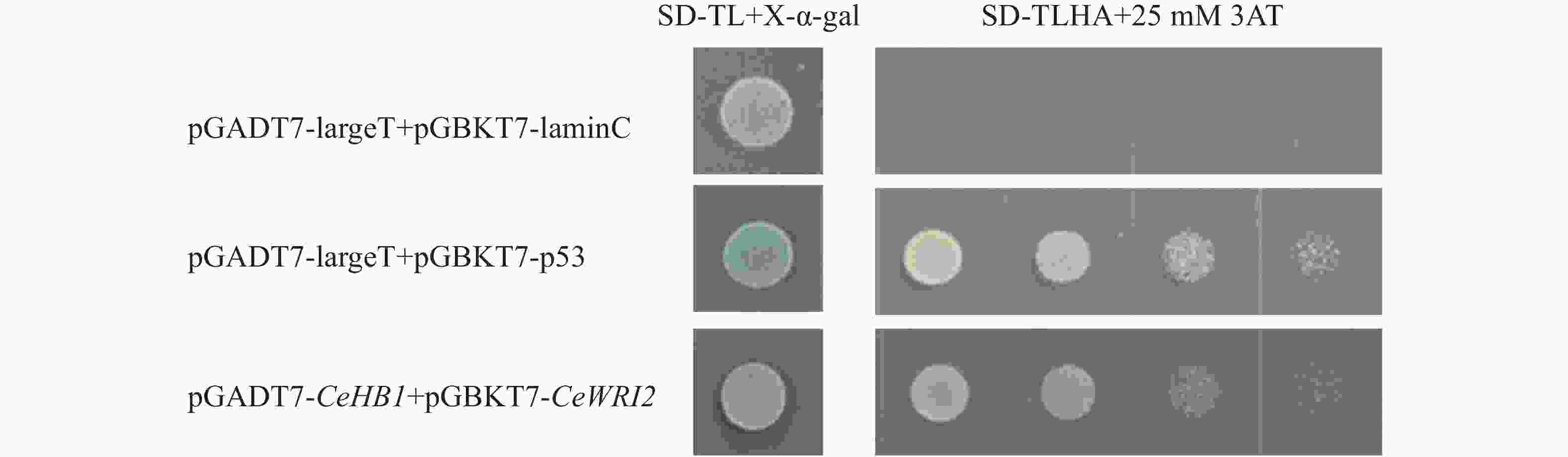
对油莎豆候选基因CeHB1进行回转验证。将pGBKT7-CeWRI2诱饵质粒与pGADT7-CeHB1质粒共转到Y2H-Gold酵母感受态,涂布SD/-Trp-Leu培养基上,28℃培养2~3 d,挑取单克隆经浓度梯度稀释后点接SD/-Trp-Leu、SD/-Trp-Leu-His-Ade+25 mM 3AT固体培养基上,28℃倒置培养2~3 d,观察酵母生长情况。
-
提取油莎豆块茎、成熟叶、叶鞘、花、花茎、根、匍匐茎组织的总RNA,使用艾科瑞反转录试剂盒进行反转录,以CePDF2作为内参[15]进行实时荧光定量PCR,每个样品设置3个生物学重复,采用2−△△Ct法对目的基因进行相对表达分析。
-
用Duncan单因素方差分析不同组织基因表达数据间的差,用Prism8软件作图。
-
以本实验室保存的
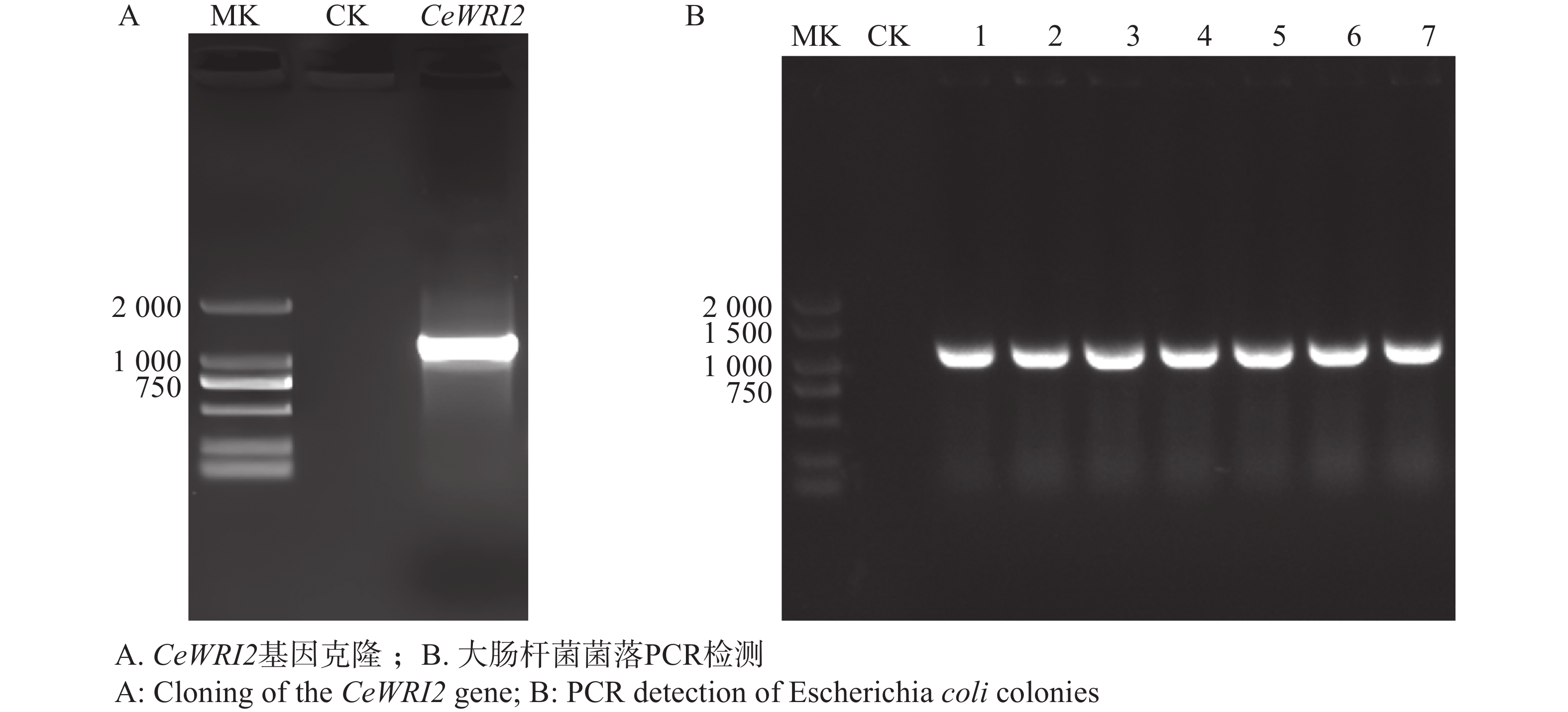
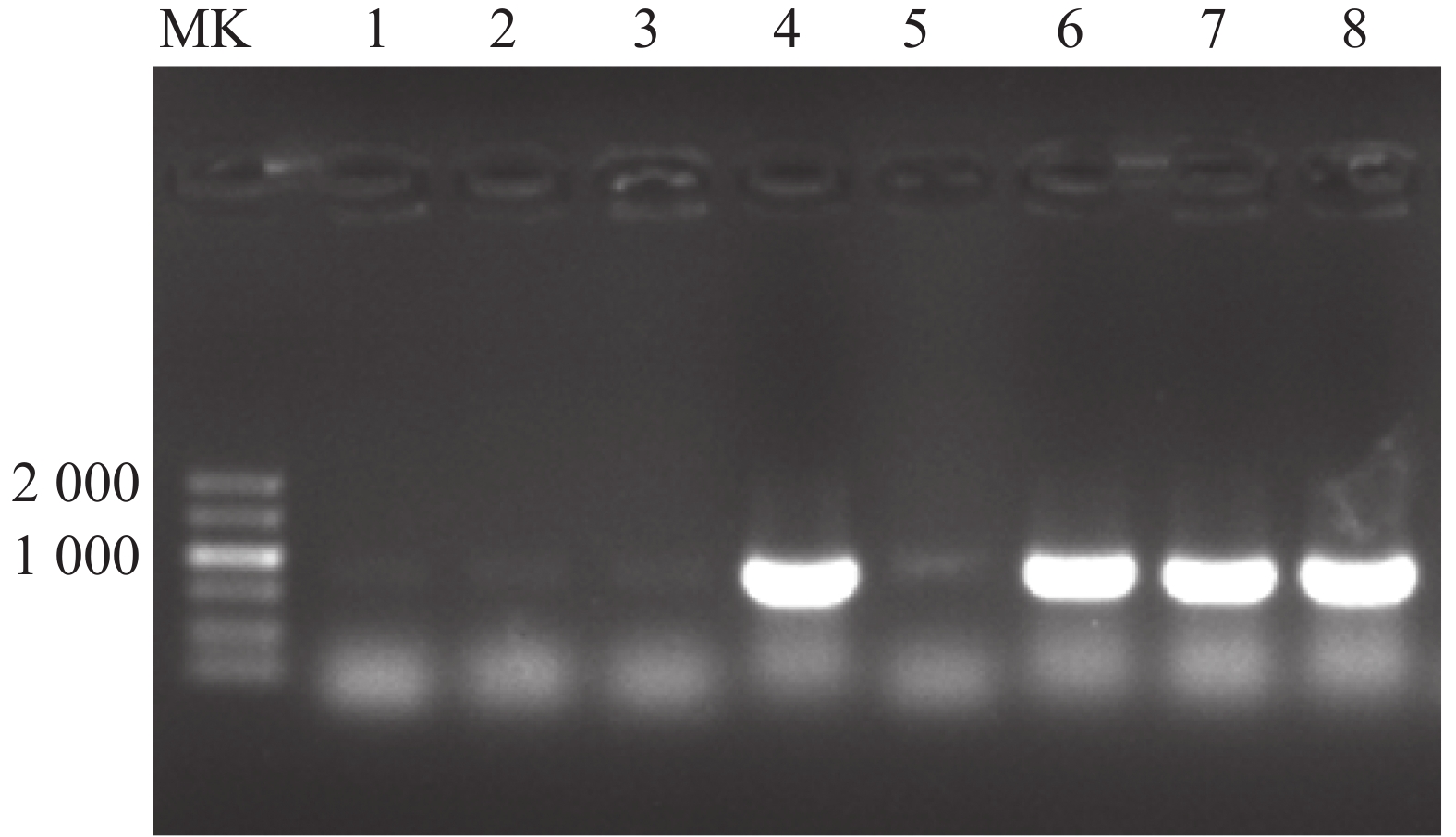
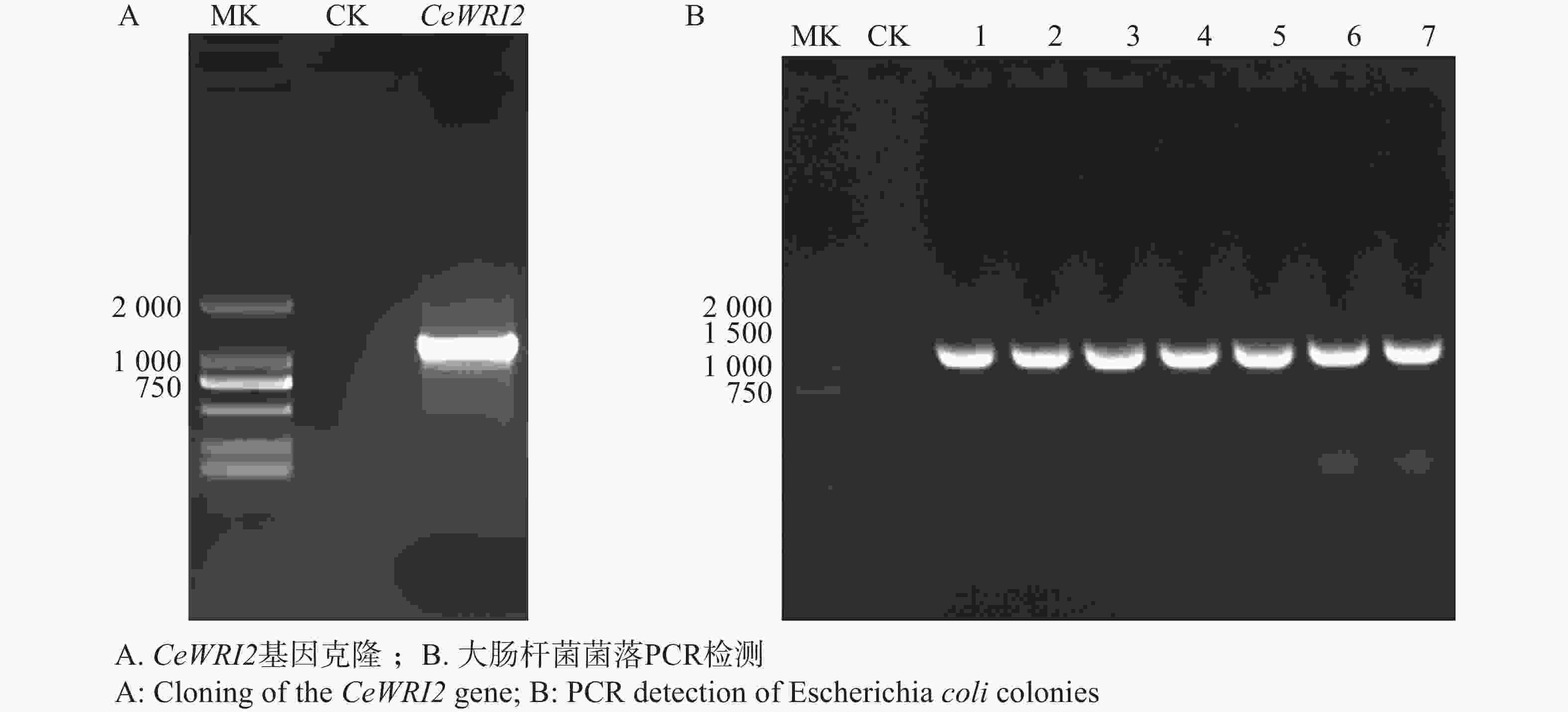
1304 -SubN-CeWRI2重组质粒为模板,扩增CeWRI2基因的完整编码区(CDS)。经1%(w)琼脂糖凝胶电泳检测,可见一条大小约1 173 bp的单一明亮条带(图1-A),与CeWRI2基因预期长度一致。切胶回收该片段后,利用同源重组技术将其克隆至pGBKT7载体中。转化后通过菌落PCR筛选阳性克隆(图1-B),经测序验证正确后提取质粒,获得pGBKT7-CeWRI2诱饵载体,供后续实验使用。 -
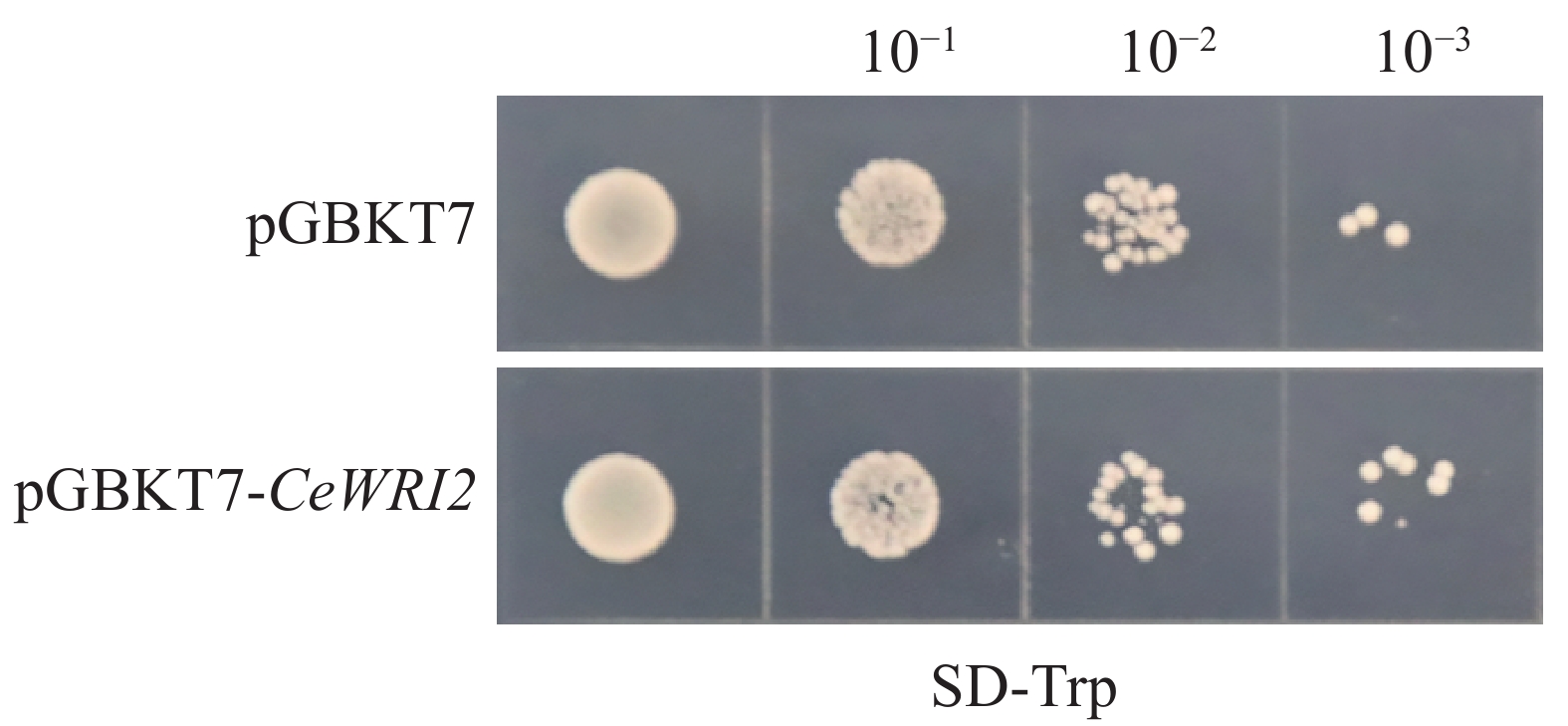
为了确保诱饵蛋白CeWRI2在酵母细胞中表达后不影响后续酵母双杂交筛选,分别将成功构建的pGBKT7-CeWRI2诱饵载体与空载pGBKT7转化至Y2H-Gold酵母感受态细胞中。对比结果显示,2种质粒转化后的酵母菌落生长状态未见明显差异(图2),说明CeWRI2未对酵母细胞的正常生长产生毒性影响,所构建的载体可用于酵母双杂交,筛选与其互作的蛋白。
-
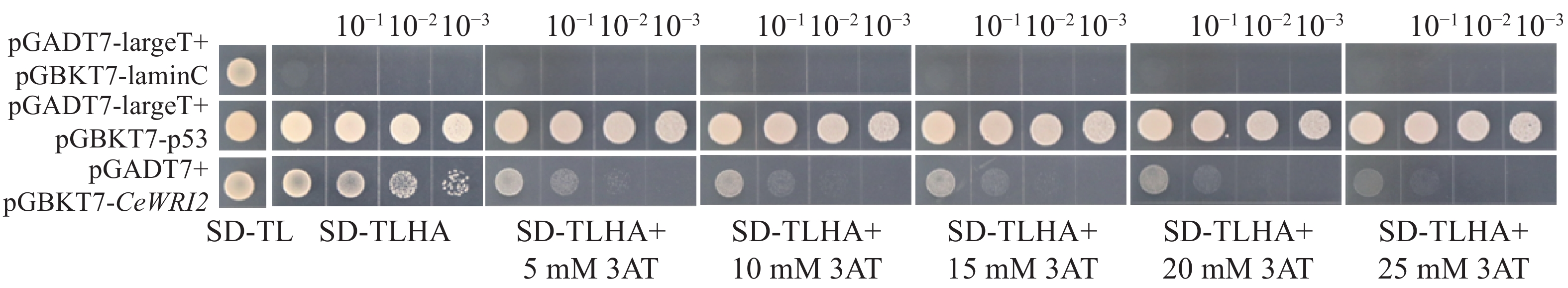
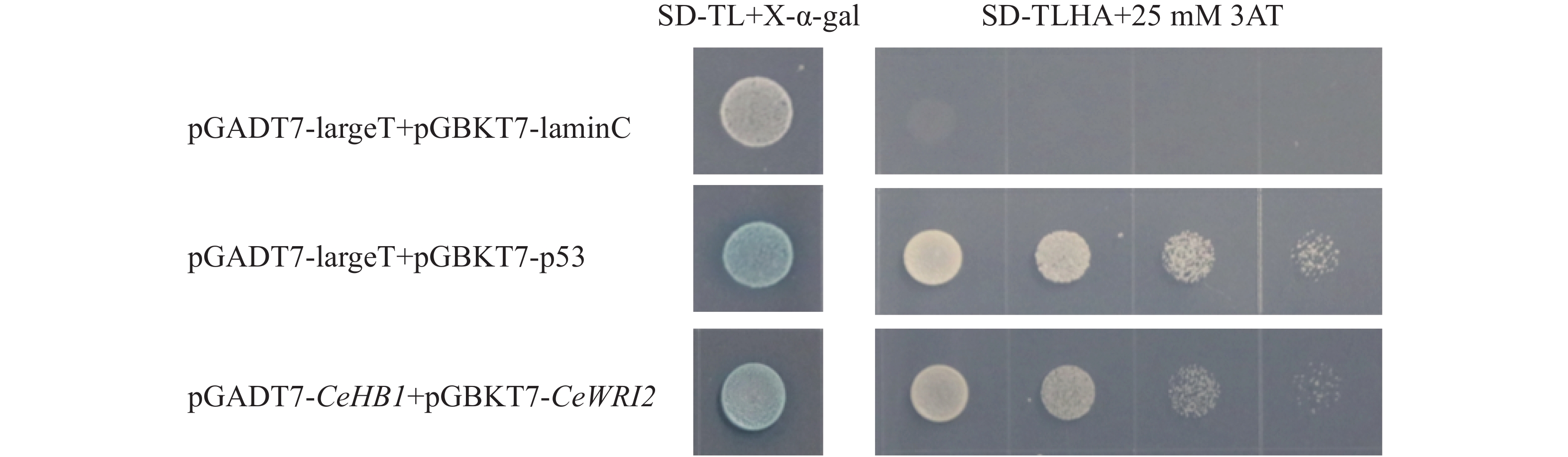
为了避免诱饵蛋白CeWRI2自激活造成酵母双杂交筛选出现假阳性结果,将pGBKT7-CeWRI2与空载pGADT7共转化至Y2H-Gold酵母菌株。结果由图3显示,在SD/-Trp-Leu-His-Ade缺陷培养基上,阳性对照(pGADT7-largeT+pGBKT7-p53)与实验组(pGADT7+pGBKT7-CeWRI2)均可正常生长,而阴性对照(pGADT7-largeT+pGBKT7-lamC)则无法生长,表明CeWRI2本身具有转录自激活能力。进一步实验发现,在培养基中添加25 mmol·L-1
3-AT(3-amino-1,2,4-triazole)可有效抑制该自激活现象;后续酵母双杂交实验均添加25 mmol·L−1的3-AT。
-
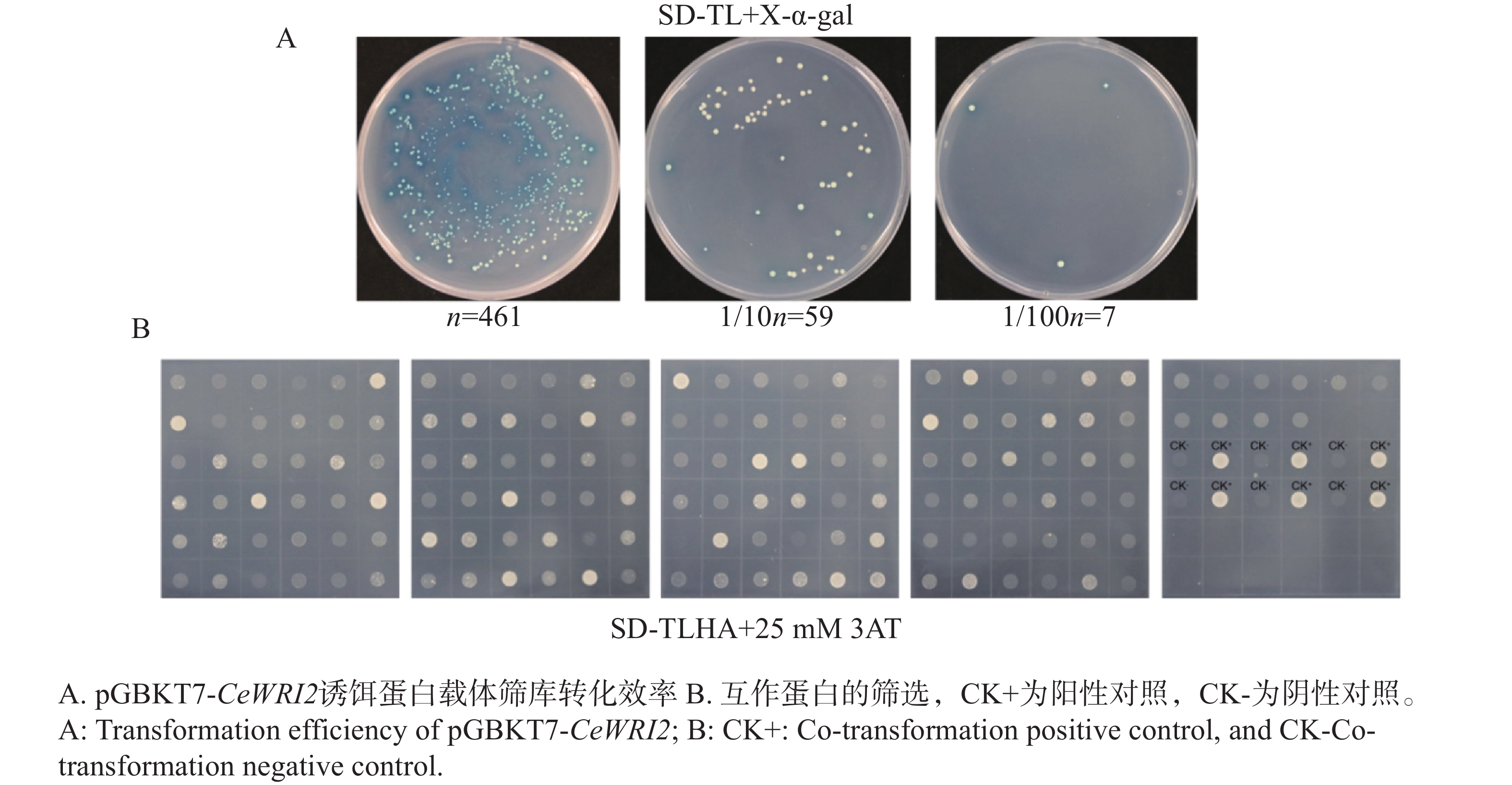
将含有pGBKT7-CeWRI2的Y2H-Gold酵母菌液培养至0D600=0.6,制备感受态,利用本课题组保存的油莎豆pGADT7-cDNA文库质粒,对CeWRI2的互作蛋白进行筛选。转化效率通过涂布SD/-TL平板检测。每100 μL转化混合物获得约461个克隆,1/10稀释在SD/-TL/X-α-gal平板上长出59个克隆,1︰100稀释长出7个克隆(图4-A)。最终在SD/-Trp-Leu-His-Ade缺陷型培养基上获得49个阳性酵母克隆(图4-B)。提取阳性酵母菌质粒,转入TOP10酵母感受态,用pGADT7的载体引物进行菌落PCR检测并测序,测序结果通过NCBI网站以及油莎豆本地BLAST序列比对共筛选出能进行功能注释的17个候选蛋白信息(表2)。这17个蛋白中仅有2个为转录因子分别属于HD-ZIP和VOZ家族,其同源蛋白在植物生长发育和逆境胁迫响应等过程起重要作用;其余15个则为功能蛋白,功能蛋白又分为9种分子功能,包括信号转导与激酶活性、物质转运、蛋白质稳态、代谢与能量调控、核酸稳态、细胞结构与抗氧化以及底物识别与结构域蛋白。基于CeWRI2的筛库结果,选择编号1的候选蛋白同源异形盒−亮氨酸拉链蛋白HOX16-like开展后续功能研究,该蛋白属于HD-ZIP转录因子家族中的HD-ZIP I亚家族,包含1个高度保守的HD结构域[16]。前期研究表明,HD-ZIP蛋白主要通过脱落酸(ABA)介导的信号转导途径调节下游逆境相关基因的表达,并通过调节植物的生长发育来调节植物的抗逆性[17]。由于ABA在油脂调控中的作用,因此推测该蛋白可能与“碳−氮再分配”相关。
编号Code GenBank登录号
GenBank accession number基因注释
Gene annotation可能的生物学功能
Putative function所属类别Family/Category 转录因子
(Transcriptional factor)1 XM_047193152.1 HOX16-like蛋白
homeobox-leucine zipper protein HOX16-likeABA信号转导调控下游逆境基因表达与植物发育[18] Homeobox-ZIP(HD-ZIP)转录因子家族 2 XM_073138857.1 维管植物单锌指蛋白
1transcription factor VOZ1-like促进植物开花[19]和降低非生物胁迫耐受力[20] VOZ(Vascular plant One-Zinc finger)转录因子家族 功能基因
(Functional protein)3 XM_078315846.1 MAPKKK3-like蛋白激酶
Mitogen-activated protein kinase kinase kinase 3-like介导植物逆境应答与发育信号
转导[21]信号转导与激酶活性 4 XM_078324884.1 WNK6型丝氨酸/苏氨酸蛋白激酶
Probable serine/threonine-protein kinase WNK6参与光周期开花调控[22]和渗透胁迫响应[23] 信号转导与激酶活性 5 XM_078303601.1 磷酸糖/磷酸转运体
sugar phosphate/phosphate translocator磷酸丙糖−无机磷酸反向转运[24] 物质转运 6 XM_078322050.1 TOC75-III叶绿体外被膜易位通道的β−桶孔蛋白
TOC75-III, the β-barrel pore protein of the
chloroplast outer-envelope translocation channel介导核编码前体蛋白ATP/GTP-依赖型跨膜导入[25] 物质转运 7 XM_003746044.1 DDB1-CUL4相关因子7
DDB1-CUL4-associated factor 7参与蛋白质泛素化/蛋白质降解调控蛋白质降解[26] 蛋白质稳态
(泛素-蛋白酶体途径)8 XM_078299691.1 DnaJ A6-like HSP40共伴侣蛋白 响应非生物胁迫,维持细胞蛋白
稳态[27]蛋白质稳态
(分子伴侣)9 MF782862.1 真核翻译起始因子4Aeukaryotic translation initiation factor 4A DEAD-box RNA 解旋酶,参与翻译起始[28] 蛋白质稳态
(翻译调控)10 XM_023888370.2 叶绿体DnaJ 8型分子伴侣chloroplastic chaperone protein DnaJ 8 维持叶绿体蛋白稳态与光合作用效率[29] 蛋白质稳态
(叶绿体分子伴侣)11 XM_078310458.1 多聚泛素polyubiquitin 作为蛋白降解的通用标签[30] 蛋白降解相关 12 XM_078301212.1 ANAH类水解酶Adenine nucleotide alpha hydrolases-like 水解ADP-核糖等[31] 代谢与能量调控 13 XM_078317190.1 烯醇化酶2(Enolase 2, ENO2) 参与糖酵解[32],调控逆境基因表达[33] 代谢与能量调控 14 XM_078298727.1 Tudor型核糖核酸酶(Tudor-RNase 2-like) 维持细胞RNA稳态[34] 核酸稳态 15 XM_078320453.1 细胞骨架蛋白Tubulin β-7 构成微管,参与细胞骨架形成[35] 细胞结构与抗氧化
(细胞骨架)16 XM_078304760.1 过氧化氢酶Bcatalase isozyme B 催化过氧化氢分解,起抗氧化作用[36] 细胞结构与抗氧化
(抗氧化酶)17 XM_078324765.1 Met-10+ like / Kelch repeat双结构域蛋白 底物识别型调控蛋白[37] 调控蛋白
(底物识别)Table 2. Information CeWRI2 interacting proteins
-
为进一步验证候选蛋白CeHB1与CeWRI2蛋白的互作关系,进行酵母双杂交点对点验证。在油莎豆本地数据库中获取CeHB1编码序列,设计特异性引物,CeHB1-F/R(表1),以油莎豆块茎cDNA为模板克隆CeHB1基因,构建pGADT7-CeHB1重组质粒。阳性克隆测序验证后(图5),与pGBKT7-CeWRI2诱饵载体共转到Y2H-Gold酵母菌株。转化后在SD/-Trp-Leu+X-α-gal培养基上均能生长,说明pGADT7-CeHB1和pGBKT7-CeWRI2已转化酵母并表达。挑取单克隆点于SD/-Trp-Leu-His-Ade+25 mM 3AT固体培养基上培养,除阴性对照外,所有的实验组均能正常生长,表明CeWRI2与CeHB1存在蛋白互作关系(图6)。
-
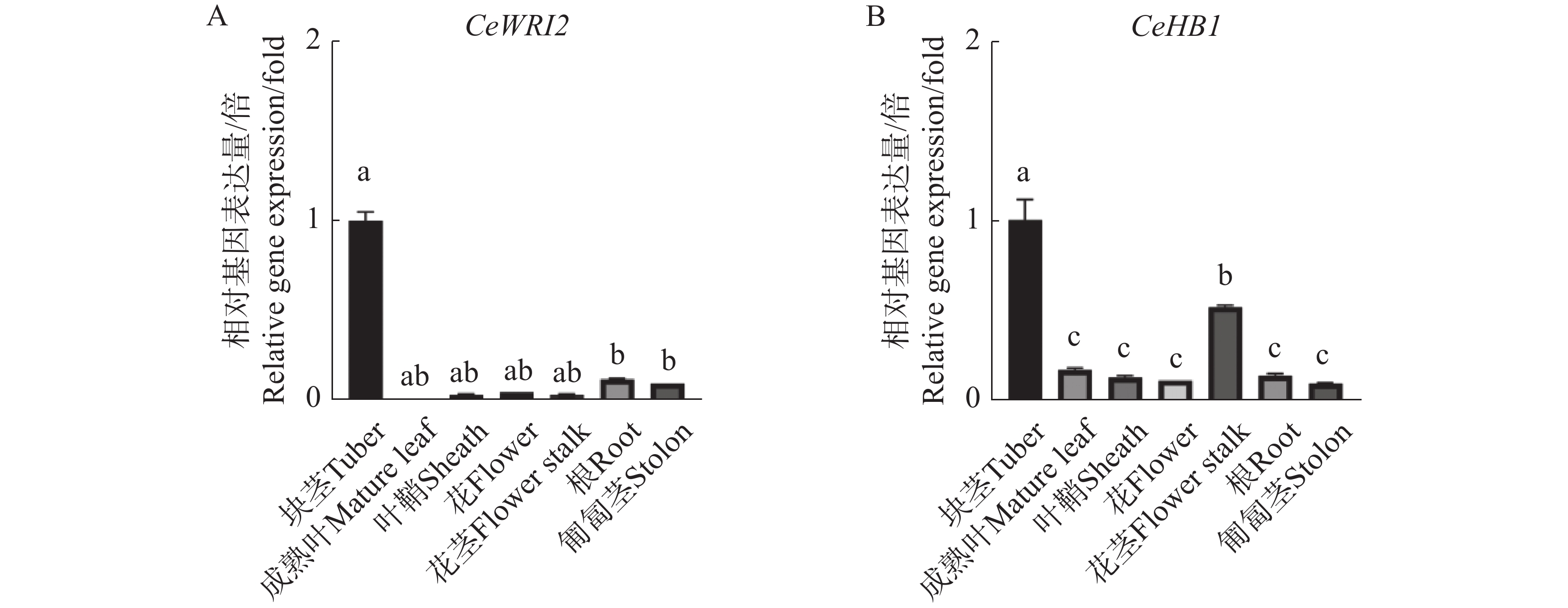
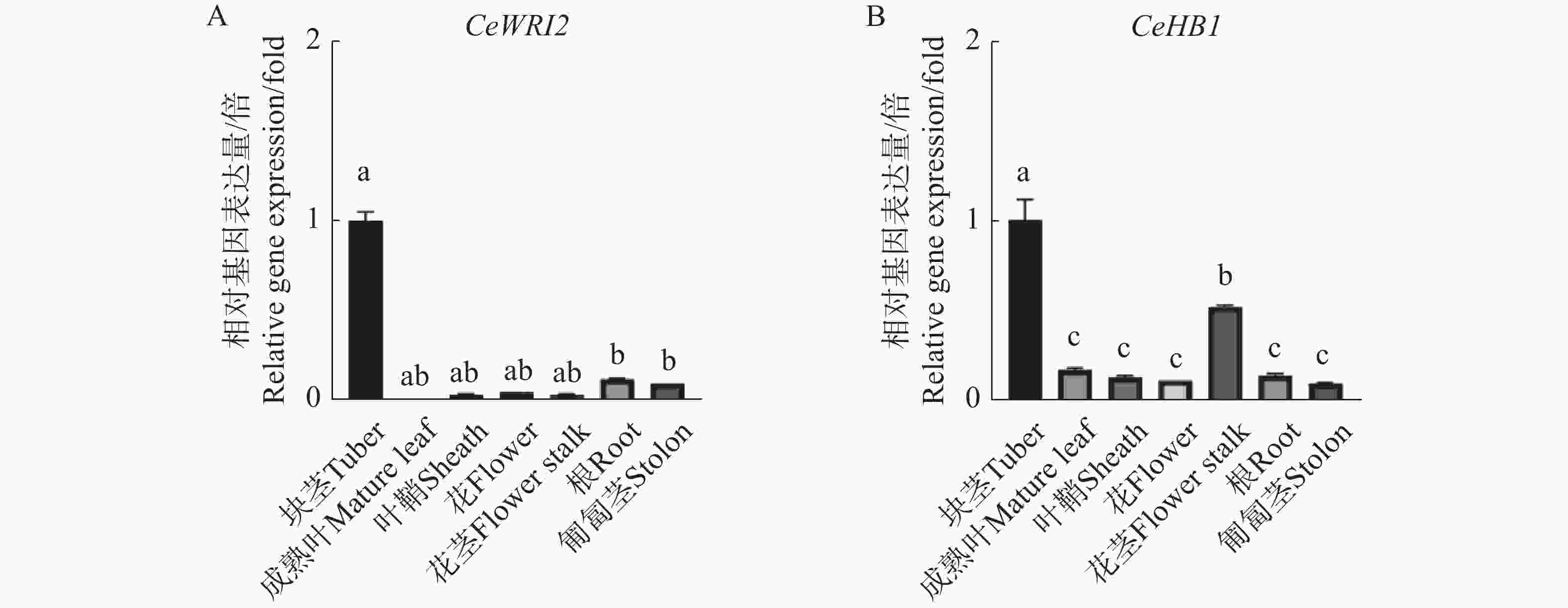
为了揭示CeHB1基因的表达特性,通过实时荧光定量分析了CeHB1在油莎豆叶片、叶鞘、花、花茎、匍匐茎、根和块茎这7个主要组织中的表达模式(图7)。结果表明,CeHB1在油莎豆块茎中的表达丰度最高,其次是花茎,在其余组织中表达水平显著降低(图7-B)。结果表明,CeWRI2(图7-A)与CeHB1的表达模式具有高度相似性,两者均在块茎中表达量最高,表现出明显的协同表达趋势。这说明CeHB1有可能通过调控油莎豆块茎的生长发育或油脂合成相关基因的表达,参与油莎豆中的油脂积累。
-
WRI2属于AP2/ERF转录因子超家族中的AP2亚族(APETALA2-like group),其特征为含有1~2个约60~70个氨基酸的AP2/ERF DNA结合结构域。在拟南芥中,WRI2与WRI1、WRI3、WRI4共同构成WRI1-like亚组(亦称ANT类群),在调控脂肪酸从头合成及碳源分配中发挥重要的作用。在拟南芥中,存在3个成员,AtWRI1、AtWRI2和AtWRI3/4。其中,AtWRI2不能互补atwri1-1的功能,被认为无法参与油脂的代谢调控[38]。但在牛油果中,PaWRI2具有转录激活功能,并且已经证实WRI2在牛油果中参与油脂的调控[11]。课题组前期研究发现,油莎豆块茎中克隆的WRI1旁系同源基因CeWRI2与牛油果PaWRI2具有相似的理化性质。随着块茎发育,CeWRI2的表达量逐渐上升,且与油脂积累趋势呈正相关,提示其可能参与油脂代谢调控。进一步实验表明,CeWRI2定位于细胞核,并具有转录激活活性。该基因能够互补拟南芥wri1-1突变体表型,且在烟草叶片中瞬时过表达可显著提高油脂含量[13]。推测CeWRI2可能通过与其他转录因子相互作用,调控脂肪酸(Fatty acids,FA)合成和TAG合成相关基因的表达,从而在油莎豆油脂合成中可能发挥重要作用。
本研究通过酵母双杂交技术,筛选与油莎豆转录因子CeWRI2的互作蛋白,成功获得17个候选互作蛋白,为解析其调控块茎油脂积累的分子机制提供了关键线索。17个候选蛋白中,有2个为转录调控因子,分别属于Homeobox-ZIP(HD-ZIP)转录因子家族和VOZ(Vascular plant One-Zinc finger)转录因子家族;HD-Zip I亚家族成员通常响应ABA等逆境信号,调控生长发育[17];拟南芥中的AtVOZ1蛋白和AtVOZ2蛋白均已被证明是作为转录因子发挥功能[39],且能够促进拟南芥开花[40];但在调控开花途径中具有功能冗余,并可以降低拟南芥对非生物胁迫的抗性,增加其对生物胁迫的抗性[20,41]。获得的15个功能蛋白,这些蛋白广泛参与糖与能量代谢、蛋白质稳态、信号转导及细胞结构维持等过程,暗示CeWRI2可能作为“代谢协调枢纽”,通过多维互作网络调控油脂合成。
基于上述筛选,本研究进一步聚焦于HD-ZIP家族成员CeHB1,尽管目前尚无直接证据表明CeHB1本身参与油脂合成,但有研究表明,在拟南芥中响应ABA与干旱胁迫的转录因子MYB96,被证实能直接激活油脂合成关键基因(如DGAT1和PDAT1),从而诱导营养组织中的三酰甘油积累[42];ABA信号通路的核心转录因子ABI4,也被证明可直接结合并激活油脂合成限速酶基因DGAT1的启动子,从而影响种子油脂积累[43]。本研究通过酵母双杂交实验,初步确认其与CeWRI2存在互作。组织特异性表达分析显示,CeHB1在油莎豆不同组织中的表达具有明显差异,其在块茎中的转录水平显著高于其他组织。块茎是油莎豆储存油脂和淀粉的主要库器官,因此,CeHB1的高表达暗示其潜在角色与“库强度”建立或发育有关。然而,本结果仅反映静态表达差异,后续应结合块茎发育不同时期以及基因功能丧失实验,进一步验证CeHB1是否确为调控油莎豆块茎油脂积累的关键因子。本研究仅是初步结果,后续将利用荧光素酶互补实验(Luciferase Complementation Assay,LCA)、双分子荧光互补实验(Bimolecular Fluorescence Complementation,BiFC)等技术在植物体内验证互作,并进一步探究互作对CeWRI2转录活性、蛋白稳定性及亚细胞定位的影响。未来工作应结合转录组、代谢组与ChIP-seq等多组学技术,动态解析CeWRI2及其互作因子调控的下游网络,从而系统地阐明油莎豆块茎高效积累油脂的分子机制,为油莎豆开发利用奠定坚实的理论基础。
Screening and identification of proteins interacting with CeWRI2 in Cyperus esculentus
DOI: 10.15886/j.cnki.rdswxb.20260017
- Received Date: 2025-12-28
- Accepted Date: 2026-02-26
- Rev Recd Date: 2025-02-15
-
Key words:
- Cyperus esculentus /
- CeWRI2 /
- yeast two-hybrid /
- protein-protein interaction /
- lipid biosynthesis regulation
Abstract: Yellow nutsedge (Cyperus esculentus) is an emerging oil crop characterized by its efficient oil accumulation in tubers. However, the regulatory mechanisms underlying oil biosynthesis remain unclear. Previous studies have demonstrated that CeWRI2 not only complements the Arabidopsis wri1-1 mutant but also significantly increases oil content when overexpressed in tobacco leaves. To dissect the molecular network by which CeWRI2 regulates oil accumulation in tubers, 17 candidate interacting proteins were identified through yeast two-hybrid screening, including CeHB1 belonging to the HD-ZIP transcription factor family. Furthermore, yeast two-hybrid assays confirmed the interaction between CeWRI2 and CeHB1. Gene expression analysis showed that CeHB1 was expressed in various tissues including leaves, leaf sheaths, flowers, flower stems, stolons, roots and tubers, with the highest expression level observed in tubers. This expression pattern was similar to that of CeWRI2 , suggesting that CeHB1 may regulate tuber development and oil biosynthesis and accumulation by modulating CeWRI2 .
| Citation: | Wang Ruiling, Zheng Panyan, Li Na, Dong Lian, Huang Jiaquan, Zou Zhi. Screening and identification of proteins interacting with CeWRI2 in Cyperus esculentus[J]. Journal of Tropical Biology. doi: 10.15886/j.cnki.rdswxb.20260017 |








 DownLoad:
DownLoad: