-
鱼腥草(Houttuynia cordata)是三白草科多年生草本植物,2002年被纳入“药食同源”名录,在药品与食品领域均具有较高的应用价值[1-3]。研究表明,鱼腥草富含挥发油、黄酮类、生物碱以及多酚酸等多种化学成分,这些成分赋予其抗氧化、抗炎、抗菌及抗癌等生物活性[4-6]。
鱼腥草在传统生产中多采用一次性采收方式,而在中国部分地区,农户在长期实践中形成了分茬采收的经验性模式,即在生长季节内多次采收地上部分。现有生产实践认为该采收模式有助于维持较为稳定的产量与品质,但其科学依据仍缺乏系统研究,不同采收方式可能影响地上部分活性成分的积累。因此,有必要从化学成分变化及功能活性的角度,对不同采收方法进行系统比较。目前,关于鱼腥草品质形成的研究主要集中于单一采收期、不同部位以及不同生长年限的比较。例如,沈庆庆等[7]研究发现,其地上嫩茎的总黄酮含量高于地下根茎;温倪婷等[8]采用熵权法结合灰色关联度分析法综合评价鱼腥草药材的质量,结果表明,产自广西全州县的鱼腥草整体质量最优;发酵法可增加槲皮苷和槲皮素的含量[9];挥发油含量则与加工方法和采收季节有关[10]。然而,关于鱼腥草地上部分在不同采收季节及同一生长季内不同采收茬次条件下,其化学成分变化与抗氧化活性之间的关联尚缺乏系统研究。采收季节和茬次可能通过影响活性成分的积累水平,进而影响鱼腥草的抗氧化活性。阐明不同采收方法下抗氧化活性的变化规律及其物质基础,对于科学评价鱼腥草生物活性并指导合理采收具有重要意义。
本研究通过UPLC-Q-TOF-MS的代谢组学技术,结合体外抗氧化活性评价方法,系统分析不同茬次及不同采收季节鱼腥草地上部分的代谢物组成及其抗氧化能力,阐明其化学成分的动态变化规律,旨在为鱼腥草分茬采收方式的科学评价与合理应用提供理论依据和数据支撑。
-
供试样品于2022年2月栽培于中国广西省桂林区灵川县灵田镇种植场(25°23′51.1″N, 110°18′58.2″E)。该种植场属于亚热带季风气候,夏季高温多雨,冬季温和湿润,平均气温19℃,年降雨量1 166.6 mm。在同一栽培地内,根据生长季内不同时段及分茬采收方式收集鱼腥草地上部分。具体方案如下:7月第1批,7月12日(果期)采收鱼腥草地上部分;10月第1批,10月采收鱼腥草地上部分;7月第2批,将7月份采收后重新长出的第2批鱼腥草地上部分于10月采收。上述样品均经中山市中智药业集团有限公司贾世清中药师鉴定为三白草科蕺菜属植物鱼腥草(Houttuynia cordata)的干燥地上部分。样品的采集信息详见表1。
样品名称
Sample分组
Group生长模式
Growth pattern收集时间
Collection TimeYA1 采收方法1: 7月第1批 土培 2022−07−12 YA2 采收方法1: 7月第1批 土培 2022−07−12 YA3 采收方法1: 7月第1批 土培 2022−07−12 YA4 采收方法1: 7月第1批 土培 2022−07−12 YB1 采收方法2:10月第1批 土培 2022−10−20 YB2 采收方法2:10月第1批 土培 2022−10−20 YB3 采收方法2:10月第1批 土培 2022−10−20 YB4 采收方法2:10月第1批 土培 2022−10−20 YC1 采收方法3:7月继10月第2批 土培 2022−10−20 YC2 采收方法3:7月继10月第2批 土培 2022−10−20 YC3 采收方法3:7月继10月第2批 土培 2022−10−20 YC4 采收方法3:7月继10月第2批 土培 2022−10−20 Table 1. Collection information of 12 batches of Houttuynia cordata harvested by different methods
-
G2-XS Q-TOF型液质联用仪(美国沃特世公司);甲醇、乙腈、甲酸,均为质谱级,购自德国默克公司;超纯水(明澈D24UV型超纯水机制备);无水乙醇(广东广试试剂技术有限公司,批号:2022100218,纯度≥ 99.7 %);2,2−联氮−双(3−乙基苯并噻唑啉−6−磺酸)试剂(纯度≥ 98 %)和0.1 mol·L−1 PBS 缓冲液(泉州市益达科技有限公司,批号:20220831A,pH7.4);亚硝酸钠(广东光华化学厂有限公司,批号:XK13-201-00020);硝酸铝(天津科密欧化学试剂有限公司,批号:20150202,纯度: ≥ 99.0%);1 mol·L−1 氢氧化钠溶液(上海麦克林生化科技有限公司,纯度:95%);过硫酸钾(天津大茂化学试剂厂有限公司,纯度:99.5%);槲皮素(中国食品药品检定研究院,批号:100081-201610,纯度:99.8%)。
-
样品经阴干处理后进行粉碎过筛。准确称取0.2 g粉末,加入25 mL φ=80%甲醇溶液,超声提取30 min。补重后取上清液经0.22 μm滤膜过滤即得样品溶液,质量控制(QC)样由所有样品液各取70 μL等体积混合。
采用ABTS自由基清除法测定抗氧化活性。准确称取0.3 g粉末,加入20 mL 无水乙醇,超声提取30 min后离心(10 000 r·min−1,5 min),收集上清液作为提取液。
-
采用ACQUITY UPLC HSS T3色谱柱(2.1 mm × 150 mm,1.8 μ)。流动相为0.1 %甲酸水溶液(A)和(1︰1)乙腈-甲醇(B);流速为0.2 mL·min−1;进样体积2 μL;柱温35℃。梯度洗脱程序如下:0~5 min(0%~12% B);5~13 min(12%~19% B);13~15 min(19%~24% B);15~27 min(24%~38% B);27~36 min(38%~52% B);36~38 min(52%~0% B);38~40 min(0% B)。
电喷雾离子源(ESI),MSE、负离子检测模式、毛细管电压2.0 kv(ESI-)、离子源温度100℃、锥孔气流速50 L·h−1、锥孔电压40 V、脱溶剂气温度250℃、脱溶剂气流速600 L·h−1、低能量通道碰撞电压6 eV、高能量通道碰撞电压40~50 eV、质量扫描范围100~
1200 ,亮氨酸—脑啡肽进行精确质量校正([M-H]-:554.2620, [M+H]+: 556.2766)。 -
不同采收方法下鱼腥草的总黄酮含量采用紫外分光光度法测定,以槲皮素为标准品,将1 mL醇提物和0.3 mLw= 1%亚硝酸钠溶液加入到10 mL EP管中静置6 min,加入0.3 mL w=10 %硝酸铝溶液,再静置6 min后加入4 mL 1 mol·L−1氢氧化钠溶液。溶液用无水乙醇稀释至10 mL,在510 nm处测定吸光度。样品的总黄酮含量使用标准曲线方程计算。
将7 mmol·L−1ABTS溶液和4.9 mmol·L−1过硫酸钾溶液混合,避光条件下储存18 h后制得ABTS·+母液,将母液在734 nm下调整至0.7吸光度即得ABTS·+反应液。取不同采收方法的鱼腥草醇提物1 mL加入5 mL ABTS·+反应液混匀反应10 min,在734 nm下测定吸光值,每组重复测定3次。ABTS自由基清除率(SC)按以下公式计算:
式中,SC为ABTS自由基清除率(%),A测定为样品溶液与ABTS反应液测得的吸光值;A对照为样品溶液与无水乙醇测得的吸光值;A空白为无水乙醇与ABTS反应液测得的吸光值。
-
MS数据采用MassLynx 4.2和UNIFI进行预处理。主成分分析(PCA)与正交偏最小二乘判别分析(OPLS-DA)在SIMCA 14.1软件中完成,相关性分析通过迈维代谢平台进行。热图由TB-tools绘制,统计检验在SPSS 26.0软件中完成。
-
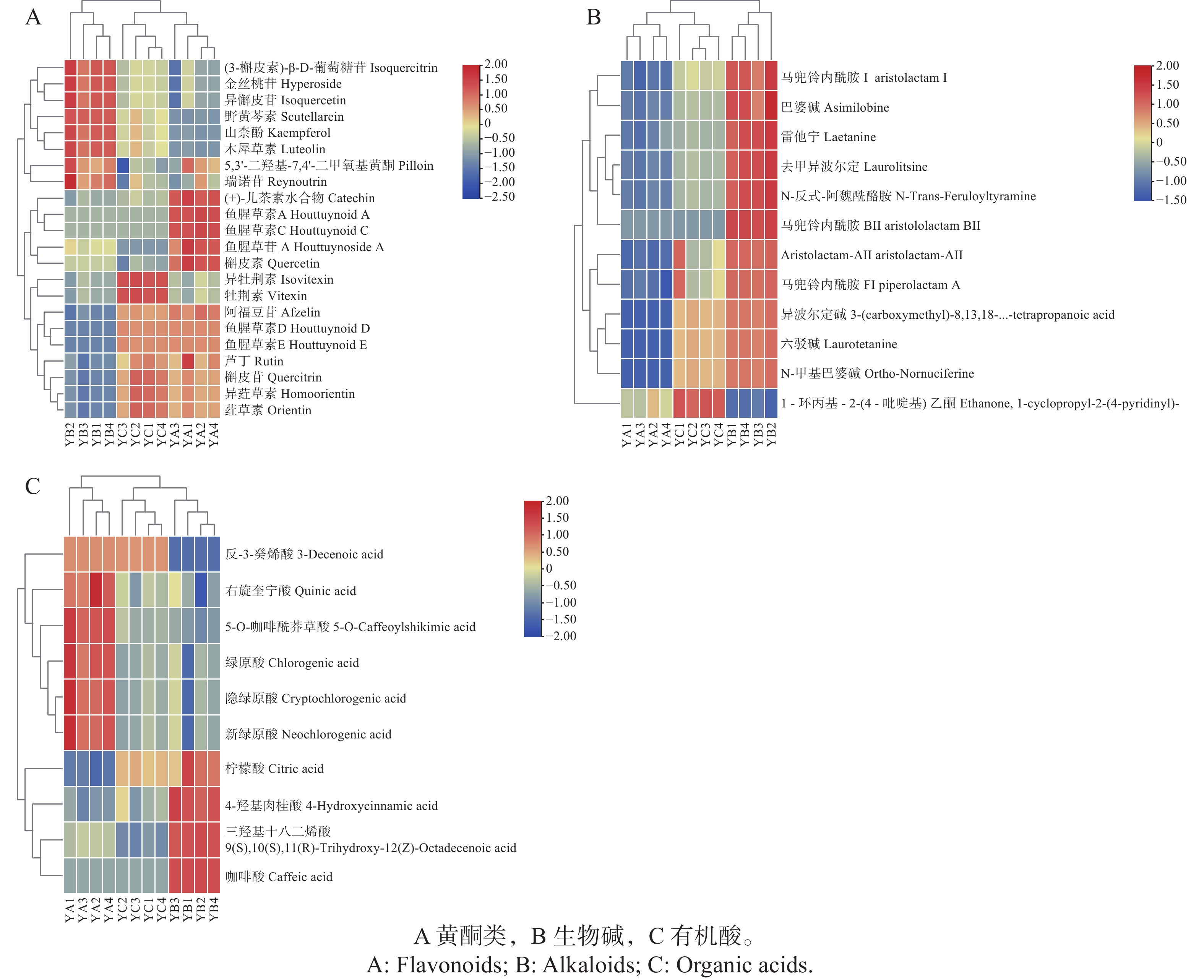
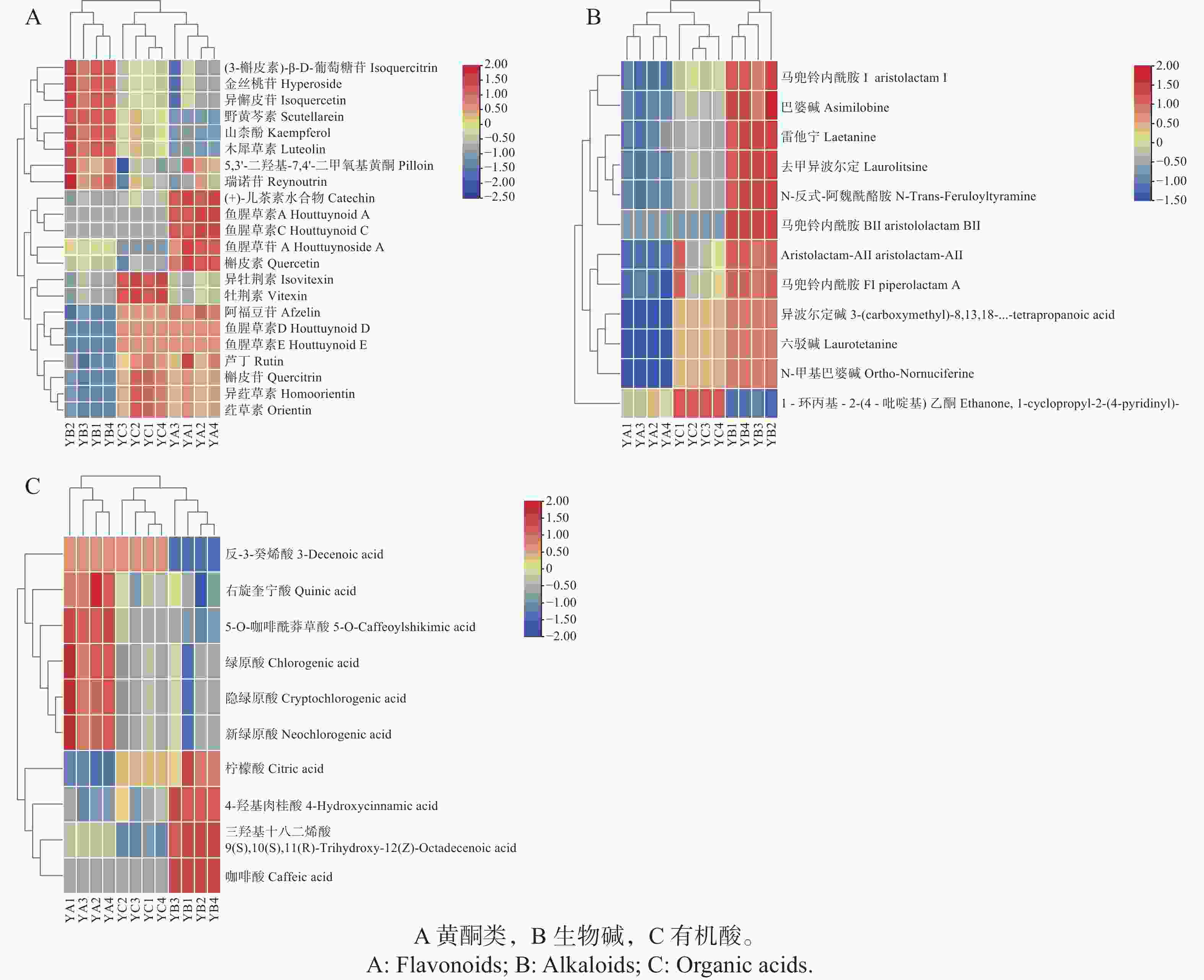
在12批鱼腥草样品中共鉴定出60种代谢物(表2)。在已鉴定的成分中,黄酮类占比最高,为36.67%,其次是生物碱(20.00%)和有机酸(16.67%)。进一步分析表明,不同采收方法下代谢物类别的相对组成存在差异,采收方法1中黄酮类和有机酸代谢物所占比例较高,而采收方法2中生物碱类代谢物比例相对较高(图1-A—C)。
编号Code 分子式Molecular formula 观测值/(m/z)
Observed value /(m/z)质谱碎片离子
Fragment ions物质
Compound类别
Classification1 C4H7NO4 132.029 7 114.019 0 L-天门冬氨酸 L-aspartic acid 氨机酸类 2 C6H10O4 191.055 4 129.018 6 丁二酸二甲酯 Butanedioic acid dimethyl eater 酯类 3 C7H12O6 191.055 2 173.044 3 右旋奎宁酸 Quinic acid 有机酸类 4 C6H8O7 191.018 8 111.007 8, 129.017 6, 173.007 7 柠檬酸 Citric acid 1 有机酸类 5 C9H12N2O6 243.061 3 175.024 6 阿糖尿苷/尿苷 Uridine 核苷类 6 C10H13N5O4 312.093 7 134.038 3 腺苷 Adenosine 核苷类 7 C10H13N5O5 282.083 3 108.020 0, 133.015 0, 150.041 6 鸟苷 Guanosine 核苷类 8 C16H18O9 353.087 3 111.044 2, 135.044 0, 161.023 1 绿原酸 Chlorogenic acid 有机酸类 9 C16H18O9 353.087 3 134.036 2, 135.044 0, 179.033 8 隐绿原酸Cryptochlorogenic acid 1 有机酸类 10 C16H18O9 353.087 3 173.044 4, 191.054 9 新绿原酸 Neochlorogenic acid 1 有机酸类 11 C11H12N2O2 203.081 6 116.049 7 L-色氨酸 L(-)-tryptophan 氨基酸类 12 C17H14O6 359.076 1 109.029 0, 125.023 4, 175.038 1 5,3'-二羟基-7,4'-二甲氧基黄酮 Pilloin 1 黄酮类 13 C17H20O9 367.104 0 127.049 8, 145.060 5, 277.026 5 绿原酸甲酯 Chlorogenic acid methyl ester 1 酯类 14 C17H20O9 367.104 0 250.091 7, 245.041 8 3-咖啡酰奎尼酸甲酯
3-O-Caffeoylquinic acid methyl ester1酯类 15 C17H20O9 367.104 0 127.049 9, 145.060 5, 326.104 6 新绿原酸甲酯 Neochlorogenic acid methyl ester 1 酯类 16 C17H17NO2 312.123 4 152.071 0, 197.058 8 巴婆碱 Asimilobine 1 生物碱类 17 C18H19NO4 312.123 4 297.099 4 雷他宁 Laetanine1 生物碱类 18 C18H19NO4 312.123 5 227.033 9, 239.033 8, 279.071 0 去甲异波尔定 Laurolitsine 1 生物碱类 19 C18H19NO4 312.123 2 297.098 6 N-反式-阿魏酰酪胺 N-trans-Feruloyltyramine 1 生物碱类 20 C9H8O4 179.034 3 134.036 4, 135.044 1 咖啡酸 Caffeic acid 1 有机酸类 21 C19H21NO4 326.139 0 − 异波尔定碱 3-(carboxymethyl)-8,13,18-
trimethyl-21H,23H-Porphine-2,7,12,
17-tetrapropanoic acid 1生物碱类 22 C19H21NO4 326.138 6 152.070 5 六驳碱 Laurotetanine 1 生物碱类 23 C18H19NO2 326.138 6 197.056 3 N-甲基巴婆碱 Ortho-nornuciferine 1 生物碱类 24 C19H30O8 431.192 3 135.044 2, 245.081 5 长寿花糖甙 Roseoside 其他类 25 C21H22O11 215.128 4 − 鱼腥草苷 A Houttuynoside A 1 黄酮类 26 C16H16O8 335.076 6 134.036 0, 135.043 9, 289.070 2 5-O-咖啡酰莽草酸 5-O-Caffeoylshikimic acid 有机酸类 27 C15H14O6 289.071 0 125.023 5 (+)-儿茶素水合物 Catechin 黄酮类 28 C10H11NO 206.081 3 − 1 - 环丙基 - 2-(4 - 吡啶基)乙酮
Ethanone, 1-cyclopropyl-2-(4-pyridinyl)-生物碱类 29 C9H8O3 209.044 8 117.034 0 4-羟基肉桂酸 4-Hydroxycinnamic acid 有机酸类 30 C13H20O3 269.141 2 121.028 3, 133.028 4 吐叶醇 Vomifoliol 1 醇类 31 C27H30O16 609.146 8 299.019 2, 462.079 9 芦丁 Rutin 黄酮类 32 C21H20O12 463.088 6 151.002 9, 300.027 4 金丝桃苷 Hyperosine 黄酮类 33 C21H20O12 463.088 6 108.020 6, 151.002 8, 243.029 1 异懈皮苷 Isoquercetin 黄酮类 34 C21H20O12 463.088 6 243.029 1, 300.027 4, 323.016 7 (3-槲皮素)-β-D-葡萄糖苷 Isoquercitrin 黄酮类 35 C20H18O11 433.077 2 271.023 7, 300.026 3 瑞诺苷 Reynoutrin 黄酮类 36 C21H20O11 447.092 8 151.002 5, 178.997 4, 271.023 8 异荭草素 Homoorientin 黄酮类 37 C21H20O11 447.092 8 283.023 5, 315.050 8, 323.015 6 荭草素 Orientin 黄酮类 38 C21H20O11 447.092 8 151.002 5, 300.026 6 槲皮苷 Quercitrin 黄酮类 39 C16H11NO3 264.065 5 249.042 1 马兜铃内酰胺 AII Aristolactam AII 生物碱类 40 C16H11NO3 264.065 3 231.029 0, 248.034 5 马兜铃内酰胺 FI PiperolactamA 生物碱类 41 C21H20O10 477.103 6 271.023 8, 341.066 7 阿福豆苷Afzelin 1 黄酮类 42 C21H20O10 431.097 9 283.060 2, 339.050 3 异牡荆素 Isovitexin 黄酮类 43 C21H20O10 431.097 9 161.023 4, 281.046 2, 311.055 2 牡荆素 Vitexin 1 黄酮类 44 C15H10O7 301.034 6 163.038 6 槲皮素 Quercetin 1 黄酮类 45 C9H16O2 201.112 9 − 丙位壬内酯 酯类 46 C15H10O6 285.040 1 133.028 3 山柰酚 Kaempferol1 黄酮类 47 C15H10O6 285.040 1 132.021 2, 133.028 3, 134.035 0 木犀草素 Luteolin 1 黄酮类 48 C15H10O6 285.040 1 145.028 6 野黄芩素 Scutellarein 黄酮类 49 C10H12O 193.086 1 − 2,4,5-三甲基苯甲醛 2,4,5-Trimethylbenzaldehyde 1 醛类 50 C10H12O 201.112 3 − 2,4,6-三甲基苯甲醛 Mesitaldehyde 1 醛类 51 C17H11NO4 292.060 6 249.042 1, 277.036 8 马兜铃内酰胺 I Aristolactam I 生物碱类 52 C17H11NO4 292.068 8 249.042 1, 277.037 1 马兜铃内酰胺 BII Aristololactam BII 生物碱类 53 C33H38O13 641.224 4 − 鱼腥草素A Houttuynoid A1 黄酮类 54 C33H38O13 641.224 4 − 鱼腥草素C Houttuynoid C1 黄酮类 55 C32H40O13 631.240 3 − 鱼腥草素D Houttuynoid D 黄酮类 56 C32H40O13 631.240 3 − 鱼腥草素E Houttuynoid E 黄酮类 57 C10H18O2 215.128 2 125.096 6 反-3-癸烯酸 3-Decenoic acid 有机酸类 58 C18H34O5 329.231 8 211.132 8 三羟基十八二烯酸 9(S),10(S),11(R)-Trihydroxy-12(Z)-octadecenoic acid 有机酸类 59 C11H20O2 229.143 4 165.127 9 桃醛 2(3H)-Furanone, 5-heptyldihydro- 醛类 60 C9H8O2 193.050 0 − 二氢香豆素 Dihydrocoumarin 苯丙素类 注: 1代表23个差异代谢物 ,“−”代表未检出 Note: 1 represents 23 differential metabolites; “−” stands for not detected. Table 2. Component identification of Houttuynia cordata Thunb harvested by different methods
-
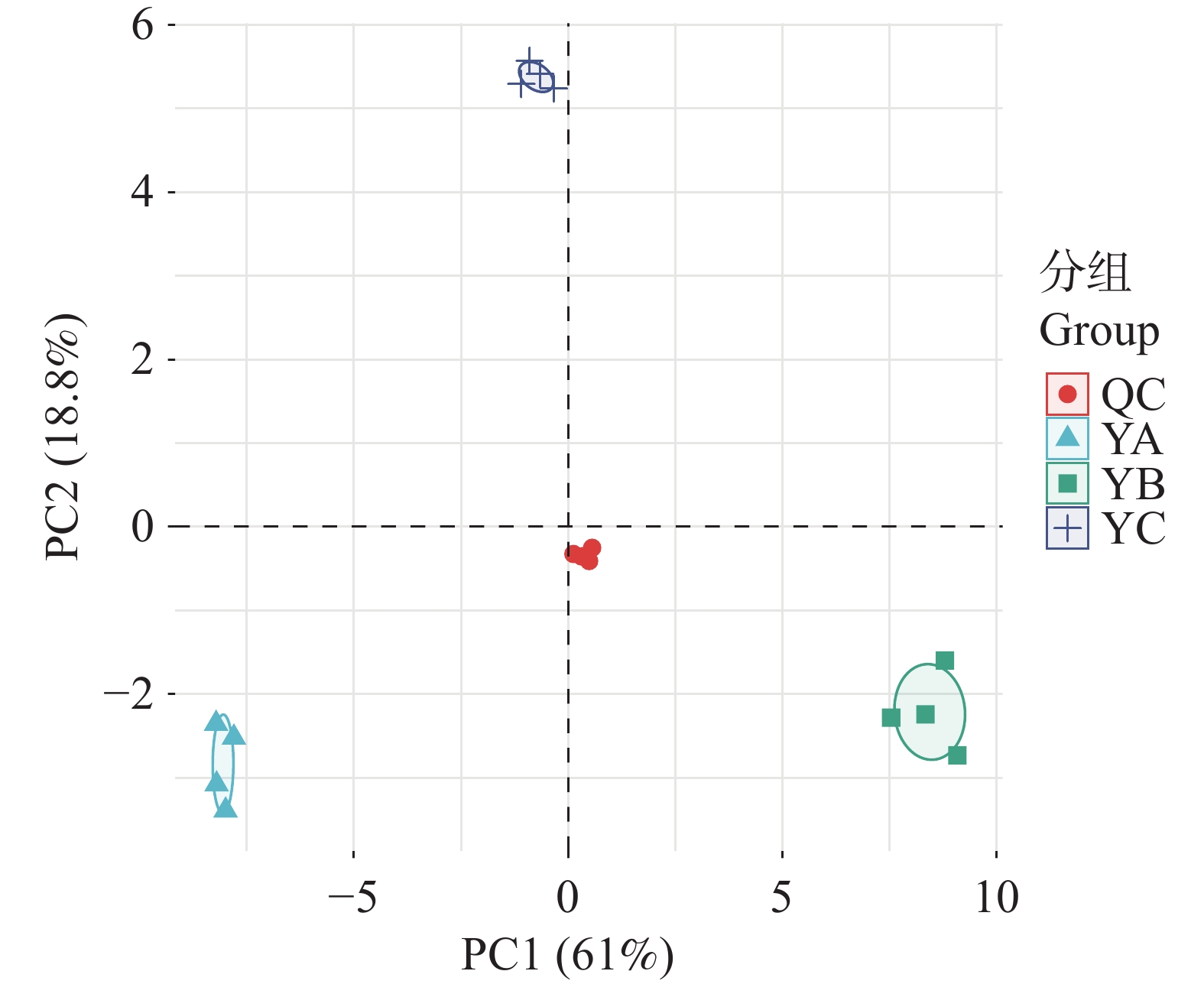
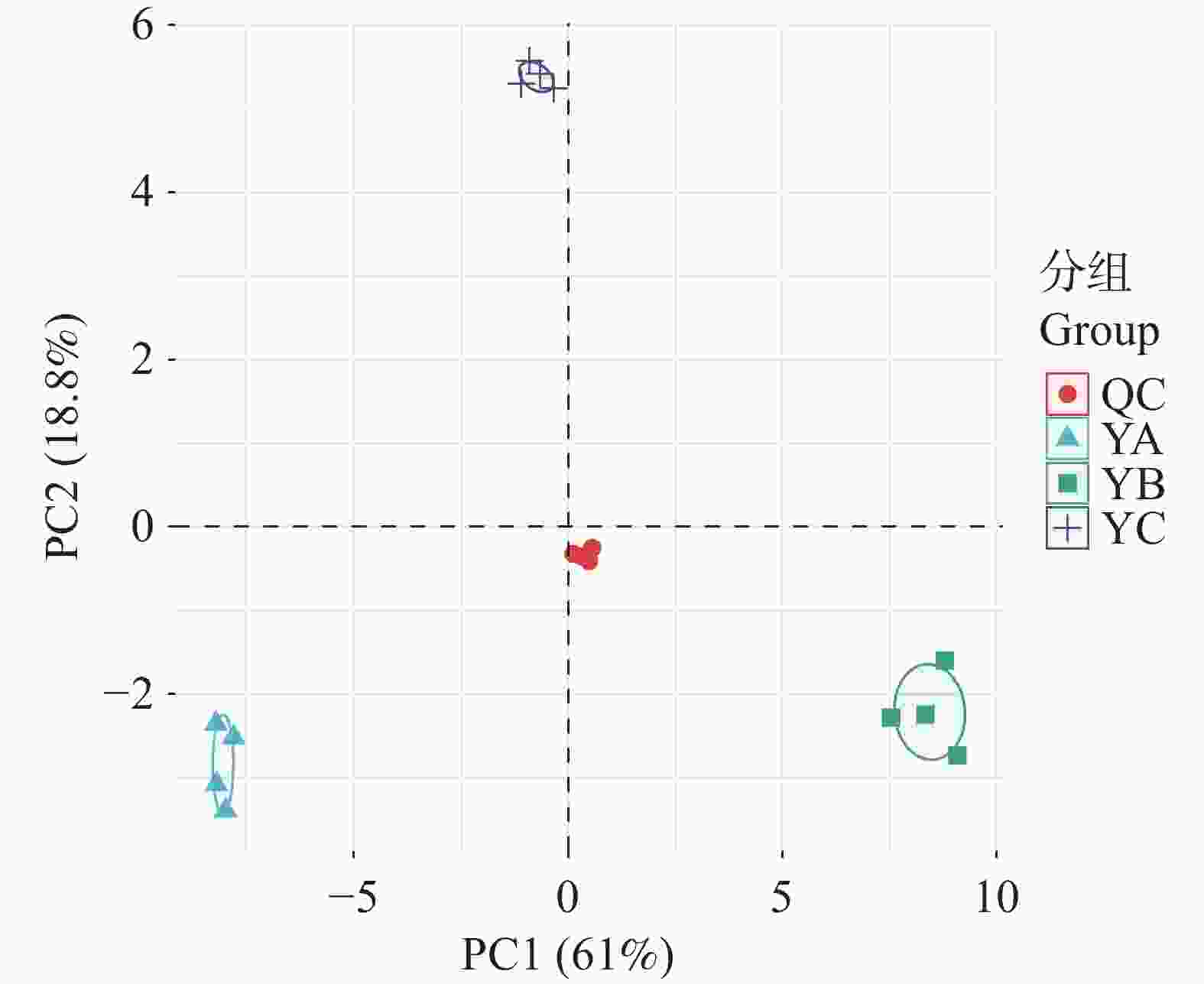
采用主成分分析(PCA)对所有鉴定代谢物进行解析,如图2所示,质量控制(QC)样本紧密聚集,证明了数据的均一性与可靠性。各组试验样本在PCA得分图上呈现明显分离,表明采收方法是导致鱼腥草代谢物差异的主要因素。通过满足VIP>1和P<0.01的条件,共筛选出23种差异代谢物(表2),包括3种酯类(13.04%)、4种有机酸(17.39%)、6种生物碱(26.09%)和10种黄酮类(43.48%)代谢物。
-
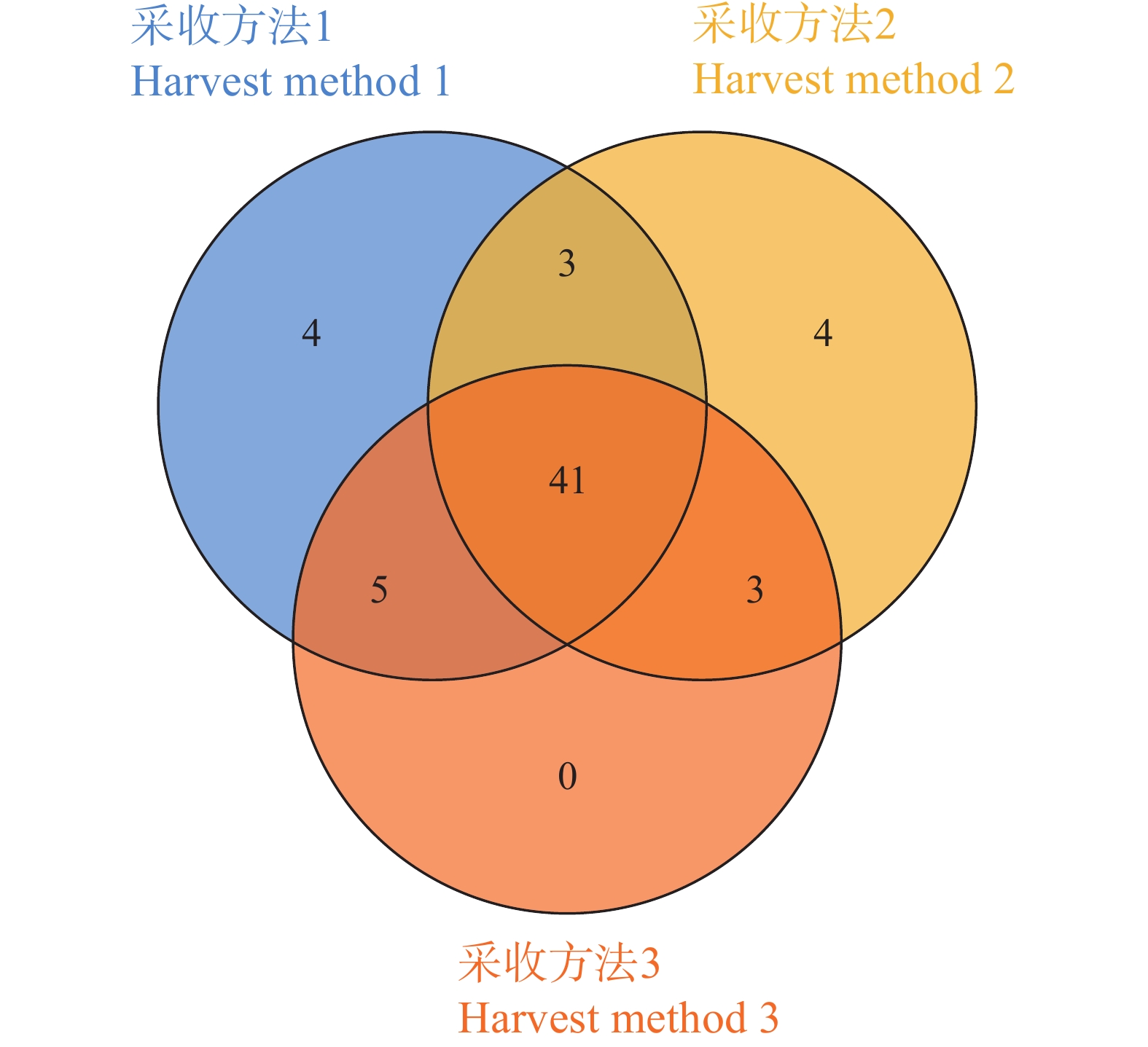
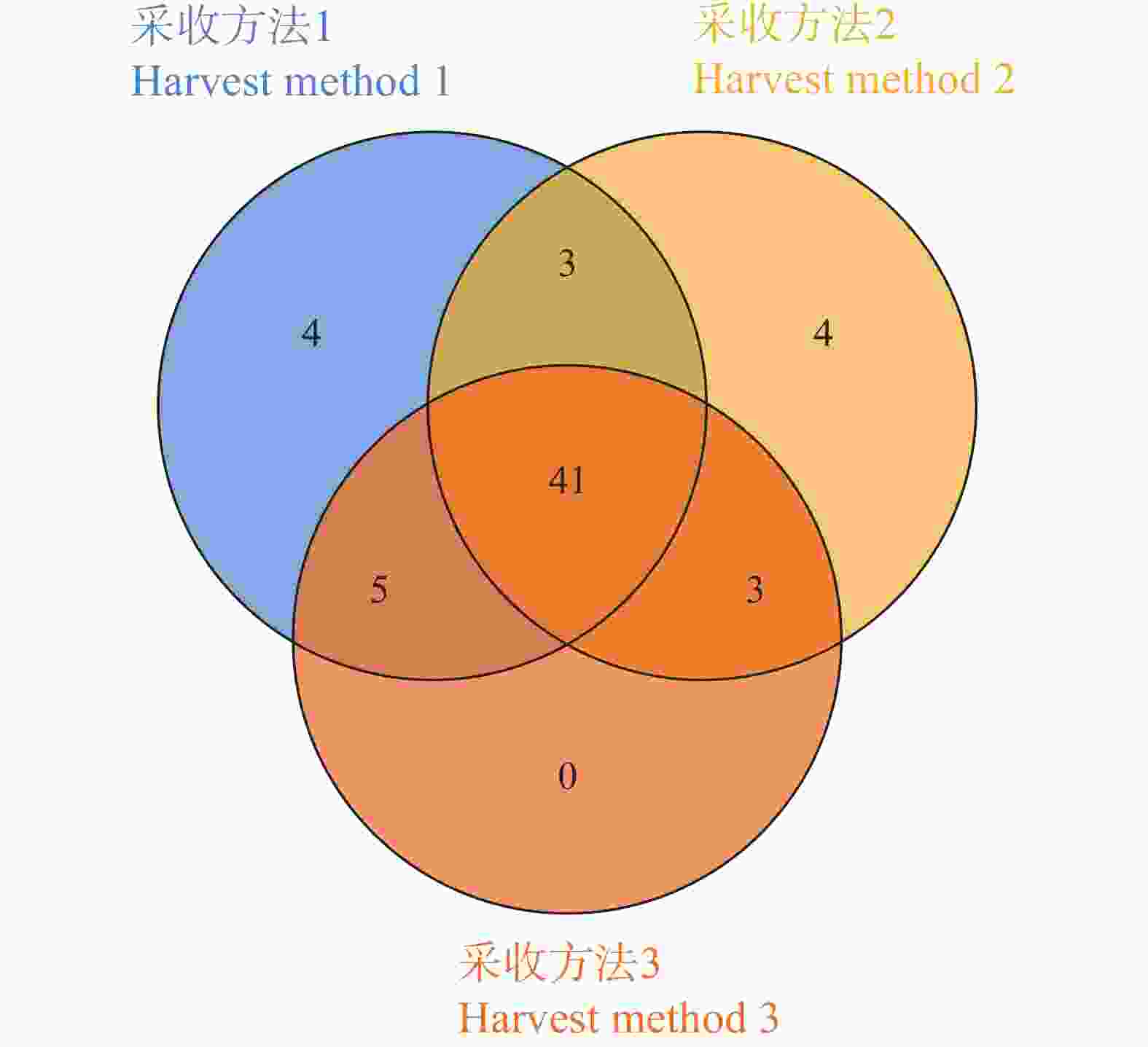
为确定不同采收方法下鱼腥草的关键差异代谢物,对三种采收方法进行维恩图分析,从图3可知,采收方法1的代谢物数量最多,有53种,其中有4种特有代谢物,分别为桃醛、二氢香豆素、鱼腥草素 A、鱼腥草素 C;采收方法2有51种代谢物,其中,4种特有成分分别为2,4,5−三甲基苯甲醛、2,4,6−三甲基苯甲醛、咖啡酸、马兜铃内酰胺BII;采收方法3共鉴定出49种成分,其中大多数与采收方法1重合,其余与采收方法2重合,未检测到其特有代谢物。
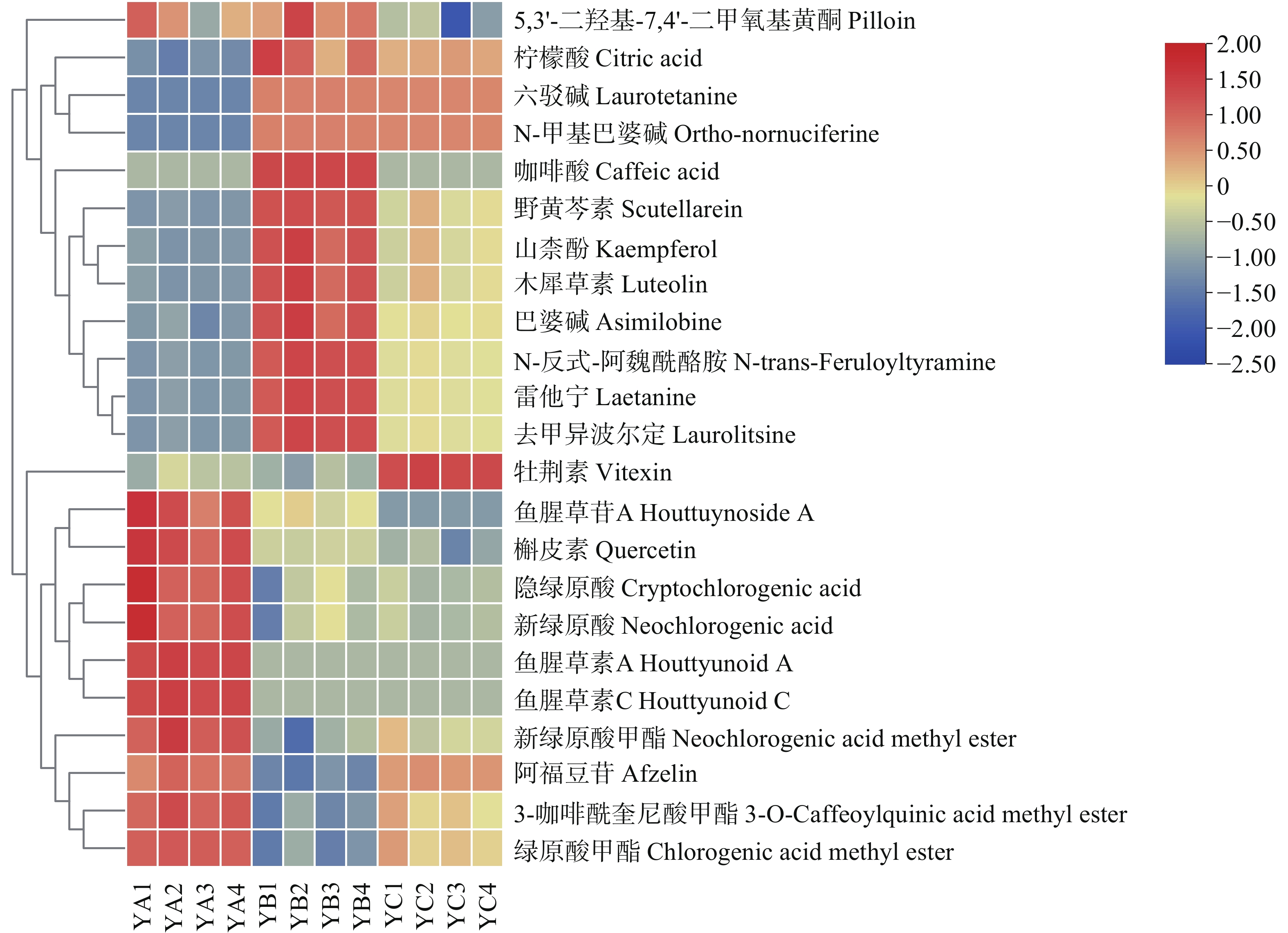
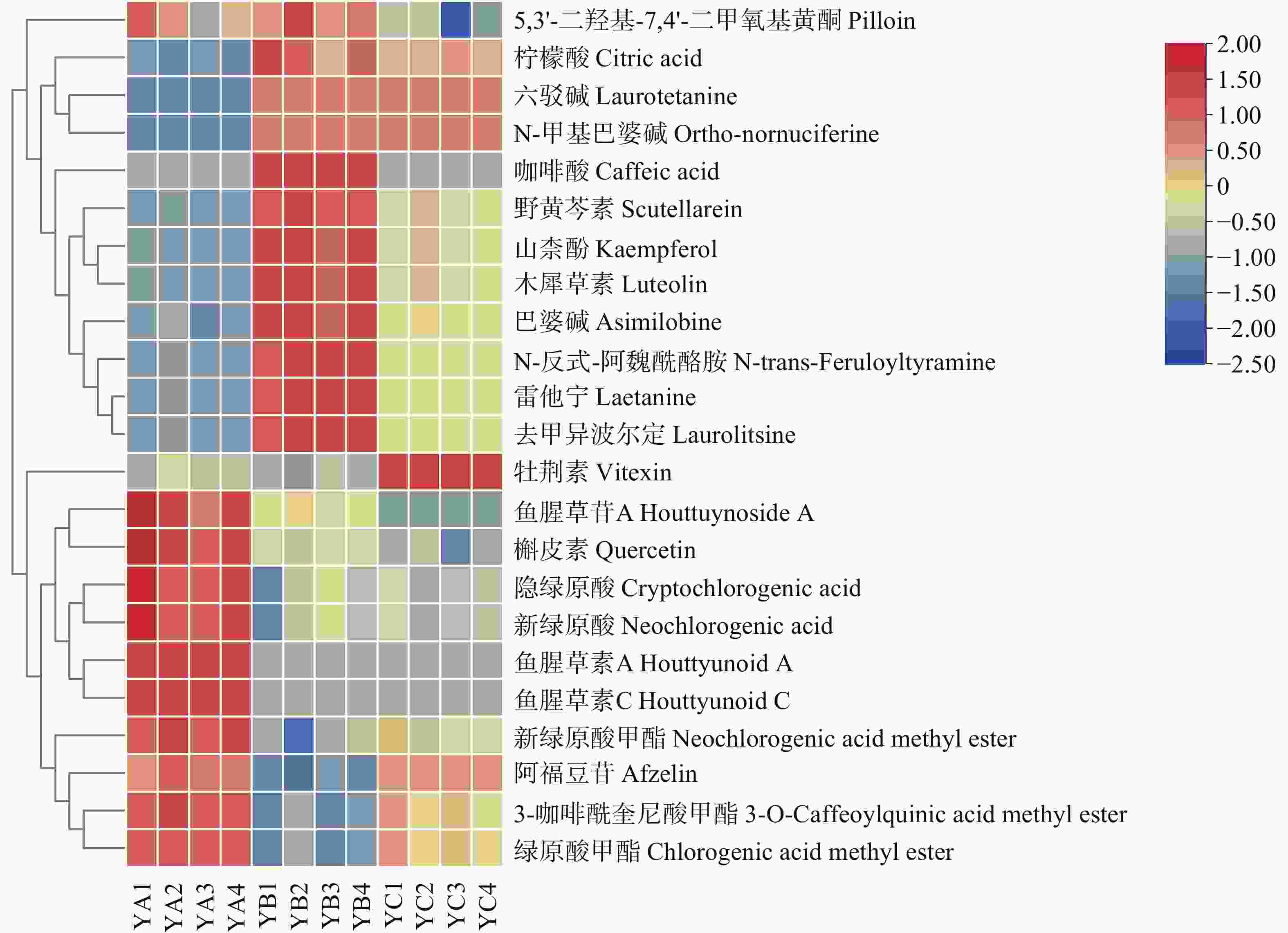
为进一步揭示不同采收方法下鱼腥草代谢物的差异特征, 对23种差异代谢物进行热图分析。从图4可知,3种采收方法的样本分布于不同簇中,表明采收方法对鱼腥草代谢物具有影响。具体而言,在采收方法1和采收方法2中各有12种成分相对富集;而采收方法3中有8种成分相对富集。说明不同的采收方法会影响特定代谢物的相对分布水平。
-
从表3可知,3种采收方法所得的鱼腥草均表现出较强的ABTS自由基清除能力,其中采收方法1的清除率最高(99.22%±0.30%),采收方法3次之(98.43%±0.20%)。多重比较结果显示,采收方法1与采收方法2、采收方法2与采收方法3之间均存在显著差异(P< 0.05),而方法1与方法3之间无统计学差异。方法1所采收的鱼腥草具有最强的体外抗氧化能力,且其与方法3在抗氧化活性上效果等同。
组别
Group总黄酮含量/%
Flavonoid content/%ABTS自由基清除率/%
ABTS free radical
scavenging rate/%采收方法 1 25.79±0.59a 99.22±0.30a 采收方法 2 17.66±2.33b 97.24±0.06b 采收方法 3 22.82±1.56c 98.43±0.20a 注:数据以平均值±标准差(SD)表示。 同列中不同字母的样本在 P<0.05 的水平上有显著差异。 Note: The data was shown by the mean ± standard deviation(SD). Samples in the same column with different letters are significantly different at the P<0.05 level. Table 3. Results of total flavonoid content and ABTS free radical scavenging rate of Houttuynia cordata Thunb
通过标准曲线(y = 1.102 6x + 0.052 9, r = 0.999 5)对鱼腥草总黄酮含量(TFC)进行定量分析,测得所有样品的TFC范围为17.66%~25.79%。其中,采收方法1的TFC最高,达25.79%±0.59%,其次为方法3(22.82%±1.56%)与方法2(17.66%±2.33%)。Tukey检验表明,不同采收方法间的TFC差异均达到统计学显著水平(P< 0.05)。
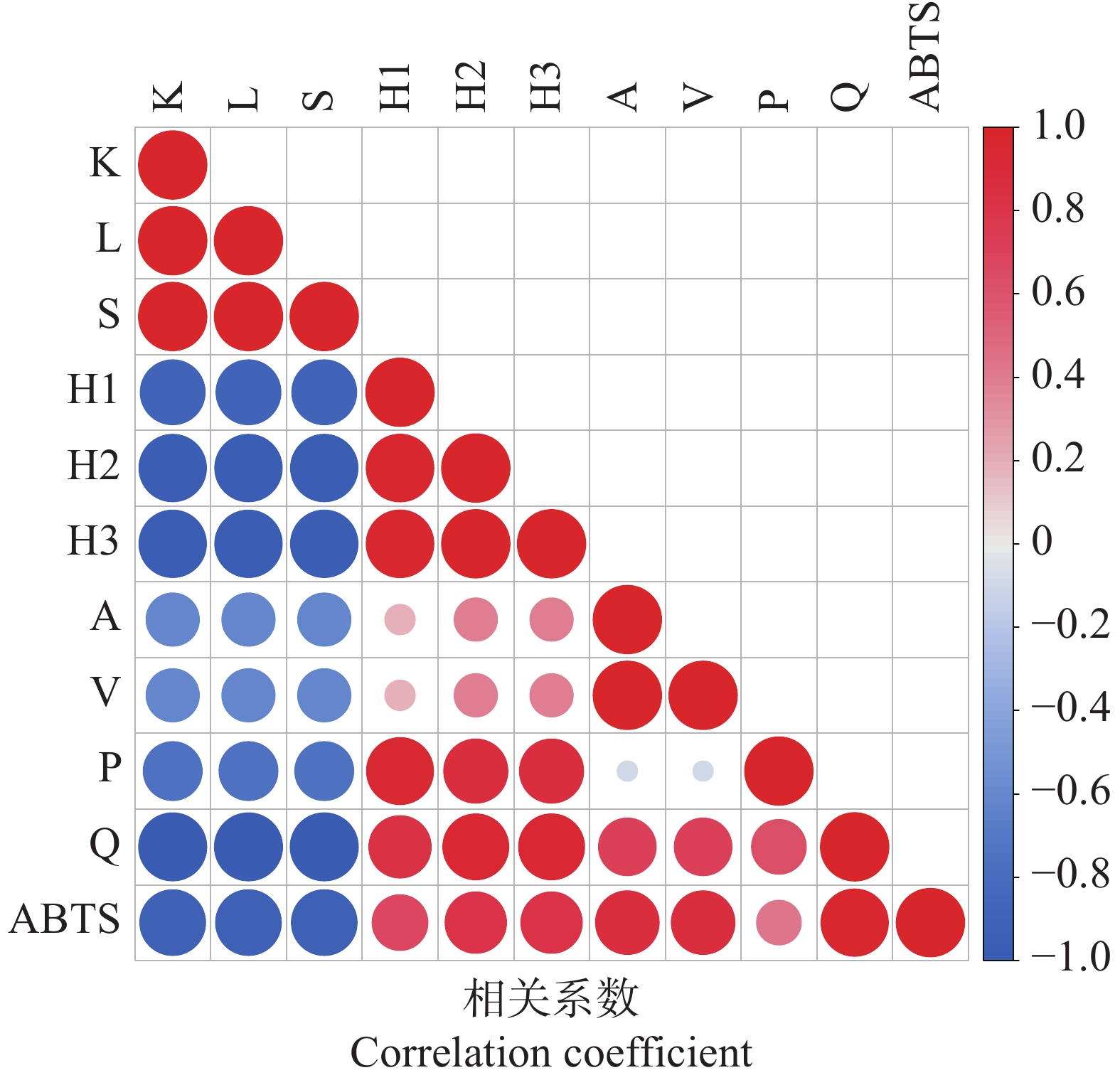
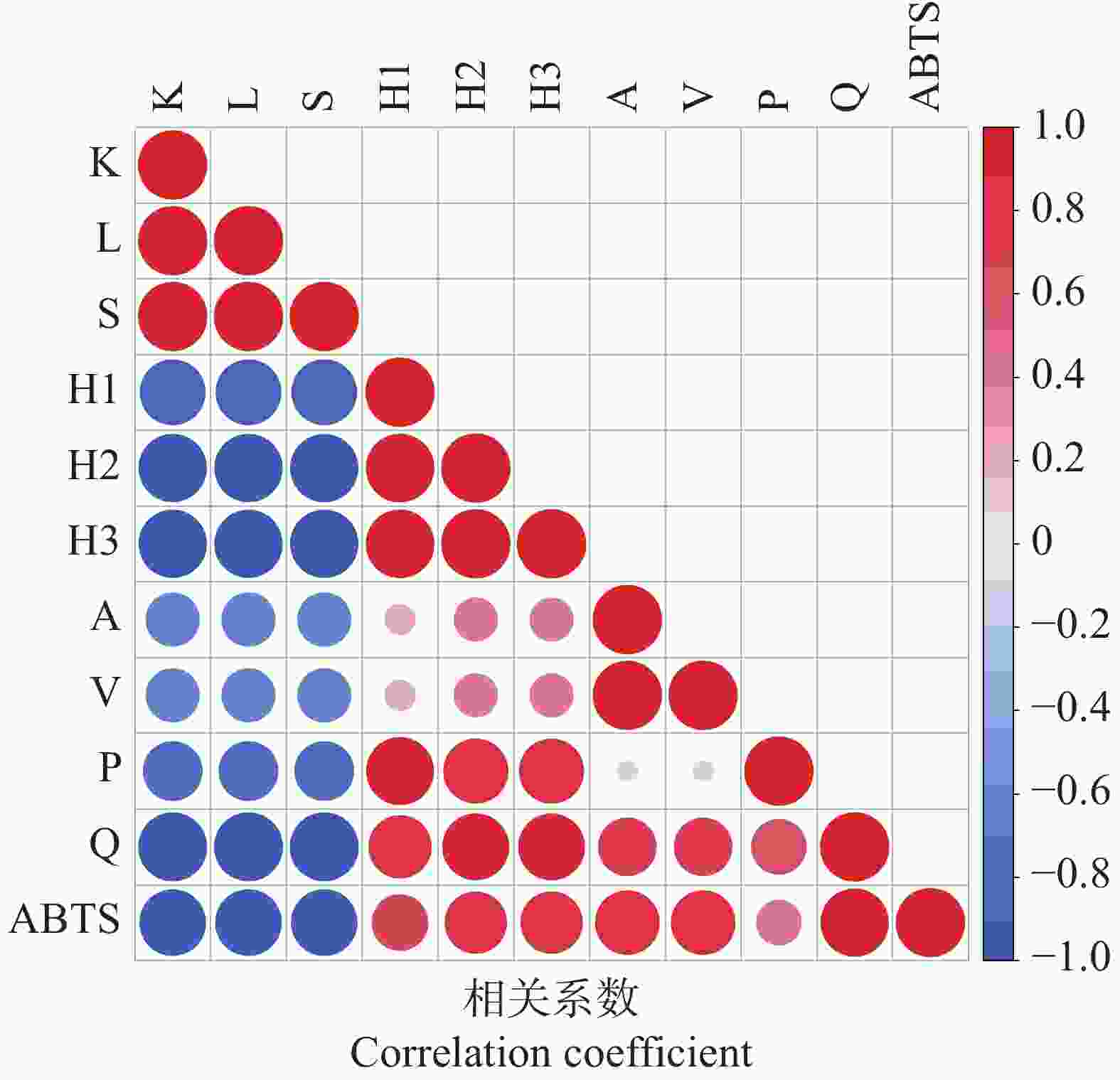
将筛选的10种黄酮类成分进行ABTS自由基清除能力相关性分析,结果表明(图5),其抗氧化能力存在显著差异。其中,山奈酚、木犀草素和黄芩素与抗氧化活性呈显著负相关(r = −0.923),说明并非所有黄酮类代谢物均具有抗氧化作用。相比之下,5,3'−二羟基−7,4'−二甲氧基黄酮(r=0.425)、鱼腥草素 A(r=0.663)、鱼腥草苷A(r=0.806)、鱼腥草素 C(r=0.806)、阿福豆苷(r=0.865)、牡荆素(r=0.865)和槲皮素(r=0.968)与抗氧化活性呈正相关。其中,鱼腥草苷A、Houttuynoid C、阿福豆苷、牡荆素和槲皮素因其相关系数大于0.800,被筛选为抗氧化标志物。
-
药用植物的产量与品质在很大程度上受采收方式与时间的影响,因其生长过程具有明显的季节性变化[11]。陈胜璜等[12]的研究表明,鱼腥草挥发油含量从7—9月逐渐下降,然后在10月逐渐回升。本研究结果进一步证实,不同采收时间会影响鱼腥草地上部分次生代谢物分布差异。7月份采收的样品中,有机酸与黄酮类成分相对富集;10月份采收的样品生物碱类成分的相对富集。 值得注意的是,7月份采收后于10月份采收的第2茬样品呈现出一种独特的高效再生代谢物特征。尽管生长期较短,总黄酮的含量低于7月份采收样品,但整体代谢物组成与7月份样品高度相似,且体外抗氧化活性未表现出显著差异。上述结果表明,再生组织在一定生长周期内可优先保障与抗氧化活性直接相关的关键黄酮成分的合成,从而在总体成分积累降低的情况下,仍能维持较高的抗氧化能力。
黄酮类化合物合成与积累程度主要受到周围环境因子以及自身生长发育的协同调控[13-14]。有研究表明,强光、高温及水分波动等环境胁迫可诱导活性氧产生并激活苯丙烷代谢途径,从而促进黄酮类物质合成[15-18]。7月份广西地区典型的高温、强光及频繁的暴雨天气对鱼腥草构成了一种复合型环境胁迫, 从而促进黄酮类成分的积累。然而10月份的气温趋于温和稳定,为其生长提供了相对稳定的环境条件。在此背景下,鱼腥草的代谢重心由防御响应转向生长发育,优先促进地下茎的生长与养分积累,用于合成防御性次生代谢产物的代谢通量相应降低,从而使黄酮类成分维持在基础水平。
黄酮类化合物的抗氧化活性与其分子结构密切相关,多羟基取代及芳香环共轭体系有助于增强其自由基清除能力[19]。本研究筛选出的5种标志性抗氧化活性成分均为黄酮类化合物。进一步说明该类物质在鱼腥草抗氧化功能形成中具有关键作用。已有研究表明,槲皮素、阿福豆苷和牡荆素具有较强的抗氧化活性[20-23]。而鱼腥草苷A和鱼腥草素C虽相关研究相对有限[24],但结合其结构特征及本研究实验结果推测,其亦可能参与鱼腥草抗氧化功能的形成。因此,这些关键成分含量的变化直接影响鱼腥草的质量和药理功效,可以作为鱼腥草采收方式品质评价的标志性成分。
本研究结果表明,采收方法对鱼腥草地上部分的化学成分组成与抗氧化活性具有显著影响。在7月份采收黄酮类成分积累较高,并且分茬采收可以提高经济效益;在10月份采收生物碱类成分积累较高。这一发现不仅为优化鱼腥草的采收方法提供了科学依据,也为建立其全面的质量评价标准奠定了理论基础。
Effects of harvest methods on the chemical composition and antioxidant properties of Houttuynia cordata Thunb.
DOI: 10.15886/j.cnki.rdswxb.20250207
- Received Date: 2025-12-30
- Rev Recd Date: 2026-02-19
- Available Online: 2026-03-05
-
Key words:
- Houttuynia cordata Thunb. /
- harvest methods /
- metabolomics /
- antioxidant capacity
Abstract: A method based on UPLC-Q-TOF-MS was established for the systematic characterization and comparison of metabolic profiles and in vitro antioxidant activities in the aerial parts of Houttuynia cordata under different harvest methods (first and second crops in July, and first crop in October). Untargeted metabolomics integrated with multivariate statistical analysis was employed to deeply investigate the dynamic regulatory influence of harvesting approaches on the accumulation of secondary metabolites. Moreover, the ABTS radical scavenging assay was applied to validate antioxidant capacity and to explore its correlation with compositional characteristics. The results showed that 23 differential metabolites were identified in the samples collected by different harvest methods. Among all the harvest methods, Method 1 yielded the highest number of identified metabolites (53), followed by Method 2 (51) and Method 3 (49), respectively. More importantly, Houttuynoside A, Houttuynoid C, Afzelin, Vitexin and Quercetin were identified as key biomarkers associated with antioxidant capacity, among which Quercetin had the highest correlation with antioxidant capacity.
| Citation: | Zhang Yue, Chen Shuzhen, Zhao Yu, Yang Zerui, Ma Yonglin, Wang Jiwen, Ma Hongliang. Effects of harvest methods on the chemical composition and antioxidant properties of Houttuynia cordata Thunb.[J]. Journal of Tropical Biology. doi: 10.15886/j.cnki.rdswxb.20250207 |






 DownLoad:
DownLoad: