-
遗传多样性是生物多样性的核心组成部分,不仅反映物种的历史演化过程,也决定了其应对环境变化的能力与适应范围,是维系物种适应能力、生态系统稳定性及恢复潜力的重要基础[1-3]。随着全球气候变暖和人类活动加剧,热带森林面临着严重的生态胁迫,特别是热带低地雨林,强烈的人类干扰导致栖息地破碎化和物种数量丧失,使其成为全球生物多样性丧失最严重的生态系统之一[4]。因此,了解热带雨林优势树种的遗传多样性水平及其分布,对于制定科学的保护策略和维持生态系统长期功能具有重要意义。
热带森林物种组成复杂,环境异质性、微地形差异及外界干扰共同影响种群内部基因扩散的距离和格局[5-6]。植物的固着生长,种子与花粉扩散能力受限,短距离的基因流加速了近缘个体在空间上聚集分布[7],导致种群内基因型在空间上非随机分布,从而产生小尺度空间遗传结构(fine-scale spatial genetic structure, FSGS)[8]。FSGS的强弱和空间尺度不仅反映种子与花粉的扩散能力,也记录生境异质性和局地更新过程对种群遗传格局的综合影响[9-11],因此,将FSGS与环境因子(海拔梯度等)结合分析,有助于深入理解热带雨林优势树种的空间遗传动态及维持机制。
龙脑香科(Dipterocarpaceae)是亚洲热带低地雨林的重要建群种,占森林底面积的20%~50%,在冠层种占比超过50%[12]。青梅(Vatica mangachapoi)是海南岛龙脑香科仅有的3个物种之一[13],广泛分布于海南岛中南部山区的低地雨林中,其翅果依赖风力传播[14],理论上具有较长基因流的潜质。目前对青梅的研究主要集中于群落组成[15]、种质资源调查[16]和基因组学等[17-18],而基于分子标记开展的小尺度空间遗传结构特征的研究报道仅局限于单一种群开展[19],缺乏不同种群间的比对,难以揭示环境因子对FSGS的影响机制。
海南热带雨林国家公园霸王岭片区与吊罗山片区具有显著的微地形差异,且风场环境及台风驱动的自然干扰频率不同[20-22],是探讨异质生境对青梅FSGS驱动机制的理想区域。本研究以霸王岭和吊罗山片区的青梅为对象,聚焦海拔梯度与地理隔离双重影响,利用微卫星分子标记(simple sequence repeats, SSR)系统评估其遗传多样性、遗传结构以及小尺度空间遗传格局,旨在揭示异质生境对青梅种群遗传变异的塑造机制,并为这一海南岛热带森林优势树种的保护和管理提供科学依据。主要研究问题包括:
1)海南热带雨林国家公园霸王岭片区和吊罗山片区内青梅的遗传多样性水平如何?
2)海拔梯度与地理隔离是否驱动种群间的遗传结构分化?
3)青梅种群的小尺度空间遗传结构特征如何?不同种群之间FSGS的强度是否存在差异?
通过回答上述问题,弥补海南龙脑香科树种在FSGS影响因素方面的研究空缺,深化对热带雨林植物空间遗传格局的理解,并为热带森林生态系统的保护与基因资源管理提供理论参考。
-
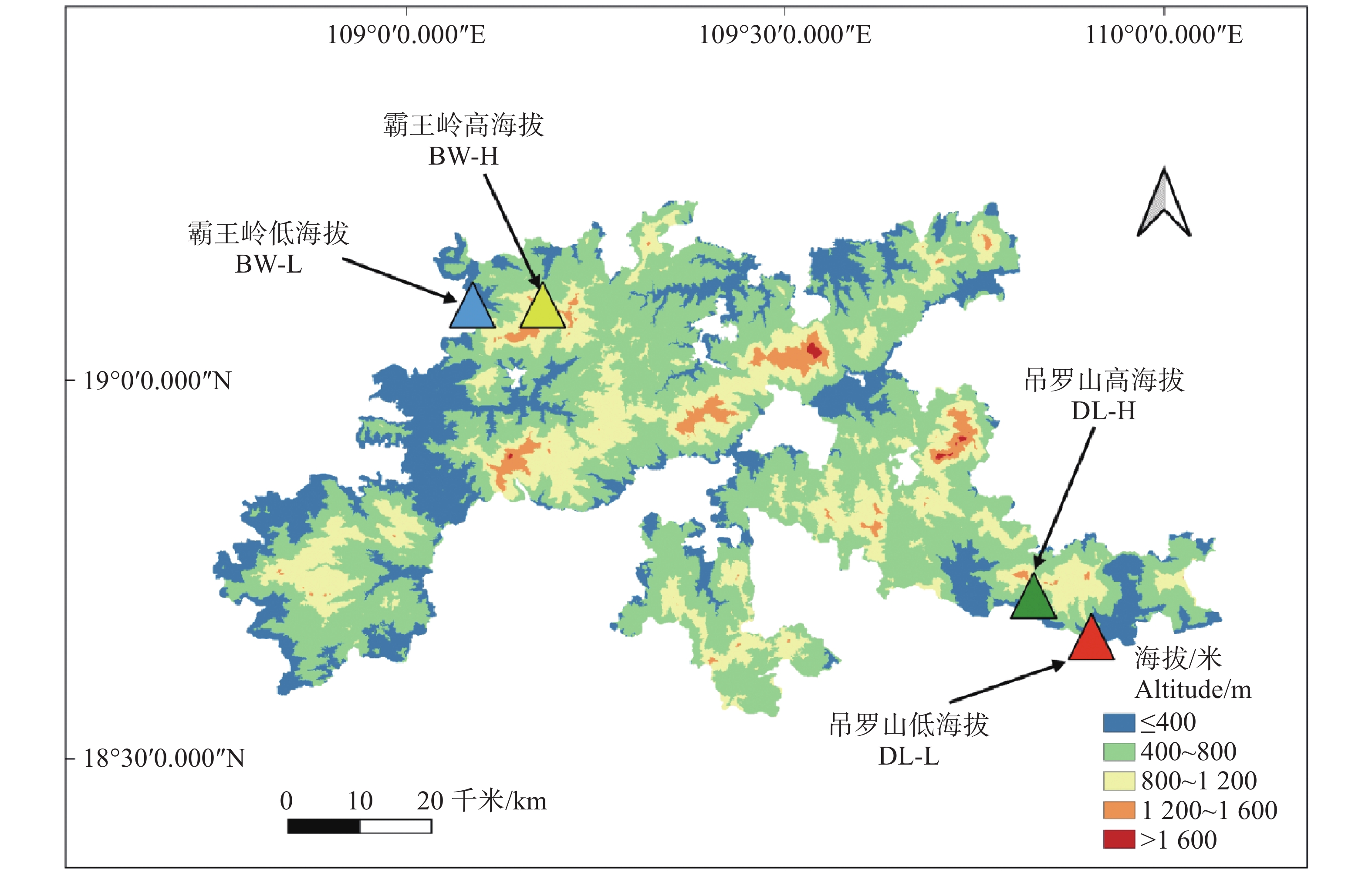
研究区域位于海南热带雨林国家公园霸王岭和吊罗山片区(图1),二者分别位于海南岛西北部与东南部,均具备典型的热带雨林生境和显著的海拔梯度。基于海拔与地形特征,在两个片区内各设置高、低海拔样地各1个:其中高海拔样地为BW-H(霸王岭,海拔589 m)、DL-H(吊罗山,海拔542 m),低海拔样地为BW-L(霸王岭,海拔188 m)、DL-L(吊罗山,海拔163 m)。每个样地按系统抽样法采集胸径(DBH)≥ 5 cm的青梅个体[23],样本量分别为:BW-H 90株,BW-L 100株,DL-H 93株,DL-L 89株,共计372株(表1)。为保证样本空间独立性,个体间距设置为 ≥ 10 m。采集的成熟叶片擦拭干净后放入硅胶中干燥保存[24],同时记录GPS坐标、树高、冠幅及胸径等数据。该采样设计兼顾地形异质性和种群分布特征,有效降低空间自相关性,确保后续遗传多样性及空间遗传结构分析的可靠性。
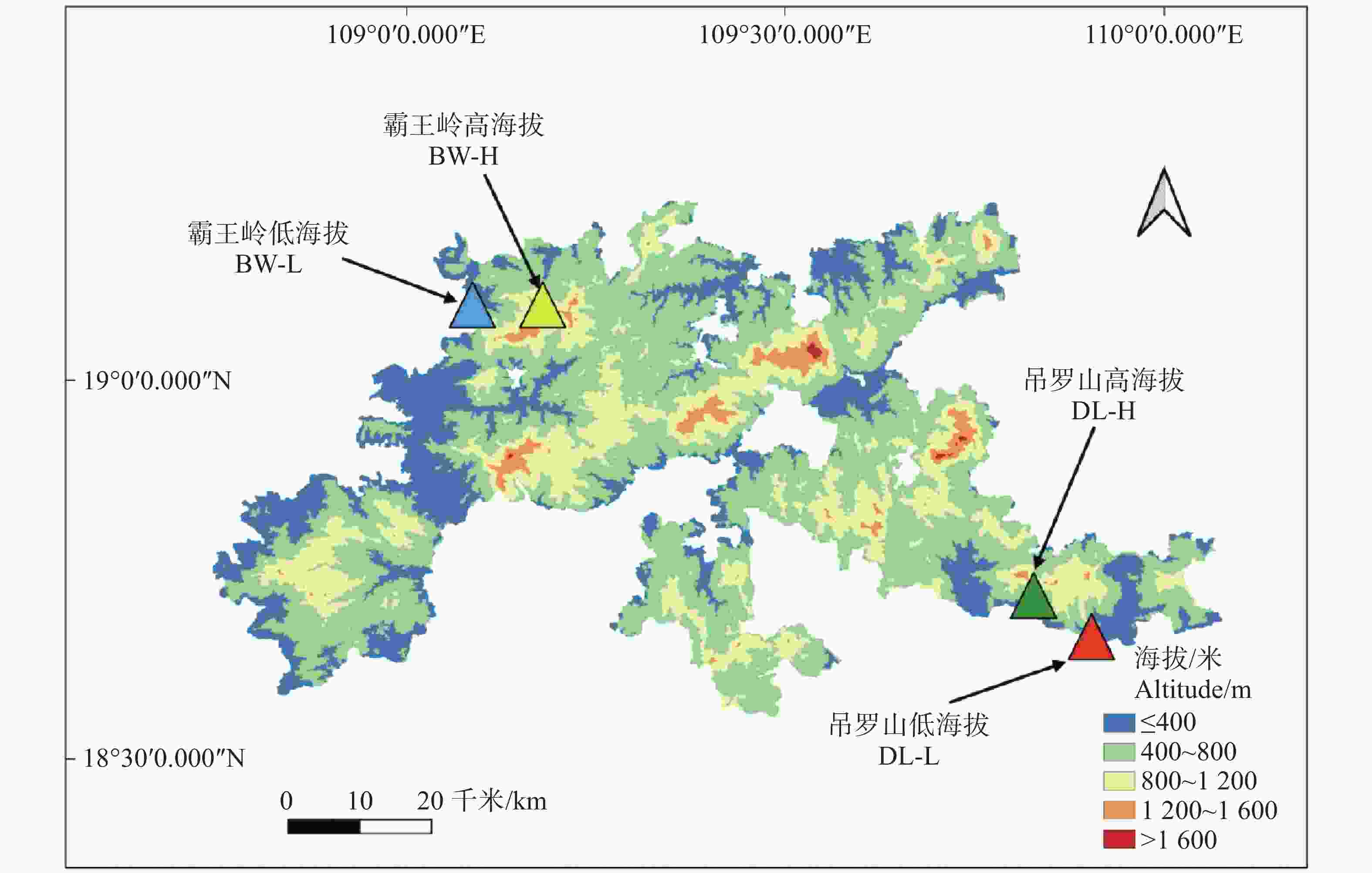
Figure 1. Map of the area under survey and sampling sites at Bawangling and Diaoluoshan regions in Hainan Tropical Rainforest National Park.
种群
Population地点
Location纬度
Latitude经度
Longitude海拔/米
Altitude /m样本量/个体数
Sample size/Number of individualsBW-H 霸王岭片区
斧头岭19°06′46″ 109°11′54″ 589 90 BW-L 霸王岭片区
水电站19°06′33″ 109°06′05″ 188 100 DL-H 吊罗山片区
枫果山18°42′04″ 109°50′11″ 542 93 DL-L 吊罗山片区
南喜沟18°40′04″ 109°54′27″ 163 89 Table 1. Sample information on the Vatica mangachapoi populations.
-
采用改良CTAB法提取叶片基因组DNA [25]。依据青梅已开发的SSR引物[26],经过琼脂糖凝胶电泳检测扩增稳定性、验证多态性,最终筛选出7对扩增稳定、多态性高的引物用于后续实验(表2)。PCR反应体系为10 μL,包含1.0 μL DNA模板(约50 ng)、Taq PCR Master Mix 5 μL、正反向引物各0.5 μL及H2O 3 μL。扩增程序为:95℃预变性5 min,随后35个循环(95℃ 20 s,52~62℃ 15 s,72℃ 30 s),最后72℃延伸7 min。扩增产物经ABI 3730xl毛细管电泳分离检测后,使用GeneMarker软件进行基因型判读,确保分型数据准确性[27]。
引物
Primer引物序列(5’-3’)
Primer sequence(5’-3’)等位基因
数(Na)有效等位
基因数
(Ne)观测杂合
度(Ho)期望杂合
度(He)多态性含
量(PIC)VM1 F: GAACCCTTATTGGCCTGCCTAC
R: GGGACCAAATGACTTGAGTAATCT7 3.951 0.714 0.730 0.733 VM2 F: ACCCTAACAATTCTCTTTGTTTCCT
R: CCCCAATCTCAGTAAGGACTCA9 3.699 0.612 0.716 0.736 VM3 F: CTTGTGTCGAGCATGCATGTAT
R: TGCTGGCCTTTTATGTTAGGGT8 4.195 0.813 0.757 0.794 VM4 F: GCACTAGCACTAGCACTAGCTT
R: GGCTTTTCCAATTTCCATGGCT5 2.576 0.611 0.594 0.621 VM5 F: AGTTAAGGGACCAAATTTAGCGT
R: GTGTTTGTCAACTGGGCTTCAA5 3.499 0.565 0.707 0.712 VM6 F: TCATTTCTGTCTCACTCGACCC
R: TCATCGACGAATCACTGTTCGA7 3.779 0.720 0.731 0.749 VM7 F: GGGCAGCCTCGTAAATCAATTAC
R: ATTACCTGGCACAACCTTAGCC10 6.385 0.831 0.840 0.862 Table 2. Primer sequences and genetic diversity indices of the 7 SSR markers
-
基于筛选后的引物,利用GenAlex 6.51计算各位点及4个种群的遗传多样性参数,包括等位基因数(Na)、有效等位基因数(Ne)、观测杂合度(Ho)、期望杂合度(He)和多态性含量(PIC)等[28]。
-
采用STRUCTURE v2.3.4软件进行贝叶斯聚类分析:K值设置为1~10,每个K值运行10次,每次包含100 000次burn-in和200 000次MCMC模拟,通过delta K确定最佳聚类数[29]。采用GenAlex6.51软件进行种群间成对Fst值计算和主坐标分析(principal coordinates analysis, PCoA),基于Nei’s(1983)遗传距离计算种群间遗传距离,并使用MEGA11.0软件构建邻接树(neighbor-joining tree, NJ树),从不同维度验证种群遗传结构[30-32]。
-
利用SPAGeDi1.5计算个体间的亲属系数(kinship coefficient, Fij)[33],并通过9,999次随机置换检验获取95%置信区间。将其与空间距离的自然对数进行回归,获得回归斜率(bF)。FSGS强度按公式Sp=-bF/(1-F(1))计算,其中F(1)为第一距离类的平均亲缘系数。
-
本研究共筛选了7对高度多态性的SSR标记,并在372个个体完成基因分型分析。结果显示,各位点均表现出较高的遗传多态性(表2)。平均等位基因数(Na)为7,平均有效等位基因数(Ne)为4.012,平均观察杂合度(Ho)为0.695,平均期望杂合度(He)为0.725。7个位点的平均多态信息含量(PIC)为0.744,其中VM7的PIC值超过0.85,该位点在解析青梅种群遗传结构时具有较高的辨识能力[34]。总体而言,所选SSR引物在青梅材料中具有稳定扩增性和较高信息量,为遗传多样性及FSGS分析提供了可靠分子基础。
4个青梅种群均表现出较高的遗传多样性(表3)。等位基因数(Na)在6.286~8.143范围内变动,其中DL-H最高、BW-H最低;有效等位基因数(Ne)在3.917~4.091间波动,平均有效等位基因数为4.012。4个种群观测杂合度(Ho)和期望杂合度(He)范围分别为0.660~0.723和0.722~0.728。
种群
Population等位基因数(Na)
Number of
alleles有效等位基因数(Ne)
Effective number of alleles观测杂合度(Ho)
Observed heterozygosity期望杂合度(He)
Expected heterozygosityBW-H 6.286 4.091 0.723 0.726 BW-L 6.714 4.043 0.722 0.728 DL-H 8.143 3.997 0.660 0.726 DL-L 7.286 3.917 0.675 0.722 平均 Mean 7.107 4.012 0.695 0.726 Table 3. Genetic diversity statistics of the four Vatica mangachapoi populations.
-
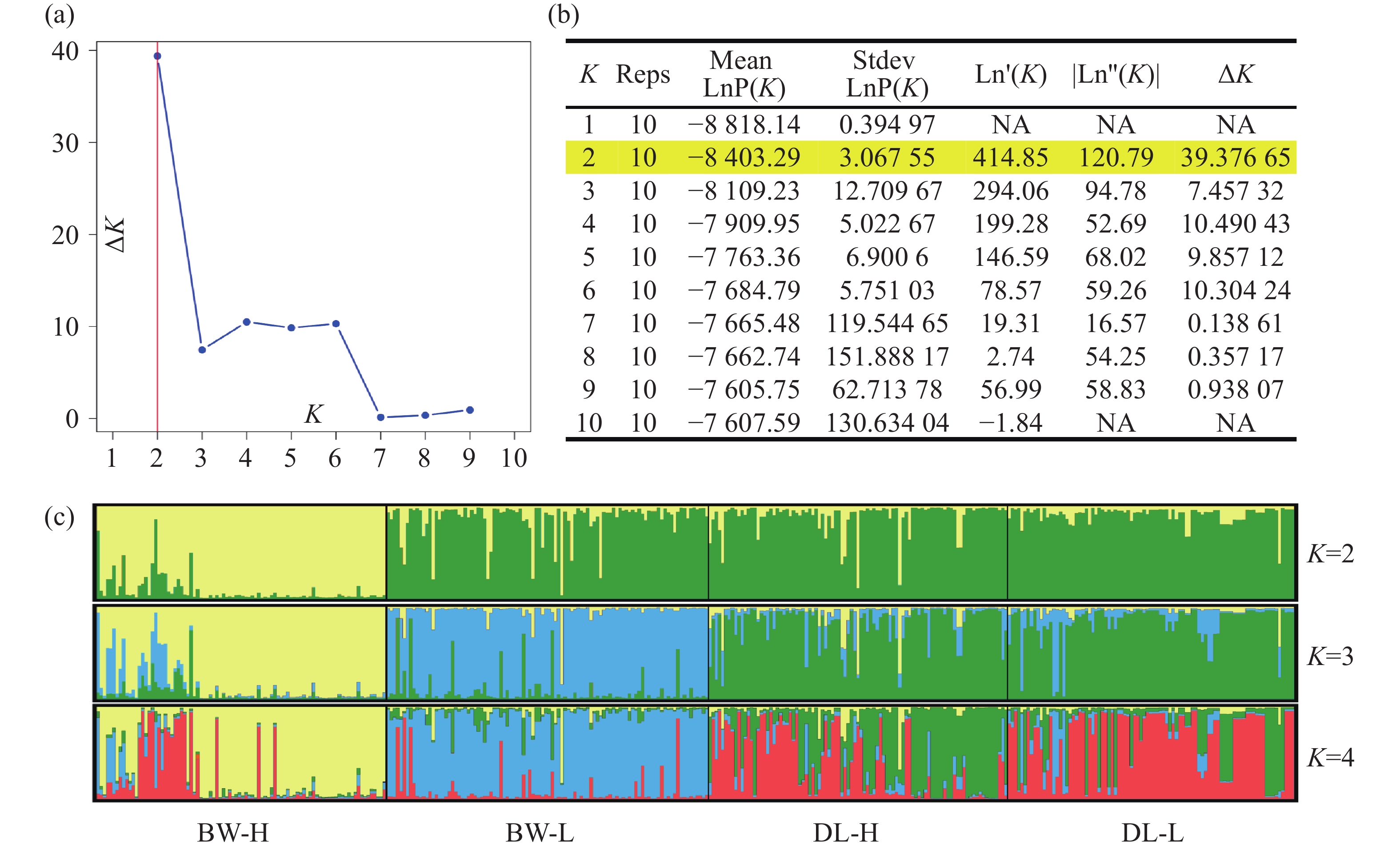
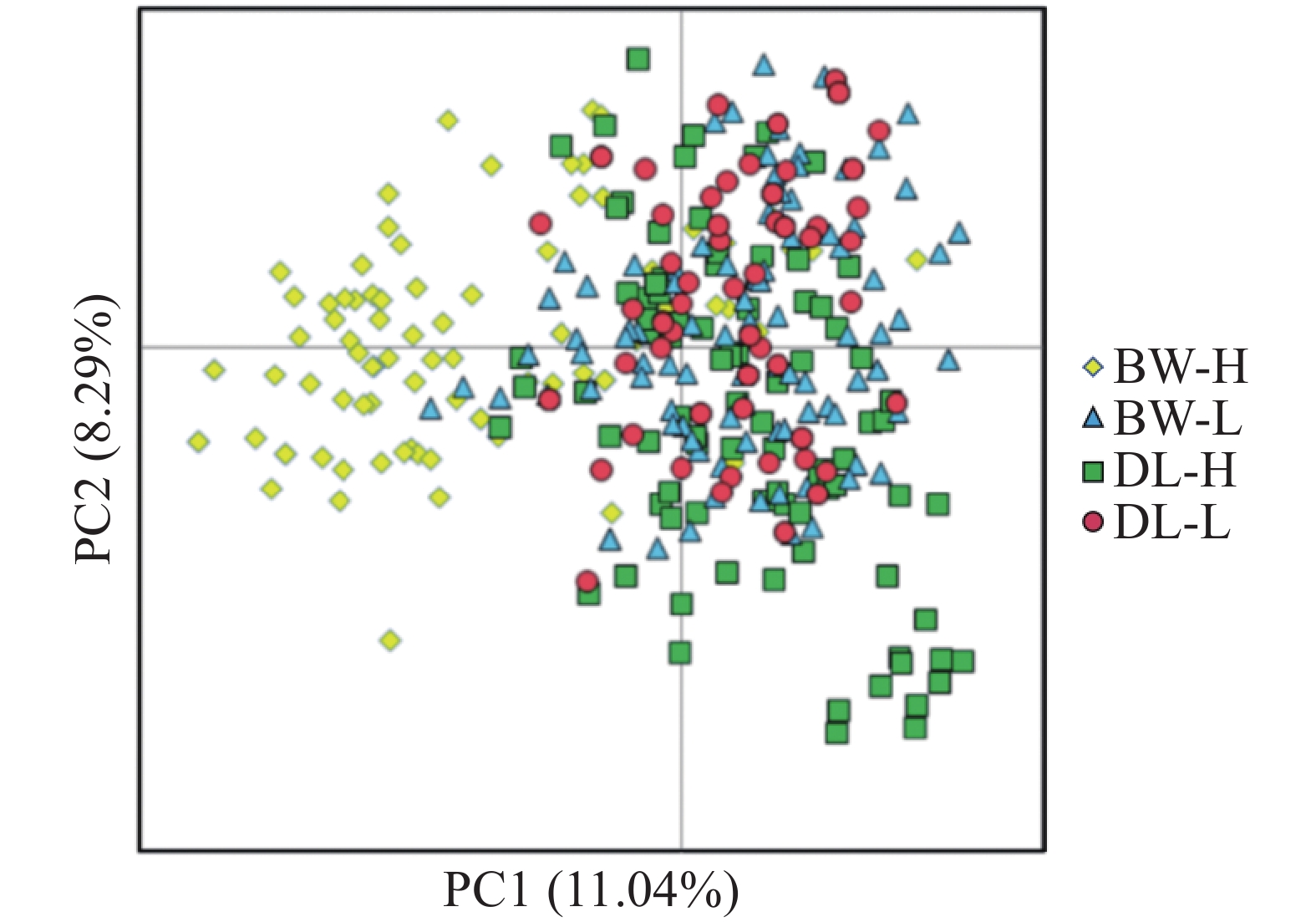
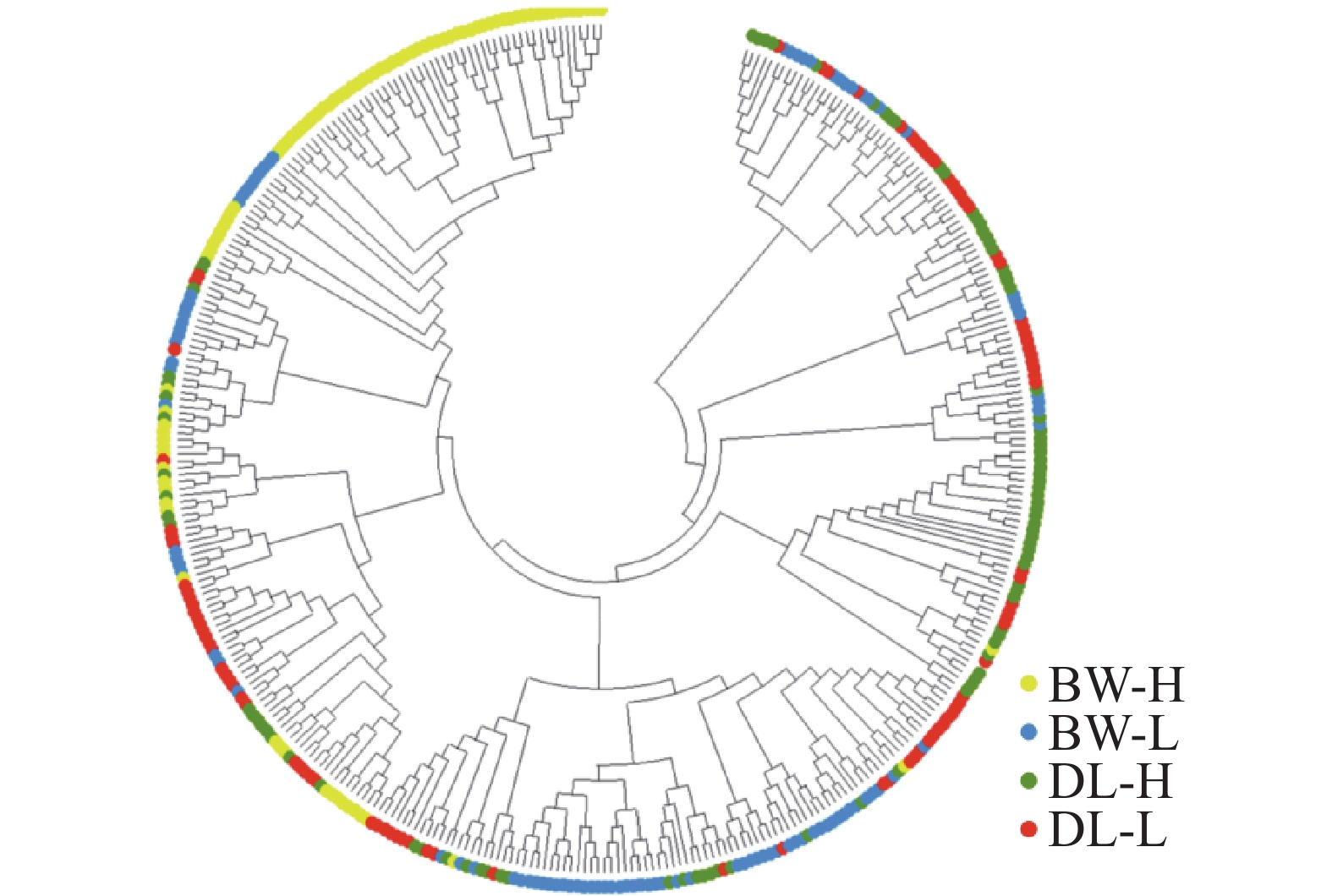
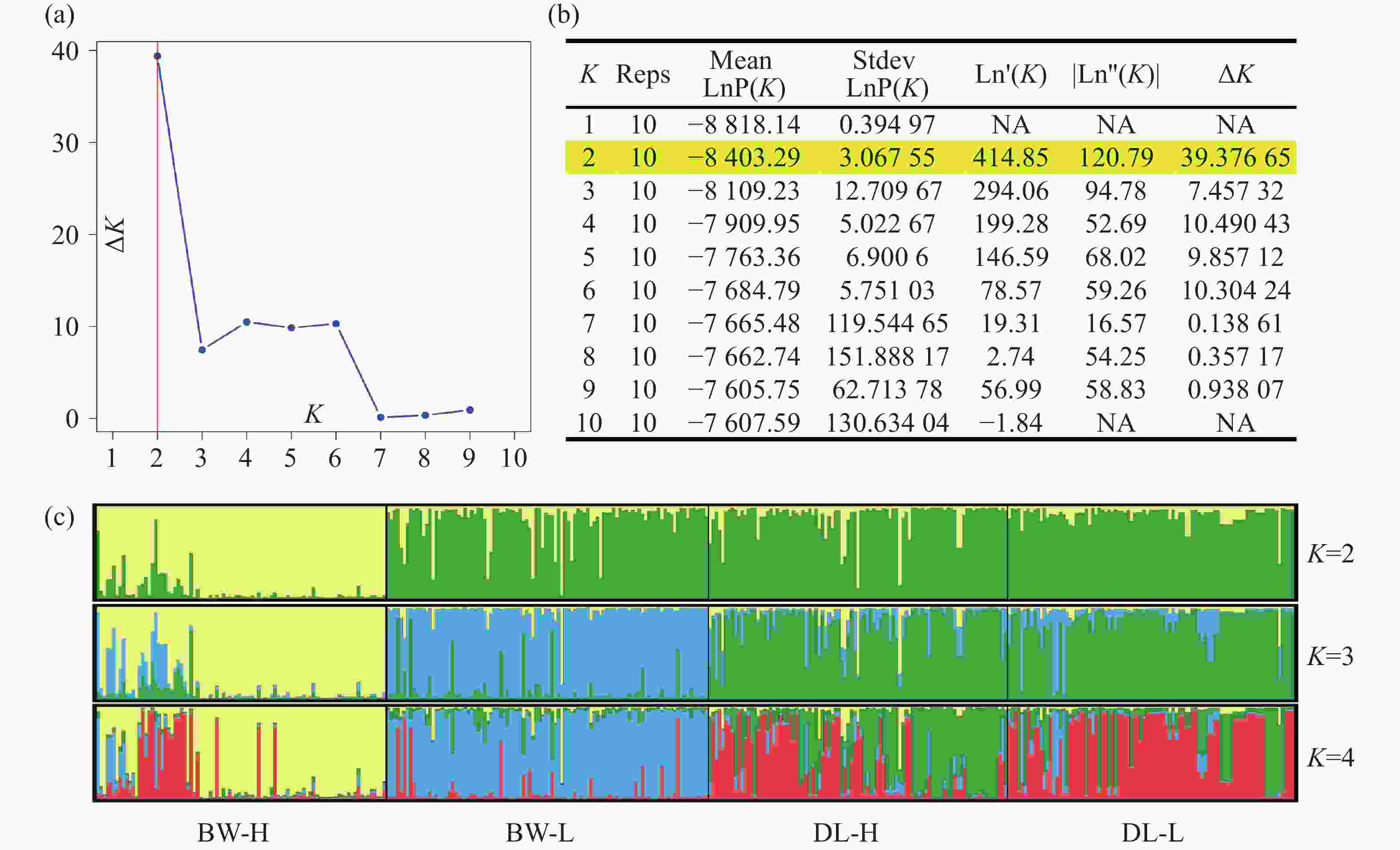
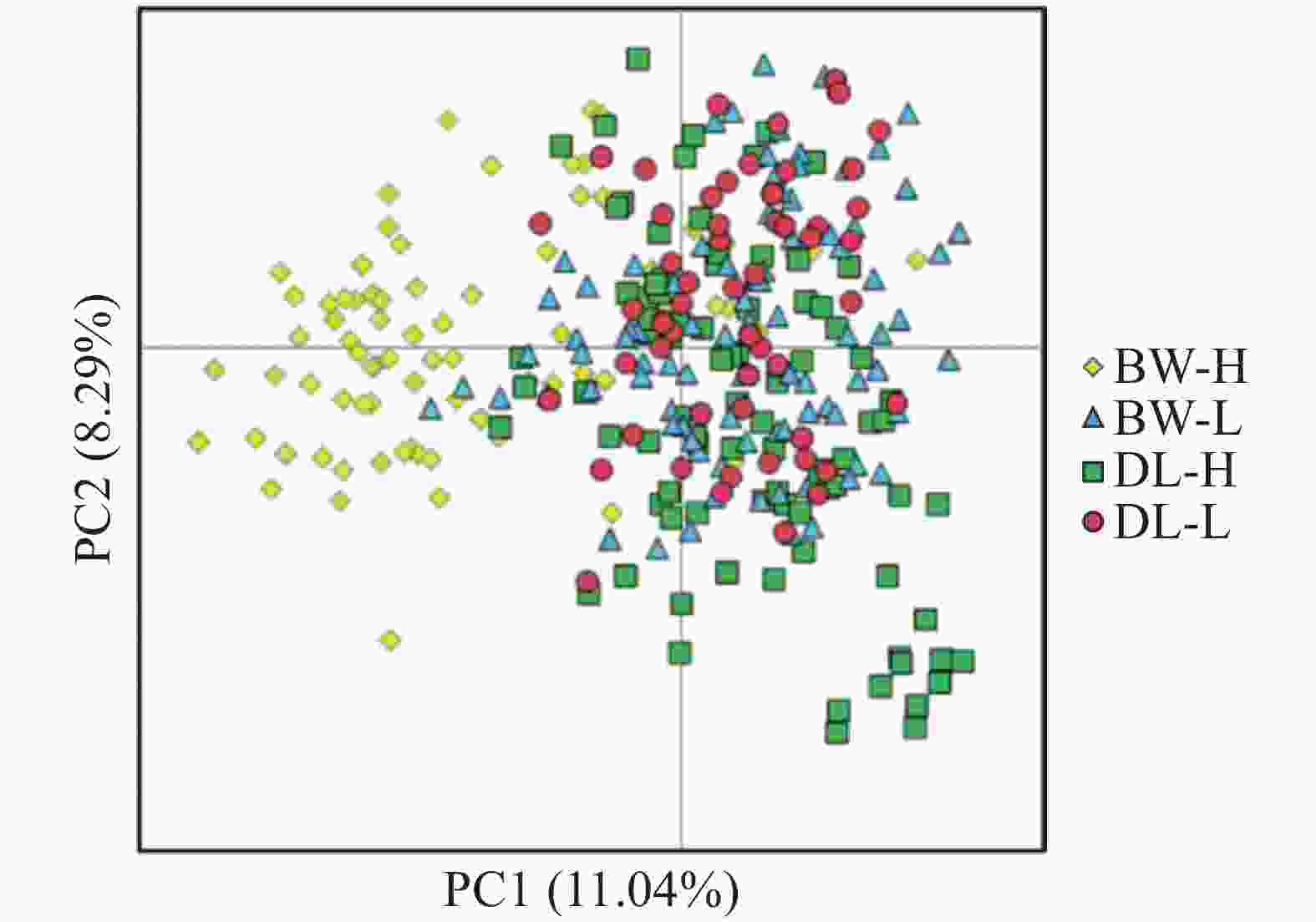
STRUCTURE 分析结果显示,K = 2时,delta K值最大(图2-a),表明青梅存在两种遗传组分,两种组分混杂在各个种群中,霸王岭高海拔种群(BW-H)与其他3个种群存在一定分化。基于Nei’s(1983)遗传进行的PCoA的两个主坐标共解释了22.13%的变异(图3),BW-H种群(黄色方块)在PC1轴的负向区域呈现显著的独立聚集,与其他3个种群的样本分离度较高;而DL-H(绿色方块)、BW-L(蓝色三角)、DL-L(红色圆点)的样本主要集中在PC1轴的正向及PC2轴的中值区域,三者间未形成清晰的种群特异性聚类,样本点相互重叠、混杂分布,无明显的遗传结构分化界限。PC1轴是驱动种群分离的核心维度,其负向区间的遗传差异主要对应BW-H种群的独立分布;PC2轴解释的遗传变异占比较低(仅8.39%),无法有效区分DL-H、BW-L、DL-L之间的遗传结构,因此,这3个种群的样本在空间上呈现聚集重叠的特征。NJ树显示研究种群的部分个体(图4),如霸王岭高海拔与低海拔种群的部分个体聚在一起,但4个种群的个体在总体上彼此混杂,没有呈现出明确的遗传分化。此外,种群间遗传分化系数(Fst)分析显示(表4),BW-H与其他,3个种群间遗传分化程度较大(Fst = 0.052~0.058),而其余种群间的遗传分化较弱(Fst = 0.018~0.028)。综上,STRUCTURE、PCoA、NJ 树及Fst结果在整体趋势上保持一致,表现为霸王岭高海拔种群(BW-H)在遗传组分构成及空间分布上表现出一定差异,而其余3个种群之间样本重叠度较高,未显示出明确的种群特异性遗传组分。
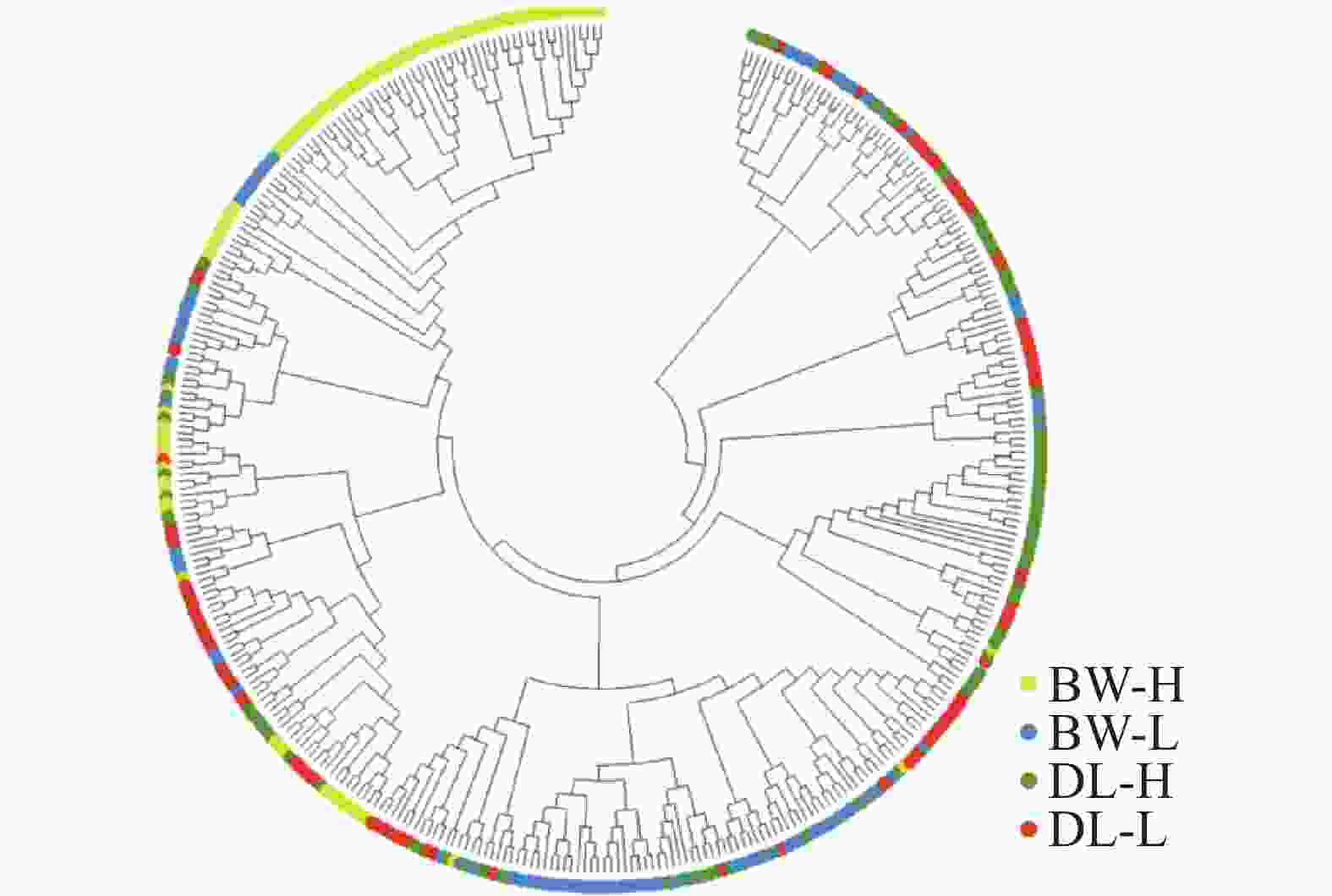
Figure 4. Neighbor-joining tree of all individuals from the four Vatica mangachapoi populations based on the Nei’s (1983)genetic distance
种群
PopulationBW-H BW-L DL-H DL-L BW-H 0.000 BW-L 0.058 0.000 DL-H 0.057 0.028 0.000 DL-L 0.052 0.029 0.018 0.000 Table 4. Pairwise genetic differentiation (Fst)between the Vatica mangachapoi populations.
-
采用SPAGeDi 1.5软件对4个种群FSGS进行分析,其强度参数(Sp)如表5所示。DL-H种群的FSGS强度最强(Sp =
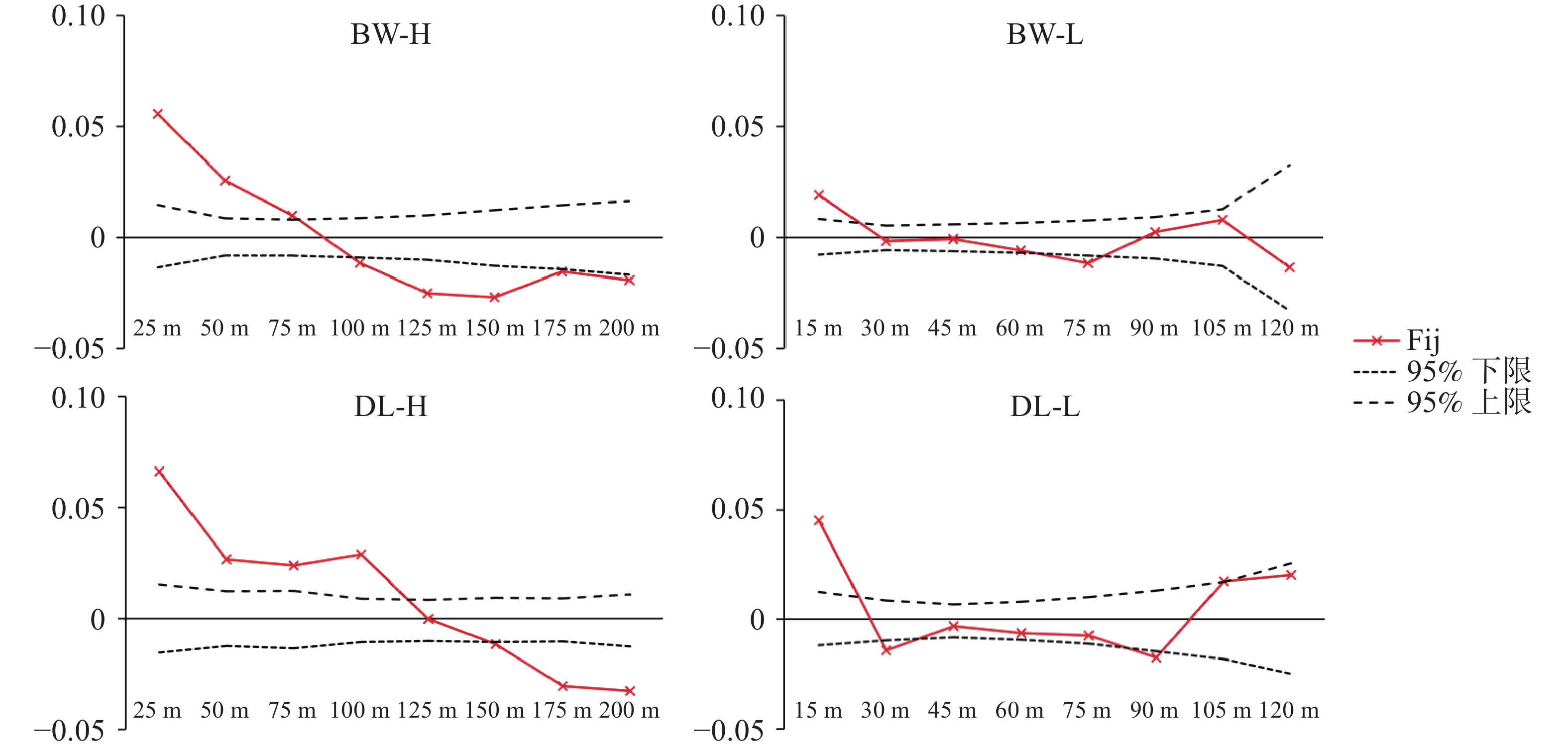
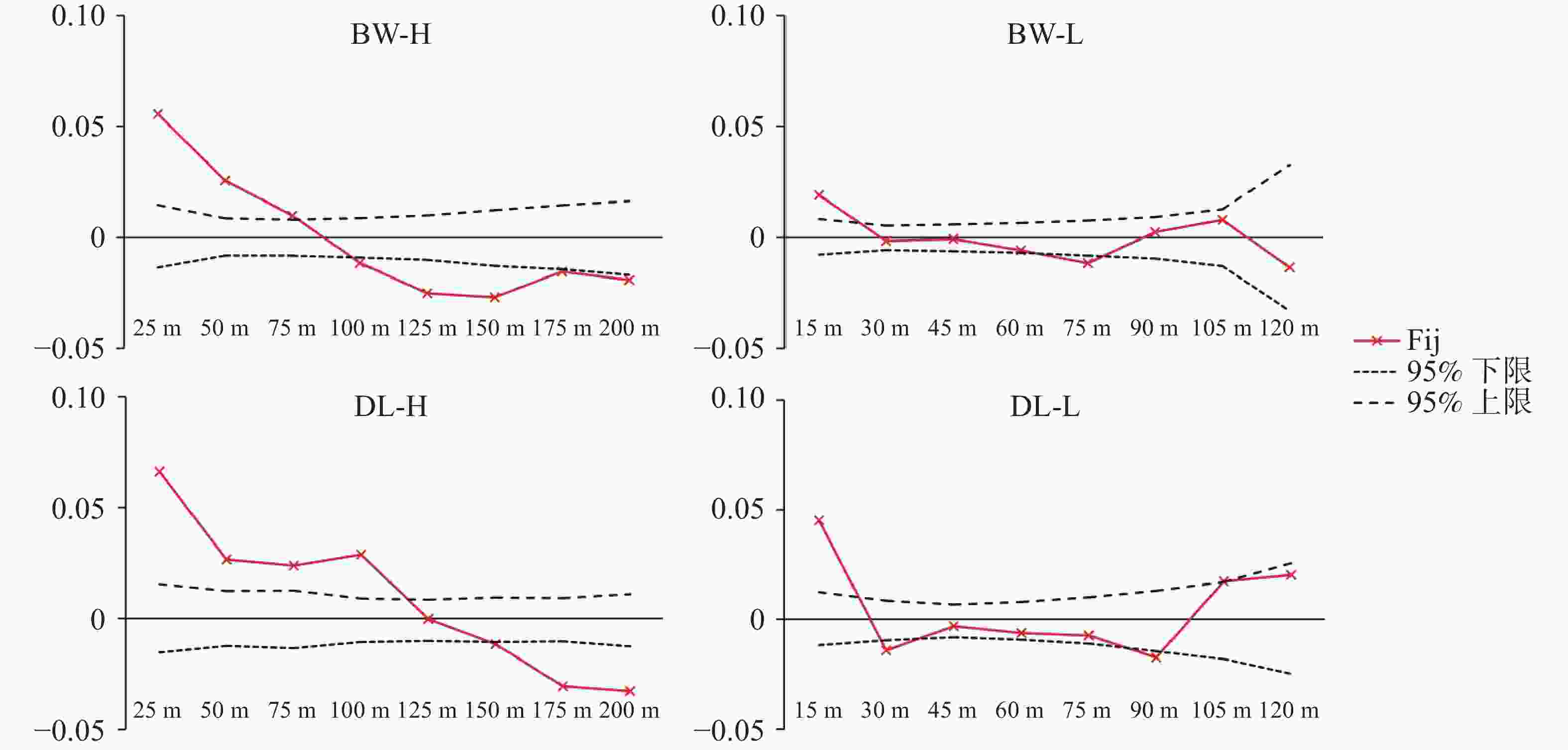
0.0440 ),而BW-L最弱(Sp =0.0096 )。4个种群的成对亲缘系数Fij随空间距离的变化趋势清晰地反映了上述差异(图5)。所有种群在最短距离等级内均表现出显著的正遗传相关性,即Fij值显著高于基于999 9次置换检验得到的95%置信区间上限。随距离增加,4个种群的变化轨迹明显不同:BW-H的Fij匀速下降,并在约85m处趋近于零;BW-L的Fij在25 m处进入置信区间,曲线在整个距离范围内最为平缓;而DL-H种群在75 m处出现了Fij回升,暗示了局部斑块内的家族聚集现象,DL-H在较远距离(110 m)内Fij仍维持较高水平;DL-L的Fij的下降速率最快,在25 m处降至零值并持续波动。种群
Population第一距离等级平均亲缘关系系数F(1)
Mean kinship coefficient(first distance class)回归斜率bF
Regression slope
(vs. ln-distance)FSGS强度Sp
Intensity of FSGSBW-H 0.0556 − 0.0340 0.0360 BW-L 0.0167 − 0.0094 0.0096 DL-H 0.0663 − 0.0410 0.0440 DL-L 0.0453 − 0.0160 0.0168 Table 5. FSGS related parameters of populations in Vatica mangachapoi based on SSR markers.
-
本研究基于微卫星标记系统评估了海南热带雨林国家公园青梅种群的遗传多样性,结果表明,青梅整体遗传多样性水平较高(Na = 7.107, He = 0.726),显著高于同域分布的另外两种濒危龙脑香科物种坡垒(H. hainanensis,Na = 2.458, He = 0.409)[35]和铁凌(H. reticulata,Na = 3.636, He = 0.599)[36]。后两者因近几十年生境急剧破碎化,有效种群规模下降而经历了明显的遗传漂变,导致等位基因大量丢失。尽管两种坡垒属植物均为同源四倍体,理论上应保存更丰富的遗传变异信息,但因历史干扰强烈、种群高度收缩,实际遗传多样性反而明显低于青梅[18,37-38]。
青梅较广泛地分布于海南岛低地雨林中,较大的林分面积为种群间基因交流提供了基础[39]。青梅具翅果,风力可使种子实现中等距离扩散(10 m以内)[40],有利于维持片段化青梅种群的遗传多样性。此外,龙脑香科大多数物种以异交为主,花粉流可能跨越种群破碎化造成的间断,从而抵消生境扰动对遗传多样性的不利影响[41-42]。本研究团队在野外的观察结果表明,青梅的潜在传粉者包括蓟马等小型昆虫,花粉扩散距离可能局限在数百米内,而翅果借助飞行可实现短距离种子传播,这种扩散机制能够在小范围维持一定水平的基因流,从而降低近交衰退并保持较高水平的遗传变异[19,43-45]。
检测到霸王岭高海拔群体(BW-H)与同地低海拔群体(BW-L)及两个吊罗山群体间相对略高的遗传分化,其本质是BW-H与其他群体在等位基因频率上的差异。导致这一差异的可能原因有突变率差异、自然选择和遗传漂变。考虑到SSR标记普遍被认为是中性进化的,因此,群体间SSR等位基因频率的差异主要受随机因素影响[46]。同一地点高低海拔群体的地理距离(霸王岭10 km,吊罗山8.3 km)已经超过了文献中报道的龙脑香科种子和传粉传播距离[47-48],发生当代基因流的可能性不大。群体间等位基因的频率差异可能更多的受遗传漂变的影响,当然也不排除霸王岭两个群体原有基因库的差异,以及突变率随机波动的贡献。将来可以借助单拷贝直系同源的核基因,或者基因组水平单核苷酸多态性数据深入分析和探讨霸王岭高低海拔群体等位基因频率差异的原因。
青梅高水平的遗传多样性是其优势种地位、异交繁育系统与有效扩散机制综合作用的结果,而区域尺度上的地理阻隔则塑造了其主要的遗传结构分化。该结果提示未来青梅保护管理需关注区域间遗传单元的独立性,同时维持连续生境以促进局地尺度的基因流,从而保障其长期遗传稳定性。
-
龙脑香科植物多数表现出显著的小尺度空间遗传结构,其中基因流受限所导致的近缘个体空间聚集被认为是FSGS形成的主要机制,特别是在100 m以内的空间尺度上,有限的种子扩散能力普遍被视为驱动龙脑香科树种FSGS的关键因素[51-53]。本研究结果发现,与多数龙脑香科植物比,青梅的FSGS强度处于一个中间水平:整体上弱于无翅果、扩散能力极弱的铁凌(Sp =
0.0228 )[54]和高度破碎化生境下的Vateriopsis seychellarum(Sp = 0.050 0)[55],但高海拔青梅(Sp = 0.044 0)又高于如Vateria indica(Sp = 0.026 0~0.027 0)[56]与部分Shorea物种(Sp = 0.010 0)[52]。这种中间状态表明青梅的FSGS既受其具翅果传播优势影响,也受海拔地形、微生境以及局部扩散限制的共同调控[48]。青梅在海南热带雨林国家公园的所有样地中均呈现一定程度的FSGS,但其强度在不同环境背景下存在差异。高海拔种群的FSGS(Sp = 0.036 0~0.044 0)明显强于低海拔种群的FSGS(Sp =0.009 6~0.016 8)。在高海拔地区,陡峭地形、母树密度较低以及微尺度风向紊乱均会限制青梅翅果的实际传播距离,使其“具翅优势”难以发挥,从而增强近邻亲缘的空间聚集。这一趋势与山地雨林中生境异质性更强、物种单优结构更显著的生态特点一致,并与热带山地木本植物中常见的高海拔更易形成FSGS的规律相吻合[48]。不同区域间的FSGS强度亦存在明显差异,表现为吊罗山东部种群高于霸王岭西部种群。吊罗山高海拔种群(Sp =0.044 0)不仅整体FSGS更强,还在75 m处出现局地亲缘峰值。尽管理论上海南岛东南部山区受台风等极端天气影响更强,可能有利于种子远距离传播,但实际结果反映出局地复杂地形结构对基因扩散的限制作用强于区域风力优势,从而导致东部种群聚集程度更高。与石梅湾典型单优青梅林相比,本研究区域的FSGS水平均远高于海岸种群(Sp = 0.004 7)[19]。石梅湾生境开阔且风向稳定,有利于翅果长距离扩散,且单优青梅林开花密度极大,长距离花粉流发生的可能性远高于研究区内,从而在大范围内促进遗传均质化;而本研究区山地地貌一定程度上限制了扩散,增强了近缘个体的空间聚集的可能[43,48]。
青梅FSGS的形成并非单一传播特征决定,而是扩散能力、微环境因子等协同作用的结果。高海拔与复杂微地形显著加强亲缘聚集,而低海拔连续林分和稳定风场则弱化FSGS;区域差异进一步说明微环境结构可显著改变同一物种的空间遗传格局。本研究从种内尺度揭示了青梅FSGS的环境敏感性,为理解热带龙脑香科树种在异质山地环境中的更新扩散机制以及保护管理策略提供了重要参考。
-
基于本研究的遗传特征,提出以下保护与管理建议:1)优先保护高海拔种群的核心生境。高海拔种群FSGS强度显著,基因扩散受限,更易受生境破碎化威胁,需建立就地保护小区,减少人为干扰对地形与植被连续性的破坏;2)维持低海拔区域的生境连通性。低海拔种群基因交流频繁,是种群间遗传连通的“纽带”,需避免过度开发导致的生境断裂,保障花粉与种子的自然传播路径;3)实施针对性的遗传调控措施。对于DL-H等FSGS较强的种群,可通过人工辅助授粉、跨种群幼苗移栽等方式,引入同源区域低海拔种群的基因,缓解遗传隔离压力;4)建立种质资源库与长期监测体系。收集不同区域、海拔的青梅果实,异地建立种质资源库,同时开展种群遗传多样性动态监测,为保护策略的优化提供数据支撑[33]。这些建议可为热带龙脑香科树种的保护提供参考,也为海南热带雨林国家公园的生物多样性管理提供科学依据。
-
本研究基于SSR分子标记,明确了海南热带雨林国家公园青梅种群整体遗传多样性水平较高,平均期望杂合度(He)为0.726,显著高于海南岛同属龙脑香科其他物种,略高于沿海区域青梅种群,种群遗传组分混杂、样本重叠度较高,其广泛的分布范围、风力传播特性与较强的生境适应能力是维持高遗传多样性和遗传均质的关键因素。小尺度空间遗传结构存在明显海拔差,高海拔种群表现出更强的空间聚集(Sp = 0.036 0~0.044 0),低海拔种群基因交流更为频繁,表现出较弱的FSGS(Sp = 0.009 6~0.016 8)。基于上述遗传特征,建议优先保护高海拔核心种群、维持低海拔生境连通性,并通过人工辅助基因交流与种质资源库建设,提升青梅种群的遗传稳定性与适应潜力,为热带森林生态系统的保护与恢复提供支撑。
Fine-scale spatial genetic structure of Vatica mangachapoi (Dipterocarpaceae)
DOI: 10.15886/j.cnki.rdswxb.20250182
- Received Date: 2025-11-27
- Accepted Date: 2026-02-24
- Rev Recd Date: 2026-02-13
-
Key words:
- Vatica mangachapoi Blanco /
- SSR markers /
- Hainan Tropical Rainforest National Park /
- genetic diversity /
- fine-scale spatial genetic structure (FSGS)
Abstract: Vatica mangachapoi Blanco, a member of the genus Vatica (Dipterocarpaceae), is a dominant species in the tropical lowland rainforests of Hainan Island. Understanding its genetic dynamics and fine-scale gene dispersal patterns is essential for elucidating the ecological adaptation of dominant tree species in tropical ecosystems. In this context 372 individuals across different elevational gradients were sampled from Bawangling and Diaoluoshan within Hainan Tropical Rainforest National Park to evaluate genetic diversity, population structure, and fine-scale spatial genetic structure (FSGS) using seven microsatellite loci. The results revealed a relatively high overall genetic diversity in V. mangachapoi (Na = 7.107, He = 0.726), markedly higher than that of other two dipterocarps on Hainan Island, Hopea hainanensis (Na = 2.458, He = 0.432) and H. reticulata (Na = 3.636, He = 0.599). STRUCTURE analysis found that the high altitude population at Bawangling (BW-H) differentiated to some extent with the other three populations, while PCoA and NJ tree analyses could not detect clear genetic differentiation among the four populations. FSGS analyses indicated stronger spatial clustering of genotypes in high-elevation populations (Sp =
| Citation: | Zhu Siqi, Duan Jiyu, Tang Liang. Fine-scale spatial genetic structure of Vatica mangachapoi (Dipterocarpaceae)[J]. Journal of Tropical Biology. doi: 10.15886/j.cnki.rdswxb.20250182 |






 DownLoad:
DownLoad: